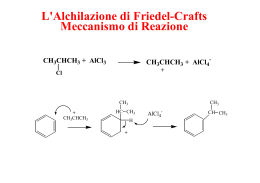
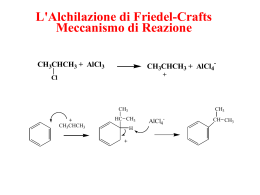
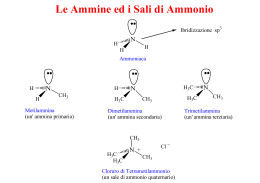
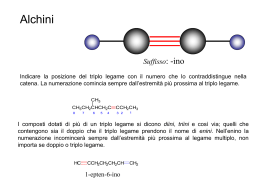
RIPASSO Chimica organica Gruppi Funzionali Contenenti Legami Multipli CarbonioCarbonio Gruppo Funzionale Nome Esempio Nome IUPAC Nome Comune Alchene H2C=CH2 Etene Etilene Alchino HC@CH Etino Acetilene Arene C6H6 Benzene Gruppi Funzionali Contenenti un Atomo Elettronegativo Legato al Carbonio con un Legame Singolo Gruppo Funzionale Nome Esempio Nome IUPAC Nome Comune Alogenuro H3C-I Iodometano Ioduro di metile Alcol CH3CH2OH Etanolo Alcol Etilico Etere CH3CH2OCH2CH3 Dietil etere Etere Ammina H3C-NH2 Amminometano Metilammina Nitro Composto H3C-NO2 Nitrometano Tiolo H3C-SH Metantiolo Solfuro H3C-S-CH3 Dimetil solfuro Metil mercaptano Gruppo Funzionale Nome Esempio Nome IUPAC Nome Comune H3C-CN Etanonitrile Acetonitrile Nitrile Aldeide H3CCHO Etanale Aldeide acetica Acido carbossilico H3CCOCH3 Propanone Acetone Estere H3CCO2H Acido Etanoico Acido acetico Cloruro acilico H3CCO2CH2CH3 Etil etanoato Acetato di etile Ammide H3CCOCl Etanoil cloruro Cloruro di acetile H3CCON(CH3)2 N,NDimetiletanammide N,N-Dimetilacetammide (H3CCO)2O Anidride Etanoica Anidride acetica Chetone Anidride acilica Alcani lineari Gli alcani noti anche come idrocarburi saturi sono molecole organiche costituite solo da carbonio e idrogeno con esclusivamente legami singoli. •Formula molecolare CnH2n + 2 •Ibridazione sp3 del carbonio •E’ una serie omologa Nomenclatura alcani lineari I nomi degli alcani semplici non ramificati sono costituiti da una radice che indica il numero di carboni che costituisce la catena e dalla desinenza ano (definita anche suffisso) che indica la classe di appartenenza. La tabella seguente riporta i nomi degli alcani lineari semplici. Radicali alchilici Rimuovendo un idrogeno da una catena alchilica si ottiene un radicale alchilico. Il nome di un radicale alchilico si ottiene sostituendo il suffisso ano dell’alcano corrispondente con il suffisso ile. Il nome dei radicali alchilici è molto importante per la nomenclatura degli alcani ramificati. Nomenclatura d’uso di sostituenti ramificati Per sostituenti ramificati costituiti da una catena principale a 2, 3, 4 e 5 atomi di carbonio è possibile utilizzare nomi d’uso. I principali nomi d’uso che possono essere usati nella nomenclatura IUPAC sono riportati nell’immagine a lato e ricordano le unità strutturali iso e neo oppure il tipo di carbonio sostituito (sec per secondario e tert per terziario). Isomeri di struttura Esistono 2 possibili strutture che possiamo scrivere per un alcano a 4 C (formula molecolare C4H10): una struttura lineare e una ramificata. Butano e isobutano sono isomeri di struttura. Per un alcano di formula C5H12 possiamo scrivere 3 possibili strutture. Ancora una volta una lineare, il pentano, e due ramificate. Cicloalcani Ciclopropano Molecola piana. Forte tensione angolare degli atomi ibridati sp3 (60°) Ciclobutano Molecola non piana. Forte tensione angolare, angolo di legame 88°. Ciclopentano Molecola non piana. Angolo di legame 105°. Più stabile perché l’angolo di legame si avvicina a quella dell’ibrido sp3. Presenti stereoisomeri configurazionali (cis-trans) se vi sono sostituenti alchilici. Cicloesano Molecola non piana. Gli H sono legati ai C mediante legami equatoriali (sul piano dei C) o assiali (sopra o sotto il piano dei C). Gli isomeri assumono 2 conformazioni “a sedia” per rotazione degli H che da assiali diventano equatoriali e vice versa. I sostituenti voluminosi vengono legati preferenzialmente in posizione equatoriale a causa della repulsione sterica con gli altri H assiali. Conformazione meno stabile è “a barca”, sempre a causa dell’ingombro sterico degli H. Alcheni Ogni atomo di C che forma un doppio legame è detto trigonale, in quanto legato a 3 atomi e non a 4. La rotazione attorno al doppio legame è impedita. Gli atomi di C del doppio legame e gli H ad essi legati si trovano sullo stesso piano. L’angolo di legame del C trigonale è di 120°. Il legame è più corto (1,34 Å vs 1.54 Å). Solo 3 dei 4 orbitali del C vengono ibridati a formare ibridi sp2 che giacciono su un piano a formare un triangolo equilatero. Il quarto elettrone si trova su un orbitale non ibridato (sp2 perché è 1 orbitale s e 2 orbitali p) perpendicolare al piano dei tre orbitali ibridi. Il doppio legame è dato dal legame σ tra due orbitali ibridati ed un legame π dell’orbitale non ibridato. Questo spiega perché il doppio legame non può ruotare. Addizione di acidi Gli acidi alogenidrici (H-X) attaccano gli alcheni fornendo un alogeno alcano (alogenuro alchilico) H H H H3C C CH2 + H Cl H3C C CH2 C C H+ Cl H H + C C C C Cl- Cl Le reazioni di addizione elettrofila avvengono in posizione trans 12 Regola di Markovnikov Nell’addizione di elettrofili asimmetrici agli alcheni: Si forma sempre l’isomero che deriva dal catione intermedio più stabile, cioè quello più sostituito In pratica l’anione si lega al carbonio più sostituito Anche l’alchene deve essere asimmetrico H3C H CH3 C C+ H3C CH3 H3C CH3 C C H3C CH3 H3C C+ H3C CH3 C H CH3 13 Addizione di acqua (meccanismo) L’acqua non è un elettrofilo sufficientemente forte da attaccare il doppio legame in tempi brevi (anzi è un nucleofilo) È necessario utilizzare un catalizzatore acido (H+) CH3 H H H3C C C CH3 H3C C C CH3 H CH3 H+ 1a fase: attacco del protone al doppietto + 2a fase: formazione del carbocatione più stabile (terziario) H H O H + H3C C C CH3 H CH3 3a fase: entra il nucleofilo 14 Benzene e composti aromatici Il rapporto tra C e H del C6H6 fa pensare ad una struttura altamente insatura. Se confrontata all’esano (C6H14) ed al cicloesano (C6H12). Il benzene, però, non si comporta come un composto insaturo (non decolora le soluzioni di bromo come gli alcheni e gli alchini e non viene facilmente ossidato dal permanganato di potassio, né subisce le reazioni di addizione degli alcheni ed alchini. Al contrario dà soprattutto reazioni di sostituzione analogamente agli alcani. A differenza del cicloesano la struttura del benzene è piana e gli atomi di C sono ibridati sp2, quindi due di questi obitali sono impegnati a fare un legame con i C adiacenti ed il terzo a fare un legame con H. L’orbitale p non ibridato di ciascun C è perpendicolare al piano dei carboni; gli orbitali p si sovrappongono lateralmente a formare orbitali che danno origine ad una nuvola elettronica al di sopra ed al di sotto del piano dell’anello benzenico. STEREOCHIMICA ISOMERI DI STRUTTURA Sono composti che hanno la stessa formula molecolare, ma diversa formula di struttura Gli atomi sono legati tra loro in successione differente STEREOISOMERI sono composti che hanno la stessa formula molecolare, gli atomi sono reciprocamente legati nello stesso ordine (o sequenza) gli atomi sono disposti in maniera diversa nello spazio cioè hanno configurazioni disposizioni spaziali diverse) diverse (cioè CICLOESANO: conformazione a sedia e a barca STEREOISOMERI Se sono interconvertibili per rotazione intorno ad un legame allora sono detti ROTAMERI o CONFORMERI Se sono interconvertibili solo per rottura e riformazione dei legami allora sono detti ISOMERI CONFIGURAZIONALI ISOMERIA GEOMETRICA (CIS-TRANS) è un fenomeno proprio di alcuni cicloalcani, delle molecole organiche contenenti due atomi asimmetricamente sostituiti e legati tra loro con un doppio legame. ENANTIOMERI Si definiscono enantiomeri due molecole che hanno la stessa formula molecolare, in cui gli atomi sono reciprocamente legati nello stesso ordine formano una coppia di immagini speculari non sovrapponibili GLI ENANTIOMERI Differiscono per il fatto che Hanno diversa reattività verso altri composti “otticamente attivi” un enantiomero fa ruotare a destra il piano della luce polarizzata, mentre l’altro lo fa ruotare a sinistra Dato un particolare enantiomero, come posso indicare in modo univoco la sua configurazione e il suo nome? Si ricorre alle regole di Cahn-Ingold-Prelog (CIP o convenzione R-S) che permettono di descrivere la configurazione di uno stereocentro definendola rispettivamente R (dal latino rectus, quindi destrorsa) o S (dal latino sinister, quindi sinistrorsa) in base all’ordine con cui i differenti sostituenti sono disposti intorno allo stereocentro. Regole di Cahn-Ingold-Prelog (convenzione R-S) Stabilire l’ordine di priorità dei quattro gruppi legati al centro stereogeno Guardare il centro stereogeno dalla parte opposta a quella in cui c’è il gruppo a priorità minore Collegare i tre gruppi rimasti con una freccia che va dal gruppo a priorità maggiore a quello a priorità minore Freccia con senso orario la configurazione è R Freccia con senso antiorario la configurazione è S (R)-nome (S)-nome DIASTEREOISOMERI Si definiscono diastereoisomeri i composti che sono stereoisomeri, ma non sono enantiomeri, in quanto non sono l’uno l’immagine speculare dell’altro Sono sostanze chimiche completamente diverse tra di loro: cioè hanno proprietà chimiche e fisiche diverse Tra i 4 possibili stereoisomeri del 3-Bromo-2-butanolo quanti diastereoisomeri si avranno? 1) 2) 3) 4) 1) e 3) sono diastereoisomeri 1) e 4) sono diastereoisomeri 2) e 3) sono diastereoisomeri 2) e 4) sono diastereoisomeri
Scaricare