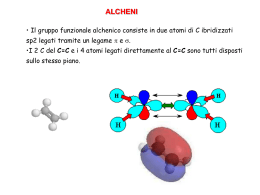
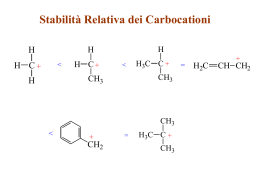
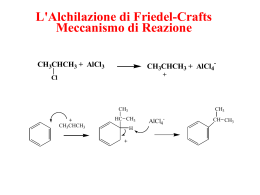
Gli Alcheni : struttura e nomenclatura Alcheni Gli alcheni sono idrocarburi che contengono un doppio legame carbonio-carbonio sono anche detti “olefine” o idrocarburi insaturi La formula molecolare è CnH2n I cicloalcheni, come i cicloalcani, hanno 2 H in meno rispetto al corrispondente idrocarburo saturo hanno cioè una insaturazione Nomenclatura degli alcheni H2C CH2 Etene o Etilene (sono entrambi accettati nella nomenclatura IUPAC) H2C CHCH3 Propene (Propilene è talvolta usato ma non è un nome IUPAC) Nomenclatura degli alcheni H2C CHCH2CH3 1) Si individua la catena più lunga che contiene il doppio legame 2) Si sostituisce al suffisso –ano del nome dell’alcano non ramificato con lo stesso numero di atomi di carbonio, la desinenza -ene. 3) Si numera la catena nella direzione che consente di dare al doppio legame il numero più basso possibile. Nomenclatura degli alcheni H2C CHCH2CH3 1-Butene 1) Si individua la catena più lunga che contiene il doppio legame 2) Si sostituisce al suffisso –ano del nome dell’alcano non ramificato con lo stesso numero di atomi di carbonio, la desinenza -ene. 3) Si numera la catena nella direzione che consente di dare al doppio legame il numero più basso possibile. Nomenclatura degli alcheni H2C CHCHCH2Br CH3 4) Se è presente un sostituente si identifica la sua posizione con un numero. Il doppio legame ha la precedenza sui gruppi alchilici e sugli alogeni quando la catena è numerata. Il composto in alto è 4-bromo-3-metil-1-butene. Nomenclatura degli alcheni H2C CHCHCH2OH CH3 4) Se è presente un sostituente si identifica la sua posizione con un numero. Il gruppo idrossi ha la precedenza sul doppio legame . Il composto in alto è 2-metil-3-buten-1-olo. Gruppi Alchenilici metilene H2C vinile H2C CH allile H2C CHCH2 isopropenile H2C CCH3 Nomenclatura dei Cicloalcheni Cicloesene 1) Si sostituisce la desinenza –ano del cicloalcano con lo stesso numero di carboni con il suffisso -ene. Nomenclatura dei Cicloalcheni CH3 CH2CH3 1) Si sostituisce la desinenza –ano del cicloalcano con lo stesso numero di carboni con il suffisso -ene 2) Si numera partendo dal doppio legame nella direzione che da il numero più basso al primo sostituente Nomenclatura dei Cicloalcheni CH3 6-Etil-1-metilcicloesene CH2CH3 1) Si sostituisce la desinenza –ano del cicloalcano con lo stesso numero di carboni con il suffisso -ene 2) Si numera partendo dal doppio legame nella direzione che da il numero più basso al primo sostituente Struttura e legame negli alcheni Struttura dell’Etilene angoli di legame: H-C-H = 117° H-C-C = 121° distanze di legame: C—H = 1,10 A C=C = 1,34 A planare Legami nell’Etilene σ σ σ σ σ Scheletro dei legami σ Ciascun carbonio è ibridizzato sp2 Legami nell’Etilene Ciascun carbonio ha un orbitale p semipieno Legami nell’Etilene La sovrapposizione laterale degli orbitali p da origine al legame π Legami nell’Etilene Isomeria degli Alcheni Conseguenze della mancanza di rotazione attorno al doppio legame C-C Isomeria geometrica Isomeri Gli isomeri sono composti che hanno la stessa formula molecolare Isomeri isomeri Costituzionali Stereoisomeri Isomeri isomeri Costituzionali connettività differente Stereoisomeri stessa connettività; diversa disposizione degli atomi nello spazio Isomeri isomeri Costituzionali Stereoisomeri Gli alcheni possono presentare tutte e due le isomerie. Consideriamo gli alcheni isomeri di formula C4H8 H CH2CH3 C H3C C H CH3 C H 1-Butene C H H 2-Butene H3C isomeri Costituzionali di formula C4H8 H C H3C C H 2-Metilpropene Soffermiamoci sul 2-butene H3C CH3 C H H H3C C C H cis-2-Butene H C CH3 trans-2-Butene Negli alcheni esiste anche la isomeria geometrica Poichè non c’è rotazione intorno al doppio legame Gli stereoisomeri dovuti alla isomeria geometrica Sono isomeri configurazionali Condizione necessaria per l’esistenza di isomeria geometrica Notazione Stereochimica cis (sostituenti identici o analoghi dallo stesso lato) trans (sostituenti identici o analoghi da parte opposta) Figura L’interconversione degli alcheni isomerici non si verifica normalmente. Infatti si dovrebbe rompere un legame π. cis trans La nomenclatura cis/trans è ambigua e non può essere applicata universalmente Per questo motivo è stata introdotta la nomenclatura E-Z degli Alcheni isomerici Il sistema di Nomenclatura E-Z E : i sostituenti a priorità maggiore dal lato opposto Z : i sostituenti a priorità maggiore dallo stesso lato maggiore C minore minore C maggiore Entgegen maggiore C minore maggiore C minore Zusammen Il sistema di Nomenclatura E-Z Domanda: Come sono ordinati i sostituenti? Risposta: Sono ordinati per numero atomico decrescente. maggiore C minore minore C maggiore Entgegen maggiore C minore maggiore C minore Zusammen Il sistema di nomenclatura di CahnIngold-Prelog (CIP) R. S. Cahn Sir Christopher Ingold Vladimir Prelog Le regole di priorità del sistema (CIP) applicate alla stereochimica degli alcheni sono le stesse di quelle impiegate per l’assegnazione configurazionale R-S dei centri stereogenici Regole del sistema CIP (1) I sostituenti vengono ordinati secondo numero atomico decrescente Br > F Cl > H maggiore Br C minore F Cl maggiore H minore C Regole del sistema CIP (1) I sostituenti vengono ordinati secondo numero atomico decrescente Br > F Cl > H maggiore Br C minore F Cl maggiore H minore C (Z )-1-Bromo-2-cloro-1-fluoroetene Regole del sistema CIP (2) Quando due atomi sono identici allora si valuta il numero atomico dell’atomo ad essi immediatamente legato (3) La priorità viene stabilita al primo punto di differenza —CH2CH3 priorità maggiore di —CH3 —C(C,H,H) —C(H,H,H) Regole del sistema CIP (4) Il confronto del numero atomico degli atomi legati al carbonio in esame procede dal punto di attacco lungo il resto della catena carboniosa. —CH(CH3)2 priorità maggiore di —CH2CH2OH —C(C,C,H) —C(C,H,H) Regole del sistema CIP (5) Gli atomi vengono valutati uno alla volta. Non si fa la somma del numero atomico di un intero gruppo —CH2OH priorità maggiore di —C(CH3)3 —C(O,H,H) —C(C,C,C) Regole del sistema CIP (6) I doppi e i tripli legami vengono considerati alla stregua di legami semplici, raddoppiando o triplicando gli atomi che vi si trovano. —CH=O priorità maggiore di —CH2OH —C(O,O,H) —C(O,H,H) Effetto dei sostituenti sulla stabilità degli alcheni Effetto Elettronico Gli alcheni disostituiti sono più stabili di quelli monosostituiti Effetto Sterico gli alcheni trans sono più stabili dei cis Effetto dei sostituenti sulla stabilità degli alcheni Elettronico i gruppi alchilici stabilizzano il doppio legame più dell’H gli alcheni più sostituiti sono più stabili di quelli meno sostituiti Effetto dei sostituenti sulla stabilità degli alcheni Effetti Sterici gli alcheni trans sono più stabili dei cis gli alcheni cis sono destabilizzati dalle tensioni steriche di van der Waals tensione di van der Waals tra i due metili in cis cis-2-butene Figura cis e trans-2-Butene trans-2-butene tensione di van der Waals tra i due metili in cis cis-2-butene Figura cis e trans-2-Butene trans-2-butene Tensione sterica di van der Waals Gli effetti sterici causano una notevole differenza di stabilità tra il cis e trans-(CH3)3CCH=CHC(CH3)3 il cis è 10,5 kcal/mol meno stabile del trans CH3 H3C H3C H3C C C C H CH3 C H CH3 Esempi di Nomenclatura di Alcheni Esempi di Nomenclatura di Alcheni Esempi di Nomenclatura di Alcheni Cicloalcheni Cicloalcheni il Ciclopropene e il ciclobutene hanno una notevole tensione angolare Cicloalcheni di dimensioni superiori, come il ciclo pentene e il cicloesene, possono incorporare un doppio legame nell’anello senza soffrire di una grossa tensione angolare. Proprietà fisiche degli alcheni Gli alcheni hanno proprietà simili a quelle degli alcani con pari numero di atomi di carbonio, rispetto ai quali presentano una densità un po’ più alta e un punto di ebollizione un po’ più basso. PREPARAZIONE DI ALCHENI: Deidroalogenazione degli Alogenuri Alchilici Disidratazione degli alcoli a alcheni Deidrogenazionedegli alcani Reazioni di β-Eliminazione: il doppio legame si forma attraverso reazioni di eliminazione deidrogenazione degli alcani: X=Y=H disidratazione degli alcoli: X = H; Y = OH deidroalogenazione degli alogenuri alchilici: X = H; Y = Br, etc. X C β Cα Y C C + X Y Reazioni di β-Eliminazione deidrogenazione degli alcani : processo industriale; non regioselettivo disidratazione degli alcoli : acido-catalizzata deidroalogenazione degli alogenuri alchilici : promossa dalle basi X C β Cα Y C C + X Y Deidroalogenazione E’ un metodo utile per la preparazione degli alcheni Cl NaOCH2CH3 etanolo, 55°C (100 %) oppure NaOCH3 in metanolo, o KOH in etanolo Regioselettività KOCH2CH3 Br + etanolo, 70°C 29 % 71 % viene seguita la regola di Zaitsev infatti si forma l’alchene più sostituito Deidroalogenazione Quando l’alogenuro alchilico è primario, viene normalmente usato tert-butossido di potassio in dimetil solfossido CH3(CH2)15CH2CH2Cl KOC(CH3)3 dimetil solfossido CH3(CH2)15CH (86%) CH2 Meccanismo di Deidroalogenazione degli Alogenuri Alchilici: Meccanismo E2: •Alogenuri alchilici 2°ingombrati e 3° danno buone • rese. •Effetti stereoelettronici: eliminazione anti •Segue la regola di Zaitsev: si forma in prevalenza l’alchene più stabile. Meccanismo E1: •Alogenuri alchilici 3° con basi deboli •Se la SN è competitiva (RX 1°), usare una base ingombrata. •Le basi ingombrate estraggono l’idrogeno meno ingombrato formando l’alchene meno sostituito. Il Meccanismo E2 è un processo bimolecolare concertato che avviene in un unico stadio con un singolo stato di transizione: rottura del legame C—H e contemporanea formazione del legame π
Scaricare