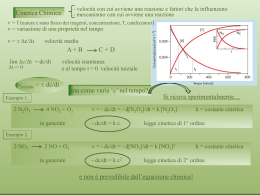
Prevalenza di reagenti Reazione reversibile 2 NO2 N2O4 Diretta N2O4 2 NO2 Inversa Equilibrio 2 NO2 N2O4 Stato di Equilibrio Equilibrio dinamico Equilibrio Prevalenza di prodotti aA+bB Le concentrazioni all’ equilibrio [M] sono costanti cC+dD [C]c [D]d Keq = [A]a [B]b Legge di azione di massa Costante di equilibrio ⇆ a A + b B + ... K c C + d D + ... aj = [J] / cj0 aj = Pj / Pj0 per un gas aj = 1 per un solido o un liquido c d [C ] [ D ] ... K a b [ A] [ B ] ... K c aC a aA c PC a PA d aD b aB d PD b PB ... ... ... ... 2 H2(g) + I2(g) ⇆ 2 HI(g) N2(g) + 3 H2(g) ⇆ 2 NH3(g) Kc Kd [ HI ] [ H2] [ I 2] [ NH 3 ] Kc è un numero 2 3 Kd in L2 / mol2 [ N 2] [ H 2 ] 3 2 NH3(g) ⇆ N2(g) + 3 H2(g) Ki [ N 2] [ H 2 ] [ NH 3 ] 2 Ki = 1 / Kd Ca(OH)2(s) ⇆ Ca2+ (aq) +2 OH- 2+ (aq) H2CO(aq) + H2O ⇆ H2C(OH)2(aq) - 2 K [Ca ] [OH ] [ H 2 C ( OH ) 2 ] K [ H 2 CO ] Kc [Ni(CO)4 ] Ni(s) + 4 CO(g) ⇆ Ni(CO)4(g) Kp [CO] 4 PNi (CO ) 4 4 CO P K > 1 equilibrio spostato verso destra ( prodotti) (a) K < 1 equilibrio spostato verso sinistra ( reagenti) (b) Quoziente di reazione , Q [Mc]c [Md]d Q= [Ma]a [Mb]b [M] = molarità in condizioni di non-equilibrio Tempo Q > Keq equilibrio si sposta verso i reagenti Q < Keq equilibrio si sposta verso i prodotti Q = Keq stato di equilibrio Specie 1 Specie 2 Specie 3 ... Composizione iniziale ... Variazione di composizione ... Composizione finale ... 2 NH3(g) ⇆ N2(g) + 3 H2(g) [ N 2 ][ H 2 ]3 x(3x)3 -10 K 2 • 10 [ NH 3 ]2 (0,2 2 x) 2 NH3 N2 H2 Composizione iniziale 0,2 0 Variazione di composizione -2x x 3x Composizione finale 0,2 - 2x x 3x x = 7,4•10-4 0
Scaricare