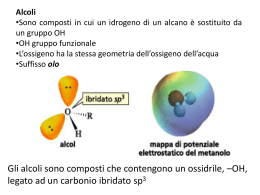
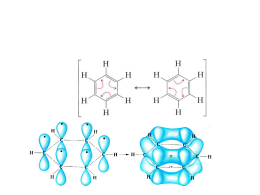
Proprietà dei SOSTITUENTI legati ad ANELLI ETEROCICLICI La reattività dei SOSTITUENTI può essere notevolmente influenzata dalla NATURA dell’eterociclo e dalla POSIZIONE nell’anello Influenza degli anelli eterociclici sulla reattività dei sostituenti N ≥ > Z N > N O > N > > S N R Sostituenti ALOGENI: vengono sostituiti più facilmente dai nucleofili -NH2: i sali di diazonio sono meno stabili (tranne che per gli N-ossidi) -CH3: più “attivo” (CH2- viene stabilizzato). Utile nelle applicazioni sintetiche -CH=CH2: l’addizione di Michael è più favorita Anelli benzenici fusi: minore -reazioni con elettrofili S (più aromatico è l’anello, maggiore è la probabilità che l’elettrofilo vada in α) N minore maggiore O N maggiore Anelli benzenici fusi: COOH -reazione di ossidazione N COOH COOH COOH N NO2 Anelli benzenici fusi: -effetto della sostituzione sull’anello benzenico N N NO2 HO N OMe N Alchil gruppi (reattività simile al toluene): -l’ossidazione con KMnO4, CrO3 dà i corrispondenti acidi carbossilici o chetoni -bromurazione radicalica con N-bromosuccinimmide: H3C H3C NBS N N Cl Cl O H3C O BrH2C R R NBS N H3C N BrH2C O R O R Ammino gruppi: -attacco da parte di elettrofili: Reazioni in competizione ad N eteroaromatico: H+, Met+, RX (facile e reversibile) ad NH2: RCOCl, HNO2, RNO, NO2+ ad β-C: Cl +, NO2+, SO3 (difficile e irreversibile) E+ E+ N E+ NH2 competizione fra l’azoto esociclico e quello endociclico nelle reazioni di metilazione e ossidazione Ammino gruppi: MeI RCO3H IN imped. sterico N Me Me N N Me Me N N O Me Me Me Me Me Me Me N N N Me Me O RCO3H MeI N Me N IMe N Me Me Me RCO3H MeI N Me N N N I- Me Me N N O Reattività in catena laterale di sostituenti adiacenti all’azoto piridinico (vedi gruppi adiacenti al carbonile): perdita di un protone Me N Y H O Y H -OH: sono acidi (confronta con gli acidi carbossilici) -NH2: sono meno basici (confronta con le ammidi) -alchili: sono “attivi” (confronta con gli alchil chetoni) Z Y H Tautomeria: N YH N H Y -OH: esiste per circa il 99% nella forma piridone (confronta con gli ac. carboss.) -NH2: esiste per circa lo 0.1% nella forma piridoimmina (confronta con le ammidi) -SH: esiste per circa il 99.9% nella forma piridotione (confronta con gli ac. tiocarboss.) Me O Me YH HO Y Decarbossilazione: Me O Me CH2 HO CH2 H N CH2 N H O N H C H2 O Carbossimetile: decarboss. a 50° C (confronta con β-chetoacidi) H O CH2 O H N H Carbossile: decarboss. a 200° C (confronta con α-chetoacidi) O Me Me O O O H O H Reazione di Michael: Vinil/Etinil-Py: subiscono R. di Michael (confronta con chetoni αβ-insaturi) NuN CH2 C H N N CH H2 C OH C H2 N H2 C Nu C H CH2 H Nu- β-idrossietil Py: subiscono reaz. opposta alla R. di Michael (confronta con β-idrossi chetoni)
Scaricare