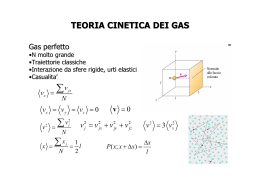
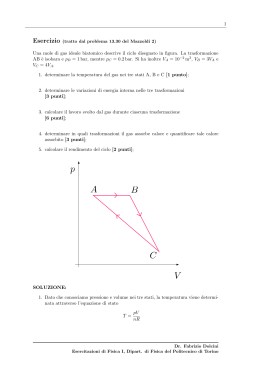
Fisica 1 B, AA 2004-05 II prova in itinere del 24-06-2005, ore 9.00, durata 2 ore Regole per p.i. e appelli (LEGGERE ATTENTAMENTE PRIMA DI COMINCIARE): 1) la prova è valida se affrontata individualmente; ogni tipo di comunicazione, verificata durante o dopo la prova, comporta l’invalidazione della stessa. L’avvistamento del telefonino comporta l’immediata espulsione. 2) la prova va affrontata senza alcun ausilio di libri di testo e/o appunti; sul banco devono trovare posto solo testo della prova ed i fogli forniti (uno solo da consegnare con le soluzioni e lo svolgimento), penna e calcolatrice numerica. 3) i dati necessari alla soluzione sono forniti nel testo della prova. 4) ogni esercizio è accreditato di un punteggio; la sufficienza è 18, mentre il punteggio totale è 36. 5) le p.i. possono sostituire un solo appello estivo; il risultato delle p.i. è automaticamente annullato quando si partecipa ad un appello regolare estivo. 6) il voto finale viene composto dal risultato delle prove scritte e dalla discussione dell’elaborato che (eventualmente) include domande di carattere teorico sul corso; la discussione è più approfondita nelle situazioni di limite per assestare la sufficienza o l’eccellenza, e nei casi di dubbia paternità della prova. 7) nella soluzione dei problemi, sempre fornire prima il procedimento ed il risultato simbolico e successivamente il risultato numerico; il testo va consegnato su un singolo foglio (quattro facciate) e deve essere scritto in forma leggibile; non verrà considerato nessun altro foglio incluso, così come le soluzioni che risultano ambigue a causa di disordine o scrittura poco leggibile del candidato. 8) il foglio che si desidera sia considerato al fine della valutazione deve riportare oltre al NOME e COGNOME anche il NUMERO DI MATRICOLA. 1) Tre moli di gas ideale monoatomico sono contenute in un recipiente di capacità termica trascurabile. Il sistema è successivamente posto in contatto con una sorgente termica alla temperatura di 70°C. Raggiunto il nuovo stato di equilibrio si osserva che la variazione di entropia della sorgente è 500 J/K. Calcolare la variazione di entropia del gas. (7 punti) 2) Un gas ideale biatomico, che si trova inizialmente alla pressione di 5 bar, compie una trasformazione isoterma che lo porta alla pressione di 2 bar. Successivamente subisce una trasformazione isocora e quindi una adiabatica tali da riportarlo allo stato iniziale. Disegnare il ciclo risultante nel piano P-V e valutarne il rendimento. (6 punti) 3) Due moli di gas perfetto, uno monoatomico, l’altro biatomico, inizialmente a pressione P0 = 2 atm e volume V0 sono compresse a metà del volume iniziale adiabaticamente e in modo reversibile. Calcolare le pressioni finali dei due gas. (5 punti) 4) Un serbatoio di volume V1 = 10 l è riempito con una mole di aria alla temperatura T1 = 283 K. Mediante una compressione isotermica il volume è portato a V2 = 2 l. Successivamente il gas viene fatto espandere adiabaticamente fino al volume di 20 l. Le trasformazioni sono tutte reversibili. Si consideri l’aria un gas perfetto biatomico. Calcolare a) la temperatura finale, b) il lavoro compiuto dal gas nelle due trasformazioni. (5 punti) 5) Un contenitore metallico (peso atomico = 56, Cv = 25J/mole K, m = 50 kg) si trova inizialmente alla temperatura T0 = -50 °C. 10 l di acqua a 20°C vengono versati al suo interno. Calcolare a) la temperatura finale di equilibrio sapendo che il calore latente dell’acqua è 3.33 105 J/kg e b) le variazioni di entropia del contenitore e dell’acqua. c) Se i coefficienti di dilatazione volumica dei componenti fossero tutti uguali, valutare se il sistema compie lavoro verso l’esterno. Supporre trascurabile lo scambio termico con l’aria. (7 punti) 6) Un serbatoio termico alla temperatura T0 = 500 K è posto in contatto con una massa di materiale di capacità termica C0 = 104 J/K alla temperatura T1= 400 K attraverso una sbarra di rame di sezione A = 10 cm2, lunghezza L = 50 cm e conducibilità termica K = 400 W/m K. a) Calcolare la potenza iniziale che fluisce lungo la sbarra. b) Calcolare il calore acquisito dalla massa fino al raggiungimento dell’equilibrio termodinamico del sistema. c) A partire dai valori ottenuti, stimare il tempo necessario per raggiungere l’equilibrio. (6 punti) Soluzioni II prova in itinere Fisica IB 24-06-05 Esercizio 1 TSorgente = 343.15 K Tigas = QSorgente ncV QSorgente = TSorgente ∆S Sorgente = 171.6 kJ TSorgente = −99.6 J / K ∆S gas = ncV ln Tigas + TSorgente = 4937 K Esercizio 2 γ = 1.4 p A = 5atm p B = 2atm; QSorgente = −Q gas = −ncV (TSorgente − Tigas ) T A = TB = T p nRTp A V = nRT ln A Q AB = L AB = nRT ln B = nRT ln pB nRTp B VA V γ −1 nRTp γ −1 p γ −1 5 B Q BC = ∆Eint BC = ncV (TC − TB ) = ncV A T − T = ncV T − 1 = n RT B − 1 p γ −1 VC nRTp A 2 A V B = VC γ −1 QCA = 0 Qh = Q AB Qc = −Q BC p 1 − B Q 5 pA η = 1− c = 1− Qh 2 p ln A pB p A B = 0.16 C V Esercizio 3 pi = 2atm; V f = Vi ; 2 piVi γ = p f V fγ = p f gas monoatomico γ = 1.67 1 2γ Viγ p f = 2 γ pi p f = 2 γ pi = 6.36 atm; gas biatomico γ = 1.40 p f = 2 γ pi = 5.28 atm Esercizio 4 V1 = 10 l ; V2 = 2 l ; V T1 = 283K ; T2V2γ −1 = T3V3γ −1 T3 = T2 2 V3 V3 = 20l ; γ −1 V = T1 2 V3 γ −1 = 113K V 5 5 Liso = nRT1 ln 2 = −3.78kJ ; Ladiab = − ∆Eint 23 = − n R(T3 − T2 ) = −n R (T3 − T1 ) = 3.5kJ 2 2 V1 Esercizio 5 T1 = 223.15K; Ta = 293.15K; Tfase = 273.15K; m = 50Kg; m a = 10Kg; c v = 25J/(moleK); Pm = 56g/mole; c a = 4186J/(Kg K); L = 3.33 ⋅ 10 5 J/Kg; ( ) Q a = Q a1 + Q a2 = ma c a T fase − Ta − ma L = −0.87 MJ − 3.3MJ = −4.17 MJ Qm = ( ) m cV T fase − T0 = 1.12 MJ Pm Qm > Q a1 quindi l' acqua arriva alla temperatura di transizione di fase, ma siccome Qm < Q a non si trasforma tutta in ghiaccio. La temperatura di equilibrio è Tfase . Detta x la frazione di acqua che si trasforma in ghiaccio e xm a la massa di ghiaccio formata si ha ( ma c a T fase ∆S m = ∆STOT ( ) ) m cV T fase − T0 = 0 − Ta − xma L + Pm T fase m = 4.5kJ / K cV ln Pm T0 = ∆S m + ∆S a = 0.52kJ / K ( ) ∆Vm = 3α Vm T fase − T1 = 3α Vm ∆Tm ( ) x= T fase ∆S a = ma ca ln Ta ( ) xma L − = −3.98kJ / K T fase ) ∆Va = 3α Va T fase − Ta = −3α Va ∆Ta ⇒ il sistema compie lavoro verso l' esterno se ∆V > 0 cioè ( m cV T fase − T0 Pm = 0.0837 ma L ma c a T fase − Ta + ∆V = 3α(Vm ∆Tm − Va ∆Ta ) V m > V a ∆ Ta ∆ Tm Esercizio 6 T0 = 500 K ; T1 = 400 K ; c0 = 104 J / K ; A = 10 cm 2 ; L = 50 cm; K = 400 W /( Km); dQ A Q = K (T0 − T1 ) = 80W Q = c0 (T0 − T1 ) = 10.4kJ t > t min = = 130s dt L (dQ dt )max
Scaricare