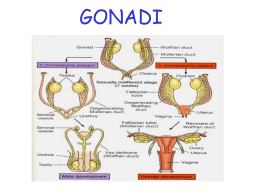
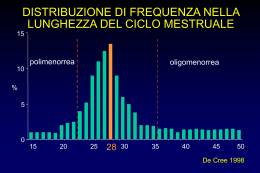
IRSUTISMO E IPERANDROGENISMO LA SINDROME DELL’OVAIO POLICISTICO Stefano Venturoli Clinica Ginecologica e Fisiopatologia della Riproduzione Umana Università di Bologna Alma Mater Studiorum La sindome dell’ovaio policistico rappresenta probabilmente il disordine endocrino più frequente nella popolazione femminile e’ la causa primaria di: IRREGOLARITA’ MESTRUALI ANOVULATORIETÀ STERILITA’ e SUBFERTILITA’ MANIFESTAZIONI ENDOCRINO/METABOLICHE DISAGI ESTETICI E DI IMMAGINE DEFINIZIONE La definizione stessa di “sindrome dell’ovaio policistico” è complessa, controversa: si discute ancora sui criteri e i parametri di riferimento per formulare la diagnosi. Tuttavia, “poiché essa è una sindrome”, si caratterizza per * un insieme di sintomi che si accompagnano alla * presenza di ovaia con struttura policistica. ANATOMIA DELL’OVAIO POLICISTICO • L’ovaio policistico è un ovaio che anatomicamente ed istologicamente si presenta come un ovaio: • • • • • aumentato di volume, con albuginea biancastra ed ispessita per fibrosi stromale, numerosi follicoli distribuiti alla periferia, in differente grado di sviluppo, maturazione ed atresia cellule della teca interna luteinizzate, ipertrofiche e iperplastiche. Al suo interno non si trovano segni di dominanza follicolare e di ovulazione (corpi lutei o albicanti) o comunque essi sono infrequenti (l’argomento è tuttora controverso), mentre è aumentato lo stroma ovarico , rispetto l’ovaio normale. STORICAMENTE: SINDROME DI STEIN- LEVENTHAL (*grosse ovaia policistiche, *irsutismo, *obesità, *oligoamenorrea e *sterilità anovulatoria) DESCRITTA PER LA PRIMA VOLTA NEL 1935 microcisti corticali (ovaio micropolicistico) REPERTI ECOGRAFICI DI PCO: ASRM/ESHRE Consensus Meeting, 2003 - n° > 12 follicoli tra 2-9 mm di diametro medio, a disposizione corticale e midollare - stroma ovarico abbondante e iperecogeno - dimensioni ovariche > norma (volume > 10 cm 3 ) (ovaio normale) (ovaio PCO) SINTOMI e SEGNI CLINICI CARATTERIZZANTI • I sintomi/segni clinici che caratterizzano la sindrome sono variabili e variabile è la loro presenza e la loro combinazione nelle donne: sono comunemente descritti come tipici e caratterizzanti, • 1) l’ oligomenorrea , l’ amenorrea, la polimenorrea • 2) una condizione di anovulatorietà o di pauci ovulatorietà, • 3) segni clinici di iperadrogenismo ( ipertricosi o franco irsutismo, seborrea , acne e alopecia, acantosi) • 4) Si possono associare l’aumento di peso, del grasso viscerale o l’obesità che, pur se stimati con grande approssimazione, sono presenti non più del 50% dei casi. PCOS: Diagnostic criteria revised (1990 2003) • 1990 criteria (both 1 and 2) – Chronic anovulation – Clinical and/or biochemical hyperandrogenism … and exclusion of other aethiologies • Revised 2003 criteria (2 out of 3) - Oligo- and/or anovulation - Clinical and/or biochemical signs of hyperandrogenism - Polycystic ovaries (US) … and exclusion of other aethiologies (CAH, androgensecreting tumors, Cushing’s syndrome, etc.) EZIOPATOGENESI DELLA SINDROME e sua importanza clinica • E’ un quadro patologico caratterizzato da un aumento di produzione ovarica di androgeni, che • a) esordisce alla pubertà, e • b) diviene eclatante nella età adolescenziale e nella piena fertilità. Comporta: 1) problemi clinici complessi (disturbo della ovulazione, alterazioni della fertilità, manifestazioni estetiche ed alterazioni metaboliche) 2) implicazioni sulla salute, differenti nelle differenti età della vita, dalla puberta’, attraverso l’età adulta e fino alla menopausa ( sindrome metabolica, vasculopatie, cardiopatie, tumore endometriale) PROBLEMI CLINICI COMPLESSI TRATTAMENTO DELLE PAZIENTI PCOS: OBIETTIVI Immediati A Breve Termine A Termine Risoluzione Correzione Prevenzione • sintomi • squilibri endocrini • squilibri metabolici • irregolarità del ciclo • anovulatorietà • sterilità • complicanze cardiache • complicanze vascolari • complicanze diabetiche e metaboliche • complicanze ginecologiche Acne, irsutismo, Alopecia, seborrea PCOS : EZIOPATOGENESI MULTIFATTORIALE: IPOTESI EZIOPATOGENETICHE • OVARICA • GnRH e LH • INSULINA E IGF-I • GENETICA • PERIFERICA • ALTRE EZIOPATOGENESI “OVARICA” • un danno primario intrinseco all’ovaio, verosimilmente collegato al citocromo P450 che ne regola i meccanismi steroidogenetici e che lo predispone ad una * maggiore produzione di androgeni (Androstendione e Testosterone), per lo più da parte dei piccoli follicoli e di quelli in via di divenire atresici, con un * deficit di aromatizzazione delle cellule della granulosa. IPOTESI OVARICA L’aumento degli androgeni intraovarici ( e quindi plasmatici) potrebbe essere (è comunque) la chiave di lettura del processo. L’ovaio, normalmente, ottimizza la sintesi di estrogeni ed androgeni in modo tale da proteggere il follicolo dall’eccesso androgenico. L’ovaio coordina la secrezione tecale LH-dipendente degli androgeni, con la secrezione estrogenica delle cellule della granulosa, FSH-dipendente. La steroidogenesi è sotto il controllo unitario del citocromo P 450 che nella PCOS è alterato e modula i FB ipotalamo/ipofisari Controllo della steroidogenesi GRANULOSA FSH Estradiolo TECA Testosterone Insulina LH Eccesso di Androgeni Diminuzione di Estrogeni Alterato Controllo dell’asse Ipotalamo/Ipofisario EZIOPATOGENESI “IPOTALAMICA” • una anomalia secretoria dell’ ipotalamo che in virtù di un * accelerato (picchi più ampi e frequenti) e *desincronizzato ritmo pulsatile circadiano (inversione del ritmo giorno-notte nella fase di rilascio dell’LH , maggiore nelle ore diurne) porta l’ipofisi a liberare quote superiori di LH, alterando il rapporto FSH/LH e attivando la steroidogenesi in senso androgenico IPOTESI dell’ALTERATO RILASCIO DI LH L’alterato rilascio di LH ipotalamico potrebbe essere una altra la chiave di lettura del processo che stimola gli androgeni e disturba l’ovlazione. L’ontogenesi della ipersecrezione di LH nella PCOS si realizza (verosimilmente) nel periodo pubero-adolescenziale. Elevati livelli di LH, l’aumento della frequenza ed ampiezza delle sue pulsazioni e l’alterato ritmo circadiano possono persistere nel tempo e cristallizzarsi. Resta ignoto perché e cosa determina la definitiva cristallizzazione dell’alterata secrezione di LH (o la sua risoluzione) SINDROME DELL’OVAIO POLICISTICO L’ipotalamo ha una congenita aumentata capacità di rilascio di GhRH incrementando la frequenza e l’ampiezza delle pulsazioni di LH e FSH VEDI IMMAGINE IN Regolazione della Funzione Gonadica La de-sincronizzazione del ritmo di rilascio circadiano (maggiore rilascio nelle ore diurne vs ore notturne) fra soggetti con PCOS e soggetti normali suggerisce un * intrinseco, primario danno al sistema di rilascio centrale del GnRH e delle gonadotropine EZIOPATOGENESI “INSULINEMICA” • un aumento della resistenza insulinica a carico dei muscoli e del tessuto adiposo, comporta un *aumento compensatorio di insulina circolante. • L’insulina in sinergia con l’LH contribuisce all’aumento della * stimolazione androgenica ovarica sia nelle donne grasse che nelle donne magre. TECA Testosterone Insulina LH EZIOPATOGENESI “INSULINEMICA” • • L’obesità ed in particolare l’aumento del grasso addominale, metabolicamente molto attivo, si collega con l’iperinsulinemia e l’iperandrogenemia. Il grasso addominale è in grado di dismettere in circolo acidi grassi liberi che favoriscono l’insulino-resistenza e l’instaurarsi del circolo vizioso insulina, androgeni e obesità centrale. IPOTESI DELL’INSULINA, INSULINALIKE GROWTH FACTOR (I) Pubertà: fisiologico incremento della resistenza insulinica (muscoli scheletrici e fegato) mediato dall’aumento puberale del GH iperinsulinemia compensatoria regola le concentrazioni di IGF-I Insulina e le IGF-I esercitano un effetto mitotico sulle cellule granulosa/teca e aumentano la steroidogenesi, potenziando l’effetto delle gonadotropine IPOTESI DELL’INSULINA, INSULINALIKE GROWTH FACTOR (II) L’Insulina e le IGF-I favoriscono anabolismo proteico, effetto mitotico sulle cellule della granulosa/teca , la steroidogenesi, potenziando l’effetto delle gonadotropine Alla riattivazione della secrezione pulsatile delle gonadotropine, tutti i fattori coinvolti determinano una iperstimolazione ovarica e della teca con eccesso produttivo di androgeni VEDI IMMAGINE in Regolazione della Funzione Gonadica Andamento dei livelli plasmatici di insulina in relazione all’età e variazione dello stato “naturale” di resistenza insulina dell’età puberale IPOTESI DELL’INSULINA, INSULINALIKE GROWTH FACTOR (III) Lo stato PCOS-like dopo la pubertà declina con il declinare della resistenza insulinica Solo in alcuni casi persiste, sia per il persistere della iperinsulinemia che si pone come fattore patogenetico persistente, sia per la associazione di altri fattori patogenetici IPOTESI GENETICA Le basi genetiche sono ancora sconosciute: la familiarità è evidente ma le modalità di trasmissione sono ancora ignote La PCOS è un disordine oligogenico nel quale 1) l’interazione di alcuni fattori genetici “The insuline receptor gene” o “The insuline gene variable number of tandem repeats (INS VNTR)” sembrano predisporre alla anovulatorietà e al diabete tipo 2 2) Ma anche la presenza di numerosi elementi comportamentali (alimentazione , principi nutrizionali alterati, attività fisica…) sembrano determinare i tipici ed eterogenei fenotipi clinici e biochimici della sindrome. IN SINTESI L’ovaio è predisposto ad una maggiore produzione di Androgeni che: - stimolano i recettori periferici per gli androgeni (unità pilosebacea) - modificano la pulsatilità dell’ipotalamo - stimolano la crescita della massa grassa ( addominale) - aumentano l’ atresia follicolare e quindi la anovulatorietà L’ipotalamo è predisposto ad una maggiore liberazione di LH che: - stimola la steroidogenesi androgenica e impedisce l’ovulazione L’ aumentata resistenza periferica e l’ Iper Insulinemia: - stimolano la produzione ovarica di androgeni (sinergicamente all’LH) e modificano la steroidogenesi da parte della massa grassa addominale (ghiandola periferica) - stimolano la crescita della massa grassa, la dislipidemia per lipogenesi SEGNI CLINICI DA MEMORIZZARE (Diagnosi) • • • • Struttura ovarica policistica Aumento volumetrico delle ovaia Irregolarità mestruali (oligo 60 % - poli 6% - amenorrea 30 %) Segni clinici di iperandrogenismo (irsutismo 30-60%, acne -seborrea 40-60 % , alopecia) • Sovrappeso o Obesità (40-50%) • Anovulatorietà o pauciovulatorietà • Sterilità (40-60 %) SEGNI LABORATORISTICI DA MEMORIZZARE (Diagnosi) • • • • • • Iperandrogenemia (A. T.) e SHBG ↓ Elevate concentrazioni di LH Aumentata frequenza ed ampiezza delle pulsazioni di LH De-sincronizzazione del ritmo circadiano ↑dell’ LH Elevato rapporto LH/FSH Iperinsulinemia –Insulinoresistenza (60-70 % PCOS obese. 20-30 % PCOS magre) • Disordini lipoproteici ( ↑LDL e TGL, ↓ HDL) PRINCIPI DI TERAPIA Poiché la sindrome: - ha un andamento cronico ed - è di fatto irreversibile, avviare una terapia prevede sempre * una precisa programmazione a breve , medio e lungo termine, * che tenga conto della età della paziente e del momento biologico che sta vivendo, ma anche * della fase evolutiva della patologia ( che frequentemente subisce fasi di riacutizzazione o di quiescenza) e in sintesi, che rispetti gli obiettivi complessivi della donna durante la sua vita. TRATTAMENTO DELLE PAZIENTI PCOS: OBIETTIVI Immediati A Breve Termine A Termine Risoluzione Correzione Prevenzione • sintomi • squilibri endocrini • squilibri metabolici • irregolarità del ciclo • anovulatorietà • sterilità • complicanze cardiache • complicanze vascolari • complicanze diabetiche e metaboliche • complicanze ginecologiche Acne, irsutismo, Alopecia, seborrea PRINCIPI DI TERAPIA: obiettivi immediati Acne, Irsutismo, Alopecia, Seborrea La terapia a breve prevede la soluzione dell’iperandrogenismo: l’obiettivo può essere raggiunto eliminando l’eccesso degli androgeni e impedendone l’azione sui recettori periferici. L’impiego degli antiandrogeni da soli (Flutamide, Finasteride) e delle associazioni EP con l’utilizzo di progestinici antiandrogenici (Ciproterone acetato, Drospirenone, Dienogest, Clormadinone) risolvono, per il periodo di assunzione dei farmaci, il problema dell’iperadrogenismo. PRINCIPI DI TERAPIA: obiettivi a medio termine squilibri metabolici, squilibri endocrini, irregolarità del ciclo, anovulatorietà, sterilità Un obiettivo di medio termine è rappresentato dal tentativo di correggere le condizioni dismetaboliche: l’uso dei correttori dell’iperinsulinismo (es. Metformina), e la normalizzazione dietetica, sono le armi terapeutiche oggi a disposizione il cui uso va correttamente programmato nel contesto degli interventi previsti. PRINCIPI DI TERAPIA: obiettivi a medio termine squilibri endocrini, squilibri metabolici, irregolarità del ciclo, anovulatorietà, sterilità • La definitiva correzione degli * squilibri endocrini e delle irregolarità del ciclo rappresentano ancora oggi un problema parzialmente irrisolto, mentre il * miglioramento della ovulazione o l’induzione della ovulazione con finalità del superamento della infertilità, sono facilmente perseguibili con il Clomifene, il Serofene o le Gonadotropine sintetiche o estrattive. • PRINCIPI DI TERAPIA: obiettivi a termine complicanze cardiache, complicanze vascolari, complicanze diabetiche Ancora tutta da impostare culturalmente e sperimentalmente è la strategia terapeutica a lungo termine finalizzata alla prevenzione dei danni diabetici e cardiocircolatori che prevedono sempre e comunque una impostazione corrette delle abitudini di vita e di quelle alimentari. • ERROR: undefined OFFENDING COMMAND: PCOS.ppt STACK: (Microsoft PowerPoint - 3) /Title () /Subject (D:20130423075034) /ModDate () /Keywords (PDFCreator Version 0.8.0) /Creator (D:20130423075034) /CreationDate (stefano.venturoli) /Author -mark-
Scaricare