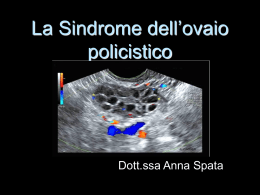
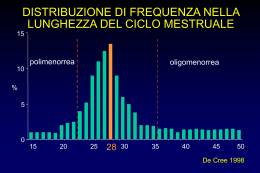
Dossier Infertilità La sindrome dell’ovaio policistico Giorgio Tresoldi SIMG, Milano La sindrome dell’ovaio policistico (polycystic ovary syndrome, PCOS) è uno dei più comuni disordini ormonali nelle donne, essendo presente nel 5-10% delle donne in età fertile 1. Attualmente la diagnosi di PCOS viene posta in base ai criteri proposti nel 2003 dal Rotterdam ESHRE (European Society of Human Reproduction and Embryology) /ASRM (American Society or Reproductive Medicine) PCOS Consensus Workshop Group che definisce come PCOS la presenza di almeno due dei seguenti criteri: • oligomenorrea e/o anovulazione; • segni clinici e/o biochimici di iperandrogenismo; • ecostruttura policistica dell’ovaio; in assenza di iperplasia surrenale congenita, sindrome di Cushing e tumori surrenalici o ovarici secernenti androgeni 2. Nel caso tali criteri non siano soddisfatti totalmente si può parlare di un quadro PCOS-like. La PCOS viene in questo modo definita come una patologia funzionale e non primariamente come un’alterazione anatomica dell’apparato genitale: l’ingrandimento delle ovaie e la loro presentazione cistica (cioè proprio ciò che indusse Stein e Leventhal a dare questo nome alla sindrome) non sono necessari per fare diagnosi di PCOS e per converso, la loro sola presenza non permette di fare diagnosi. Pur essendo caratterizzata da un’ampia eterogeneità di quadri clinici, nella pratica clinica quotidiana il medico di medicina generale (MMG) di solito viene interpellato dalla paziente affetta da PCOS per uno o più dei seguenti problemi: irregolarità mestruale, infertilità, segni di iperandrogenismo oppure sovrappeso/obesità. • Le irregolarità mestruali sono di solito associate ad anovulazione che è la causa della oligomenorrea (meno di nove cicli mestruali/anno; cicli di durata media superiore a 36-40 giorni). L’anovulazione può comparire anche prima che si instauri l’oligomenorrea e in circa il 30% dei casi l’anovulazione è accompagnata da amenorrea secondaria, che insorge dopo un periodo di oligomenorrea di durata variabile. • L’iperandrogenismo, le cui manifestazioni cliniche più caratteristiche sono irsutismo ed acne (anche se questa da sola non costituisce un elemento diaN. 6 • Dicembre 2009 gnostico). Frequente è il riscontro di seborrea e cute grassa mentre di solito non si riscontrano i segni di virilizzazione tipici delle forme di iperandrogenismo grave quali alopecia temporale, modificazione in senso maschile del timbro della voce e ipertrofia del clitoride. La valutazione biochimica dell’iperandrogenismo è legata ai livelli di testosterone totale e libero 3. • Ecostruttura policistica dell’ovaio: il solo riscontro ecografico di presenza di microcisti ovariche non è patognomonico della PCOS in quanto si può riscontrare anche in altre endocrinopatie, non caratterizzate da iperandrogenismo (esempio iperprolattinemia e amenorrea da stress). Secondo i criteri di Rotterdam sono definite policistiche le ovaie in “presenza di almeno un ovaio che mostri 12 o più follicoli con diametro medio 2-9 mm, a prescindere dalla loro disposizione, e/o un volume ovarico totale > 10 ml3, esaminate con sonda transvaginale” e la valutazione deve essere effettuata sia in scansione longitudinale sia trasversale 2. È sufficiente che una sola ovaia abbia questi caratteri, se valutata in fase follicolare e in assenza di utilizzo di terapia estroprogestinica. La distribuzione periferica dei follicoli e l’ipertrofia dello stroma ovarico possono essere presenti, ma non sono necessari per la diagnosi, in quanto la misura del volume ovarico si è dimostrata un indicatore sufficiente nella pratica clinica. Non è attendibile una valutazione ecografica per via soltanto transaddominale, soprattutto in donne che sono spesso in sovrappeso 4. I sintomi esordiscono solitamente in epoca puberale (attenzione a un pubarca precoce: è un campanello d’allarme perché indicatore di una precoce secrezione androgena), ma possono modificarsi spontaneamente nel tempo. Proprio ciò rappresenta il pericolo per noi medici: inseguire e trattare di volta in volta un segno (l’acne, le irregolarità mestruali, l’infertilità …) senza affrontare e risolvere il problema fondamentale. L’iperinsulinemia secondaria all’insulino resistenza e l’associata iperincrezione di androgeni con diminuzione della sex hormone-binding globulin (SHBG), costituiscono il momento centrale della patogenesi della PCOS. Rivista della Società Italiana di Medicina Generale Circa il 25-50% delle pazienti affette da PCOS sono sovrappeso/obese (body mass index, BMI > 25). Tuttavia nelle donne affette da PCOS l’iperinsulinismo non è presente solo nelle pazienti obese, (circa il 70-80% delle obese sono iperinsulinemiche), ma anche nel 30-40% delle pazienti magre o normopeso, forse per fattori eredo-costituzionali e familiari (genitori e/o nonni diabetici). L’obesità delle donne con PCOS è una obesità di tipo androide, caratterizzata cioè dal rapporto vita/fianchi WHR (waist-hip ratio) > 0,80, che è già di per sé causa di insulino-resistenza e di aumento della increzione di androgeni. Non a caso, infatti, il calo ponderale nelle pazienti PCOS obese è un mezzo efficace per ridurre gli androgeni, incrementare la sensibilità periferica all’insulina e in generale per migliorare il quadro ormonale 5. L’insulina induce iperandrogenismo stimolando le cellule della teca ovarica. Tuttavia, vari studi hanno evidenziato la possibilità che non tutte le donne con insulino-resistenza e iperinsulinismo sviluppino iperandrogenismo. Ciò supporta l’ipotesi che esistano due sottopopolazioni di pazienti PCOS, una con assente ipersensibilità ovarica all’insulina e una con marcata ipersensibilità ovarica all’insulina, quest’ultima caratterizzata da un’aumentata produzione ovarica di androgeni 6. Le conseguenze a lungo termine della PCOS vanno quindi ben al di là del solo apparato genitale e comprendono più elevati rischi di sviluppare patologie di tipo metabolico, cardiovascolare e neoplastico. Le donne con PCOS, infatti, possono andare incontro con maggiore frequenza a 7: • obesità con distribuzione del grasso di tipo androide; • IGT (ridotta tolleranza al glucosio) e diabete mellito di 2 tipo; • ipertensione arteriosa e disfunzione vascolare endoteliale; • dislipidemia mista con VLDL (very low density lipoprotein) e LDL (low density lipoprotein) elevate; HDL (high density lipoprotein) basse e trigliceridi elevati; • aterosclerosi delle coronarie e dei vasi periferici e cerebrali; • iperplasia e carcinoma dell’endometrio (vedi poi). Non è confermato l’aumento di rischio di tumore dell’ovaio e della mammella segnalato negli scorsi anni in pazienti affette da PCOS. È difficile in queste pazienti discriminare il rischio dovuto alla sola PCOS da quello dovuto all’obesità, all’anovulazione, all’infertilità e alle numerose terapie ormonali cui queste pazienti vengono sottoposte. Tutte le conseguenze metaboliche presenti nelle donne affette da PCOS sono simili a quelle dei pazienti affetti da sindrome metabolica, che è notoriamente una situazione clinica predisponente e predittiva di aterosclerosi, in particolare di malattia coronaria e cerebrovascolare 8. Valutazione clinico-diagnostica In ambulatorio, di fronte ad una paziente che lamenta irregolarità mestruale, infertilità, segni di iperandrogeniRivista della Società Italiana di Medicina Generale smo e spesso sovrappeso/obesità, il MMG dovrà porre diagnosi differenziale con tutti quei quadri che generino sintomi o segni simili a quelli della PCOS (Tab. I). TABELLA I. Diagnosi differenziale della PCOS. • Amenorrea delle sportive • Iperprolattinemia/prolattinoma • Ipotiroidismo primitivo • Tumori virilizzanti ovarici o surrenalici • Iperplasia surrenalica congenita ad esordio tardivo • Acromegalia • Sindrome di Cushing • Menopausa precoce • Obesità semplice • Condizioni correlate all’uso di farmaci (androgeni, acido valproico, ciclosporina, ecc.) Anamnesi: considerare lo sviluppo puberale, l’epoca del menarca, le caratteristiche del ciclo mestruale e in particolare il momento di inizio delle irregolarità mestruali e l’eventuale nascita prematura (forse correlata all’insorgenza di PCOS). Verificare la modalità d’esordio dei segni di iperandrogenismo e la loro evoluzione, poiché un esordio rapido (2-6 mesi) deve far sospettare la presenza di un tumore androgeno-secernente, mentre un andamento graduale con esordio nell’adolescenza è più tipico della PCOS. Rilevante è anche indagare sulla possibile assunzione di farmaci ad azione androgenica. L’esame obiettivo ha lo scopo di: • accertare e quantificare i segni di iperandrogenismo quali irsutismo, acne, seborrea ed eventuali segni di virilizzazione; • constatare la presenza di obesità valutando il BMI, la circonferenza addominale e la stima della distribuzione del grasso corporeo (ginoide o androide) tramite il calcolo del rapporto vita/fianchi (WHR); • verificare la presenza di ipertensione arteriosa, dei segni della sindrome di Cushing e l’acanthosis nigricans (espressione cutanea di iperinsulinismo). Le indagini di laboratorio 9 sono di ausilio per la diagnosi differenziale e per la valutazione del rischio di complicanze metaboliche. Il loro razionale è il seguente: 1. escludere una gravidanza con beta HCG; 2. confermare l’eccesso di androgeni mediante: testosterone, nella PCOS può essere normale, basso o aumentato; utile soprattutto per escludere tumori virilizzanti; testosterone libero, solitamente aumentato soprattutto nelle donne con PCOS; utile per stabilire la diagnosi e il monitoraggio delle terapie; didroepiandrosterone (DHEA), un suo valore molto Dossier Infertilità 31 Dossier Infertilità 32 3. 4. 5. 6. elevato dovrebbe suggerire la presenza di una virilizzazione di origine surrenalica; 17-OH-progesterone permette di escludere un deficit di 21-beta idrossilasi e quindi una forma ad esordio tardivo di iperplasia surrenale; cortisolo ematico e urinario 24 ore per escludere la s.di Cushing; LH, FSH e estradiolo permettono di escludere un ipogonadismo ipogonadotropo o una menopausa precoce; inoltre il loro rapporto (di solito elevato nella PCOS) è un ulteriore indicatore della presenza della patologia; TSH e prolattina per escludere patologie tiroidee ed ipofisarie. Per il controllo ormonale di base, si consiglia di procedere in questo modo: se la paziente mestrua, si eseguono 3 prelievi, il primo tra il 3° e 6° giorno del ciclo, il secondo tra il 16° e il 20° giorno del ciclo e il terzo prelievo tra il 26° e il 30° giorno del ciclo, qualora la donna mestruasse ogni 40-50 giorni. In caso di amenorrea, si eseguono due prelievi a random, a distanza di 15 giorni l’uno dall’altro. La diagnosi ormonale di PCOS è certa quando sono presenti i seguenti valori: LH > 10 mUI/ml ; LH/ FSH > 2,5; estradiolo (in fase follicolare) > 60 pg/ ml; androstenedione > 2,5 ng/ml; testosterone > 1 ng/ml, (in particolare aumenta la quota libera attiva per concomitante riduzione dei livelli di SHBG); 17-OHP > 2 ng/ml (di regola non supera gli 8 ng/ml. Se vengono superati si deve ipotizzare un deficit surrenalico) 10. 7. glicemia o test con carico orale di glucosio (OGTT). La American Diabetes Association riconosce la PCOS come fattore di rischio che giustifica lo screening per il diabete mellito 11. Non vi è accordo unanime sull’opportunità di uno screening per l’alterata tolleranza glucidica in tutte le donne con PCOS. Gli “Standard Italiani per la cura dl diabete mellito” suggeriscono l’OGTT 12; 8. l’insulina e le indagini che servono a documentare e quantificare l’insulino resistenza non sono considerate indagini di routine nelle pazienti con PCOS. Infatti la insulino resistenza nelle obese è sostanzialmente sempre presente e nelle non obese le indagini di laboratorio proposte (insulina a digiuno; OGTT; clamp euglicemico; rapporto glicemia/insulina o G/I ratio; HOMA test: insulina x glicemia/22,5; QUICKI index) non sono sempre precise o sono indaginose. Una curva da carico orale di glucosio (OGTT con 75 g di glucosio) permette di valutare l’andamento della glicemia e stima la secrezione di insulina. Nella pratica quotidiana è la soluzione più semplice, economica e redditizia per il tipo e la quantità di informazioni che permette di ottenere; 9. quadro lipidico come indicatore di rischio cardiovascolare; 10. la polisonnografia può essere utile se la paziente è obesa, russa e il rischio per apnee è aumentato. Approccio terapeutico Le scelte terapeutiche saranno in funzione del tipo e della entità dei disturbi per i quali la paziente si è rivolta a noi, delle priorità e delle attese di salute che la paziente ha in quel momento della sua vita e divergono drasticamente se la paziente desidera o meno una gravidanza. Nel caso vi sia desiderio di gravidanza, infatti, la terapia avrà come obiettivo principale la ricerca del concepimento e non potrà invece risolvere alcuni dei disturbi legati all’iperandrogenismo. Di questo la paziente va resa consapevole. Gli obiettivi dell’azione terapeutica sono: 1. ridurre gli androgeni circolanti e dei segni di androgenizzazione; 2. ridurre la resistenza all’insulina e prevenire le complicanze metaboliche a lungo termine e diminuire il rischio cardiovascolare; 3. cercare di raggiungere il peso ideale; 4. controllare la ciclicità mestruale e/o dei sanguinamenti disfunzionali e individuare la forma di contraccezione più adatta per ciascuna paziente; 5. correggere l’infertilità mediante induzione dell’ovulazione spontanea e/o migliorando la risposta alle terapie di induzione dell’ovulazione; 6. proteggere l’endometrio e prevenire il carcinoma dell’endometrio; 7. prevenire delle apnee notturne. A. Strategie non farmacologiche L’unica misura terapeutica che è proponibile in tutte le pazienti e che può avere effetti positivi su tutti gli aspetti della PCOS perché interviene sul meccanismo “patogenetico” della PCOS è la riduzione del peso corporeo mediante una dieta adeguata e un programma sistematico di esercizio fisico aerobico. Attività fisica e calo di peso hanno un significativo impatto non solo sul quadro metabolico, ma anche sulla funzione ovarica e sul ripristino della fertilità delle pazienti sovrappeso. Le donne obese infatti hanno una risposta peggiore alle terapie di induzione della ovulazione (clomifene citrato e gonadotropine esogene), e nelle tecniche di fecondazione assistita (fertilization in vitro embryo transfer, FIVET; intra cytoplasmic sperm injection, ICSI) hanno una minor percentuale di gravidanze e un’aumentata frequenza di aborti spontanei. Pur non essendovi chiare evidenze degli effetti della dieta e dell’esercizio fisico nelle donne con PCOS non obese, sembra prudente suggerire anche a loro di mantenere il peso entro i valori normali 13. Così come accade nei pazienti con sindrome metabolica, l’attività fisica aumenta la sensibilità all’insulina, riduce il peso corporeo, il grasso viscerale e sottocutaneo meglio Rivista della Società Italiana di Medicina Generale della dieta e ha effetti positivi su diversi fattori di rischio cardiovascolare purché sia regolare, sufficientemente intensa e prolungata nel tempo 14. Una passeggiata a passo rapido per 30-40 minuti almeno tre (meglio cinque) volte la settimana per le persone poco allenate; oppure – se si è allenati – un’ora tre volte a settimana di attività aerobica (nuoto, bicicletta, corsa) costituiscono un adeguato programma di attività fisica. B. Strategie farmacologiche B.1 Obiettivi terapeutici nelle pazienti che non cercano la gravidanza B.1.1 Ridurre l’iperandrogenismo Obiettivo primario, ma che implica una terapia a lunga scadenza (non inferiore a 12 mesi) e i cui segni possono ricomparire alla sospensione del trattamento. Possibili strategie per ridurre il livello di androgeni possono essere: • contraccettivi orali (CO). I risultati ottenuti con estroprogestinici (15-20 μg/cp di etenil-estradiolo, EE) sono del tutto paragonabili a quelli con elevato dosaggio 15, eccetto che nelle pazienti francamente obese, per le quali è opportuno usare un CO con 30 μg/cp di EE. Tra i progestinici abbinati all’EE il ciproterone acetato (CPA) ha un’azione antiandrogena potente in grado di bloccare il legame periferico degli androgeni con i loro recettori ed è pertanto efficace, in associazione con EE, per il trattamento dell’irsutismo, dell’acne/seborrea e dell’alopecia di natura ovarica o secondaria a lievi deficit enzimatici del surrene 16. Anche drospirenone e clormadinone Acetato sono risultati efficaci nel miglioramento dei segni dell’iperandrogenismo; • anti-androgeni: flutamide, finasteride e spironolattone sono composti sprovvisti del tutto o in parte di attività ormonale steroidea, in grado però di competere selettivamente con i siti recettoriali androgenici o di ridurre l’attività enzimatica intracellulare (5αreduttasi). Usati spesso per patologie prostatiche nel maschio, sono somministrati abitualmente abbinati con un contraccettivo estro-progestinico per il loro rischio teratogeno in caso di concepimento di un feto maschio. La paziente deve essere adeguatamente informata di questo e dare il suo consenso esplicito e scritto alla terapia. Flutamide, al dosaggio giornaliero di 250-500 mg per os viene prescritta in terapia continuativa per almeno 6-12 mesi riducendo la dose del 50% ad intervalli di 4 mesi se si riscontra una miglioramento della sintomatologia. I tempi di recidiva dei sintomi dopo sospensione, sono più prolungati rispetto ad altri farmaci. A causa della sua possibile tossicità epatica vanno effettuati controlli degli indici di funzionalità epatica già a partire da un mese dopo l’inizio del trattamento. La finasteride, che inibisce la produzione di DHT (deidroRivista della Società Italiana di Medicina Generale testosterone) bloccando l’attività dell’enzima 5alfareduttasi, può influenzare positivamente i segni di irsutismo ma non agisce sull’acne e la seborrea. Lo spironolattone (diuretico antagonista dell’aldosterone) inibisce la sintesi ovarica e surrenalica di androgeni, mediante competizione con il recettore per gli androgeni e inibendo direttamente l’attività enzimatica 5α-reduttasica. Induce una risposta clinica direttamente correlata al suo dosaggio e richiede un controllo periodico della potassiemia. Viene spesso utilizzato (50-200 mg/die x os) associato ai contraccettivi orali di cui limita l’azione sodio ritentiva e potenzia l’azione antiandrogena; • GnRh analoghi: sopprimono la secrezione ipofisaria di LH bloccando l’attività ovarica e determinando un quadro di marcato ipoestrogenismo, responsabile della comparsa di sintomi simil-menopausali. Per tale motivo sono utilizzati solo per brevi periodi (3-4 mesi) e nelle forme più severe di iperandrogenismo della PCOS ed è necessario che vengano associati ad un trattamento sostitutivo estro-progestinico che anzi conviene in genere iniziare prima e somministrare il GnRh (la cui assunzione va iniziata il 1° giorno della mestruazione) solo dopo 1-2 cicli di estro-progestinici; • la rimozione dei peli (meccanica, laser, ecc.) è spesso un necessario completamento delle terapie farmacologiche 17. B.1.2 Riequilibrare l’insulino-resistenza Primariamente con il calo ponderale, ma anche con farmaci che aumentano la sensibilità periferica all’insulina, detti perciò insulino-sensibilizzanti: metformina e i glitazonici e gli inositolofosfoglicani (IPG). Metformina e glitazonici attualmente hanno come unica indicazione autorizzata in Italia il diabete mellito tipo 2, pertanto la loro prescrizione nelle pazienti con PCOS è “off-label”. Gli IPG sono di fatto integratori. La metformina 18 è una biguanide utilizzata da molto tempo nella terapia del diabete di 2 tipo in pazienti sovrappeso. Agisce come insulino-sensibilizzante inibendo il rilascio epatico e l’assorbimento intestinale di glucosio e riducendo la gluconeogenesi. Viene usata a dosi variabili da 250 mg bis die nei casi lievi, sino ad arrivare ad 1 g x 3 die nei casi più severi. È controindicata in caso di insufficienza epatica o renale (la creatininemia deve essere < 1,3 mg/dl), scompenso cardiaco e in tutte quelle condizioni patologiche e non (alcool!!) che predispongono all’acidosi lattica. Raramente determina ipoglicemia e può essere somministrata anche a pazienti con insulinoresistenza non diabetici. Provoca spesso nausea, vomito, disgeusia e disturbi gastrointestinali, ma non sono mai stati riportati effetti collaterali gravi a parte l’acidosi lattica. Nelle pazienti affette da PCOS la somministrazione di metformina provoca una riduzione dei livelli serici di insulina, di testosterone libero e totale, e un rialzo di SHBG. La metformina Dossier Infertilità 33 Dossier Infertilità 34 contribuisce a ridurre alcuni fattori di rischio cardiovascolari (pressione arteriosa e colesterolo LDL) ed ha effetti anche sulla capacità riproduttiva favorendo, in terapie a breve-medio termine (3-6 mesi), l’ovulazione spontanea e la percentuale di gravidanze. Migliora inoltre la risposta alle terapie con farmaci induttori dell’ovulazione: nelle terapie con metformina e clomifene citrato infatti i tassi di ovulazione e di gravidanze sono più alti rispetto a quelle con clomifene citrato da solo. Il suo utilizzo in gravidanza è controverso. Potrebbe essere indicato per ridurre la percentuale di aborti spontanei e il rischio di diabete gestazionale nelle donne con PCOS, tuttavia – benché sia ritenuto sicuro (categoria B della Food and Drug Administration) – sono disponibili solo studi osservazionali di coorte di piccole dimensioni con risultati contrastanti sui possibili effetti del farmaco sul feto 19. È utilizzabile nella terapia di pazienti con PCOS sia obese sia normopeso. Nelle normopeso i maggiori risultati si ottengono quando sia presente anche iperandrogenismo e iperinsulinemia, quindi in quel gruppo di donne PCOS magre in cui l’ovaio presenta una maggior sensibilità e risposta ovarica all’insulina in termini di biosintesi androgenica 20. Nella paziente obesa la perdita di peso corporeo attraverso una dieta ipocalorica ipoglucidica è spesso efficace nel ripristinare la regolare ciclicità mestruale e/o l’ovulazione. Recentemente sono apparse in letteratura segnalazioni circa un suo effetto di riduzione del rischio di neoplasie (prevalentemente ormono-correlate) probabilmente in relazione al suo effetto su IGF-1 21. I glitazonici sono farmaci insulino-sensibilizzanti che sono agonisti dei recettori nucleari PPAR gamma (peroxisome proliferator activated receptor) presenti in molti tessuti, ma prevalentemente negli adipociti e nelle miocellule. Il pioglitazone e il rosiglitazone aumentano la ritenzione idrica e sono controindicati in presenza di insufficienza cardiaca. Negli USA sono entrambi approvati per l’uso nelle donne in PCOS con la raccomandazione di un monitoraggio intensivo della funzione epatica. Recenti osservazioni segnalano un aumentato rischio di fratture non tipicamente osteoporotiche (mani e piedi) nelle donne trattate con glitazoni 22. Esistono in commercio attualmente anche prodotti di associazione tra metformina e glitazoni. L’ipotesi della presenza di un difetto nel segnale di trasduzione dell’insulina ha fatto porre l’attenzione sulla funzione dei secondi messaggeri del segnale dell’insulina, quali gli IPG sui quali esistono per ora solo studi preliminari 23. B.1.3 Prevenire il carcinoma dell’endometrio L’associazione della PCOS con il carcinoma endometriale è stata osservata da tempo. La presenza di anovulazione cronica associata a livelli estrogenici premenopausali, comporta una condizione di iperestrogenismo relativo che, perdurando negli anni, può condurre a iperplasia endometriale ed aumentato rischio di carcinoma, condizione peraltro associata anche all’obesità e al diabete mellito. Per questo alcuni 24 raccomandano di indurre farmacologicamente un flusso pseudomestruale almeno ogni 3-4 mesi nelle donne con PCOS e oligomenorrea grave o amenorrea. L’assunzione di contraccettivi orali combinati sembra avere un effetto protettivo sull’iperplasia endometriale. B.2 Obiettivi terapeutici nella paziente che desidera una gravidanza B.2.1 Determinare un’efficace stimolazione follicolare e la successiva ovulazione mediante: • clomifene Citrato (CC): farmaco di prima scelta per indurre l’ovulazione nelle pazienti con anovulazione cronica ma con normale funzionalità ipofisaria. Agisce a livello ipotalamico inducendo un’aumentata sintesi e rilascio di FSH e LH. La ripetizione dello schema terapeutico in più cicli successivi aumenta la probabilità di successo, ma dopo 6 cicli a dosi piene senza ovulazione bisogna considerare il cambiamento della terapia; • gonadotropine esogene: terapia proponibile dopo fallimento con clomifene. Necessita di controlli ecografici seriati e adeguamento progressivo del dosaggio e si associa un aumentato rischio di sindrome da iperstimolazione ovarica (OHSS) con un maggior numero di gravidanze gemellari. Tale rischio viene ridotto dall’utilizzo di gonadotropine ricombinanti low-dose dimostratesi efficaci e sicure per ottenere un’ovulazione monofollicolare; • GnRh pulsatile: possibilità terapeutica teorica, ma scarsamente praticabile per il costo e le difficoltà tecniche. Nelle pazienti desiderose di gravidanza si dovrà cercare di ottenere un ripristino del peso corporeo ideale anche in considerazione dell’aumentato rischio di diabete e di malattie metaboliche in cui la donna potrebbe incorrere in caso di gravidanza e sarà possibile anche far precedere la ricerca del concepimento da un periodo di 3-6 mesi durante i quali si cerca di ridurre l’iperandrogenismo, secondo le indicazioni esposte più sopra. Nella gestione della paziente affetta da PCOS è possibile e a volte necessario attuare terapie complesse combinando molecole di vario tipo: per esempio nei casi di PCOS marcata è possibile associare metformina, flutamide e contraccettivi orali con drosperinone. Va però ribadito che il cambiamento dello stile di vita resta la misura terapeutica essenziale, soprattutto nelle pazienti soprappeso. Le pazienti tendono a sottostimare l’importanza dello stile di vita. Anche qui l’opera del MMG è essenziale: chiarire che non esistono terapie definitive; che le terapie farmacologiche dei vari segni della PCOS funzionano fin tanto si utilizzano; chiarire costi e benefici delle terapie antiandrogene ed estroprogestiniche, degli induttori dell’ovulazione e dei Rivista della Società Italiana di Medicina Generale SIMG - SOCIETÀ ITALIANA DI MEDICINA GENERALE Via Del Pignoncino 9/11, 50142 Firenze • Tel. 055 700027 • Fax 055 7130315 • [email protected] • www.simg.it La presente scheda di iscrizione deve essere rispedita alla SIMG, via Del Pignoncino 9/11, 50142 Firenze, in originale oppure anche via fax allo 055 7130315, unitamente al pagamento della quota associativa pari a Euro 125,00 da effettuarsi tramite: • versamento sul c/c postale n. 14768501 intestato a SIMG - Società Italiana di Medicina Generale, via Del Pignoncino 9/11, 50142 Firenze; • inviando assegno circolare Non Trasferibile intestato a SIMG - Società Italiana di Medicina Generale, via Del Pignoncino 9/11, 50142 Firenze; • bonifico bancario personale effettuato a favore del conto corrente bancario intestato a: SOCIETA’ ITALIANA MEDICINA GENERALE; presso: Banca Nazionale del Lavoro, Agenzia di Sesto Fiorentino. IBAN: IT13W0100538100000000001982; • con carta di credito inviando la relativa autorizzazione (v. allegato) completa di firma in originale; • con Rid richiedendo la modulistica alla segreteria SIMG. Il sottoscritto dott./prof. Cognome .................................................................................................... Nome ........................................................................................ Nato a ....................................................... prov.................. Il ............... / ............... / ............. residente a ................................................................................ Prov. ........................... Cap........................................... Via .............................................................................................................................................................. Tel. (casa) ....................................................................................................... Tel. (studio) ................................................................................................................. Fax .......................................................... Cellulare ............................................................ E-mail:.................................................................................................. Codice fiscale ....................................................................................................... Partita IVA............................................................................................................ Anno di laurea ............................................................... Università di ............................................................................................................................................... Specializzazioni: 1) ........................................................................ 2) ......................................................................... 3) .................................................................. Attività: ® MG ® Universitario ® Libero Professionista ® Specialista Lingue: ® Inglese ® Francese ® Tedesco ® Spagnolo ® ........................................................................................... Eventuale II indirizzo: (Studio/Abitazione/Indirizzo/fiscale) via ................................................................................................................................................................. Località .................................................................................................................................... Prov. ..................................... Cap ................................................... A conoscenza dello statuto SIMG In fede ............................................................................................................................... Data ....................................................................... Firma socio presentatore..................................................................................................... Autorizzazione Il sottoscritto ..................................................................................................................................................................................... Nato a ................................................................................................................................. il ......................................................... Residente a ...................................................................................................................................................................................... Via/piazza .............................................................................................................................................................. n. ..................... Documento di riconoscimento.................................................................................. n....................................................................... Rilasciato da: ....................................................................................................................... il ......................................................... Titolare carta di credito VISA n. .......................................................................................................................................................... Titolare carta di credito Mastercard n. ............................................................................................................................................... Scadenza:......................................................................................................................................................................................... Autorizza La SIMG Società Italiana di Medicina Generale a prelevare dalla carta di credito sopra descritta l’importo di: € ................................................ (................................................................................................................................................ ) .................................................... lì, ............................................................................................................................................... .............................................................................................. Firma e timbro SIMG DI SOCIETÀ ITALIANA MEDICINA GENERALE € 0,60 SIMG SOCIETÀ ITALIANA DI MEDICINA GENERALE Via Del Pignoncino 9/11, 50142 Firenze DOMANDA DI ISCRIZIONE Euro 125,00 quota per il 2010 SIMG - SOCIETÀ ITALIANA DI MEDICINA GENERALE Via Del Pignoncino 9/11, 50142 Firenze • Tel. 055 700027 • Fax 055 7130315 • [email protected] • www.simg.it Il sottoscritto dott./prof. ..................................................................................................................................................................................................................... Via ................................................................................................................................................................................................................... n. ............................ Cap .............................................. Città ........................................................................................................................................................... Prov......................... Tel. (casa) ...................................................................... Tel. (studio) ..................................................................... Fax ..................................................................... Cellulare ............................................................................................................... E-mail:................................................................................................................. Codice fiscale ....................................................................................................... Partita IVA............................................................................................................ chiede che gli venga inviata in abbonamento la Rivista di Politica Professionale della Medicina Generale - SIMG allego copia della ricevuta di versamento sul c/c postale n. 14768501 intestato a: SIMG - Società Italiana di Medicina Generale - per l’importo di € 25,82 Data ....................................................................... In fede ............................................................................................................................... La presente scheda deve essere spedita alla SIMG, via Del Pignoncino 9/11, 50142 Firenze in originale oppure anche via fax allo 055 7130315 Euro 125,00 quota per il 2010 SIMG DI SOCIETÀ ITALIANA MEDICINA GENERALE € 0,60 SIMG SOCIETÀ ITALIANA DI MEDICINA GENERALE Via Del Pignoncino 9/11, 50142 Firenze DOMANDA DI ABBONAMENTO sensibilizzanti all’insulina costituiscono compiti inderogabili per chi come il MMG ha (deve avere) una visione d’insieme della salute delle loro pazienti. Bibliografia 1 2 3 4 5 6 7 8 9 10 11 12 13 Ehrmann DA. Polycystic ovary syndrome. N Engl J Med 2005;352:1223-36. Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group. Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome. Fertil Steril 2004;81:19-25. Chang RJ. A practical approach to the diagnosis of polycystic ovary syndrome. Am J Obstet Gynecol 2004;191:713-7. Balen AH, Laven JS, Tan SL, Dewailly D. Ultrasound assessment of the polycystic ovary: international consensus definitions. Hum Reprod Update 2003;9:505-14. Franks S. Polycystic ovary syndrome. N Engl J Med 1995;333:853-61. Baillargeon JP, Nestler JE. Polycistic ovary syndrome: a syndrome of ovarian hypersensitivity to insulin? J Clin Endocrinol Metab 2006;91:22-4. Royal College of Obstetricians and Gynaecologists. Longterm consequences of polycystic ovary syndrome. London: RCOG 2003. National Institutes of Health. Third Report of the National Cholesterol Education Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III – ATPIII). Circulation 2002;106:3143-421. Richardson MR. Current Perspectives in Polycystic Ovary Sindrome. Am Fam Physician 2003;68:697-706. Santagni S, Rattighieri E, Lanzoni C, Ricchieri F, Ricchieri F, Chierchia E, et al. Gestione ambulatoriale della paziente con policistosi ovarica. Ginecorama 2009;1:27-9. American Diabetes Association. Screening for type 2 diabetes. Diabetes Care 2007;30(Suppl. 1):S4. AMD-SID-Diabete Italia. Standard Italiani per la cura del diabete mellito. Linee guida e raccomandazioni. Torino: Infomedica 2007. Salehi M, Bravo-Vera R, Sheikh A, Gouller A, Poretsky L. Pathogenesis of polycystic ovary syndrome: what is the role of obesity? Metabolism 2004;53:358-76. Rivista della Società Italiana di Medicina Generale 14 15 16 17 18 19 20 21 22 23 24 Ross R, Dagnone D, Jones PJ, Smith H, Paddags A, Hudson R, et al. Reduction in obesity related comormid condition after diet-induced weigth loss or exercise-induced weight loss in men. A randomized, controlled trial. Ann Intern Med 2000;133:92-103. Van der Vange N, Blankenstein MA, Kloosterboer HJ, Haspels A, Thijssen J. Effects of seven low-dose combined oral contraceptives on sex hormone binding globulin, corticosteroid binding total and free testosterone. Contraception 1999;41:345-52. Holdaway IM, Croxson MS, Ibbertson HK, Sheehan A, Knox B, France J. Cyproterone acetate as initial treatmentand mainteinance the rapy for hirsutism. Acta Endocrino Copenh 1985;109:522-9. ACOG Practice Bulletin. Polycystic ovary syndrome. Clinical management guidelines for obstetrician-gynecologists. Obstet Gynecol 2002;100:1389-402. Barbieri RL. Metformin for the treatment of polycystic ovary syndrome. Obstet Gynecol 2003;101:785-93. Lord JM, Flight IHK, Norman RJ. Insulin-sensitising drugs (metformin, troglitazone, rosiglitazone, pioglitazone, Dchiro-inositol) for polycystic ovary syndrome (Cochrane Review). In: The Cochrane Library, Issue 4. Chichester: John Wiley and Sons 2002. Genazzani AD, Lanzoni C, Ricchieri F, Baraldi E, Casarosa E, Jasonni MV. Metformin administration is more effective when non-obese patients with polycistic ovary sindrome show both hyperandrogenism and hyperinsulinemia. Gynecol Endocrinol 2007;23:146-52. Landman GW, Kleefstra N, van Hateren KJ, Groenier KH, Gans RO, Bilo HJ. Metformin associated with lower cancer mortality in type 2 diabetes (ZODIAC-16). Diabetes Care 2009 Nov 16 [Epub ahead of print]. Short R. Fracture risk, a class effect of glitazones. BMJ 2007;334:551. Papaleo E, Unfer V, Baillargeon JP, De Santis L, Fusi F, Brigante C, et al. Myo-inositol in patients with polycystic ovary syndrome: a novel method for ovulation induction. Gynecol Endocrinol 2007;23:700-3. Royal College of Obstetricians and Gynaecologists. Longterm consequences of polycystic ovary syndrome. London: RCOG 2003. Dossier Infertilità 35
Scaricare