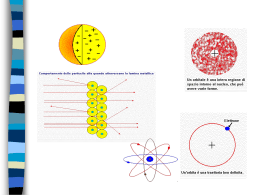
e blu verde e grigio rispettivamente Pz, Px e Py. Le energie di questi tre tipi di orbitale sono rappresentate dal seguente diagramma 2p 2s 1s E ORBITALI Quando un atomo di Carbonio si muove nello spazio, esso, se non è sottoposto a sollecitazioni energetiche di nessun tipo, si muove come un astronave nello spazio nella sua configurazione elettronica stabile 1s2 2s2 2p2 . Qui sono rappresentate le forma dei tre tipi di orbitale: Giallo 1S Viola 2s ELETTRONI Si ricorda che le frecce rappresentano gli elettroni che sono sugli orbitali. Ce ne sono due sul primo livello 1s, due sul secondo livello 2s ed uno ciascuno su due dei tre orbitali 2p. Si ricorda che la differenza di energia fra i tre tipi di orbitali è Rappresentata dalla distanza fra i livelli Sulla freccia E. I tre livelli 2p sono degeneri, cioè stanno alla stessa energia 2p 2s 1s Nel primo livello 1s e nel secondo 2s di elettroni ce ne sono 2 e stanno a spin invertito. Ciò sta a significare che quando due elettroni sono costretti a stare nello stesso livello energetico, essi ruotano in due sensi diversi: uno in senso antiorario ed un altro in senso orario e quindi sono accoppiati. Questo si può spiegare anche con la legge che dice che due elettroni devono possedere almeno un numero quantico diverso.(principio di esclusione). Da un punto di vista energetico, questo significa che un elettrone prima di andare ad un orbitale superiore occupa l’orbitale, seppur parzialmente occupato da un altro elettrone, che però si trova ad un livello energetico inferiore. Gli ultimi due elettroni che sono nel livello più alto, invece, potendosi disporre su uno qualsiasi dei tre livelli p (che sono alla stessa energia) si mettono dove meglio possono stare: uno in ogni orbitale. Infatti in questa maniera non si disturbano energeticamente.(principio della massima molteplicità). La rappresentazione testè fatta dell’atomo di carbonio spiega come tale atomo si bivalente. Questo è spiegato dal fatto che Nel primo livello 1s e nel secondo 2s di elettroni ce ne sono 2 e stanno a spin invertito. Ciò sta a significare che quando due elettroni sono costretti a stare nello stesso livello energetico, essi ruotano in due sensi diversi: uno in senso antiorario ed un altro in senso orario e quindi sono accoppiati. Questo si può spiegare anche con la legge che dice che due elettroni devono possedere almeno un numero quantico diverso.(principio di esclusione). Da un punto di vista energetico, questo significa che un elettrone prima di andare ad un orbitale superiore occupa l’orbitale seppur parzialmente occupato da un altro elettrone che però si trova ad un livello energetico inferiore. Gli ultimi due elettroni che sono nel livello più alto, invece, potendosi disporre su uno qualsiasi dei tre livelli p/che sono alla stessa energia) si mettono dove meglio possono stare: uno in ogni orbitale. Infatti in questa maniera non si disturbano energeticamente.(principio della massima molteplicità) 2P 2S 1S IL carbonio ha una configurazione elettronica: 1s2 2s2 2p2 . I 2 elettroni dei livelli 1s Sono troppo bassi di energia, e ciò si vede dalla distanza dal livello 2 s, per poter subire interferenze durante un avvicinamento con una altro atomo. Invece,gli elettroni dei livelli 2 s e 2 sono, fra di loro energeticamente vicini. (la distanza infatti è piccola).
Scaricare