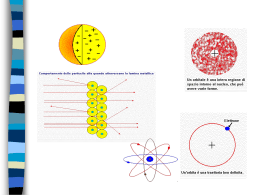
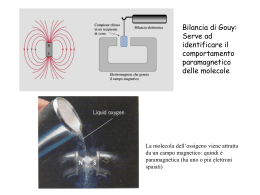
La struttura dell’atomo Modulo 3 U.D. 2 Chimica Prof. Augusto Festino Liceo Scientifico “G. Salvemini” A.S. 2005/06 La struttura dell’atomo La doppia natura della luce L’atomo di Bohr Il modello atomico a strati Equazione d’onda ed orbitali Numeri quantici Configurazione elettronica degli elementi Radiazione elettromagnetica onde e fenomeni ondulatori Equazioni matematiche e rappresentazioni grafiche che descrivono un fenomeno ondulatorio: una oscillazione periodica (nel tempo e nello spazio) di un parametro lunghezza d’onda (spazio o tempo tra due punti nella stessa fase, es. tra due creste frequenza (numero di oscillazioni complete nell’unità di tempo) no spostamento di materia sì spostamento di energia Onde acustiche si propagano per successive compressioni e decompressioni del mezzo (aria, acqua, metallo) particelle che si allontanano e si avvicinano tra loro onde elettromagnetiche Lunghezza d’onda luce, elettricità, magnetismo sono fenomeni ondulatori descritti da onde elettromagnetiche che si spostano senza sostegno di un mezzo tutte alla stessa velocità (3 108 m/sec = c) si differenziano per e per , inversamente proporzionali tra loro =c/ E = h (h= costante di Planck) energia portata da un quanto (“pacchetto” di energia di quantità finita) Fotoni di luce blu e rossa spettri di emissione degli elementi una luce che attraversa un prisma, si scompone in una serie di righe, una per ogni onda che la compone a ogni riga corrisponde una quantità definita di energia che dipende dalla sua frequenza un elemento eccitato -cui si fornisce energia- emette una luce costituita da un insieme didionde spettro emissione ogni elemento ha un suo caratteristico spettro di emissione”carta di identità” dell’elemento Un atomo eccitato di Litio emette un fotone di luce rossa per passare ad un livello più basso di energia Atomi di Idrogeno che ricevono energia da una sorgente esterna eccitandosi Gli atomi di idrogeno eccitati rilasciano energia emettendo fotoni Un atomo eccitato di idrogeno emettendo un fotone ritorna al suo stato stazionario Niels Bohr (1885-1962) e l’atomo di idrogeno Bohr misurò l’energia associata a ogni onda emessa da atomi di idrogeno (1 protone e 1 elettrone) eccitati ipotizzò che l’elettrone potesse assorbire solo quantità discrete di energia (quanti) con cui vincere l’attrazione del nucleo e allontanarsi da esso di una quantità legata all’energia assorbita, e quindi “ricadere” al suo posto, cedendo i quanti assorbiti la frequenza () dell’onda emessa dall’elettrone eccitato = differenza di energia tra le due”posizioni” o distanze dal nucleo alle quali può collocarsi (ΔE= h ) assorbendo e cedendo alternativamente l’energia atomo di Bohr gli elettroni si muovono su orbite stazionarie caratterizzate da livelli di energia definiti non sono possibili posizioni “intermedie” l’elettrone che si muove sul “suo” livello (quello più vicino possibile al nucleo) non perde energia e quindi non cade sul nucleo Energia ed elettroni energia Stato eccitato fornendo energia a un elettrone, questo assume uno stato eccitato e “salta” su di un livello energetico superiore e poi ricade al suo livello emettendo - sotto forma di luce l’energia che aveva assorbito Elettrone: onda o corpuscolo? 1924: Louis De Broglie se l’onda elettromagnetica si può comportare da particella (quanto , da cui dipende anche l’effetto fotoelettrico), la particella - elettrone- si può comportare come onda elettromagnetica (descritta dall’equazione di Schrödinger-1926) Energia associata con materia E=mc2 mc2= h onda E=h 1927: principio di indeterminazione di Heisenberg non si possono misurare contemporaneamente posizione e velocità dell’elettrone ma solo esprimere con una equazione la probabilità di trovare l’elettrone su di una porzione di spazio attorno al nucleo Dal modello atomico di Bohr si passa quindi al modello atomico corrente Rappresentazione fisica degli orbitali s e p Gli orbitali vengono rappresentati come porzioni di spazio nelle quali è massima la probabilità di trovare un elettrone orbitale s orbitale py orbitale px I 3 orbitali p orbitale pz Relative sizes of the spherical 1s, 2s, and 3s orbitals of hydrogen. The three 2p orbitals. The shapes and labels of the five 3d orbitals. Forma e nomi dei 7 orbitali f Numeri quantici la porzione di spazio dove è massima la probabilità di trovare un elettrone: ORBITALE ogni elettrone viene identificato da 4 numeri quantici in un atomo non possono esistere 2 elettroni con tutti e 4 i numeri quantici uguali principio di esclusione del Pauli (1925) n principale : da 1 a 7 (interi) = livello di energia dove si trova [dimensione dell’orbitale] sottolivello: per ogni valore di n : da 0 a (n - 1) [forma dell’orbitale] m magnetico: per ogni valore di : da - a + [numero di “direzioni” nello spazio dell’orbitale] spin ogni elettrone assume un valore :o -½ , o + ½ [verso di rotazione dell’elettrone sul proprio asse Numeri quantici e distribuzione elettronica n=1 =0 m= 0 -½ +½ -½ +½ =0 n=2 =1 =0 n=3 =1 =2 I livello energia, 1 orbitale s, 2 elettroni m= 0 --1 m= 0 +1 m= 0 --1 m= 0 +1 -2 -1 m= 0 +1 +2 -½ +½ -½ +½ -½ +½ II livello energia 1 orbitale s, 3 orbitali p 8 elettroni -½ +½ -½ +½ -½ +½ -½ +½ -½ +½ -½ +½ -½ +½ -½ +½ -½ +½ III livello energia 1 orbitale s, 3 orbitali p 5 orbitali d 18 elettroni Distribuzione elettronica: rappresentazione grafica Ogni orbitale viene rappresentato da un quadrato: s px,y,z Gli elettroni vengono indicati con frecce ↑↓ ↑ orbitale con un elettrone semioccupato Un elettrone da solo elettrone spaiato o singoletto ↑↓ orbitale con 2 elettroni completo 2 elettroni in un orbitale doppietto Principio di esclusione del Pauli in un orbitale 2 soli elettroni con spin opposto: (↑↓) Energia degli orbitali orbitali che si trovano allo stesso livello di Energia hanno diversa energia: • orbitale s : meno energetico ; viene sempre riempito per primo in ogni livello • 3 orbitali p hanno uguale energia massima distribuzione degli elettroni • 5 orbitali d : energia maggiore rispetto l’orbitale s del livello successivo che verrà quindi riempito prima ordine di distribuzione elettronica 4 d, 5 p,… 3 d, 4 p, 5 s 3 p, 4 s 5s 5p 5d 5f 2 p 3 s, 4s 4p 4d 4f 2s massima distribuzione = gli elettroni in un particolare livello tendono a distribuirsi su tutti gli orbitali dello stesso tipo 1s 3s 3p 2s 1s 2p 3d E 3d 3p 3s 2p 2s 1s Gli elettroni occupano sempre gli orbitali a più bassa energia ! Scrittura rapida della distribuzione elettronica numero arabo livello di energia lettera minuscola tipo di orbitale “esponente” numero di elettroni Livello energia 2p3 Numero elettroni orbitale Livello 2 di Energia 5 elettroni da distribuire ↑ ↑↓ 2s 2 ↑ 2p3 ↑ distribuzione elettronica II e III livello 2s 2 px 2 py 2 pz Elemento Li litio ↑ 3s 3 px 3 py 3 pz Na sodio ↑ Be berillio ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ ↑↓ Mg magnesio ↑↓ ↑ B boro ↑↓ C carbonio ↑ ↑ ↑ ↑ ↑ N azoto ↑↓ ↑ ↑ O ossigeno ↑↓ ↑↓ ↑↓ ↑ ↑↓ F fluoro Elemento ↑↓ ↑↓ ↑ Al alluminio ↑ ↑ ↑ ↑ ↑ P fosforo ↑↓ ↑ ↑ S zolfo ↑↓ ↑↓ ↑ Cl cloro Si silicio Regola dell’ottetto il livello più esterno -qualunque esso sia, escluso il I°non può ospitare più di 8 elettroni Gli elettroni periferici si distribuiscono tra l’orbitale s e i 3 orbitali p (esclusi H e He, livello 1: un orbitale s) un atomo tende a raggiungere la stabilità di un gas nobile ossia a mostrare un livello esterno completo gli atomi -dello stesso elemento o di elementi diversisi avvicinano ed attirano reciprocamente i rispettivi elettroni periferici per raggiungere l’ottetto la forza con cui un nucleo attira elettroni forza elettrostatica tra nuclei di atomi diversi e gli elettroni legame chimico elettronegatività Configurazione elettronica degli atomi distribuzioni elettroniche Metalli I e II gruppo K 1s22s22p63s23p64s1 Ca 1s22s22p63s23p64s2 Orbitali p semiliberi: gruppi III, IV, V, B 1s22s22p1 C N 1s22s22p2 1s22s22p3 Completamento doppietti orbitali p: gruppi VI, VII, gas nobili O 1s22s22p4 F 1s22s22p5 Ne 1s22s22p6 Elementi transizione riempimento orbitali d del livello precedente Sc 1s22s22p63s23p63d14s2 Ti 1s22s22p63s23p63d24s2 V 1s22s22p63s23p63d34s2 Cr 1s22s22p63s23p63d54s1 Gas nobili o inerti: ultimo livello completo 2s ↑↓ 2 px ↑↓ 2 py ↑↓ 2 pz Ne neon ↑↓ 3s ↑↓ 3 px 3 py 3 pz ↑↓ ↑↓ ↑↓ Ar argon Un caso particolare: elio 2 elettroni che completano l’unico orbitale -s- del primo livello 1s ↑↓ He elio ↑ H idrogeno Scrittura rapida tra parentesi quadra, la distribuzione fino al gas inerte del periodo precedente Mg 1s22s22p63s2 S 1s22s22p63s23p23p13p1 Ar 1s22s22p63s23p23p23p2 [Ne]3s2 o p [Ne]3s23p23p13p1 p ur 2 2 2 2 e [Ne]3s 3p 3p 3p
Scaricare