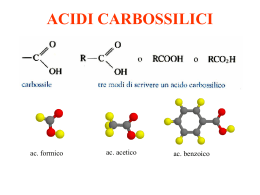
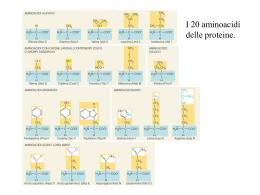
Derivati degli Acidi Carbossilici: Le Ammidi Classe IVa Liceo Scientifico Marta Franceschetti Derivati degli Acidi Carbossilici Alogenuro Acilico Anidride Estere Ammidi: l’ossidrile (-OH) è sostituito con un gruppo amminico (-NR2) Dove si trovano le Ammidi? Urea: prima molecola organica sintetizzata in laboratorio (diammide) Polimeri: - Sintetici - Proteine Isetticidi: Autan Antibiotici: Penicillina Ammidi: Nomenclatura Primarie Etanammide (Acetammide) Benzenammide (Benzammide) Cicliche Secondarie Terziarie Dietanammide (Diacetammide) Trietanammide (Triacetammide) Antibiotici: Penicilline e Cefalosporine 1928 Batteriologo A. Fleming: Nelle vicinanze della muffa Penicillium notatum lo stafilococco moriva Penicillina G La penicillina funge da substrato all’enzima Transpeptidasi durante la sintesi della parete batterica. L’enzima è inattivato, il batterio privo di parete muore. Cefalosporina C Interazioni elettrostatiche - Proprietà fisico-chimiche I punti di ebollizione e di fusione piuttosto elevati delle ammidi sono determinati dalla possibilità di instaurare legami idrogeno. Le ammidi a basso peso molecolare sono solubili in acqua. Via via che la catena si allunga, la solubilità in acqua diminuisce. Caratteristiche del legame ammidico: Formule di risonanza Le Ammidi sono meno basiche delle Ammine: il doppietto elettronico sull’azoto è infatti delocalizzato, quindi meno disponibile. Il legame ammidico ha un parziale carattere di doppio legame Blocco rotazionale lungo quel legame Il legame C-L si accorcia progressivamente all’aumentare del peso della risonanza tra i derivati degli acidi carbossilici Reattività: Sostituzione nucleofila acilica • Forte delocalizzazione del doppietto dell’N, riduzione della carica positiva a carico del carbonio carbonilico. • NR2 maggior basicità. • NR2 minor capacità come gruppo uscente. Reattività verso la sostituzione nucleofila acilica Grande stabilità delle Ammidi Ottenimento di un’Ammide Cloruro Acilico + Ammina Idrolisi dei derivati degli acidi carbossilici Ammide + Acido Cloridrico …infatti in natura non esistono cloruri aciclici Ammidi Inerzia Chimica Elevata presenza in natura Le molecole della vita: LE PROTEINE = Polimeri biologici di Aminoacidi Trasporto-Emoglobina Enzimi-Catalizzatori biologici Contrazione muscolare Protezione immunitaria-Anticorpi Struttura Che cosa è un POLIMERO? = Molecola di grandi dimensioni (macromolecola) 104<PM<107 Dalton - Costituito da unità più piccole (monomeri) - Unite da legami covalenti - Si ripetono un elevatissimo numero di volte - Ogni monomero ha almeno due gruppi funzionali Struttura: Origine: Omopolimeri: costituiti da un solo monomero Naturali: Polisaccaridi, Proteine, Quarzo… Eteropolimeri: due o più monomeri diversi Sintetici: Polivinilici, Poliuretani, Poliesteri, Poliammidi… Meccanismi di polimerizzazione: -Polimeri di condensazione: reazione tra monomeri avviene con eliminazione di piccole molecole (H2O, HCl, CH3OH) - Polimeri di addizione: successive addizioni di unità molecolari Che cosa è un AMINOACIDO? I due gruppi funzionali rendono l’Aminoacido sia Acido che Basico. Zwitterione: molecola neutra nel suo complesso, ma che possiede sia cariche negative che positive. I gruppi R possono essere Acidi, Basici, Neutri polari o non polari. Migrazione in un campo elettrico La migrazione si arresta in corrispondenza del Punto Isoelettrico = valore di pH per il quale un composto esiste sottoforma zwitterionica. Uno zwitterione non dà migrazione elettroforetica. Proteine e Aminoacidi possono essere separati in funzione del loro PI per elettroforesi su gel. a-Aminoacidi della serie L Formazione del Legame Peptidico = Legame Ammidico Rigidità del Legame Peptidico: Planarità La funzione della proteina è legata alla sua STRUTTURA Proteine: Struttura Primaria e reattività del gruppo R INSULINA Proteine: Struttura Secondaria Struttura Secondaria ad a-elica • • • • Legami idrogeno tra Aminoacidi della stessa catena NH e CO puntano in direzioni opposte paralleli all’asse dell’elica I gruppi R puntano verso l’esterno dell’elica Elica avvolta in senso orario, 3.6 aminoacidi ogni giro Struttura Secondaria ad b-foglietto • Guppi NH e CO di catene adiacenti puntano uno verso l’altro in modo che siano possibili Legami idrogeno tra Aminoacidi di catene polipeptidiche diverse che corrono antiparallele • I gruppi R sono alternativamente sopra e sotto i piani del foglietto Cheratina e Permanente 1. 2. Agenti riducenti rompono i legami S-S della cheratina dei capelli. Un’emulsione ossidante ripristina i ponti S-S, ma in posizioni differenti conferendo una diversa geometria al capello Struttura Terziaria Struttura Quaternaria Anemia Falciforme Acido Glutammico (aa acido) sostituito con Valina (aa neutro) Diverso avvolgimento della catena b Hb S Cambiamento nella struttura primaria si riflette nella perdita di forma e di funzione Precipitazione dell’Hb nel globulo rosso che assume forma “a falce” Denaturazione: la proteina perde la sua struttura tridimensionale quindi la sua funzione fisiologica Es: Denaturazione dell’Albumina nell’uovo La denaturazione delle proteine avviene al crescere della temperatura e in altre condizioni estreme, quali una forte variazione della concentrazione salina o in presenza di alte concentrazioni di alcune sostanze (dette denaturanti), quali l’urea, SDS (sodio dodecil-solfato). Polimeri sintetici: Poliammidi Nylon Famiglia di poliammidi sintetiche prodotte per condensazione Nylon 6,6 (1935 Du Pont USA) + Esametilendiammina Acido Adipico Caratteristiche Fibre Tessili • Legami idrogeno intra- e intermolecolari dati dalla presenza di gruppi NH e CO. • Regolarità delle catene. • Elasticità. • Resistenza all’abrasione. • Durezza. Fibre di Poliammide al microscopio Polimeri sintetici: Poliarammidi Kevlar • Grande resistenza alle trazioni e agli urti. 1,4 – fenilendiammina (diammina aromatica) Cloruro di tereftaloile (acido aromatico) • Vastamente utilizzato dalle corde degli alpinisti ai giubbotti antiproiettile Bibliografia • CHIMICA ORGANICA di Peter, Vollhardt Neil, Schore Ed. Zanichelli • CHIMICA di Dudley Herron, Kukla, DiSpezio, Schrader, Erickson, Cacciatore Ed. Le Monnier • IL SISTEMA CHIMICO di Tenca, Cozzi, Caratto Ed. Marietti Scuola • GENETICA di Russell P.J. EdiSES
Scaricare