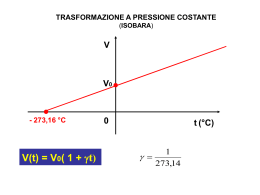
Laurea Triennale in SCIENZE MOTORIE corso integrato FISICA e STATISTICA disciplina : FISICA MEDICA STATO GASSOSO parte I - GAS PERFETTI - GAS REALI a GAS PERFETTI (volume proprio nullo) molecole puntiformi urti elastici (stesse particelle prima e dopo l'urto) prima parametri termodinamici : p, V, t (sistema termodinamico semplice) dopo prima prima urti non elastici (anelastici) dopo dopo 1 GAS PERFETTI LEGGI dei GAS PERFETTI legge di Boyle : t = costante pV= costante Ia legge di Gay-Lussac: p = costante Vt = Vo(1 + t) IIa legge di Gay-Lussac: V = costante pt = po(1 + t) 1 == 273° legge di Avogadro : gas 1 e gas 2 V1=V2 , p1= p2 , t1= t2 N1= N2 2 GAS PERFETTI condizioni iniziali po Vo 0°C dopo un'isoterma p' V 0°C dopo un'isocora (condizioni finali) p V t°C poVo = p' V p = p' (1 + t) pV = poVo (1+ t) equazione di stato dei gas perfetti 3 GAS PERFETTI legge di Avogadro : n = 1 mole u.m.a. po = 1 atm C 12 grammomolecola (mole) No = 6.02 1023 molecole 12.000 u.m.a. Vo (1 mole) = 22.41 litri NTP = condizioni normali di temperatura e pressione (1 atmosfera, 0°C) 4 GAS PERFETTI temperatura assoluta T = t (°C) + 273° V = Vo (1 + t ) 273° t = – 273°C V=0 t < – 273°C V < 0 non reale t = – 273°C limite in natura pV = poVo (1+ t) T 273° + t pV = poVo 273° 5 GAS PERFETTI poVo T= nRT pV = 273° n = n° moli R = costante dei gas perfetti n = 1 mole poVo 1 atm 22.4 = 0.082 atm = R= = 273° K mole 273 K mole 105 Pa 22.4 10–3 m3 = 8.325 J = 273 K mole K mole 6 GAS PERFETTI p = p1 + p2 + p3 + ... miscuglio di gas perfetti p1 = n1 V RT, p2 = n2 V RT, p3 = n3 V RT, ........... ntotale = n = n1 + n2 + n3 + ... legge di Dalton p = p1 + p2 + p3 + ... = = (n1 + n2 + n3 + ... ) V RT = n RT V 7 GAS REALI molecole occupano volume proprio v urti elastici e non elastici gas reale condensazione (fase liquida) solidificazione (fase solida) isoterme di un gas reale (p,V) T > Tc gas non può in alcun modo passare alla fase liquida (causa agitazione termica) Tc = temperatura critica 8 GAS REALI p isoterme di un gas reale Tc = temperatura critica gas pc T > Tc liquido vapore vapore saturo o Vc Tc T < Tc V 9 GAS REALI equazione di stato dei gas reali equazione di Van der Waals ai (V – bi ) ( p + 2 ) = R T V covolume – bi gas perfetto V n = 1 mole gas i-esimo gas reale V volume disponibile singola molecola = V – bi 10 GAS REALI ai termine di pressione aggiuntivo 2 V pressione urti elastici + urti non elastici pressione interna > pressione pareti (manometro) • forze intermolecolari attirano molecole periferiche verso l'interno pressione aggiuntiva n° molecole gas x n° molecole periferiche d x d = d2 V–2 11 GAS REALI gas reale gas perfetto quando : a) temperatura t >> Tc b) lontano dalle condizioni di condensazione (bassa pressione e grandi volumi) gas fisiologici e di impiego medico azoto ossigeno anidride carbonica acqua protossido d'azoto N2 O2 CO 2 H 2O N 2O Tc – 147.1°C – 118.8°C + 31.3°C +374.1°C + 39.5 °C 12 GAS REALI ARIA : N2, O2 gas perfetti a t = + 37°C CO2 gas perfetto a t = + 37°C (in aria presente in traccie ) H2O, N2O gas reali 13 GAS REALI N2O = gas anestetico in bombole ad alta pressione (fase liquida + fase vapore saturo) (atm) p 150 100 50 o O2 svuotamento bombola (t = 25°C) N 2O frazione di N 2O 3/4 1/2 1/4 0 frazione di O 2 14 I Gas • Def. gas perfetti: se le molecole sono puntiformi e gli urti sono elastici • Leggi dei gas perfetti: a t costante, pV=costante; a p costante, Vt=V0(1+ t); a V costante, pt=p0(1+ t); =1/273 • Equazione di stato dei gas perfetti: pV=nRT, dove p è la pressione, V è il volume, n è il n.ro di moli (1 mole=6.02x1023 molecole!), R è la costante dei gas perfetti e T è la temperatura assoluta (in Kelvin!) • Def. gas reali: se le molecole hanno un volume proprio e gli urti sono anche non elastici • Def. temperatura critica: temperatura al di sopra della quale il gas non può diventare liquido 15
Scaricare