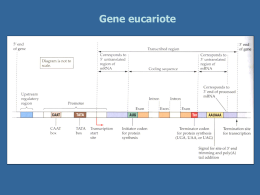
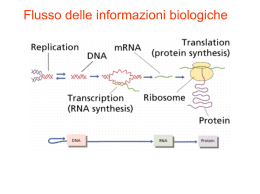
UNIVERSITÀ DEGLI STUDI DI TORINO CORSO DI LAUREA IN BIOTECNOLOGIE CURRICULUM AGRARIO TESI DI LAUREA DI I LIVELLO “Meccanismo e significato dell’ RNA interference (RNAi): principali applicazioni nelle piante” Relatore: Prof. Sergio Lanteri Correlatore: Dott. Alberto Acquadro Candidato: Davide Scaglione Anno accademico 2005/2006 Indice Introduzione e cenni storici……………………………………………………….3 Introduzione………………………………………………………………..............3 La scoperta dell’RNAi……………………………………………………………..4 Il silenziamento mediato da siRNA (small interfering RNAs)……...……...9 Un nuovo campo di ricerca………………………………………………...............9 Prime luci sul meccanismo………………………………………………...............9 Meccanismo base dell’RNAi mediato da siRNA………………………..………..10 Geni coinvolti nell’RNAi……………………………...………………………….11 RNAi in cellule di mammifero……………………………………………………14 Il ruolo dei microRNAs (miRNA) nello sviluppo delle piante…………….15 Cenni storici………………………………………………………...…................. 15 Biogenesi e traslocazione dei miRNA………………………………………….…15 Silenziamento mediato dai miRNA………………………………………….……17 Alla ricerca dei miRNA…………………………………...……………................18 I miRNA e lo sviluppo delle piante……………………...………………….…….19 L’RNAi nel nucleo……………………………...…………………………………21 Il mistero della metilazione…………………………………………...…………...21 Il nucleo: un “nuovo sito” di ricerca per l’RNAi…………………………...….….23 I processi nucleari mediati dall’RNAi………………………………………….….23 Metilazione del DNA diretta da RNA (RdDM)……………………………….…..24 La formazione e il controllo dell’eterocromatina……………………………….…26 Eliminazione di DNA………………………………………………………….…..28 Silenziamento meiotico…………………………………………………………....30 Osservazioni……………………………………………………………………….31 Silenziamento mediato da un singolo filamento…………...………………….32 Silenziamento mediato da filamento antisenso………………………….......……..32 Silenziamento mediato da filamento senso: la cosoppressione………………..…..32 Diffusione sistemica dell’RNAi e suoi repressori…………...………………..33 Un possibile “sistema immunitario”…………………………………………...…..33 I repressori virali: p19………………………………………………………….…..35 Altri repressori……………………………………………………………..………37 1 Ingegnerizzazione dell’RNAi…………………………………………………….38 Progettare i siRNA………………………………………………………..………..38 Molecole sintetiche……………………………………………………..…….....…39 Sistemi di espressione mediati da RNA polimerasi II…………………..…………40 Sistemi di espressione mediati da RNA polimerasi III…………………..………...40 ihpRNA…………………………………………………………………..………...42 Sovraespressione di Esportina-5…………………………………….….…...….....43 Tecniche di somministrazione e trasformazione in pianta………………….44 Metodi bio-balistici………………………………………………………………..44 Agroinfiltrazione…………………………………………………………………..44 Trasformazione stabile………………………………………………………….…45 VIGS (Virus-induced gene silencing)……..............................................................47 Applicazioni mediche…………………………….……………………………….49 Osservazioni……………………………………………………………………...…51 Casi di studio • Soppressione del gene DET1 attraverso RNA interference nel frutto di pomodoro aumenta il contenuto di carotenoidi e flavonoidi…………………………………………………….........….…...53 • Eredità non mendeliana di informazioni extra-genomiche in Arabidopsis……..........................................................................................60 Bibliografia………………………………………………………………………….68 2 Introduzione e cenni storici Introduzione La genetica inversa (“Reverse Genetics”) rappresenta la via preferenziale per lo studio della funzione biologica di una proteina e consiste nel produrre un genotipo mutante a livello di uno o più geni d’interesse, e nell’esaminarne il corrispondente fenotipo. Di solito, le mutazioni vengono indotte a seguito ricombinazione omologa (“Reverse Genetics”) o identificandole in popolazioni di mutanti (“Forward Genetics”). La scoperta di metodi specifici di silenziamento genico ha aumentato la potenzialità e l’efficienza dell’approccio ‘Reverse Genetics’. Inizialmente furono utilizzati frammenti di DNA o RNA antisenso per silenziare geni di interesse, permettendo di studiare gli effetti fenotipici e dedurre così la funzione biologica del gene. Queste tecniche però si dimostrarono non sempre così specifiche e talvolta poco efficienti. Recentemente è stato evidenziato un nuovo meccanismo di silenziamento genico naturale, mediato da RNA a doppio filamento. In diversi organismi è stato osservato che l’RNA a doppio filamento (dsRNA) è in grado di indurre silenziamento genico sequenza-specifico. Questo processo, chiamato RNA interference (RNAi) è ubiquitario negli animali e nelle piante ed è stato oggetto di intensi studi negli ultimi 10 anni. Molto è ormai noto sul meccanismo molecolare alla base dell’RNAi, tuttavia alcuni aspetti devono ancora essere chiariti e su questi si concentrerà la ricerca nei prossimi anni. Nel nematode Caenorhabditis elegans il silenziamento genico mediato da RNAi può essere indotto a seguito della sua semplice immersione in dsRNA o nutrendo lo stesso con ceppi di E. coli esprimenti specifici dsRNA: sono necessarie poche molecole di dsRNA per cellula per dare inizio ad un effettivo silenziamento genico. Si è notato, inoltre, che l’effetto di silenziamento indotto in C. elegans viene anche ereditato per diverse generazioni. Questo fenomeno ha generato un interesse enorme nella comunità scientifica, soprattutto perché può essere utilizzato per studiare le sequenze geniche accumulate nei database biologici fino ad oggi, alle quali sarebbe così possibile dare più facilmente un significato funzionale (Sugimoto et al., 2004). 3 La scoperta dell’RNAi La scoperta dell’RNAi avvenne nel tentativo di trovare nuovi metodi per studiare la funzione di determinati geni in C. elegans usando la tecnologia dell’“RNA antisenso”. Studiando la funzione del gene par-1, Guo & Kemphues (1995) iniettarono l’RNA antisenso del gene stesso nel nematode. Questo gene codifica per una serina-tirosina kinasi, implicata nell’asimmetria di divisione cellulare (la prima divisione) a livello embrionale, generando cellule figlie diverse per dimensioni, componenti citoplasmatiche e destino di differenziazione. Questo esperimento, come atteso, determinò un fenotipo letale. Effettuando però il controllo con l’iniezione del RNA senso, si ebbe sbalorditivamente lo stesso effetto. A quel tempo, però, a causa delle limitate conoscenze, questo risultato fu attribuito ad un’ipotetica saturazione dei fattori necessari alla traduzione di par-1. Già prima dei risultati di Guo and Kempheus (1995), fenomeni analoghi, che in futuro si sarebbero dimostrati collegati con l’RNAi, erano stati osservati, ma erano rimasti senza spiegazione. Nel 1995, il gruppo di ricerca di Jorgensen, nel tentativo di aumentare l’attività del gene della calcone sintasi (un enzima coinvolto nella produzione di specifici pigmenti), introdusse dei transgeni in petunia. Inaspettatamente la pigmentazione non aumentò, anzi si ebbe una variegazione del colore e, in alcuni casi, la totale perdita di colore. Questo fenomeno fu definito “co-soppressione”, intendendo la soppressione sia del gene introdotto, sia quello endogeno. In seguito, la “co-soppressione” venne ricondotta al PTGS (post trascriptional gene silencing) poiché, in tutti i casi, il fenomeno era il risultato di una degradazione dell’RNA trascritto. Inoltre, questa degradazione posttrascrizionale era osservata anche per transgeni espressi da piante, batteri o sequenze virali. Mentre si parlava di PTGS in piante, un fenomeno molto simile denominato “quelling” (repressione) era già stato osservato nei funghi (Pandit and Russo, 1992; Romano and Macino, 1992). Nel 1996, Cogoni et al., nel tentativo di incrementare la produzione di un pigmento arancione trasformarono una coltura di Neurospora crassa con un plasmide contenente un segmento del gene al1 ottenendo come risultato fenotipi albini. Questi risultati confermarono le precedenti osservazioni sul silenziamento genico indotto da transgeni, e dimostrarono che il fenomeno della metilazione del DNA non era obbligatorio per la sua induzione. 4 Nel 1998 Fire et al. catalogarono questi fenomeni isolati sotto un principio comune: l’RNA interference (RNAi). Sempre lavorando su C. elegans, essi focalizzarono i loro studi sul gene unc22 (responsabile della produzione di una proteina del miofilamento), il cui trascritto è presente in centinaia di copie nelle cellule dei muscoli striati. Una diminuita attività del gene generava fenotipi con limitata coordinazione motoria, mentre una totale perdita di funzionalità dello stesso si mostrava in muscoli strutturalmente difettosi, compromettendone la motilità. I risultati indicarono che l’introduzione di una soluzione contenente filamenti di RNA senso ed antisenso era almeno dieci volte più efficace del solo utilizzo dei singoli filamenti. Analisi elettroforetiche mostrarono che, all’interno dell’organismo, il materiale iniettato si conformava per la maggior parte come doppio filamento (dsRNA). Di contro, osservarono che un tempo prolungato tra l’iniezione del filamento senso e di quello antisenso dava un drastico calo di efficienza, fino alla totale assenza di effetto (Tab. 1). Questo fenomeno venne spiegato con il fatto che l’ssRNA (single strand RNA) viene rapidamente degradato nel citoplasma e che, presumibilmente, è necessaria la struttura a doppio filamento per il riconoscimento da parte di un eventuale meccanismo cellulare. Anche la presenza dei due tratti in cis su di un singolo filamento diede risposta nulla. Sorprendentemente, gli effetti di questa interferenza genica si mostravano sia nei soggetti iniettati che nelle loro progenie: nonostante nelle prime cellule embrionali gli mRNA, per effetto dei processi di differenziazione, fossero velocemente degradati. Verosimilmente, pochissime erano le molecole di dsRNA sufficienti a generare l’interferenza; i valori saggiati non sarebbero stati sufficienti se il fenomeno dell’RNAi fosse stato di tipo stechiometrico (tra dsRNA ed mRNA). Questa considerazione suggerì l’esistenza di una componente catalitica o di un evento di amplificazione che rendesse possibile l’RNAi partendo da basse concentrazioni di dsRNA. Gli stessi risultati si ottennero ripetendo l’approccio su altre proteine quali fem-1, hlh-1 e unc-54. Figura 1: Stadi di sviluppo embrionale di Caenorhabditis elegans; il nematode è uno dei principali modelli per lo studio della regolazione genetica durante gli stadi di differenziazione tissutale. 5 Tabella 1: Preparazioni di RNA iniettate in C. elegans ermafroditi. 6÷10 esemplari per prova. 0,5 ·106 ÷ 1 ·106 molecole per iniezione nelle gonadi. Dopo 4 ÷ 6 ore (per evitare di prendere uova già fertilizzate prima dell’inoculo) si è iniziato a saggiare le nuove uova prodotte ad intervalli di 12 e 24 ore. Per esaminare gli effetti dell’interferenza di dsRNA a livello cellulare gli autori usarono linee transgeniche esprimenti due differenti “green fluorescent proteins” (gfp) nei muscoli e, in altri casi, attraverso ibridazioni in situ. L’iniezione di dsRNA specifica per la gfp generò una marcata riduzione della frazione fluorescente delle cellule (Fig.2). Tre importanti conclusioni vennero tratte dal lavoro di Fire et al.(1998): 1. il dsRNA complementare a sequenze promoter o introniche non produceva un’interferenza rilevabile; 2. l’iniezione di dsRNA produceva la diminuzione o la totale eliminazione dell’mRNA endogeno; per dimostrare ciò venne usato come trascritto bersaglio mex-3, abbondante nelle gonadi e nei primi stadi embrionali, nei quali è facile eseguire ibridazioni in situ. Nei soggetti iniettati con dsRNA derivato da mex-3 non venne rilevato mRNA mex-3. Mentre individui iniettati con solo antisenso purificato di mex-3 mantennero comunque alti livelli di mRNA dello stesso (Fig.3); 6 3. l’interferenza mediata da dsRNA riesce ad attraversare le barriere cellulari. Infatti, l’iniezione di dsRNA (per unc-22, LacZ o gfp ) nelle cavità della testa o della coda produssero una specifica e consistente interferenza anche nella progenie, diffondendo quindi fino agli organi riproduttivi. Si è recentemente attribuita alla diffusione di questa interferenza il ruolo del gene SID-1, probabile trasportatore intercellulare di sequenze iniziatrici dell’RNAi. Figura 2: Analisi dell’RNA interference in tessuto e singole cellule. Progenie ottenuta da genitori iniettati con ds-RNA. a,d,g: giovane larva; b,e,h: adulto; c,f,i: parete cellulare di adulto ingrandita. In ogni prova l’esemplare è stato trasformato con i costrutti presenti in Figura 2bis. Nella prima colonna è mostrata l’iniezione di controllo di ds-unc22A, la quale non dà riduzione dell’attività fluorescente sia a livello nucleare che mitocondriale, in quanto non va ad agire su nessuno dei costrutti espressi. Nella seconda colonna (d,e,f) si evidenzia come l’iniezione di dsgfpG risulti in un notevole riduzione della fluorescenza: solo due cellule esprimono sia a livello nucleare che mitocondriale la gfp. L’iniezione di ds-lacZL, in terza colonna (g,h,i), risulta in un’interferenza solo a livello nucleare sulla GFP-LacZ, mentre a livello mitocondriale la GFPLacZ continua ad essere espressa. Le barrette orizzontali indicano la lunghezza di 20µm. Figura 2bis: Il costrutto nucleare viene silenziato sia da ds-gfp che da ds-lacZ. IL costrutto mitocondriale viene invece solo silenziato da ds-gfp (vedi Figura 2). 7 Figura 3: Effetto dell’interferenza dell’RNA di mex-3 sull’mRNA endogeno di embrioni di C. elegans. Ibridazione in situ con sonda specifica per l’mRNA di mex-3. a: Controllo negativo con assenza di sonda b:Embrione di genitori non iniettati (pattern di espressione di mex-3 normale). c:Embrione di genitori iniettati con RNA antisenso; la presenza di mRNA rispetto al fenotipo wild-type è calata ma resta comunque elevata. d: Embrioni di genitori iniettati con ds-RNA di mex-3B; mRNA di mex-3B assente nell’embrione. Questo esperimento fu il primo nel suo genere e gettò le basi per la messa a punto di metodi di silenziamento genico specifici attraverso l’applicazione di dsRNA esogeno, applicabile ed espandibile a tutti gli organismi. Studi successivi (Baulcombe et al., 1999; Zamore et al., 2000) spiegarono il meccanismo base dell’RNA interference; questo avvenne con saggi su lisati delle cellule embrionali allo stadio S2 di Drosophila. In altri esperimenti si pose l’attenzione su RNAs di ~25 nucleotidi presenti solo in piante soggette a co-soppressione ed assenti nelle piante in cui non si presentava il fenomeno del silenziamento; da questi emerse che l’mRNA endogeno veniva tagliato nella regione complementare al dsRNA e il taglio era effettuato in un intervallo di 21-23 nucleotidi. Molto presto, attraverso approcci genetici e molecolari, divenne chiaro il meccanismo dell’RNAi. Si chiarirono così le basi su di un meccanismo che da subito si capì essere un potentissimo strumento ai fini della ricerca di base, ed una possibile alternativa a strategie terapeutiche per malattie (come HIV e cancro) per le quali fino ad ora non si è trovato un rimedio generale e mirato. Nel prossimo paragrafo verranno discussi in dettaglio i meccanismi che stanno alla base di questo fenomeno. 8 Il silenziamento mediato da siRNA (small interfering RNAs) Un nuovo campo di ricerca La scoperta dell’RNAi come potente e facile metodo di silenziamento genico destò repentinamente l’attenzione dell’intera comunità scientifica. I risultati dei primi esperimenti, citati nel paragrafo precedente, promossero la realizzazione di moltissimi altri lavori di ricerca. L’ubiquità del fenomeno permise infatti il suo studio su molte specie. Molti esperimenti, infatti, si basavano sulla semplice immersione in dsRNA o attraverso alimentazione con batteri esprimenti dsRNA. Lo screening genico era quindi molto facilitato e permise la rapida identificazione di geni coinvolti nell’RNAi in C. elegans e il ritrovamento di loro omologhi in Drosophila, piante e funghi dimostrò che i fenomeni, che prima venivano etichettati come PTGS (post-trascriptional gene silencing), quelling e co-soppressione erano tutti parte di un unico processo le cui radici affondano in un unico meccanismo ancestrale. Inoltre, organismi precedentemente poco studiati per la loro complessità genetica, poterono diventare fonte di informazioni per la comunità scientifica. Prime luci sul meccanismo Nelle piante in cui si osservava il fenomeno dell’RNAi si trovavano piccole sequenze di RNA chiamate “small interfering RNAs”: siRNA. Si è scoperto che a generare questi siRNA era un enzima ribonucleasico della superfamiglia delle RNAsi III, chiamato Dicer. Studi su C. elegans hanno fatto emergere l’esistenza di geni strettamente coinvolti nel meccanismo dell’RNAi (Mello et al., 2000): rde-1 e rde-4 (rde sta per “RNAi deficient”), indispensabili per generare gli elementi responsabili dell’interferenza, ma non utili al protrarsi della stessa; rde-2 e mut-7 sembrano invece implicati nella seconda fase del processo. I primi geni si sono anche mostrati coinvolti nell’ereditarietà del fenomeno; in Dicer si è osservata infatti un’altissima similarità con rde-1. 9 Meccanismo base dell’RNAi mediato da siRNA Il modello funzionale dell’RNAi consta di due fasi fondamentali: quella di “iniziazione” e quella “effettrice”. Nella fase iniziale, i dsRNA immessi nella cellula (in maniera diretta, attraverso transgene o virus) vengono “digeriti” in corte molecole di dsRNA chiamate siRNA (small interfering RNAs), lunghe da 21 a 23 paia di basi. Dati sperimentali provano che i siRNA vengono prodotti dall’enzima Dicer (una ribonucleasi bidentata), un membro della super famiglia delle RNAsi III, (dsRNAspecifiche ribonucleasi), il quale taglia i dsRNA attraverso una reazione ATPdipendente. Successive rielaborazioni degradano i siRNA a duplex di 19-21 bp con un prolungamento di due nucleotidi al 3’. Nella fase effettrice, i duplex siRNA si legano ad un complesso nucleasico e formano quello che viene chiamato “RNA-induced silencing complex”: RISC. Dopo tale legame, i siRNA vanno incontro ad una denaturazione a singolo filamento (reazione ATP-dipendente), necessaria per l’attivazione del complesso RISC. Inoltre, è necessaria una fosforilazione al 5’ del siRNA duplex perché esso possa incorporarsi in RISC (Nykanen et al., 2001); questa modificazione viene svolta da una chinasi endogena (Schwarz et al., 2002). Il complesso così attivato, usando come stampo il singolo filamento incorporato, va a tagliare filamenti di mRNA complementari allo stesso (Fig.4). Il taglio avviene a circa 12 nucleotidi dal 3’ del siRNA antisenso. Analisi biochimiche (Hutvagner et al., 2002) indicano che l’RNAsi presente nel complesso RISC è diversa da Dicer. Nei paragrafi successivi verranno meglio chiarite le caratteristiche e le differenze dei processi di RNAi a seconda che essi siano mediati da siRNA, miRNA, shRNA e le loro diverse potenzialità. Figura 4: esemplificazione schematica del meccanismo dell’RNAi mediato da siRNA. 10 Geni coinvolti nell’RNAi Gli “iniziatori” Due geni di C. elegans, rde-1 e rde-4 si presuppongono coinvolti nella fase iniziale dell’RNAi. Il gene rde-1 è membro di una grande famiglia di geni ed è omologo a qde2 in Neurospora crassa (qde sta per “quelling deficient”) e ad AGO1 di Arabidopsis thaliana (AGO sta per ARGONAUTE; AGO-1 è stato precedentemente studiato come gene coinvolto nello sviluppo di Arabidopsis). Anche se l’esatta funzione di questi geni non è ancora chiara, un gene studiato in mammiferi, della famiglia di RDE-1, è stato identificato come fattore di iniziazione dell’RNAi (Sharp et al., 2001; Silhavy et al., 2002). Per quanto concerne gli ARGONAUTI, essendosi dimostrati coinvolti sotto molti aspetti funzionali dell’RNAi in Arabidopsis, verranno meglio illustrati in un paragrafo successivo. Gli “effettori” Geni importanti per la fase effettrice in C. elegans sono rde-2 e mut-7. Questi geni sono stati identificati in esemplari eterozigoti che non erano in grado di trasmettere l’RNAi alla progenie omozigote. Nematodi con rde-2 o mut-7 mutati si dimostravano difettivi per l’RNAi. Mut-7 codifica per una proteina che ha omologia al dominio nucleasico dell’ RNAsi D e ad una proteina implicata nella sindrome di Werner (progeria adulta), caratterizzata nel rapido invecchiamento dell’uomo (Grishok et al., 2000). RNA polimerasi – RNA dipendente: un sistema di amplificazione La potenza dell’RNAi, riscontrata in tutti gli esperimenti, è stata attribuita ad un processo di amplificazione, proprio del meccanismo di interferenza. Questa amplificazione può avere come bersaglio i dsRNA, al fine di produrre più siRNA, o i siRNA stessi. In questo modo i complessi RISC hanno la possibilità di effettuare un maggior numero di reazioni ribonucleasiche sequenza-specifiche (“tagli”). Recenti indagini hanno dimostrato che i siRNA complementari all’mRNA bersaglio funzionano da primer per un RNA polimerasi-RNA dipendente (RdRP) che trasforma l’mRNA in dsRNA, il quale a sua volta sarà il substrato di Dicer. Questo passaggio amplifica così la risposta dell’RNAi, la quale può autoalimentarsi fino a quando tutto l’mRNA bersaglio non è degradato. Il silenziamento genico mediato da RNAi diventa così uno dei più eleganti ed efficienti meccanismi in natura (Zamore et al., 2002). I geni qde-1 di 11 Argonauti Ago1 Topo Ago2 (endonucleasi) Ago3 Ago4 RNAsi III RDE-1 (RNAi) C. elegans Drosha (miRNA) TRBP Spindle-E (eterocromatina) R2D2 (siRNA) Armitage (formazione RISC) Pasha (pre-miRNA) RRF-1 (RNAi somatico) SMG-2 (RNAi) EGO-1 (RNAi in progenie) PPW-2 (silenz. Trasposoni) MUT-14 (silenz. Trasposoni) RFR-3 DCR-1 (RNAi e miRNA) Drosha (miRNA) A.thaliana) (RNAi in progenie) DCL1 (miRNA) SDE3 DCL2 (correlata a virus) DCL3 (eterocromatina) (VIGS e PTGS) QDE-2 (quelling) Altri Tudor-SN (RNAi e miRNA) Exportin-5 (trasporto miRNA) Germin4 (miRNA) VIG (RNAi e miRNA) FXR (RNAi e miRNA) Loquacious (miRNA) Tudor-SN (RNAi e miRNA) Drosha (miRNA) DRH-1/DRH-2 (RNAi) (Petunia, Tabacco, AGO4 (eterocromatina) N. crassa DGCR8 ALG-1 e ALG-2 (miRNA) AGO1 (miRNA e PTGS) dsRNA binding proteins Gemin 3 (miRNA) PPW-1 (RNAi in progenie) Piante RdRP Dicer Aubergine (eterocromatina) Dicer-1 (miRNA) D. Melanogaster Ago1 (miRNA) Dicer-2 (RNAi) Ago2 (siRNA) Elicasi Eri-1 , RDE-3, RDE-4 (RNAi) SID-1, MUT-7 MUT-8, VIG-1, (silenziamento RNAi) TSN-1 SGS2/SDE1/RDR6 Hyl1 (miRNA) HEN1,SGS3 (virus, PTGS) DRB4 RDR2 (silenz. cromatina) SDE4/sub-unità polim. IV HASTY (trasporto miRNA) QDE-1 (quelling) QDE-3 (quelling) Tabella 2: principali geni coinvolti nel fenomeno dell’RNAi, scoperti fin’ora. Tra parentesi sono indicate le funzioni in cui sono coinvolte o la molecola con cui interagiscono. Neurospora, SDE1/SGS-2 in Arabidopsis ed EGO-1 in C. elegans sembrano codificare la stessa RdRP. I dati degli esperimenti su questi geni confermano la loro indispensabile funzione nell’RNAi. Mutanti di Arabidopsis per SDE1/SGS-2 si dimostrano incapaci di generare RNAi in seguito ad introduzione di dsRNA attraverso transgene; gli stessi però generano risposta a seguito di replicazione endogena mediata da virus. Probabilmente questo risultato è dovuto al fatto che la carenza di RdRP viene vicariata dalla RNA polimerasi virale. Altri geni coinvolti nel silenziamento Molti geni implicati nell’RNAi sono stati identificati attraverso screening su mutanti di Arabidopsis (Tab.1). Questi codificano putativamente per RNA polimerasi RNAdipendente (SGS2/SDE1), per una proteina “coiled coil” (SGS3), una proteina contenente domini PAZ e Piwi (essenziali per il funzionamento di RISC) (AGO1) e una RNA elicasi (SDE3). I geni putativi SGS2/SDE1 sono correlati a QDE-1 in Neurospora e a EGO-1 in C. elegans, le proteine PAZ/Piwi (AGO) a QDE-2 in Neurospora e a RDE-1 in C.elegans, l’RNA elicasi a SDE3 ed SMG-2 di C. elegans e Mut-6 di Chlamydomonas. Mut-t di C. elegans codifica per una proteina simile ad RNAsi D, mentre Dicer di Drosophila codifica per una RNAsi III. Ortologhi di Dicer in Arabidopsis sono stati identificati: CAF, SIN1, SUS1. Gli Argonauti Gli argonauti sono proteine facenti parti di una grande famiglia, molto conservata, i cui membri sembrano andare a formare la maggior parte del complesso RISC; esse sono 12 quindi implicate come effettori del processo di silenziamento ad opera dell’RNAi ed in altri fenomeni correlati in molti organismi, come funghi, piante e mammiferi. I ruoli degli Argonauti 1 e 2 (chiamati Ago1 e Ago2 in Drosophila) sono quelli meglio definiti. Ago2 è stato identificato come una componente del complesso RISC, essenziale per l’RNAi mediato da siRNA (Okamura et al., 2004). Ago2 è necessaria alla denaturazione dei siRNA a doppio filamento e alla loro integrazione nel complesso (solo il filamento antisenso). Embrioni deficienti di Ago2 restano comunque in grado di effettuare RNAi mediato da miRNA. Ciò suggerisce l’esistenza di più proteine che svolgono un ruolo simile a quello di Ago2. Viceversa, Ago1, indispensabile per il taglio dell’RNA guidato da siRNA, è anche richiesto per la produzione di miRNA (Okamura et al., 2004) L’associazione di Ago1 con Dicer-1 e i pre-miRNA suggerisce inoltre che Ago1 sia coinvolto nella biogenesi dei miRNA. Gli Argonauti si mostrano anche coinvolti nello sviluppo e nella differenziazione cellulare. Le proteine argonaute hanno dimensioni di circa 100 kD, fortemente basiche e contengono due domini comuni chiamati PAZ e Piwi (Cerutti et al., 2000). Il dominio PAZ è costituito da 130 amminoacidi ed è stato anche identificato in Dicer (Bernstein et al., 2001). Anche se non si conosce ancora l’esatta funzione del dominio PAZ, si ipotizza che esso sia necessario per un’interazione proteina-proteina, probabilmente per una omo- o eterodimerizzazione (Cerutti et al., 2000). Essendo queste proteine molto basiche, si pensa possano legare il DNA. Miwi, un omologo di Piwi in topo, è stato trovato associato ad un complesso con l’mRNA bersaglio in vivo (Deng e Lin, 2002); ciò ha fatto dedurre che il dominio Piwi sia implicato nel legare l’mRNA bersaglio nel complesso RISC. Successivamente Ago1 si è scoperto legare ribomopolimeri in vitro (Kataoka et al., 2001). Sicuramente le proteine argonaute sono coinvolte nel processo dell’RNAi, sia indirettamente che direttamente, ma sono comunque necessari ulteriori studi biochimici per poter scoprire la loro precisa funzione nel metabolismo dell’RNA. RNAi in cellule di mammifero In cellule di mammifero sono state riscontrate molte più difficoltà nell’indurre l’RNAi. Questo perché a seguito dell’introduzione di dsRNA, spesso a rispondere non è un sistema di silenziamento sequenza-specifico, ma un sistema che inibisce tutta l’espressione globalmente. In questi casi ad interagire con il dsRNA, introdotto in cellule di mammifero, è una proteina kinasica (DAI o PKR) che va a scatenare la 13 risposta immunitaria dell’interferone bloccando globalmente la trascrizione. Un altro evento di silenziamento genico osservato in mammiferi è quello mediato da una ribonucleasi (RNAsi L), attivata da dsRNA, che agisce attuando una degradazione non specifica dell’mRNA. Utilizzando invece i siRNA, i quali non azionano la risposta interferonica, si è riusciti ad indurre il silenziamento sequenza-specifico. Questa scoperta, come descritto in seguito, si mostrerà utile al fine di poter progettare metodologie di somministrazione umana a scopo terapeutico. Attraverso lo studio dell’RNAi su colture di cellule umane HeLa, si è capito che erano i siRNA, prodotti dall’enzima Dicer, a generare il fenomeno di silenziamento genico. Altre molecole di RNA a doppio filamento, naturalmente prodotte da cellule umane (micro-RNA sequence o miRNA, vedi paragrafi successivi), e caratterizzate da precursori con una struttura a forcina, si sono mostrate anch’esse implicate nella processazione da parte di Dicer. In questo modo, collegando i miRNA endogeni al sistema di silenziamento genico dell’RNAi, si è capito che il processo in questione, oltre ad essere comune in diversi organismi, possiede la funzione di regolazione genica durante lo sviluppo. Inoltre, più recentemente, attraverso esperimenti su lievito, si è scoperto che il meccanismo dell’RNAi è coinvolto nella regolazione della cromatina. Prima analizzare tutte le possibili varianti e funzioni dell’RNAi è necessario fare un quadro generale sul meccanismo. Il ruolo dei microRNAs (miRNA) nello sviluppo delle piante Cenni storici Circa venti anni fa venne isolato un mutante di C.elegans per il gene lin-4 e lo stesso venne clonato. Analisi genetiche e molecolari misero in evidenza che lin-4 agiva come regolatore negativo di lin-14 (Ambros et al., 1989; Arasu et al., 1991). Sorprendentemente lin-4 non aveva una open reading frame ed era localizzato in un gene che non sembrava essergli correlato in alcun modo. Ciò nonostante risultava molto conservato nei nematodi e codificava per due piccoli trascritti di 22 e 61 nucleotidi (lin4S e lin-4L). La sequenza di lin-4S era interna a lin-4L e complementare a sette ripetizioni nel 3’-UTR di lin-14. Grazie ad altri esperimenti si acquisirono prove sufficienti a costruire un modello di funzionamento e correlazione tra questi geni. Lin4S era in grado di bloccare la traduzione di lin-14 appaiandosi per complementarietà 14 alla regione 3’-UTR di quest’ultimo. Fino al Febbraio 2000, questo fenomeno era l’unico riportato in letteratura, quando Reinhart e collaboratori trovarono un altro gene che funzionava in maniera simile: let-7. L’estrema similarità fra i due casi fece ipotizzare che tali piccoli trascritti (chiamati successivamente miRNA) giocassero un importante ruolo nella regolazione genica e nello sviluppo. Queste scoperte, negli ultimi anni, si unirono ai risultati ottenuti negli esperimenti di silenziamento genico mediato da dsRNA (discussi nei paragrafi precedenti). MicroRNA (miRNA) e small interfering RNA (siRNA) venivano processati dagli stessi enzimi, i quali erano presenti come ortologhi in diversi organismi viventi, dai funghi ai mammiferi. Biogenesi e traslocazione dei miRNA I miRNAs sono piccoli RNA lunghi circa 22 nucleotidi; derivano da trascritti non codificanti e funzionano come repressori nella regolazione genica in eucarioti. I miRNA di piante e animali differiscono per sequenza, quantità, pattern di espressione e localizzazione genomica. Alcuni di essi possiedono un proprio locus, altri, invece, sono contenuti all’interno di regioni introniche di altre sequenze codificanti, spesso nello stesso senso; questo suggerisce che probabilmente vengano trascritti in concomitanza del loro gene ospite. I miRNA quindi vanno a fare parte di tutte quelle sequenze che fino ad ora sono state annotate come intergeniche o unità policistroniche. Studi su piante ed animali hanno rilevato che i miRNA vengono trascritti dall’RNA polimerasi II a partire dal loro stesso promotore. Essendo geni di classe II (pri-miRNA) possiedono introni, sono poliadenilati e con cap al 5’. Questi pri-miRNA sono dotati di una sequenza che li conforma in una struttura secondaria a forcina, non perfettamente complementare. Il miRNA funzionale è contenuto in uno dei due bracci della forcina. La struttura dei pri-miRNA è essenziale per il riconoscimento e la processazione da parte di una ribonucleasi di classe III (RNAsi III) che li taglia in più piccoli miRNA (chiamati pre-miRNA). Negli animali si è provato che questo processo è eseguito nel nucleo ad opera del “microProcessor protein complex”, il quale include Drosha (RNAsi III) e Pasha (dsRNA-binding protein). Il taglio dei pri-miRNA in pre-miRNA nel nucleo, esso avviene a carico dell’attività di Drosha; il taglio da pre-miRNA a miRNA maturi avviene nel citoplasma ad opera di Dicer: si è infatti osservata sui miRNA maturi la tipica elaborazione di questo enzima, che consiste nel lasciare due nucleotidi liberi al 3’, con un monofosfato al 5’ della stessa terminazione, e al 3’ opposto un 15 gruppo idrossile. Il passaggio dal nucleo al citoplasma dei pre-miRNA risulta quindi un evento fondamentale della biogenesi dei miRNA. Mutanti per geni coinvolti nella biogenesi dei miRNA in Arabidopsis thaliana hanno permesso di osservare aberrazioni nello sviluppo. Un esempio è il gene DCL-1 (Dicerlike 1) coinvolto nella formazione del complesso nucleare che taglia i pri-miRNA. Una mutazione nel dominio elicasico risulta in un accumulo di pri-miRNA (Watanabe et al., 2004). Nei mammiferi il trasporto dei pre-miRNA nel citoplasma avviene attraverso l’Esportina 5 in cooperazione con Ran-GTP. L’ortologo equivalente nelle piante è HASTY (HST) che coopera con AtRAN1 (ortologo di Ran-GTP). Mutanti hst-3 per HST risultano in un accumulo di pre-miRNA nel nucleo, nonché in difetti nello sviluppo. Il gene HEN1 fa invece parte della famiglia delle metiltransferasi; esso effettua un metilazione mirata esclusivamente ai duplex miRNA maturi. Il significato di questa operazione non è del tutto chiaro. Due sono le ipotesi: la prima propone la metilazione come semplice protezione da esonucleasi; la seconda invece propone un modello in cui i gruppi metile servono come riconoscimento per i passaggi successivi nel processo di silenziamento. Silenziamento mediato dai miRNA Generalmente i miRNA maturi vengono integrati in un complesso chiamato miRNP (simile a RISC per i siRNA). I miRNA interagiscono con l’mRNA target attraverso complementarità delle basi. Due tipi di meccanismi sono stati individuati a carico del silenziamento mediato dai miRNA: uno prevede la degradazione dell’mRNA bersaglio, l’altro il blocco della traduzione dello stesso. L’azione di uno o dell’altro processo è discriminato dalla complementarietà tra mRNA e miRNA. Nel caso di un perfetto appaiamento occorre il taglio dell’mRNA mediato dal complesso, come avviene per il silenziamento mediato da siRNA (Fig.5). Se l’appaiamento risulta invece non perfetto il miRNA si lega alla regione 3’UTR dell’mRNA bloccandone la traduzione. 16 Questi miRNA, vista la loro natura regolatrice, si trovano molto conservati all’interno di molte specie, e in alcuni casi arrivano a costituire l’1% del genoma, mostrandosi componente come regolatore il più rappresentativo. Figura 5: schema della biosintesi dei miRNA e del loro processo di silenziamento genico. E’ da notare la possibilità che i miRNA maturi entrino nello stesso pathway che gestisce i siRNA. Quest’ultimo, come si discuterà nei prossimi capitoli, può essere inibito da soppressori, sia di origine endogena (ADARs, ERI-1) che virale (p19). Alla ricerca dei miRNA Gli approcci sperimentali finalizzati alla scoperta di nuove sequenze miRNA coinvolte nella regolazione cellulare sono stati affiancati da analisi computazionali. Si tratta di algoritmi che ricercano, nel genoma della specie di interesse, possibili sequenze geniche. In questo caso gli algoritmi vanno a cercare sequenze la cui struttura secondaria potrebbe essere quella di un miRNA , ovvero a forcina, che risultano abbastanza conservate. Alcuni di questi programmi sono miRscan e miRseeker. I vari risultati vengono valutati in base a punteggi che tengono conto della complementarietà dei due bracci, la presenza di basi consenso, di uracili all’inizio della trascrizione, ecc... 17 MiRseeker inizia la ricerca confrontando due interi genomi e localizzando sequenze ortologhe conservate nelle regioni non codificanti. Queste regioni vengono poi elaborate con MFOLD (un algoritmo che deduce la struttura secondaria) valutando la qualità delle strutture a forcina che genererebbero, in termini di lunghezza ed energia libera della molecola. Vengono poi scartate le strutture che non possono essere miRNA reali, in base a pattern di divergenza dei nucleotidi. Questi strumenti si sono dimostrati molto efficaci e hanno permesso l’identificazione di molti miRNA implicati nella regolazione genica. Ciò nonostante le sequenze scoperte fino ad ora costituiscono un database ridotto rispetto alla probabile totalità esistente in natura. Figura 6: un esempio di risultato computazionale fornito da MFOLD. I miRNA e lo sviluppo delle piante La conoscenza del ruolo dei miRNA nello sviluppo delle piante si è ottenuto per la maggior parte attraverso due tipi di approcci: l’analisi dei geni necessari alla formazione dei miRNA e l’identificazione dei geni bersaglio. In screening per geni coinvolti nello sviluppo embrionale, vegetativo e riproduttivo sono stati identificati mutanti per dcl-1 di Arabidopsis. I mutanti hanno evidenziato una sovra- proliferazione di meristemi, conversione dei meristemi fiorali in meristemi indifferenziati, fioritura ritardata e sovrapproduzione di cellule embrionali sospensorie. I mutanti dcl-1 mostravano ridotti livelli di miRNA ed esprimevano i geni che sarebbero dovuti essere bersaglio del silenziamento. Mutazioni a carico di altri geni coinvolti nella biogenesi dei miRNA (HEN1), o che agiscono nel meccanismo di silenziamento genico (AGO1), causavano anch’essi fenotipi riconducibili a quelli dei mutanti per dcl-1 e difetti nella polarità delle foglie. Successivamente fu notato che il virus del mosaico della rapa interferiva con l’attività dei miRNA codificando per un soppressore dell’RNAi; questo 18 causava un espressione non controllata dei geni, bersaglio dei miRNA, determinando fenotipi con difetti morfologici paragonabili a quelli dei mutanti per dcl-1, ago1 e hen1. Si è quindi dedotto che i miRNA funzionassero da regolatori negativi nell’identità delle cellule meristematiche, nella polarità degli organi e in altri processi di sviluppo. Nelle piante, come negli animali, i miRNA hanno mostrato pattern di espressione temporanei e tessuto-specifici. Numerosi mRNA-target di Arabidopsis sono stati predetti sulla base della quasiperfetta complementarietà con miRNA; queste predizioni sono state inoltre supportate dai dati statistici e dalla conservazione filogenetica ottenuti da studi su riso. Fino ad ora sono stati identificati una quindicina di punti di taglio guidati da miRNA attraverso saggi in vivo ed in vitro. Sorprendentemente, la quasi totalità dei target di miRNA sono costituiti da geni che codificano per fattori trascrizionali, che includono APETALA2 (AP2), CUP-SHAPED COTYLEDONS1(CUC1), CUC2, PHAVOLUTA(PHV) e PHABULOSA(PHB). I geni, come descritto precedentemente sono coinvolti nell’identità di cellule meristematiche, nella polarità degli organi, nella divisione cellulare e nella differenziazione di organi. Una minoranza di mRNA target, invece, hanno mostrato di codificare per fattori indispensabili alla formazione dei miRNA stessi ed alla loro funzione. Per esempio l’mRNA di DCL1 è risultato a sua volta bersaglio di miRNA (miR162), indicando che nelle piante i miRNA possono avere un controllo a feedback negativo (Fig.7). Prove di circostanza hanno assegnato ai tagli guidati da miR165/166 un ruolo nella determinazione del pattern radiale delle foglie. I fattori trascrizionali PHV e PHB controllano rispettivamente la determinazione di una polarità adassiale (parte distale) o abaxiale (parte prossimale) nelle foglie, risultando in superfici strutturalmente e funzionalmente specializzate .I geni PHB e PHV vengono già espressi a livello dei primordi fogliari. Essi si localizzano nella parte vicino al germoglio per determinare un destino adassiale; sono invece “spenti” nella parte distale del meristema per determinare un destino di tipo abaxiale (Fig. 8). Alleli dominanti phv e phb, contenenti modificazioni nucleotidiche a carico della regione di interazione con miR165/166, generano una ridotta degradazione degli mRNA di phb e phv. Gli alleli sono così espressi ubiquitariamente già a livello di primordio fogliare generando caratteristiche morfologiche adassiali anche nella parte prossimale della foglia. Si può quindi dedurre che miR165/166 sono implicati nella regolazione trascrizionale che sta a monte del destino cellulare della polarità fogliare. 19 Figura 7: L’espressione di DCL1, che catalizza la processazione dei precursori dei miRNA è sotto un controllo a feed-back negativo da parte di miR162 (sinistra). miR165/166 regolano negativamente PHV e PHB attraverso il taglio sequenza-specifico dei loro rispettivi mRNA. Figura 8: Modello per la determinazione del destino adassiale o abaxiale in foglie di Arabidopsis. Ad oggi si è ancora nelle prime fasi di studio del ruolo dei miRNA nei processi di sviluppo e si sta cercando di comprendere come questi elementi di controllo negativo riescano così finemente ad auto-regolarsi. L’RNAi nel nucleo Il mistero della metilazione Studiando mutanti di Arabidopsis per i geni PHB (phabulosa) e PHV (phavoluta), per i quali, come descritto nei paragrafi precedenti, la mutazione generava una non perfetta complementarietà tra gli mRNA e i rispettivi miRNA, Bao et al. (2004) notarono che nelle piante wild-type erano presenti zone estese di DNA metilato (centinaia di paia di basi) a carico della regione a valle dei siti di legame dei miRNA, nei geni PHB e PHV (circa 1000 bp a valle). La metilazione risultava invece notevolmente ridotta in piante 20 con i geni mutati nelle regioni di legame per i rispettivi miRNA. Gli autori intuirono allora che l’assenza di metilazione aiutava a “de-silenziare” i geni, mentre la metilazione, e quindi il silenziamento trascrizionale, erano guidati dai miRNA. Altre osservazioni portarono poi a supporre che l’interazione tra i miRNA e il DNA non fosse diretta, ma che fosse necessaria anche un’interazione tra i miRNA e l’mRNA target (Fig.9). Bao et al. (2004) proposero così un modello del meccanismo con cui avviene la metilazione mediata da miRNA. I miRNA, localizzati nel citoplasma rientrano nel nucleo e si appaiano all’ mRNA che sta ancora finendo di trascriversi dal suo DNA codificante. Il DNA viene così metilato a valle delle sequenze di legame con i miRNA dei geni PHB e PHV grazie ad un complesso enzimatico non ancora ben determinato, che è in grado di rimodellare la cromatina. Si ipotizza che questo complesso sia guidato da un templato di miRNA o da mRNA tagliato. Probabili candidati a caratterizzare questo complesso sono varianti del complesso RISC, che incorporino le proteine argonaute o altri gruppi proteici che interagiscano con esse. In tal senso, il meccanismo con cui avviene una metilazione sequenza-specifica, limitata ad una determinata regione e ad una precisa distanza dal sito di complementarietà con i miRNA, rimane ancora in parte da spiegare. Figura 9: Modelli proposti da Bao et al. In tutti i miRNA maturi vengono prodotti dal precursore (premiRNA) e successivamente, dal citoplasma, rientrano nel nucleo. a-I miRNA ritornano nel nucleo legati al complesso RISC o a un suo simile. Attraverso la complementarietà di basi si appaia all’mRNA in via di trascrizione dai geni PHB/PHV. Il complesso a questo punto “recluta” un complesso rimodellante della cromatina che attua la metilazione. b- In questo caso, siRNA prodotti da una RNA polimerasi RNA-dipendente (RdRP) guidata da miRNA o da templati costituiti da pezzi di mRNA già tagliati da RISC vengono usati come porzione per riconoscere il gene (tratteggi rossi) e generare la metilazione a valle (tratto blu), sempre a carico di un complesso rimodellante della cromatina (arancione) c- L’mRNA tagliato da RISC in modo particolare da renderlo “marcato”viene usato come stampo di guida per eseguire la mutilazione. 21 E’ comunque probabile che la metilazione abbia solo un ruolo secondario nella regolazione di PHB e PHV. Infatti, quando vengono mutati geni coinvolti nel meccanismo di questo tipo di metilazione, gli effetti sulla pianta non sono gli stessi ottenuti negli studi di PHB descritti in precedenza; inoltre, la metilazione di altri geni non pare influenzare la loro stessa espressione. Forse più che a silenziare i geni, la metilazione serve come un’ “impronta”, lasciata dai miRNA ma che si conserva autonomamente attraverso diverse generazioni. Il nucleo: un “nuovo sito” di ricerca per l’RNAi Il silenziamento genico mediato da siRNA e miRNA presenta una notevole specificità visto che si tratta di un processo guidato da complementarietà di basi tra gli RNA. L’esperimento trattato nel paragrafo precedente ha però fatto intuire che l’RNA può anche interagire con il DNA. Per questo, negli ultimi anni, gran parte dell’interesse sui processi mediati dall’RNAi si è focalizzato sui meccanismi che si verificano a livello del genoma nucleare. A seguito sono descritti i ruoli dei dsRNA e delle proteine coinvolte in diversi processi di silenziamento genico a livello nucleare, il cosiddetto TGS (trascriptional gene silencing). I processi nucleari mediati dall’RNAi Quattro sono i processi mediati da RNAi a livello nucleare ben descritti fino ad ora. Due di questi: la metilazione del DNA diretta da RNA (RNA-directed DNA methylation: RdDM) e la formazione di eterocromatina mediata da RNAi costituiscono processi epigenetici che consistono rispettivamente nella modificazione delle citosine del DNA o delle proteine istoniche (generalmente la metilazione della lisina 9 dell’istone H3: K9H3). L’RdDM è stata maggiormente studiata e descritta in piante mentre la formazione dell’eterocromatina è stata analizzata in Schizosaccharomyces pombe, animali e piante. L’RdDM e la formazione dell’eterocromatina, sono entrambi iniziati da dsRNA, ma non è ancora stato chiarito se si tratta di due meccanismi separati o di uno. Negli organismi superiori si è notato che la metilazione del DNA e la modificazione degli istoni hanno un ruolo di “automantenimento” reciproco. In S. pombe, invece, dove si è potuto osservare la modificazione dell’eterocromatina, non si è trovata metilazione a 22 carico del DNA, facendo presupporre che i due fenomeni non siano necessariamente accoppiati. Un terzo meccanismo è l’eliminazione del DNA. Protozoi cigliati hanno mostrato la capacità di eliminare tratti di DNA durante lo sviluppo dei macronuclei. Questi tratti del genoma erano stati in precedenza, sotto l’azione del meccanismo dell’RNAi, rimodellati a livello della cromatina. Si compie così una ristrutturazione del genoma. Un ultimo meccanismo è rappresentato dal silenziamento di DNA non appaiato durante la meiosi. Questo fenomeno è stato osservato in organismi, come Neurospora crassa, in cui si è mostrato correlato alle proteine coinvolte nel fenomeno dell’RNAi. Il silenziamento meiotico ha origine nel nucleo, ma a differenza dei tre precedenti, risulta in silenziamento a livello post-trascrizionale e non genera un rimodellamento della cromatina nel locus di partenza. Nei prossimi paragrafi verranno trattati più in dettaglio questi quattro meccanismi. Metilazione del DNA diretta da RNA (RdDM) La RdDM è stata la prima modificazione epigenetica guidata da RNA ad essere scoperta in piante di tabacco (Wassenegger et al., 1994). Successivamente, si dimostrò che questa metilazione richiedeva la presenza di dsRNA che venissero processati in frammenti più piccoli (21-24 bp) correlandola fortemente all’RNAi. Nelle piante si è osservato che dsRNA contenenti sequenze omologhe a promotori potevano causare la metilazione di questi ultimi e quindi generare un silenziamento a livello trascrizionale del gene a valle. L’RdDM attua una metilazione de novo delle citosine presenti in qualsiasi contesto di sequenza, non solo in presenza dei dinucleotidi GC, considerati il tipico target della metilazione. La metilazione è decisamente ristretta a regioni di omologia del DNA con RNA, perciò, a differenza del rimodellamento della cromatina che può ampliarsi per migliaia di basi distante dal sito di omologia, è esclusivamente localizzata nel sito di omologia. La dimensione minima di questa metilazione è di ~30 bp, molto più contenuta rispetto all’eterocromatina, la quale, modificando l’intera proteina istonica agisce silenziando multipli di 147 bp. Come detto precedentemente, la maggior parte degli studi sull’ RdDM sono stati fatti su piante ed in particolare su A. thaliana, sulla quale sono stati utilizzati approcci sia di “forward genetics” che di “reverse genetics”. Sono stati utilizzati, prevalentemente, transgeni codificanti per RNA che assumessero una struttura a forcina (short hairpin 23 RNA: shRNA) e che generassero il fenomeno di metilazione specifica di promotori; un altro approccio è stato invece lo studio di geni endogeni coinvolti nel fenomeno. Queste analisi hanno portato alla conclusione che sono necessari una DNA – citosina metiltransferasi, alcuni enzimi coinvolti nella modificazione degli istoni, proteine rimodellanti della cromatina e una moltitudine di geni, già coinvolti nei processi posttrascrizionali dell’RNAi. Il processo consta inizialmente di una metilazione de novo ad opera di una DNAmetiltransferasi sito-specifica; a seguito di questa prima fase, la metilazione viene mantenuta grazie ad una modificazione istonica, la quale può comunque essere persa passivamente o attivamente, attraverso determinati meccanismi. Lo schema riportato in Fig.10 schematizza il meccanismo e i geni che sono in esso coinvolti. Figura 10: Questo modello è il risultato delle prove genetiche fatte su A. thaliana. Nel nucleo dsRNA possono essere prodotti dall’attività di una RNA polimerasi RNA dipendente (RDR2) su ssRNA oppure dalla trascrizione di DNA invertiti- ripetuti ad opera di una RNA polimerasi DNA-dipendente come la RNA polimerasi II. Gli RNA che guideranno la metilazione vengono prodotti dal taglio di dsRNA in frammenti più piccoli ad opera di enzimi della famiglia Dicer-like, di solito DCL3. Questi piccoli RNA segnale si integrano in metiltransferasi sitospecifiche (MET1 per sequenze CG e DRM2 per sequenze non-CG) e viene catalizzata la metilazione. La RdDM richiede inoltre l’azione delle proteine SNF-2-like (DRD1), probabilmente per rendere accessibile il DNA all’RNA. La metilazione delle regioni CG e CNG può essere mantenuta per molto tempo in assenza degli RNA segnale attraverso l’attività di MET1 e CMT3 (cromometilasi 3), rispettivamente. Il mantenimento della metilazione CG richiede la presenza della istone deacetilasi HDA6 e della SNF2-like DDM1. La metilazione su CNG è invece accompagnata dalla metilazione ad opera di H3K9 (non mostrata) e di SUVH4 (nota come KRYPTONITE). Anche le proteine argonaute si sono mostrate coinvolte nei processi di metilazione de novo e del suo mantenimento, rispettivamente AGO4 e AGO1. Le proteine DEMETER (DME) contenenti domini di glicosilazione del DNA e REPRESSOR OF SILENCING (ROS1) sono invece coinvolte nella perdita della metilazione e quindi la riattivazione dei geni bersaglio, i quali, a loro volta, possono essere coinvolti nella genesi di miRNA, lasciando intuire la probabilità di un finissimo sistema di autoregolazione. 24 La formazione e il controllo dell’eterocromatina In linea generale, l’eterocromatina è una porzione di DNA pressoché silente, povera di geni, mentre l’eucromatina è attiva e ricca di sequenze codificanti. Queste differenze sono causali al grado di avvolgimento della cromatina, dovuto a modificazione delle proteine istoniche su cui si avvolge il DNA. Tali modificazioni del grado di compattamento del DNA sono dovute all’acetilazione, metilazione, fosforilazione e legami con l’ubiquitina. In molte specie, le regioni eterocromatiniche sono in genere localizzate nelle regioni centromeriche. Inoltre, in molti organismi è osservabile il fenomeno PEV (position-effect variegation) che consiste in un pattern di silenziamento genico a mosaico a seconda della posizione che ha un gene localizzato tra una regione ad alta densità di eterocromatina ed una di eucromatina. Le componenti dell’eterocromatina del DNA di S.pombe, localizzate nella regione centromerica, sono costituite da elementi trasposonici ripetuti e invertiti. L’eterocromatina presente in questa regione favorisce il contatto tra i due cromatidi fratelli in prossimità del centromero, dove le due cromatine si fiancheggiano. Questa struttura si è dimostrata invece compromessa in mutanti per geni coinvolti nel meccanismo dell’RNAi, facendo presupporre che il modellamento della cromatina fosse guidato da siRNA. Queste prove furono acquisite soprattutto effettuando knockdown dei geni codificanti per gli Argonauti, Dicer e RdRP che sono presenti in singola copia in S. pombe. Nei lieviti wild-type non si osservava trascritto, senso od antisenso, delle zone ripetute a tandem. Viceversa nei mutanti, attraverso gli stessi saggi trascrizionali, era osservabile un accumulo dei trascritti di quelle regioni. Ciò non fece che confermare che gli enzimi tipicamente noti nel processo dell’RNAi erano anche implicati, come guida, nella formazione dell’eterocromatina. Altre prove ottenute in laboratorio fecero comprendere che era la trascrizione dei filamenti ripetuti e invertiti delle regioni centromeriche a generare i dsRNA che, una volta tagliati dall’enzima Dicer, venivano usati come guida dalla metiltransferasi. Gli stessi dsRNA erano a loro volta amplificati dalla RdRP. In S.pombe si è anche scoperta l’esistenza di un complesso enzimatico effettore chiamato RITS (RNA-induced initiation of trascriptional gene silencing), implicato in modificazioni a livello della cromatina. Gli studi hanno portato a caratterizzare un modello funzionale di tale complesso, composto da una proteina argonauta (AGO1), da una proteina contenente un dominio cromatinico (Chp1) e una proteina specifica di S.pombe (Tas3) (Fig.11). Questo complesso incorpora in AGO1 un siRNA specifico 25 per regioni centromeriche, il quale si andrà ad appaiare ad una sequenza in via di trascrizione (vedi precedenti modelli di Bao et al., 2004), probabilmente il suo stesso precursore (ancora non sottoposto all’azione dell’RNAi a livello post-trascrizionale). Una volta appaiato, il complesso, effettua la metilazione H3K9 (istone H3 a livello della lisina 9); inoltre, l’incorporazione di altre proteine interagenti con l’RNA, quali Cid12, Hrr1 ed un RdRP, provvede al mantenimento dello stato di avvolgimento eterocromatico di questa regione centromerica del cromosoma. Figura 11: Processo di metilazione mediato da RNAi in S.pombe. Anche su piante (A. thaliana) le ricerche hanno portato all’identificazione di siRNA coinvolti nel modellamento cromatinico. Analisi effettuate attraverso l’uso di microarray su regione eterocromatiniche ricche di trasposoni hanno rilevato la presenza di alti livelli di metilazioni H3K9 a livello di sequenze ben delimitate e che non si allargavano su zone adiacenti. Si è dimostrato che in questo meccanismo era coinvolta la proteina DDM1 della famiglia SNF2-like, in quanto, mutanti della stessa mostravano livelli ridotti dei siRNA che sarebbero implicati nel riconoscimento delle sequenze trasposoniche ripetute. Concludendo, questi studi indicano che queste sequenze ripetute e invertite hanno la potenzialità di generare siRNA, che una volta processati da Dicer, entrano nel meccanismo che li sfrutterà per eseguire una metilazione sito-specifica degli istoni nelle stesse sequenze, silenziandone la trascrizione. Questa iniziale modificazione viene poi 26 usata come stampo per il mantenimento della stessa da parte di proteine quali HP1, Swi6l o polycomb complex (Fig. 12). Figura 12: Ripetizioni invertite di trasposoni generano dsRNA. Questi, una volta processati dall’enzima Dicer guidano la metilazione ad opera di una istone metil-transferasi (HMT) sull’istone H3. Questa metilazione viene mantenuta in seguito dal polycomb complex, costituito da proteine cromatiniche che mantengono lo stato di avvolgimento durante lo sviluppo dell’organismo. Eliminazione di DNA Nel protozoo Tetrahymena thermophila coesistono due nuclei: un micronucleo diploide (avente funzione di conservare il patrimonio genetico, trascrizionalmente silente durante la crescita vegetativa) e un macronucleo poliploide (con funzione di nucleo somatico con attiva trascrizione). Il ciclo riproduttivo per coniugazione di questo protozoo è mostrato in fig.13. Nella fase in cui due micronuclei si differenziano in macronuclei avviene l’eliminazione di sequenze specifiche germinali, implicate nella riproduzione, e quindi non utili alle funzioni vegetative del macronucleo. Queste sequenze eliminate vengono dette IES (internal eliminated segment sequences) e costituiscono il 15% del genoma del protozoo. 27 Figura 13 :Ciclo di coniugazione di Tetrahymena thermophila Successivamente viene descritto come il DNA dei nuovi macronuclei possa venir sottoposto ad eliminazione da parte dell’RNAi e come questo sistema funzioni da controllo per evitare l’instaurarsi di elementi trasponibili nel nuovo macronucleo. Durante lo sviluppo del nuovo macronucleo, nei micronuclei il genoma viene completamente trascritto in dsRNA (Fig.14 ). Questo dsRNA trascritto viene tagliato da Dcl1 (enzima Dicer) in piccoli “scan RNAs” (scnRNAs) i quali, dopo essersi complessati con l’argonauta Tw1, vengono esportati nel vecchio macronucleo. Figura 14: Eliminazione del DNA a livello del macronucleo in sviluppo. Il templato usato come guida per questo processo viene ottenuto selezionando i scnRNA a livello dei vecchi macronuclei. Gli scnRNA non degradati nei vecchi andranno a eliminare le sequenze complementari nei nuovi. 28 In esso, attraverso appaiamento per omologia, gli scnRNAs vengono degradati. Rimangono però degli scnRNA non degradati, i quali, essendo derivati da sequenze germinali, non trovano omologie nel vecchio macronucleo. A questo punto gli scnRNAs rimasti migrano nel nuovo macronucleo in via di sviluppo, sempre associati alla proteina Twi1. Nel nuovo macronucleo, non ancora sviluppato, le sequenze germinali sono ancora presenti: gli scnRNA si appaieranno per omologia ad esse ed il complesso Tw1 effettuerà una metilazione H3K9. Dopodiché, il reclutamento di un proteina per la degradazione programmata di DNA (Pdd1) concluderà il meccanismo. Pdd1 userà le metilazioni H3K9 come segnale per degradare le sequenze marcate dagli scnRNAs. Questo sistema, oltre ad avere il compito di “pulire” il genoma dei macronuclei da sequenze germinali dei micronuclei, effettua un controllo sul genoma dei macronuclei in neo formazione controllandoli con quelli vecchi ed accertandosi che durante la coniugazione, o per altri motivi, non si siano instaurate sequenze estranee, come per esempio trasposoni. Silenziamento meiotico Durante la ricerca sul silenziamento genico è sempre stata considerata la possibilità che omologie DNA-DNA potesse essere un iniziatore dell’RNAi. In effetti un sistema basato su principi pressoché identici fu trovato per la prima volta nel fungo Ascobolus immersus, caratterizzato da un micelio molto filamentoso. Successivi studi su N.crassa permisero di disegnare un modello del meccanismo in questione, applicabile quindi a diversi organismi. Figura 15: Possibile modello del silenziamento a livello di appaiamento cromosomico durante la meiosi. 29 In diverse specie, il silenziamento di zone non appaiate del genoma avviene durante la meiosi. Analisi genetiche su N. crassa hanno dimostrato che per questo processo di silenziamento è necessaria una RNA polimerasi RNA-dipendente (RdRP) e una proteina della famiglia degli Argonauti (AGO), distinte però da quelle già coinvolte in altri fenomeni di silenziamento genico. In N. crassa il silenziamento meiotico avviene attraverso un passaggio di controllo in trans a livello dei cromosomi omologhi (linee tratteggiate blu tra i due cromosomi, ciascuno disegnato come linea blu continua, fig.15). Ogni regione che non è appaiata (cappio giallo) è trascritta, presumibilmente, da una RNA polimerasi-DNA dipendente. Il ssRNA risultante (cappio rosso più interno) viene usato come templato dalla RdRP Sad1 per sintetizzare dsRNA. Questo dsRNA è probabilmente processato da Dicer (DCR) in piccoli RNA (siRNA). La presenza di questi piccoli RNA in questo processo non è però ancora stata confermata. Anche se i precisi eventi che susseguono questi iniziali passaggi non sono ancora ben chiari, si presume che i siRNA vengano incorporati nella proteina argonauta sopraccitata in un complesso tipo RISC (RNA-induced silencing complex), il quale, attivandosi, va a degradare i trascritti omologhi alla sequenza interna , anche nel caso essi derivino da sequenze che non hanno difetti di appaiamento durante la meiosi (linee gialle parallele). Osservazioni Le scoperte fatte su diversi organismi hanno portato a rivelare i diversi ruoli dell’RNAi nel silenziamento sequenza-specifico a livello genomico. Anche se l’ubiquità dei fenomeni sembra permettere di generalizzare il meccanismo, è da considerare il fatto che gli organismi in cui si manifestano i fenomeni di metilazione e rimodellamento della cromatina possiedono già un sistema dedito a queste funzioni, indipendente dell’RNAi. L’RNAi assume così anche un consistente ruolo nella difesa da sequenze invasive, quali possono essere trasposoni o sequenze ripetute. Quindi, anche se tali sequenze vengono spesso considerate come “parassite”, azionando i meccanismi sopra descritti, beneficiano l’ospite a livello di regolazione genica e di struttura e funzione dei cromosomi. Molto è stato scoperto, e ancora di più rimane da conoscere per quanto concerne le vie di silenziamento a livello nucleare. I futuri studi saranno diretti soprattutto a costruire 30 modelli sul ruolo di questi processi nell’organizzazione della struttura e della funzione dei cromosomi. Silenziamento mediato da un singolo filamento Silenziamento mediato da filamento antisenso Prima della messa a punto di tecniche in grado di sfruttare il fenomeno dell’RNAi mediato da dsRNA, il sistema più frequentemente usato per generare PTGS in piante era la produzione di RNA antisenso tramite l’espressione di un transgene. I costrutti antisenso consistono di una sequenza complementare all’mRNA bersaglio, sotto il controllo di un promotore forte e costitutivo. L’appaiamento del filamento antisenso con l’mRNA ne blocca la traduzione e lo rende bersaglio di RNAsi specifiche. Negli esperimenti con RNA antisenso, in genere, si ha una efficienza in una percentuale che varia dal 5 al 20 %. La degradazione dell’mRNA varia da individuo a individuo: da nessun effetto al 99% di mRNA degradato. L’efficienza è in strettissima relazione con l’omologia esistente fra il costrutto antisenso e l’mRNA. Saggi nucleari RUN-ON (Bourque, 1995) mostrano che anche in questo caso la trascrizione del DNA non è affetta dall’introduzione del costrutto indicando un azione esclusivamente a livello post-trascrizionale. Altri possibili meccanismi sono stati pensati; una delle ipotesi più facilmente immaginabili è la formazione di dsRNA aventi come templato il filamento antisenso; tale fenomeno sembrava plausibile dal momento che i dsRNA sono ben noti iniziatori di RNAi. Ciò nonostante, Stam et al. (2000) hanno dimostrato che un’altra possibile spiegazione è la formazione di duplex di RNA grazie alla trascrizione del filamento antisenso e di un costrutto inseritosi in direzione inversa, rispetto al primo, in zone che fornissero sequenze consenso di inizio trascrizione. Questo porta alla formazione di un unico filamento di RNA la cui struttura secondaria genererà un duplex funzionale all’iniziazione dell’RNAi. Silenziamento mediato da filamento senso: la co-soppressione Nell’esperimento di Jorgensen, citato nei primi paragrafi della tesi, il gruppo di ricerca, introducendo un transgene codificante per la calcone sintasi (chs) sotto un promotore forte e costitutivo, invece di ottenere un incremento della pigmentazione dei petali in 31 petunia, osservava oltre al silenziamento del transgene anche quello del gene endogeno, con fiori a fenotipo privo di pigmentazione. Da questo esperimento venne coniato il termine co-soppressione, derivato da “co-senso soppressione” (soppressione sia del transgene senso che del gene endogeno). La causa scatenante era, in quel caso, una sovraespressione del gene. Come avveniva per il silenziamento mediato dal solo filamento antisenso, anche in questo caso erano solo poche le piante trasformate che risultavano silenziate (5-20%). Entrambi i silenziamenti, mediati da singolo filamento, si caratterizzavano quindi per una moderata efficienza. Anche in questo contesto si era pensato a meccanismi attribuibili alla trascrizione di costrutti invertiti, ma prove sperimentali su base genetica dimostravano che si trattava di un meccanismo ben diverso dal precedente. Gli studi su Arabidopsis fecero emergere la necessità della presenza dei geni sde1/sgs2 per l’instaurarsi di un fenomeno di PTGS mediato da solo costrutto senso. Tali geni, infatti, codificano per una RdRP (RNA polimerasi RNA dipendente) che userebbe come templato il filamento senso generandone il complementare su di esso. A questo punto il dsRNA ottenuto entra facilmente nel meccanismo dell’RNAi passando per Dicer e poi RISC. Il modo con cui questi mRNA senso vengono processati da RdRP non è però ancora conosciuto. Alcune ipotesi prevedono l’instaurarsi di un livello soglia di mRNA trascritto che faccia attivare l’RdRP (“threshold theory”) in caso di sovraespressione. Un’altra probabile spiegazione è che la sovraespressione generi mRNA aberranti che vengono captati dalla RdRP. Diffusione sistemica dell’RNAi e suoi repressori Un possibile “sistema immunitario” In molti organismi (piante e nematodi) si è osservata la capacità di diffusione del “segnale” di silenziamento genico dalle cellule da cui è scaturito ad altre più distanti. Un esperimento esemplificativo di questo fenomeno è stato quello eseguito da Voinnet e Baulcombe (1997). Piante di Nicotiana benthamiana trasformate per la produzione di GFP venivano infettate localmente (su una foglia) da virus che, trasformato a sua volta, portava una sequenza senso del gene della GFP. La pianta prima dell’infezione, vista la sua costitutiva espressione di GFP, mostrava una fluorescenza diffusa se sottoposta agli UV. Nel momento in cui essa veniva localmente attaccata dal virus, l’entrata nelle 32 cellule dell’RNA virale provocava l’instaurarsi di un meccanismo di silenziamento genico contro le sequenze introdotte (GFP). Ciò dimostrava che il meccanismo Figura 16: silenziamento diffuso sistemicamente ad opera dell’infezione da virus portatane il gene di GFP, già espresso endogenamente nella pianta. Figura 17: particolare di una diffusione sistemica totale del silenziamento di GFP mediato da A.tumefaciens dell’RNAi si è evoluto anche come sistema di difesa contro sequenze virali. L’analisi sotto UV della foglia infettata mostra un calo dell’espressione endogena di GFP. Questo fenomeno è riferibile alla co-soppressione (silenziamento del gene esogeno in concomitanza di quello endogeno). Tuttavia, col passare del tempo si osservava una diffusione del silenziamento al di fuori della zona infettata, fino ad interessare l’intera pianta (Fig.16). Risultati simili furono ottenuti con infezione da A. tumefaciens (Fig.17). Altri esperimenti hanno in seguito dimostrato che un’infezione da virus genera una resistenza ad esso che si diffonde per tutta la pianta rendendola “immune” ad attacchi successivi (fenomeno denominato “recovery”). Il meccanismo di questa diffusione non è ancora chiaro. Quasi sicuramente si tratta di un trasporto di sequenze che, raggiunte le cellule distanti, vengono usate come templato per generare il silenziamento sequenza-specifico. Queste sequenze, probabilmente di RNA, vengono trasportate attraverso il floema da una proteina o da un complesso proteico non ancora definito. In C.elegans si è scoperto che il gene SID-1 è coinvolto nella diffusione (probabilmente nel trasporto delle sequenze segnale) del silenziamento attraverso l’intero organismo (vedi paragrafi iniziali sulle scoperte in C. elegans). A carico di questa diffusibilità di segnale vi è sicuramente (accertato da prove sperimentali) il ruolo della RdRP (Fig.18). Questa può essere di origine virale o codificata dalla pianta stessa, tramite i geni SDE1/SGS-2 (chiamati anche RDR6). Questa (vedi paragrafo: “RNA polimerasi - RNA dipendente: un sistema di amplificazione”) fornisce un efficiente sistema di amplificazione del segnale generando 33 duplex funzionali al meccanismo di silenziamento ed usando come templato l’RNA virale, mRNA aberrante, siRNA stessi (Fig.18). Ciò permette un’elevatissima efficienza anche a bassissime dosi di inoculo. Come vedremo nei paragrafi successivi, però, questo meccanismo non ha sempre la strada libera: in molti casi, infatti, si interpongono meccanismi di soppressione del silenziamento evoluti dai virus stessi. Figua 18: Sistema con cui le sequenze virali possano innescare il meccanismo di silenziamento specifico. Molto importante è il ruolo della RdRP che permette di perpetuare ed amplificare il segnale, rendendolo disponibile anche per una diffusione sistemica, oltre che a tutti gli altri possibili sistemi di silenziamento (PTGS e TGS). I repressori virali: p19 Sulla scorta di quanto riportato precedentemente, si potrebbe affermare che le piante dispongono di un sistema che le difenderebbe da qualsiasi attacco virale. Tuttavia, purtroppo, i virus hanno sviluppato la capacità di sintetizzare soppressori dell’RNAi. Una tra le proteine più studiate, nonché la più attiva nei sistemi virus vegetale - pianta è la p19 dei tombuvirus. Questa è stata studiata cristallizzata, mostrando di essere complessata con duplex di RNA di 21 bp (Fig.19). La sua particolare struttura, che lega le estremità terminali del duplex di RNA, Figura 19: p19 cristallizzata. funziona come un calibro che seleziona molecole di una certa lunghezza e struttura terminale (Fig. 21). 34 Si è infatti analizzato che la proteina p19 lega duplex con filamenti lunghi 20-22 bp e con una porzione appaiata di 18-20 bp, lasciando quindi estremità libere al 3’ di 2 nucleotidi (Fig. 20). Figura 20: specificità di legame di p19. Figura 21: Modello di legame tra p19 e duplex di RNA. Le “reading head” sono le porzioni che discriminano la selettività ai duplex in base alla lunghezza e ai 2 nucleotidi liberi. La maggiore affinità si è mostrata per duplex di filamenti lunghi 21 bp. La p19 lega i siRNA in forma omodimerizzata, costituendosi di una parte centrale (“core”) che lega l’elica di RNA semplicemente sulla struttura zucchero-fosfato. Le porzioni ad α-elica riconoscono invece le parti terminali del duplex, costituite dai 2 nucleotidi liberi al 3’, eseguendo un controllo sulla lunghezza. Figura 22: Il virus wild-type, attraverso la sintesi di p19 blocca i siRNA (in arancione) che diffondendosi silenzierebbero l’RNA virale (sequenze nere). Il virus deficitario per la p19 (Cym19Stop), invece, non potendo bloccare la diffusione dei siRNA viene silenziato e non si diffonde. 35 Esperimenti su Nicotiana benthamiana hanno dimostrato che infezioni con Cymbidium Ringspot TombusvirusII, deficitario della sequenza codificante per la p19 (Cym19stop), vengono contrastate dal silenziamento genico innescato dalla pianta come difesa immunitaria, non permettendo la diffusione del virus. A controprova il virus wild-type (CyMRSV), bloccando le sequenze segnale che avrebbero diffuso il silenziamento dell’RNA virale, può diffondersi nella pianta causandone la morte (Fig.22). La pianta, se in seguito ad infezione da virus Cym19Stop, viene infettata con virus wild-type, mostra la capacità di resistere a quest’ultimo silenziandone, in tutti i tessuti, l’RNA. Questo risultato dimostra che le sequenze segnale, generate dall’infezione di Cym19Stop, oltre ad essersi diffuse permangono nelle cellule come “memoria” e rendono la pianta immune a successivi attacchi dello stesso virus (“recovery”). La proteina p19 ha inoltre dimostrato di avere effetti sullo sviluppo delle piante andando ad interagire con il sistema di regolazione mediato dai miRNA. E’ comunque appurato che questo repressore agisce solo a livello dei dsRNA liberi; non ha invece alcun effetto su complessi RISC che hanno già incorporato i siRNA o i miRNA. Altri repressori Sono state identificati altri elementi endogeni che agiscono negativamente sul meccanismo dell’RNAi. Uno di questi è costituito da ADARs, una adenosina deamminasi dsRNA specifica, la cui azione catalitica consiste nel convertire le adenosine in inosine. Questo editing dei dsRNA, oltre a toglierne la complementarietà agli mRNA, li rende incapaci di incorporarsi in Dicer. Un altro gene, la cui funzione è stata riscontrata nei neuroni di C. elegans, è ERI-1. Mutanti di questi geni mostrano una maggiore attività da parte dell’RNAi. Anche in questo caso, saggi biochimici hanno evidenziato che il substrato di ERI-1 sono i siRNA. Sempre in C. elegans, RFR-3, codificante per una famiglia di RdRP inattive, porterebbe ad una competizione negativa della RdRP funzionale per lo stesso substrato (vedi Fig.5 in “Il ruolo dei microRNAs (miRNA) nello sviluppo delle piante”). Un altro soppressore dell’RNAi è Hc-Pro, codificato dai Potyvirus, che agisce bloccando l’attività del complesso RISC, ma non la sua formazione. 36 Ingegnerizzazione dell’RNAi Progettare i siRNA Le metodologie con cui viene progettato un siRNA sintetico sono un aspetto molto importante della ricerca per ottenere risultati accettabili nelle prove di silenziamento. Nel disegno di un siRNA funzionale vi sono parametri di base che devono essere considerati. La regione target deve essere a valle del codone di inizio traduzione ad una distanza che varia dalle 50 alle 100 bp; l’mRNA target deve avere al 5’ una sequenza AA(N19)UU, possedere un contenuto di GC del 50% circa, sono da evitare le regioni UTR sia al 5’ che al 3’e le regione ricche di G (Elbashir et al., 2002). Ad oggi molte ditte private offrono un servizio personalizzato di sintesi di siRNA; alcune di esse sono Dharmacon, Quiagen, Ambion, MWG. Yang et al. (2002) e Vickers et al. (2003) hanno sviluppato un metodo per ottenere una migliore efficienza nella degradazione dell’mRNA bersaglio. Questo consiste nel disegnare siRNA che sia complementari a siti notoriamente sensibili all’attività dell’RNAsi H. Inoltre, recenti test hanno dimostrato che in molti casi sono più efficienti siRNA di 27 bp rispetto ai classici di 20-22 bp. Ciò probabilmente favorisce una migliore incorporazione nel complesso RISC, dal momento che queste molecole possono essere ancora tagliate da Dicer. Con il crescente interesse rivolto a queste nuove metodologie di silenziamento genico, sono stati sviluppati appositi software che attraverso algoritmi specifici, generano i migliori siRNA possibili, applicabili ad un determinato mRNA target. La potenzialità di questi software, abbinata alla possibilità di allineare, attraverso BLAST, tutte le possibili sequenze presenti nelle banche dati, permette di trovare con notevole facilità tutti i possibili target per la costruzione di un siRNA. Possono così essere individuati geni che potrebbero essere silenziati collateralmente o possibili altri bersagli in diversi organismi. Come descritto in precedenza, i semplici siRNA, in alcuni casi, non sono in grado di generare un silenziamento. Questo può essere dovuto al fatto che essi, non essendo naturalmente processati dall’enzima Dicer, possono non integrarsi correttamente nel meccanismo. Un’altra ragione, come riscontrato nei mammiferi, è lo scatenarsi della risposta immunitaria, mediata da interferone, all’introduzione di dsRNA nell’organismo; l’interferone genera un silenziamento totale della trascrizione come risultato. Nel prossimo paragrafo verranno quindi trattate metodologie di ingegneria 37 genetica utilizzate per la creazione di costrutti, in grado di generare precursori dei siRNA, introducibili nel genoma ospite senza la produzione di interferone. Molecole sintetiche In figura 23 sono mostrate le possibili molecole iniziatrici del processo di RNAi sintetizzabili in vitro, e direttamente introducibili nell’organismo, al fine di ottenere il silenziamento genico desiderato. Le molecole più semplici sono piccoli RNA sintetizzati chimicamente (siRNA); una volta introdotti nell’organismo non devono essere processati dall’enzima Dicer in quanto emulano già un suo possibile prodotto, e vengono direttamente incorporati nel complesso RISC, guidando la degradazione dell’mRNA (Fig.23a). Lunghi dsRNA devono invece essere processati da Dicer per generare diversi siRNA (Fig.23b). Vengono anche sintetizzati duplex di RNA a forcina con perfetta complementarietà dei bracci; anch’essi, tagliati da Dicer, generano siRNA funzionali (Fig.23c). In ultimo sono resi disponibili duplex di RNA a forcina con una non perfetta complementarietà tra i bracci (Fig.23d): essi emulano i pre-miRNA che fuoriescono dal nucleo e una volta processati da Dicer generano miRNA che guidano il silenziamento post-trascrizionale (per degradazione di mRNA in caso di perfetta complementarità con esso; per blocco della traduzione in caso di appaiamento parziale; vedi paragrafo “Silenziamento mediato dai miRNA”). Figura 23: molecole sintetiche utilizzabili per indurre l’RNAi artificialmente 38 Sistemi di espressione mediati da RNA polimerasi II In organismi o cellule che non possiedono, o in cui è debole, una risposta mediata da interferone è possibile utilizzare costrutti che esprimono sequenze che si conformano a forcina. Questi costrutti sfruttano i promotori della RNA polimerasi II (pol II) per guidare la loro espressione e generare sequenze a forcina che verranno processate da Dicer in molteplici siRNA (Fig. 24a). Le strutture a forcina, con i dovuti accorgimenti, possono anche emulare la struttura di pre-miRNA ed entrare nel processo di silenziamento come tali, effettuando un silenziamento per via degradativa o per blocco della traduzione (Fig.24d). Questi sistemi di espressione hanno permesso di indurre silenziamento in diversi organismi quali oociti di topo, C.elegans, D.melanogaster e permettono un’espressione dell’RNA inducibile a livello tessuto-specifico e cellulaspecifico. Ad esempio, Kennerdell e Carthew (2000) hanno messo a punto su Drosophila un sistema inducibile da Gal-4 che avesse come bersaglio il gene della ßgalattosidasi. L’attivazione del transattivatore Gal-4 era posta sotto il controllo del promotore di hsp70 (heat shock protein 70); ne risultava una trascrizione inducibile con il semplice aumento della temperatura. Nei mammiferi questo tipo di approccio, purtroppo, non è ad oggi percorribile perché la sintesi di interferone che si scatena rende vani i tentativi di utilizzare i lunghi duplex a forcina di RNA. Sistemi di espressione mediati da RNA polimerasi III Su diversi organismi sono stati sviluppati sistemi di espressione plasmidici che sfruttano l’azione dell’RNA polimerasi III, producendo piccoli RNA (siRNA), che non attivano alcuna risposta da parte dell’interferone. Due sono i principali promotori utilizzati: U6 e H1, entrambi membri della classe III dei promotori delle RNA polimerasi III. In alcuni casi, la classe III di questi promotori, a differenza della I e della II, ha la particolarità di non avere sequenze indispensabili per la trascrizione a valle del promotore. Infatti, in topo e uomo, si è sperimentato che la delezione della sequenza a valle di alcuni promotori U6 non genera effetti a livello trascrizionale. U6 e H1 contengono entrambi gli stessi set di elementi attivanti in cis (PSE, TATA box, ecc..); H1 possiede un’organizzazione più compatta di U6 e quest’ultimo richiede la presenza di una guanosina in posizione +1. Sono stati sperimentati due approcci per l’espressione mediata da promotori di polIII. Uno consiste nell’espressione separata del filamento senso e di quello antisenso da due 39 promotori indipendenti, in genere posizionati in tandem (Fig. 24b). Il secondo prevede l’utilizzo di un unico promotore a monte di una sequenza codificante per un shRNA (short hairpin RNA) a forcina. Questo trascritto sarà poi processato da Dicer, i cui tagli genereranno un siRNA funzionale per complessi RISC (Fig. 24c). Figura 24: sistemi di espressioni mediati da RNA polimerasi II e III. a- Trascrizione in un lungo dsRNA il cui taglio da parte di Dicer darà origine ad un siRNA funzionale. bSequenza senso e antisenso trascritte separatamente vanno incontro ad appaiamento formando siRNA. c- Trascrizione di shRNA che processati da Dicer formano un siRNA. d- Sequenze invertite e ripetute la cui struttura secondaria emula quella di un pre-miRNA, processabile da Dicer in miRNA maturi. Le sezione in verde sono gli spaziatori usati per consentire il ripiegamento della sequenza. Mentre l’RNA polimerasi II richiede la poliadenilazione come segnale di stop della trascrizione, l’RNA polimerasi III richiede un cluster di quattro o più residui di timina. Sono quindi più efficienti i filamenti separati o gli shRNA? La principale differenza fra i due risiede nel processamento degli shRNA da parte di Dicer. E’ difficile dire, in modo assoluto, quale delle due tecniche sia la più efficace ed occorre sempre considerare, nei mammiferi, la risposta interferonica a lunghi dsRNA. Hutvagner e Zamore (2002) hanno testato in parallelo i due approcci in estratti citoplasmatici di cellule HeLa*. L’introduzione di 100 nM di pre-miRNA di let-7, venivano processati da Dicer generando ~5 nM di miRNA maturi. Quest’ultima quantità di miRNA processati da Dicer aveva lo stesso effetto ottenuto con una prova parallela in cui venivano inseriti 100 nM di miRNA maturi sintetizzati artificialmente. * Hela: cellule tumorali immortali di Henriette Lacks, isolate da una biopsia nel 1951; sono caratteristiche di un ciclo cellulare velocissimo che ne ha permesso il diffondersi in tutto il mondo come campione per esperimenti. 40 Tale dato conferma che i dsRNA o gli shRNA processati naturalmente da Dicer sono meglio incorporati nel complesso RISC. ihpRNA Un ulteriore miglioramento della tecnologia di silenziamento, mediante shRNA, fu apportato dall’utilizzo degli ihpRNAs (intron-containing hairpin RNAs). Si tratta sempre di un costrutto contenente entrambe le sequenze ripetute e invertite a formare una struttura a forcina, ma la differenza sta nella presenza di uno spaziatore. Si dimostrò (Smith et al., 2000) che costrutti aventi come spaziatore un sequenza riconosciuta come intronica vengono meglio processati ai fini dell’RNAi. Alla base di questo fenomeno vi è lo splicing che normalmente avviene nel nucleo. Non è ancora ben chiaro come la presenza di un introne nella regione spaziatrice possa migliorare l’efficienza dei costrutti; si è comunque ipotizzato che lo splicing dell’introne permetta un migliore allineamento tra i due bracci della forcina favorendo la formazione del duplex di RNA. A questo proposito sono stati creati vettori plasmidici (per la clonazione di ihpRNA in batteri) già ingegnerizzati e contenenti un regione intronica. Ai lati di questo introne sono presenti i siti di restrizione specifici e diversificati che permettono l’inserimento di prodotti di amplificazione, quali il filamento senso e quello antisenso che appaiandosi genereranno il dsRNA funzionale all’RNAi (Fig.25 e 26). I batteri usati per la clonazione dei plasmidi sono in genere E. coli e A. rhizogenes, il quale può essere direttamente usato per infettare la pianta. I più noti plasmidi ingegnerizzati per la trasformazione con ihpRNA sono pHANNIBAL e pHELLSGATE (CSIRO, Australia) Figura 25: struttura del plasmide pHANNIBAL. Il promotore CaMV 35S ricavato dal Cauliflower mosaic virus è sfruttato per la trascrizione in pianta. La resistenza ad ampicillina è usata come marcatore di selezione (sequenza blu) per i batteri trasformati. 41 Figura 26: struttura del costrutto inserito tra LB ed RB in A. tumefaciens, sotto il controllo del promotore costitutivo 35S (per la trascrizione in pianta dopo la trasformazione ad opera del batterio). A seguito è riportato un elenco dei probabili fattori determinanti nell’efficienza di silenziamento genico mediato da siRNA: • • • • • • • • • • Incorporazione e stabilità all’interno del complesso RISC dei siRNA e miRNA Complementarietà con l’mRNA Sito di taglio dell’mRNA Sito di complementarietà tra siRNA/miRNA e mRNA Frequenza di traduzione dell’mRNA Struttura secondaria e terziaria dell’mRNA Legami dell’mRNA con proteine Quantità di polisomi ancorati all’mRNA in traduzione Abbondanza ed emivita degli mRNA bersaglio Localizzazione subcellulare Sovraespressione di Esportina-5 Plasmidi e vettori virali che esprimono shRNAs si sono affermati come strumenti essenziali per l’inibizione stabile di specifici geni. I shRNAs sono funzionalmente e strutturalmente omologhi ai pre-miRNA, gli intermedi della produzione endogena di mi-RNA. La sovraespressione di shRNAs si è dimostrata competitiva per un fattore limitante nella via biosintetica dei miRNA (Rui et al., 2005): l’esportina 5, la cui attività può essere saturata dall’abbondante presenza di shRNA, i quali, come i pre-miRNA, la utilizzano per essere trasportati al di fuori del nucleo. Tuttavia, mentre la sovraespressione di shRNAs può inibire la funzione dei miRNA, la sovraespressione di esportina 5 può avere un effetto diametralmente opposto. Inoltre, questo incremento di trasporto extra-nucleare può potenziare il silenziamento genico mediato da shRNAs e rappresentare un validissimo metodo per migliorare l’RNAi in coltura e per future applicazioni a livello clinico. 42 Tecniche di somministrazione e trasformazione in pianta • Metodi bio-balistici (transienti) • Trasformazione stabile (elettroporazione, Agrobacterium, PEG) • Agroinfiltrazione • VIGS Metodi bio-balistici Il bombardamento di particelle può essere usato per introdurre temporaneamente costrutti di DNA che producono dsRNA (Kjemtrup et al., 1998; Schweizer et al., 2000; Peele et al., 2001). Il DNA o il dsRNA è adeso a particelle di tungsteno o di oro che, attraverso una pistola vengono sparate ad altissima velocità e attraversano la parete cellulare. La presenza di dsRNA nelle cellule bombardate risulta nel silenziamento di un determinato gene. Questo metodo, pur essendo molto rapido, presenta considerevoli inefficienze. Una di queste è dovuta al fatto che solo pochi strati di tessuto possono essere bombardati, escludendo la possibilità di analizzare gli effetti del silenziamento sull’intero organismo. Questa tecnica, perciò, viene evitata in esperimenti mirati a studiare il ruolo di geni coinvolti nello sviluppo. Inoltre, tale metodologia presenta una bassa efficienza, in quanto poche cellule effettivamente ricevono dsRNA e molte, a causa del bombardamento, vengono uccise. Infine, il silenziamento non viene ereditato e rimane circoscritto al tessuto bombardato. Nonostante queste limitazioni, la tecnica, non presentando limitazioni biologiche, viene comunque usata per piante recalcitranti alla trasformazione stabile. Il bombardamento viene anche usato per analisi di singole cellule, dove lo studio è limitato a processi che si mostrano a questo livello e sono autonomi nelle singole cellule (per esempio, vie biosintetiche). Il metodo bio-balistico è anche largamente usato per studi su resistenze a malattie (Schweizer et al., 2000; Azevedo et al., 2002). Agroinfiltrazione I problemi che emergono nel trasformare artificialmente cellule vegetali possono essere aggirati tramite Agroinfiltrazione. Questa tecnica sfrutta le capacità naturali di 43 trasformazione di Agrobacterium tumefaciens su pianta. Venne usata per la prima volta nel 1997 (Schob et al.), nel tentativo di ottenere il silenziamento attraverso l’introduzione di dsRNA, ma può anche essere utilizzata per introdurre vettori VIGS (descritti in seguito). Il costrutto viene inserito nel plasmide di Agrobacterium, il quale viene coltivato e poi usato per l’inoculo. Le colture di Agrobacterium possono essere inoculate attraverso semplice infiltrazione sulle foglie della pianta; la sequenza introdotta viene integrata nel genoma e la sua trascrizione genera dsRNA, “azionando” il PTGS. E’ una tecnica rapida, facilmente realizzabile e con un basso costo; permette inoltre di agire direttamente su piante intere, senza la necessità di lavorare su protoplasti. L’effetto dell’introduzione del gene di interesse viene quindi valutato a livello dell’intero organismo. Questo metodo è molto utile soprattutto se si vogliono esaminare più geni contemporaneamente: basta co-infettare con cloni batterici contenenti i diversi costrutti di silenziamento. Trasformazione stabile La trasformazione stabile consta nell’integrazione di un gene esogeno nel genoma nucleare. Più di 120 specie di piante possono essere stabilmente trasformate, includendo le coltivazioni commerciali di maggior rilievo (alimentari, ornamentali, medicinali, fruttifere e foraggiere (Birch et al., 1997). Quattro sono i metodi disponibili: • Bombardamenti di DNA • Inserimento di DNA in protoplasti e colture cellulari attraverso PEG • Elettroporazione di protoplasmi e cellule intatte • Trasformazione mediata da A. tumefaciens Ognuna di queste metodologie varia notevolmente a seconda della specie in questione. La trasformazione stabile di un costrutto nel genoma, che produca ds-RNA, risulterà in un silenziamento del gene d’interesse in ogni cellula della pianta generata. La trasformazione del genoma in maniera persistente è un utile mezzo attraverso il quale si studiano le funzioni dei geni. Ciò nonostante è un processo che richiede tempo e non è ottimale per screening su larga scala. Inoltre, l’esperimento è inattuabile se il silenziamento è letale a livello embrionale o nei primi stadi di sviluppo. 44 Molte specie possono essere trasformate attraverso A.tumefaciens o A. rhizogenes, i quali introducono il loro DNA, stabilmente, nel genoma della pianta (Tepfer et al., 1990; Bent et al, 2000). In natura, A. tumefaciens porta un plasmide Ti che possiede i geni di virulenza (vir) e specifiche sequenze segnale che, assieme ai geni nucleari, mediano l’escissione, il trasferimento e l’integrazione del T-DNA nel genoma della pianta (Zupan et al., 2000). Il T-DNA è affiancato da sequenze ripetute di 25 bp, il “left border” e il “right border” (LB e RB). Il plasmide Ti può essere modificato e portare il DNA desiderato al posto della sequenza batterica di T-DNA. Infatti A. tumefaciens trasferisce qualsiasi sequenza contenuta tra LB ed RB (Zupan et al., 2000). La pianta più trasformata con A. tumefaciens è A. thaliana. Le piante in fioritura vengono semplicemente bagnate con una sospensione del batterio. I semi vengono poi raccolti e fatti germinare su di un substrato selettivo. Solo le generazioni T0 trasformate con successo saranno in grado di crescere sul substrato selettivo. Il fenotipo delle piante silenziate verrà poi analizzato nella generazione T1. I protocolli di trasformazione che invece richiedono l’isolamento di protoplasti sono molto difficoltosi e dispendiosi in termini di tempo. Dopo l’isolamento di protoplasti, questi vengono trasformati attraverso bombardamenti con particelle, introduzione di DNA attraverso PEG (glicole polipropilenico) o infezione da Agrobacterium. I protoplasti vengono tenuti su di un mezzo di coltura che promuova la crescita callosa e selezioni le cellule contenenti il costrutto. Da questi calli vengono poi generate le piante. Dopo aver confermato attraverso marcatori molecolari l’avvenuta crescita di piante trasformate, si potranno osservare i fenotipi della progenie di quest’ultime. E’ stata anche sviluppata una procedura per introdurre costrutti in gruppi di cellule di riso attraverso elettroporazione (Arencibia et al., 1998). Gli embrioni germinati vengono messi su terreno e indotti a callo per 2 mesi, al buio. Dopo ciò, un gruppo di cellule viene preso, diluito in una soluzione per elettroporazione con i plasmidi di interesse ed elettroporato. Le cellule vengono quindi ri-piastrate su terreno calloinducente e lasciate moltiplicare per 2 settimane al buio. La percentuale di successi di questo approccio è dell’1,5% (Arencibia et al., 1998). Sebbene molte piante possano essere trasformate, (con eccezione di Arabidopsis) questi metodi risultano troppo laboriosi e con una bassa percentuale di successo. 45 VIGS (Virus-induced gene silencing) La maggior parte dei virus delle piante possiedono un genoma a ssRNA il quale viene rilasciato all’esterno del rivestimento proteico delle particelle virali per andare ad insediarsi all’interno della cellula ospite e replicarsi attraverso una RdRP (RNA polimerasi RNA-dipendente) codificata dal virus stesso. Tale replicazione genera filamenti senso ed antisenso dello stesso templato i quali hanno la potenzialità di ibridarsi a formare dsRNA. Analogamente a quanto accade nei mammiferi, il meccanismo dell’RNAi processa i dsRNA in filamenti più corti (siRNA) per utilizzarli come templato ed andare a degradare l’mRNA o il ssRNA virale complementare. Questi dati supportano l’ipotesi che il meccanismo dell’RNAi si sia co-evoluto in diversi organismi come sistema di difesa da infezioni virali, oltre che da elementi trasponibili. I virus dispongono di caratteristiche che li rendono particolarmente utili per la ricerca su piante. L’RNA “nudo” (senza la protezione della particella virale) di molte specie di virus vegetali può essere usato direttamente per causare l’infezione. Questo RNA può essere ottenuto in vitro attraverso la trascrizione di un clone di cDNA che codifica per l’intera sequenza virale (Fig.27a). Analogamente, l’intero cDNA virale può essere inserito in un plasmide T-DNA, espresso sotto il controllo del promotore 35s di CaMV (cauliflower mosaic virus), un forte promotore costitutivo, e trasfettato in pianta attraverso agroinfiltrazione (Fig.27b,27c); questo risulterà in un infezione generata senza la presenza iniziale del virus. E’ anche possibile introdurre una sequenza esogena in una specifico locus del genoma virale mantenendo l’infettività del trascritto. Quando questo trascritto viene usato per infettare le piante, anche la sequenza introdotta artificialmente diventa bersaglio del meccanismo dell’RNAi. Ma se il virus porta artificialmente sequenze geniche della pianta stessa, si può ottenere un silenziamento specifico dell’mRNA endogeno della pianta e successivamente è possibile osservare il fenotipo deficiente di tale gene. Questo metodo, chiamato VIGS (virus induced gene silencing), è molto utilizzato in piante per analizzare la funzione dei geni. Anche se Nicotiana benthamiana è stata la prima specie sulla quale è stato applicato il VIGS, tale approccio è stato successivamente applicato in molte altre piante, tra cui A. thaliana. Il VIGS ha permesso di studiare diversi geni, da quelli implicati in vie biosintetiche a quelli coinvolti nella resistenza a patogeni e, sorprendentemente, è stato osservato che il silenziamento genico avveniva anche nelle zone meristematiche. Poichè è noto che i 46 meristemi non vengono infettati da virus, ciò ha fatto dedurre che il silenziamento viene propagato sistemicamente, probabilmente attraverso i corti duplex di RNA (siRNA). Un’altra accortezza tecnica può essere quella di inserire un promotore della pianta stessa all’interno del costrutto virale; questo approccio si è mostrato aumentare notevolmente l’efficienza del silenziamento. Gli esperimenti di maggior successo sono stati effettuati utilizzando come vettori TMV (tobacco mosaic virus), PVX (potato virus X), TRV (tobacco rattle virus) e come bersaglio del silenziamento geni reporter di piante trasformate come GFP e GUS, o geni endogeni come PDS (phytoene denaturasi, i cui fenotipi silenziati mostravano un imbianchimento delle foglie a causa della compromessa sintesi di clorofilla). Un nuovo sistema di silenziamento mediato da virus è quello che prevede l’inserimento della sequenza bersaglio nell’RNA satellite del virus che verrà inoculato. Questa tecnica è detta SVISS (satellite virus induced silencing system) e si è mostrata funzionare molto bene, soprattutto con TMV, su oltre una decina di geni endogeni (Gossele et al.,2002). Nella maggior parte degli esperimenti con il VIGS si è riportato un silenziamento a livello post-trascrizionale. Ciò nonostante, come si è visto usando TRV contenente la sequenza di un promotore della pianta, il VIGS non era solo a livello post-trascrizionale. Si è infatti osservato un silenziamento anche a livello trascrizionale, accompagnato da una metilazione del DNA stampo dell’mRNA bersaglio; inoltre, questo silenziamento a livello trascrizionale, veniva ereditato nella progenie, anche in assenza del virus. L’osservazione di questo fenomeno ha suscitato molti interrogativi e sono molte le potenziali applicazioni di questo metodo. Figura 27: a- plasmide replicabile in E. coli, in cui PVX infettivo può essere trascritto in vitro attraverso il promotore T7 della polimerasi virale. b- un plasmide T-DNA propagato in Agrobacterium, il quale, una volta inoculato su pianta, inserisce nelle cellule infettate il DNA contenuto tra LB e RB. La sequenza contenente i geni virali è sotto il controllo del promotore 35S che rende il costrutto trascrivibile dalla pianta stessa in maniera costitutiva, generando PVX infettivo c- Sistema VIGS di TRV ottenuto con due diversi plasmidi T-DNA conteneti i diversi geni virali, più il gene bersaglio su uno dei due. I due plasmidi vengono usati per creare due ceppi di Agrobacterium per poi co-infettare la pianta ed ottenere un’infezione virale attiva oltre all’espressione del gene introdotto artificialmente. Target: gene bersaglio introdotto; RdRP, M1, M2, M3, CP : geni virali necessari per l’infezione; Term : terminatore della trascrizione necessario per i costrutti sotto il controllo del promotore costitutivo 35S. 47 Applicazioni mediche L’idea di usare l’RNAi come sistema terapeutico fuventilata più di quattro anni fa, a partire dal lavoro pionieristico di Tuschl et al. (2001) relativo alla somministrazione dei siRNA. Le possibili malattie trattabili da questo nuovo approccio includono le infezioni virali, il cancro e le aberrazioni genetiche dominanti ereditabili. Il virus dell’immunodeficienza umana (HIV) è stato il primo ad essere immaginato come possibile bersaglio di questa strategia. I geni virali chiave dell’HIV (tat, rev, nef e gag) sono stati silenziati, risultando in una efficiente inibizione della replicazione virale su cellule in coltura. Risultati simili sono stati ottenuti silenziando geni cellulari quali CD4, CCR5, CXCR4, necessari all’infezione virale. Anche il virus dell’epatite C (HCV), avente un genoma a singolo filamento di RNA, è stato studiato come bersaglio di una terapia di silenziamento genico mediata da RNAi, ottenendo buoni risultati su colture. Altri virus su cui sono stati sperimentati, con successo, approcci simili sono il papilloma virus (HPV), attraverso silenziamento dei geni E6 ed E7, il virus dell’epatite B (HBV), il virus dell’influenza (attraverso siRNA specifici per il nucleocapside o per componenti dell’RNA trascrittasi). I risultati sono stati incoraggianti ma necessitano di ulteriori prove, soprattutto per quanto concerne la loro efficienza e sicurezza in vivo su modelli animali (topo) e successivamente attraverso test clinici. La specificità di sequenza dell’RNAi lo predispone come uno strumento efficace per il silenziamento di geni mutati. Questa possibilità è stata provata per la prima volta su di un oncogene, K-RAS (V12), la cui mancata espressione risulta in un blocco della crescita tumorale in assenza di ancoraggio delle cellule al tessuto (Brummelkamp et al., 2002). L’espressione del gene mutato di K-RAS (V12) è stata inibita attraverso l’espressione di shRNA sotto il controllo di una versione retrovirale del promotore H1. Il silenziamento del gene mutato ha comunque lasciato inalterata l’espressione delle isoforme non mutate dello stesso. Questa prova ha riscontrato grande successo per il fatto che questi risultati non sono stati ottenuti solo su tessuti in coltura, ma anche in modelli animali (topo). Le malattie genetiche dominanti ereditabili sono tipicamente causate dalla mutazione di un allele il cui prodotto genico è visibile anche nell’eterozigote e prevale su quello non mutato. L’eliminazione del gene mutato permetterebbe a quello normale di restaurare le corrette funzioni cellulari. L’espansione delle regioni trinucleotidiche ripetute di CAG causano la codifica di tratti arricchiti di glutammine e sono responsabili di almeno otto 48 malattie neurodegenerative umane (tra cui la Corea di Huntington e la malattia di Kennedy). L’aggregazione delle poliglutammine mutate, anche se con meccanismo non ancora del tutto chiaro, genera una neurotossicità. SiRNA che hanno come bersaglio le sequenze al 3’ o al 5’ delle ripetizioni di CAG riescono ad inibire la tossicità in cellule coltivate aprendo la possibilità a nuovo approcci terapeutici. Altri esperimenti sono stati effettuati su molecole mutate responsabili di malattie genetiche. Un esempio è l’epatite fulminante indotta dal recettore Fas mutato, la cui espressione è stata ridotta con l’iniezione di siRNA specifici in topo (Song et al., 2003) Ci sono ancora molti problemi che devono essere risolti prima che l’RNAi diventi uno strumento utilizzabile nella terapia clinica. Per prima cosa, i siRNA devono essere introdotti in grande quantità ed in molte cellule, efficientemente e stabilmente. Questo problema può essere risolto attraverso modificazioni chimiche che aumentino la stabilità, penetrabilità e l’efficienza dei siRNA. Alternativamente i siRNA possono essere introdotti attraverso l’uso di un vettore virale. Possibili candidati a questo utilizzo sono i lentivirus, i quali hanno mostrat persistere maggiormente rispetto ai siRNA “nudi”. In aggiunta, l’utilizzo di promotori inducibili/reprimibili aiuterebbe ad ottenere una trascrizione dei costrutti controllata esternamente. Un altro problema è dato dalla presenza di mutazioni all’eliche che rendono la specificità di sequenza un ostacolo. Questo può essere aggirato con l’utilizzo di diversi siRNA che permettano l’appaiamento delle sequenze anche in presenza di geni variabili nella popolazione umana.. La ricerca si è ormai buttata a capofitto nello studio di tecniche efficaci che permettano l’utilizzo dell’RNAi come terapia contro le malattie che ancora ad oggi restano non curabili. Tra le recentissime innovazioni vi è una metodica che prevede l’endocitosi, da parte di specifiche cellule, di siRNA trasportati da anticorpi monoclonali (Song et al., 2005). Osservazioni Con il continuo evolversi dei metodi e delle conoscenze, la “reverse genetics” sta acquisendo sempre più un ruolo predominante nella ricerca di base. Ad oggi, infatti, i ricercatori possiedono le informazioni derivanti dai genomi sequenziati di diversi organismi e la possibilità di consultare tali dati attraverso l’uso dei database e dei 49 software per il calcolo computazionale di sequenze nucleotidiche ed amminoacidiche. L’RNAi è lo strumento necessario per accelerare le ricerche sulla funzione dei geni sequenziati (annotazione) oltre che essere utile come applicazione per le terapie cliniche. Per quanto concerne l’ambito vegetale, nei precedenti capitoli è stata descritta la vastità di funzioni biologiche in cui è coinvolto il fenomeno dell’RNAi, implicato nella regolazione a livello trascrizionale e post-trascrizionale, nella regolazione dello sviluppo, nella difesa dai virus e nel controllo degli elementi trasponibili. Un semplice fenomeno, con un complesso e finemente regolato meccanismo proteico. Le potenzialità di questo approccio nella “reverse genetics”meritano qualche ulteriore considerazione. La più importante, consiste nell’opportunità di silenziare un gene anche quando l’organismo in studio sia già adulto. Con le precedenti tecniche di mutagenesi, infatti, il genoma veniva modificato irreversibilmente già allo stadio di cellula uovo e questo costringeva l’organismo a crescere in maniera già compromessa rispetto ad un genotipo non mutato. In alcuni casi, la mutazione comprometteva addirittura la vitalità e/o lo sviluppo dell’organismo impedendone uno studio preciso, soprattutto nello studio dei sistemi animali. Con le nuove tecnologie basate sull’RNAi, attraverso la somministrazione di siRNA o l’uso di costrutti inducibili, il silenziamento genico può essere indotto e regolato in qualsiasi momento; in tal modo è possibile escludere gli effetti collaterali residui che portano sviluppi aberranti dell’organismo. Molte organizzazioni si stanno adoperando per creare librerie su larga scala per l’RNAi. Uno screening genomico fatto utilizzando queste librerie permetterebbe di acquisire molte conoscenze sui sistemi biologici, sulle vie metaboliche, biosintetiche e sui network di segnalazione presenti negli organismi. Un esempio applicativo molto interessante sarebbe l’acquisizione di informazioni sui processi che portano al ripristino delle normali condizioni cellulari dopo un’intossicazione, oppure lo studio sulle interazioni delle popolazioni con un determinato ambiente in base alla presenza o meno di determinati geni. In studio al ‘National Institute of Allergy and Infectious Disease nel gruppo di ricerca di Lieberman (Bethesda, USA), in collaborazione con il M I T (Massachusetts Institute of Technology), sono state pensate delle applicazioni dell’RNAi contro il bioterrorismo (flavivirus e poxvirus). Ciò che ancora rimane come una forte limitazione all’affermarsi di terapie basate sull’RNAi è la modalità di somministrazione dei siRNA (o dei shRNA); non è ancora completamente chiaro come far si che una dose appropriata di molecole arrivi nei siti target e sia funzionale, generando la risposta desiderata. Inoltre 50 l’eccessivo ottimismo iniziale è stato un po’ smorzato dal fatto che spesso i risultati ottenuti in vitro non sono replicabili in vivo; ed ancora, persiste la possibilità che la somministrazione di molecole sintetiche, quali i siRNA, scatenino un rilascio, a livelli tossici, di interferone o che il silenziamento prenda come bersaglio altri geni che non erano stati predetti. Per tali ragioni, in ambito medico, l’applicazione terapeutica dell’RNAi è ancora da considerarsi agli albori. In ambito vegetale, al contrario, l’assenza di un sistema immunitario e una specializzazione delle funzioni biologiche relativamente meno complessa, ha permesso di ottenere già da subito molti risultati, soprattutto a livello di genomica funzionale. Non da meno sono le applicazioni: molti sono i progetti di ricerca che prevedono il silenziamento di geni per il miglioramento di piante economicamente importanti o l’utilizzo dell’RNAi per ottenere resistenza a determinati virus vegetali. Un interessante esempio attinente a questi ultimi aspetti è il lavoro di Ogita et al. (2003), appartenente ad un gruppo di ricerca giapponese, che silenziando, attraverso l’RNAi, il gene della theobromina sintasi (CaMXMT1) in caffè, coinvolto nella sintesi della caffeina, hanno ottenuto piante naturalmente decaffeinate senza comprometterne nessun altro aspetto fisiologico. Nelle pagine successive verranno esaminati due casi di studio che possano servire come esempio di applicazioni dell’RNAi (silenziamento del gene Det1) o come lo stesso possa divenire una possibile spiegazione di fenomeni ancora non chiari (alleli HTH revertanti). 51 Caso di studio 1 Soppressione del gene DET1 attraverso RNA interference nel frutto di pomodoro aumenta il contenuto di carotenoidi e flavonoidi. Introduzione Un’alimentazione ricca di vegetali offre un insieme di nutrienti essenziali e contribuisce ad una migliore salute. Studi epidemiologici, infatti, dimostrano che un maggior consumo di frutta e verdure si manifesta in una riduzione del rischio di malattie di tipo tumorale e cardiovascolare. Vi è quindi un particolare interesse nello sviluppare prodotti destinati all’alimentazione ricchi in vitamine, flavonoidi e carotenoidi, poiché è noto che questi sono più benefici per la salute rispetto agli integratori alimentari. Il breeding tradizionale cerca di raggiungere questo risultato, ma non sempre è possibile ottenere piante con alto tenore in bio-metaboliti, spesso a causa della ristretta base genetica. L’approccio transgenico è una valida alternativa, ma esiste un problema generalizzato di accettazione da parte dell’opinione pubblica, la quale non vede di buon occhio questo tipo di tecnologie, soprattutto se si tratta dell’inserimento di geni provenienti da altri organismi. Le bacche di pomodoro e i derivati della loro lavorazione sono, in tutto il mondo, la maggiore fonte dietetica di licopene ed inoltre contengono un’elevata quantità di ßcarotene. Una grande quantità di licopene conferisce al frutto migliori qualità organolettiche e cromatiche, che si correlano con il miglioramento dei valori nutrizionali, soprattutto per il contenuto in antiossidanti. Si è dimostrato, infatti, che una dieta ricca di licopene è associata ad una diminuzione del rischio di infarti ed aiuta nella prevenzione contro alcuni tipi di tumori, soprattutto quello alla prostata. Il ßcarotene è il più potente precursore della vitamina A; il suo deficit è uno dei più diffusi problemi alimentari nel mondo e riguarda soprattutto i bambini. L’UNICEF ha stimato che una nutrizione che preveda un apporto adeguato di vitamina A potrebbe salvare la vita a più di 2 milioni di bambini (con età compresa tra 1 e 4 anni) l’anno. I frutti di pomodoro contengono inoltre sostanze utili alla salute, quali i flavonoidi. I flavonoidi sono antiossidanti idrofilici, ed in una certa misura, complementari alla natura idrofobica dei carotenoidi. Diete ricche in flavonoidi si sono mostrate utili nel ridurre i 52 rischi di malattie coronariche, di alcune forme tumorali e di altre malattie legate all’invecchiamento (Ross et al., 2004) Sono stati fatti molti tentativi per aumentare la produzione di carotenoidi in pomodoro usando geni batterici, codificanti per enzimi coinvolti nella biosintesi. Questi approcci hanno però dato come risultato l’aumento di uno solo o pochi metaboliti e non l’auspicato incremento di tutto il flusso metabolico dei carotenoidi. Al contrario, i livelli di flavonoidi sono stati aumentati inducendo un’amplificazione dei passaggi biosintetici o utilizzando fattori di trascrizione che si sapevano esser coinvolti in questo processo. Ma anche se si sono ottenuti buoni risultati con i flavonoidi, non è stato lo stesso per i carotenoidi, per i quali non è stato possibile aumentarne i livelli, attraverso la modificazione genetica tradizionale. Un’altra strategia adottabile per incrementare il contenuto in metaboliti secondari consiste nell’agire su geni regolatori implicati nella via biosintetica scelta. Inoltre, essendo questi geni endogeni ed originari della pianta stessa, questa strategia potrebbe essere più facilmente accettata dall’opinione pubblica. Un esempio è l’etilene, ormone vegetale, la cui funzione regolatrice nella maturazione dei frutti è stata molto ben chiarita. E’ famoso l’evento di traformazione commercializzato dalla Calgene (USA), sotto il nome di pomodoro “Flavr Savr”; questi pomodori sono prodotti con la tecnologia dell’RNA antisenso e maturano molto lentamente; la loro maturazione commerciale viene indotta da etilene o molecole stimolanti la produzione di questo ormone (ad es. l’ethrel). Mutanti DET1 Recentemente è stato osservato che geni coinvolti nella trasmissione del segnale luminoso nelle piante possono influenzare la qualità del frutto (Adams et al., 2004). Questi geni sono quindi possibili “target” per migliorare la qualità organolettica dei frutti. DE-ETIOLATED1 (DET1) è un gene regolatore che inibisce segnali molecolari indotti dalla luce. Mutazioni di questo gene sono responsabili di fenotipi ad elevata pigmentazione (hp-2) in pomodoro, caratterizzati da una sovraelevata fotosensibilità. Mutanti hp-2 cresciuti sotto una normale radiazione luminosa possiedono alti livelli di antocianine; danno inoltre origine a piante più piccole e scure rispetto agli esemplari wild-type e hanno una maggiore pigmentazione localizzata nel frutto. Questa elevata pigmentazione del frutto maturo è indice di innalzati livelli di carotenoidi e flavonoidi. Un silenziamento costitutivo del gene DET-1 in pomodoro (TDET-1) ha dato come risultato un aumento del contenuto di ß-carotene e licopene nei frutti maturi. Purtroppo, 53 in concomitanza di questo effetto emergono difetti nello sviluppo, quali la riduzione dell’altezza della pianta e un habitus rimpicciolito, a forma di cespuglio. Questi fenotipi aberranti sono anche il risultato di mutanti hp-2. RNAi utilizzando TDET1 Per sfruttare gli effetti positivi nei frutti, dati dalla soppressione del gene TDET-1, senza quelli negativi, legati alla crescita della pianta, si è cercato di inibire l’accumulo di mRNA TDET-1 sfruttando l’RNA interference (RNAi) in maniera frutto-specifica. Tale risultato è stato ottenuto utilizzando un costrutto guidato da tre diversi promotori frutto-specifici (P119, 2A11, TFM7). Il costrutto era concepito in modo che, una volta trascritto, formasse una struttura a forcina ds-RNA che fosse riconosciuta e utilizzata dal meccanismo dell’RNAi (Fig.29). Come risultato si ottennero piante transgeniche, distinte per il promotore utilizzato nel costrutto, ma pressoché identiche nel fenotipo. Tutte, infatti, oltre ad avere un habitus normale e sano, mostravano una pigmentazione verde scuro nei frutti immaturi, che poi evolveva in una forte pigmentazione rosso scura in quelli maturi: caratteristiche paragonabili ai mutanti hp-2 visti in precedenza. Con il promotore P119 i frutti apparivano più scuri nella loro parte più bassa ed erano caratteristici di una colorazione “granulosa” (Fig.28b). Il promotore 2A11, come il TFM7, davano invece colorazione scura ed omogenea in ogni parte (Fig.28c e 28c). I frutti immaturi di piante transgeniche con promotore 2A11 erano di un verde più scuro rispetto ai frutti delle piante con gli altri promotori. Poichè la perdita di funzione del gene TDET-1 causa un fenotipo con chioma più scura e habitus rimpicciolito, era facile notare se l’espressione del costrutto era erroneamente modulata anche nella porzione vegetativa della pianta. Questi fenotipi aberranti vennero così scartati e non più analizzate le progenie. Figura 28:Fenotipi di piante transgeniche frutto-specifiche guidate da diversi promotori. (a) Frutti immaturi di piante wild-type (T56); (b) di piante transgeniche con promotore P119; (c) con promotore 2A11; (d) con promotore TFM7. (e) Frutti maturi , wild-type e transgeniche, con i tre differenti promotori. (f) Rispettive sezioni dei precedenti frutti. 54 I fenotipi frutto-specifici ottenuti evidenziavano che il silenziamento dell’espressione del gene TDET-1 è esclusivamente localizzato nei frutti ed è grazie alla particolare strutturazione del costrutto che esso viene riconosciuto dal meccanismo dell’RNAi (Figg.29). Promotore Senso Spaziatore Antisenso complementare Trascrizione Figura 29: modello del costrutto; concepito per andare a formare, dopo la trascrizione, una struttura a forcina (ds-RNA) riconosciuta dal complesso multienzimatico Dicer, fase iniziale del processo cellulare dell’RNA interference. Una caratteristica che permette una facile diagnosi dell’RNA interference è la degradazione dell’mRNA target in piccoli frammenti di basso peso molecolare (siRNA). Sono state quindi utilizzate una vasta gamma di tecniche per saggiare la quantità di mRNA TDET-1 nelle piante transgeniche. La RT-PCR Real Time ha permesso di quantificare l’mRNA presente nei frutti e nelle foglie (5 piante saggiate per ogni diverso costrutto). Nei frutti i valori erano nettamente inferiori rispetto a quelli rilevati nelle foglie (Fig.30a). L’mRNA estratto dalle foglie delle piante transgeniche era in quantità simile a quella rilevata nelle piante wild-type. Per analizzare successivamente i livelli di mRNA si è proceduto con una RT-PCR semi-quantitativa partendo da RNA isolato sia dai frutti che dalle foglie della stessa pianta. Queste analisi hanno rivelato che i titoli di mRNA TDET-1, nei frutti, erano notevolmente inferiori rispetto a quelli delle foglie, e questo in ognuno dei tre costrutti (Fig.30b); mentre, per le piante wild-type, i valori erano simili in diverse parti della pianta in diversi stadi di sviluppo (Fig.30c). Per meglio stimare il silenziamento di TDET-1 nei frutti si è effettuato un northern blot per RNA a basso peso molecolare, per trovare i siRNA (small interfering RNAs), segno chel’RNAi era stato attivato. SiRNA, derivati da TDET-1, sono stati riscontrati nei frutti, ma non nelle foglie (Fig.30d) o nel materiale prelevato da piante non trasformate 55 (controllo negativo). Questi risultati sono stati ottenuti per tutti i promotore fruttospecifici. Figura 30: a - Analisi RT-PCR Real Time. Confronto dei livelli di mRNA di TDET-1 tra foglie(L) e frutti(F), di piante wild-type e piante trasformate alla generazione T3; b - RT-PCR semi-quantitativa; il gene HY5 è usato come controllo positivo della sintesi di cDNA durante la retrotrscrizione. Campionamenti alla generazione T3; c - RT-PCR semi-quantitativa dei diversi tessuti delle piante wild-type (IF: frutto immaturo;BR: frutto allo stadio di rottura; S: gambo ;YL: giovane foglia; OL: foglia vecchia); d - analisi dei siRNA di frutti verdi maturi (F) e di foglie (L). I siRNA derivati dal costrutto di TDET-1 migrano alla stassa altezza di un marker a 25 nucleotidi (non mostrato). 5S rRNA è usato come controllo di caricamento. Per ogni diverso costrutto saggiato sono state utilizzate tre diverse piante della generazione T3. Analisi biochimiche dei mutanti Analisi chimiche su campioni di frutti, selezionati da piante della generazione T2, contenenti i tre promotori, hanno evidenziato che i livelli di licopene e ß-carotene erano ben più alti rispetto a quelli dei frutti di piante wild-type (Fig.31a e 31b). Il costrutto con promotore P119 ha dato livelli di ß-carotene nettamente superiori a quelli delle altre piante transgeniche; questo era anche apprezzabile visivamente in quanto i frutti di questa linea transgenica risultavano più arancioni ( Fig.28f). Da due a quattro esemplari per costrutto sono stati selezionati per successivi studi nella generazione T3. Le piante della generazione T3 si mostravano fenotipicamente normali, indicando che i siRNA non si erano trasmessi, attraverso i semi, agli organi vegetativi. Ciononostante queste piante sviluppavano frutti verdi scuri che poi evolvevano in rosso intenso, come nella generazione T2. Ripetute le analisi chimiche, i risultati erano analoghi a quelli della generazione T2: i livelli di carotenoidi e licopene erano aumentati in tutti e tre i costrutti e in particolare si riscontravano livelli elevati di ßcarotene nella linea P119. 56 Per esaminare se l’aumento di carotenoidi presenti nel frutto si accompagnava ad effetti negativi sulla qualità del frutto sono stati misurati due parametri: il peso del frutto e la concentrazione zuccherina (brix). Il peso dei frutti è rimasto invariato (tranne una lieve eccezione in una linea TFM7), come anche la concentrazione zuccherina (anch’essa con una piccola divergenza in una linea P119). Il secondo obiettivo era quello di riuscire ad aumentare la produzione di carotenoidi, contemporaneamente a quella di flavonoidi, e per fare ciò, sono state saggiate le tre linee transgeniche confrontandole con le piante wild-type. Come si era visto nei mutanti hp-2, anche in questo caso i livelli di tre principali flavonoidi risultano incrementati rispetto agli esemplari non transgenici (Fig.31c). I migliori risultati sotto questo aspetto sono stati ottenuti con le linee aventi come promotore il TFM7. I valori migliori sono comunque variabili tra un promotore e l’altro, e dipendono dal tipo di flavonoide misurato. Figura 31: Quantificazione del contenuto di flavonoidi e carotenoidi in frutti rossi maturi di piante wild-type e linee transgeniche contenenti differenti promotori frutto-specifici, alla generazione T2. Le valutazioni statistiche sono state effettuate attraverso il test di Student (ttest). a- contenuto di licopene b- contenuto di ß-carotene c- contenuto di flavonoidi 57 Discussione I precedenti tentativi di miglioramento, attraverso l’inserimento di geni batterici codificanti per enzimi coinvolti nei processi biosintetici di carotenoidi non avevano portato a risultati così soddisfacenti; inoltre, l’incremento di un carotenoide, spesso andava a detrimento di un altro. Si pensava che ciò fosse dovuto a limiti di flusso biosintetico o ad un eccessivo accumulo all’interno del frutto. Questo esperimento ha però dimostrato il contrario, riuscendo ad incrementare l’intero flusso biosintetico. E’ possibile che questa scoperta avrà delle positive ricadute anche in altre colture agroalimentari che sovraesprimono geni del metabolismo dei carotenoidi (es.: “Golden Rice”). La mancanza di effetti biochimici indesiderati è stata il frutto della combinazione di promotori frutto-specifici e dell’uso di costrutti ad alta efficienza di silenziamento. Il costrutto è stato progettato troncando e mutando una sequenza codificante del gene TDET-1 in una configurazione ripetuta e invertita (Fig.29). Inoltre, il fatto che il silenziamento persista in maniera frutto-specifica è indice del fatto che i segnali di silenziamento non si propagano dal frutto al resto della pianta. Questo probabilmente è dovuto al fatto che i frutti sono organi dediti all’accumulo di sostanze (sink) e non specializzati alla distribuzione delle stesse al loro esterno (source). Anche i semi delle nuove generazioni non mostrano segnali di silenziamento e fanno sì che la pianta esplichi la sua fase vegetativa, come gli esemplari wild-type, fino a quando la produzione di frutti non innesca i promotori, generando un silenziamento sito-specifico. Conclusioni Lo studio dimostra che una mirata manipolazione di geni regolatori può risultare nell’incremento simultaneo di più flussi metabolici; in questo caso riuscendo ad aumentare sia carotenoidi che flavonoidi, come mai prima era stato possibile. Questo è forse il primo caso in cui si riesce ad ottenere un tale risultato senza incappare in effetti collaterali sulla qualità globale del frutto o sulla produttività della pianta. Queste tecniche potrebbero essere meglio accettate dall’opinione pubblica in quando vengono sfruttati geni della stessa pianta. Inoltre, l’utilizzo combinato dell’RNAi interference e di sistemi di espressione tessuto-specifici e organo-specifici permettono di ottenere risultati che non sarebbero assolutamente perseguibili con le tecniche tradizionali di breeding 58 Caso di studio 2 Eredità non mendeliana di informazioni extra-genominche in Arabidopsis. Introduzione Un principio fondamentale della genetica mendeliana è quello per cui un allele è stabilmente ereditato da una generazione all’altra. Ciò permette quindi di predire, con calcoli statistici, i pattern di segregazione degli alleli. Sono, in ogni caso, notoriamente conosciute molte eccezioni a questa regola; tutte rappresentano casi specifici ristretti ad un set limitato di geni ( come per esempio la conversione dei geni di riconoscimento per la coniugazione in lievito) o specifici alleli (ad esempio contenenti trasposoni o sequenze ripetute). E’ stato notato che in Arabidopsis esemplari omozigoti per l’allele mutante (recessivo) del gene hothead (HTH), implicato nella fusione di organi, possono ereditare sequenze di DNA allele specifiche che non erano presenti del genoma cromosomiale dei loro genitori, ma erano presenti in generazioni precedenti; tali esemplari recuperano in questo caso l’allele wild-type del gene HTH. Questo processo sembra essere un meccanismo generale di eredità extra-genomica di sequenze di DNA. Si pensa quindi che questo ripristino genetico sia il risultato di una diretta copia di un RNA ancestrale che funziona da “memoria”. Statistiche rilevanti Sono stati trovati 11 mutazioni puntiformi nel locus HTH che mostrano la particolare proprietà di dare progenie segregante con piante a fenotipo wild-type, con alta frequenza, quando mutanti hth omozigoti siano lasciati ad auto-impollinazione. La frequenza con la quale queste piante, “revertanti”, si manifestano varia in un intervallo da 10 -1 a 10-2 revertanti per cromosoma per generazione. Questo è in rigido contrasto a molte mutazioni puntiformi che sono completamente stabili, per esempio mutante erecta (er) (Tab.3), e che seguono le leggi mendeliana dell’ereditarietà dei caratteri. 59 Tabella 3: reversione degli alleli mutati. A causa di questa alta frequenza con la quale sono stati osservati fenotipi HTH revertanti, si è sospettato che essi possano riflettere un’incompleta penetranza del fenotipo mutante o un cambio epigenetico che mascheri il genotipo mutante. Per determinare chiaramente il genotipo dei fenotipi revertanti sono stati disegnati primer PCR allele-specifici. Questi marcatori hanno chiaramente mostrato che le piante fenotipicamente wild-type osservate erano eterozigoti per l’allele HTH parentale indicando che la sequenza nucleotidica del gene HTH è stata alterata in circa il 10 % delle piante figlie. Questo dato è confermato dal fatto che, lasciando le piante revertanti ad auto-impollinazione, ed esaminando la segregazione del fenotipo HTH nella generazione figlia, si è notato che il fenotipo mutante era presente in circa il 25% dei casi. Test e osservazioni Due semplici spiegazioni potevano chiarire questo strano fenomeno della progenie revertante: 1) la contaminazione dello stock con semi wild-type; 2) out-crossing dei mutanti con polline esterno wild-type. Gli autori hanno scartate entrambe grazie ad alcuni esperimenti mirati. 1) La contaminazione dei semi non può essere una valida spiegazione perché i revertanti sono tutti eterozigoti per l’allele hth specifico ricevuto dai genitori. Per eliminare ogni possibilità di contaminazione esterna da semi, sono stati prelevati embrioni direttamente da frutti sviluppatisi su piante autofecondate e attraverso un saggio PCR con primer specifici per l’allele, sono stati genotipizzati gli embrioni. Anche in queste condizioni è stato possibile evidenziare che da genotipi omozigoti mutanti (hth/hth) originavano, frequentemente (~10 %), embrioni eterozigoti (HTH/hth). Questa tipologia di analisi permise di scartare la possibile contaminazione 60 dei lotti di semi. Inoltre sono stati osservati anche embrioni revertanti per entrambi i loci (HTH/HTH), a bassissima frequenza, i quali ereditando sicuramente uno dei due alleli wild-type dalla madre non possono essere il risultato di outcrossing (risultati osservabili in Tab.4, solo per mutazione hth-4) La frequenza di reversioni osservate genotipicamente è maggiore di quelle osservate fenotipicamente; questo sta ad indicare che si possono verificare reversioni solo a carico di alcune cellule somatiche. Tabella 4: genotipi della progenie di omozigoti mutanti. Figura 32: confronto PCR con primer specifici. Per dimostrare direttamente che i mutanti hth/hth possono essere fonte di alleli wildtype HTH è stata eseguita la seguente prova: si è cercato di trasmettere alleli HTH attraverso il polline generato da piante hth/hth. Piante Landsberg erecta (Ler), omozigoti per hth-4, sono state incrociate con il wild-type Columbia (Col) e gli embrioni derivanti sono stati genotipizzati per gli alleli HTH. Molti embrioni erano eterozigoti, come presunto, ma negli incroci in cui il maschio era omozigote per hth-4, 8 dei 164 embrioni osservati erano con genotipo HTH (freq. di reversione 4.9 x 10 -2). Nessun embrione HTH/HTH è stato rilevato quando il genitore femmina era l’omozigote per hth-4 ( 0 di 230 embrioni). Questi dati indicano che le piante hth/hth possono essere fonte di polline che porta un allele HTH e tale deviazione, rispetto all’atteso è frequente nella linea germinale maschile. Globalmente, questi dati indicano che gli alleli HTH presenti nella progenie ottenuta da auto-impollinazione di omozigoti hth/hth non sono il risultato di contaminazione da seme o contaminazione da polline. 61 Sono state considerate altre spiegazioni convenzionali per la variabilità genetica osservata sul locus hth. L’analisi della sequenza del locus ha permesso di scartare l’ipotesi dell’attività di trasposoni o di sequenze ripetute. Altre due plausibili spiegazioni potevano essere: i)l’alta frequenza di mutazioni casuali in quel tratto di genoma e ii)la correzione del gene attraverso un meccanismo di conversione. Nel primo caso, se la reversione del gene hth in HTH fosse dovuta ad un alto tasso mutazionale, nella regione genomica ci si sarebbe aspettato di trovare altre mutazioni silenti nell’allele HTH. Vista l’alta frequenza con cui l’allele mutato torna ad essere wild-type e le 1226 possibili mutazioni silenti in quel tratto codificante, ci si poteva attendere dalle 50 alle 100 mutazioni silenti. Per saggiare ciò, è stata sequenziata l’intera regione codificante e questo è stato fatto per tre diversi e indipendenti casi di reversione, ripetuti per le tre diverse reversioni ( hth-4, hth-8 e hth-10). In ogni caso la sequenza dell’allele HTH revertato era esattamente uguale alla sequenza wild-type della stessa varietà di Arabidopsis thaliana. Tale risultato esclude la possibilità di mutazioni casuali ad alta frequenza, facendo invece pensare ad un “effetto copia”, a partire da un filamento “stampo”. Il secondo caso (la conversione genica), prevede due tipologie di filamento sorgente: 1) una seconda copia del gene o la presenza di alleli non evidenziabili mediante PCR; 2) una famiglia di geni HOTHEADLIKE. La possibilità di una seconda copia nascosta dell’allele HTH negli omozigoti hth/hth è stata scartata grazie all’utilizzo di primer PCR specifici per i geni HTH; la PCR ne ha confermato l’assenza. Inoltre, per eliminare anche la possibilità della presenza di alleli HTH non amplificati dai primer è stato effettuato un Southern blot del DNA di Ler Col e Sw (Wassilewskija) e, Figura 33: DNA blot con sonde per geni htl. anche in questo caso, non si sono trovati altri frammenti ibridizzati se non quelli attesi dei due alleli hth (Fig.33). Anche la seconda classe di filamenti sorgente (famiglia genica HTH-LIKE),per una serie di ragioni, è stata scartata. Infatti, per hth-4, nessuna delle sequenze HTL presenti in database contiene il nucleotide giusto necessario per ripristinare la sequenza mutata 62 in quella wild-type. Per hth-8 e hth-10 alcune sequenze HTL conterrebbero il nucleotide appropriato alla correzione, ma se esse fossero usate per revertare l’allele, in esso si incorporerebbero altri cambi di sequenza adiacenti al nucleotide, a meno che la sostituzione non interessi solo il singolo nucleotide (Fig.34). Sulla base delle evidenze descritte sembra corretto escludere una conversione convenzionale del gene. Figura 34: allineamenti con sequenze HTL. Un’instabilità genetica diffusa Per determinare se cambi nella sequenza genetica possono verificarsi in altri regioni geniche, sono stati incrociati mutanti hth-4, hth-8 e hth-10 con background genetico Ler con wild-type di Col. Gli ibridi F1 vengono poi lasciati auto-impollinare e le piante F2 genotipizzate con markers per PCR per identificare quali di questi fossero omozigoti per l’allele mutato o per l’allele wild-type di HTH. Questi F2, inoltre, sono stati genotipizzati con markers di altri loci (Tab.5), polimorfici tra Col e Ler, in modo da discriminare gli individui omozigoti per l’allele di un genitore o dell’altro. Piante della generazione F3, scelte casualmente, sono state analizzate con questi markers per determinare l’ereditarietà dei polimorfismi. Effettivamente, nella progenie di piante F2 hth/hth è stata osservata un’alta frequenza di cambio di polimorfismo per altri loci (da Col a Ler, e viceversa), indicando che l’instabilità genetica notata su hth si ripercuote anche in altre sequenze del genoma (Tab.5). Tabella 5: instabilità di altre sequenze del genoma manifestata negli omozigoti hth/hth. 63 Questi polimorfismi sono presenti in introni, esoni e in regioni non tradotte (UTR), indicando che non è necessaria la presenza dell’mRNA dello stesso gene per causare la trasmissione di sequenze extra-genomiche. E’ stata anche notata una reversione fenotipica della mutazione er nella progenie F2 di genitori hth/hth er/er pressoché con la stessa frequenza, dimostrando che l’assenza di HTH provoca la destabilizzazione di er; sorprendentemente, invece, il genotipo HTH/HTH non ha dato segni di instabilità genetica (dati non mostrati). Analogamente, anche l’eredità dei marker polimorfici nella progenie di piante HTH/HTH è risultata stabile, coaudiuvando l’ipotesi dell’instabilità dovuta all’assenza di HTH. Riassumendo, mutazioni del gene HTH in Arabidopsis mostrano un peculiare pattern di trasmissione genetica con la quale le piante della progenie, ad un’elevata frequenza, ereditano sequenze di DNA che non erano presenti nel genoma dei genitori, e tale processo si ripercuote sull’intero genoma in situazione omozigote hth/hth. L’instabilità non è comunque casuale, ma ben mirata a ripristinare la sequenza mutata in quella wildtype; quest'ultima (allele HTH) non è presente nei genitori ma è stata presente in un antenato. E’ ipotizzabile quindi che l’allele mutato hth sia in grado di revertare in quello wildtype HTH, probabilmente perché un antenato della pianta omozigote (hth/hth) ne possedeva una copia. Ciò accade anche per altri loci polimorfici (Tab.5). In questo caso piante omozigoti per un determinato polimorfismo generano progenie con polimorfismo diverso, però solo a condizione che i genitori abbiano un antenato che possieda una copia dell’allele polimorfico ancestrale. Il processo inoltre non è casuale, ma agisce ripristinando solo il nucleotide mutato. Altri simili patterns di ereditarietà sono stati osservati precedentemente e in circostanze eccezionali. Ad esempio marcatori RAPD in peperone hanno mostrato di “sparire” per diverse generazioni per poi “riapparire” (Taller et al., 1998). Ma tali casi mostravano una frequenza nettamente inferiore di quella riportata in questo studio su piante hth/hth. Siamo quindi di fronte ad un processo di ereditarietà non-mendeliana di sequenze che vengono conservate al di fuori del DNA genomico. 64 “Backup ad RNA” L’alta specificità del meccanismo evidenziata suggerisce che si tratti di un processo mediato da uno “stampo”, e dal momento che nè saggi PCR, né “Southern blot”, hanno permesso di evidenziare alcun filamento alternativo che possa avere una funzione di “backup” genico, gli autori hanno ipotizzato che tale stampo potesse essere una molecola di RNA. E’ infatti stato proposto un modello in cui una molecola stabile di RNA, probabilmente a doppio filamento, si moltiplichi e venga trasmessa nelle generazioni; in determinate circostanze, questa potrebbe essere in grado di ripristinare la sequenza di DNA genomico mutata. Dal momento che tale fenomeno accade per tutto il genoma, come dimostrato analizzando altri loci, si è pensato che il processo sia sempre presente, anche in piante wild-type, e che l’instaurarsi dello stato hth/hth (in omozigosi) crei un effetto catalizzante di tale processo, aumentando la frequenza di ricombinazione del DNA. hth/hth hth/hth hth/hth hth/hth hth/HTH Hth/HTH hth/hth RNA ? RNAi, una possibile spiegazione Anche se quanto detto può sembrare straordinario, ed è necessaria comunque un sua ulteriore conferma sperimentalmente, gli autori sostengono che tale fenomeno sia la somma di alcuni processi già evidenziati singolarmente. Infatti, gli studi sul PTGS e RNAi indotto da dsRNA hanno dimostrato che questi possono persistere per diverse generazioni e diffondersi attraverso nell’organismo in Caenorhabditis elegans (Fire and Mello, 1998), piante e funghi (Cogoni et al., 1996). Ciò implica la possibilità che alcune sequenze nucleotidiche possano stabilmente replicarsi all’esterno del genoma, attraverso una RNA polimerasi-RNA dipendente (RdRP), come descritto nei precedenti capitoli. E’ stato anche scoperto che sia i dsRNA che i microRNA sono in grado di mediare la metilazione del DNA genomico (Wassenegqer et al., 1994; Bao et al., 2004), ed indurre una mutagenesi sito-specifica attraverso l’introduzione di 65 oligonucleotidi chimerici (DNA-RNA), sia in cellule animali che vegetali (Cole-Strauss et al., 1996). Una possibile spiegazione, non formulata dagli autori, è analoga al sistema di gestione di riarrangiamento dell’informazione genetica osservato in Tetrahymena thermophila (descritto nel capito relativo agli eventi di RNAi che intercorrono a livello nucleare). Combinando questi singoli fenomeni tra loro è stata abbozzata una spiegazione di questo eccezionale fenomeno di eredità non mendeliana. Essendo questo meccanismo in grado di creare una copia dell’informazione genetica, sotto forma di “RNA cache” (serbatoio di RNA), per poi recuperarla a seguito della sua perdita, è ipotizzabile che tale fenomeno in futuro possa essere sfruttato per ovviare al fenomeno della depressione da inbreeding presente nelle piante che si autoimpollinano. E’ inoltre molto interessante che il recupero dell’informazione genetica sia stimolato da un fattore di “stress”, in questo caso attribuito alla mancanza dell’allele dominante HTH (stato allelico hth/hth). Si può quindi immaginare che l’evoluzione abbia portato l’organismo a mantenere un collezione di alleli ritenuti indispensabili che possono riemergere in condizioni “difficili”. Una diminuzione dello stress, viceversa, tenderebbe a frenare il fenomeno favorendo così l’instaurarsi di un genotipo adatto, per esempio, ad un particolare ambiente. Gli autori si ripromettono di continuare ad indagare questo fenomeno per descrivere: i)la struttura effettiva del “temprato”; ii) il meccanismo con cui questo viene prodotto ed ereditato; iii) se il fenomeno sia comune ad altri organismi. 66 Bibliografia consultata 1. Dykxhoorn, D.M., Novina, C.D., and Sharp, P.A. Killing the messenger: short RNAs that silence gene expression. Nat. Rev. Mol. Cell. Biol. 4, 457-467 (2003). 2. Marjori, A.M., and James A.B (2005). RNAi-mediated pathways in the nucleus. Nature 6, 24-35. 3. Jover, S., Candela, H., and Ponce M.R.. Plant microRNAs and development. Int. J. Dev. Biol. 49, 733-744 (2005). 4. Mello, C.C., and Conte D. Jr. Revealing the world of RNA interference. Nature 431, 338-342 (2004). 5. Sharp PA. RNA Interference-2001. Genes Dev 15: 485-490 (2001). 6. Rui, Y., Brian, P.D., Yi Q., Ian G. M., and Bryan R. Cullen. Overexpression pf Exprtin 5 enhance RNA interference mediated by short hairpin RNAs amd microRNAs. RNA 11, 220-226 (2005). 7. Carrington, J.C., Ambros, V. Role of microRNAs in Plant and Animal Development. Science. Vol. 301 (2003). 8. Fire A, Xu S, Montgomery MK, Kostas SA, Driver SE, and Mello CC. Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. Nature 391: 806-811 (1998). 9. Tessa N. Campbell, Francis Y.M. Choy. RNA Interference: Past, Present and Future. Curr. Issiues Mol. Biol. 7:1-6 (2005). 10. Waterhouse, P.M., and Helliwell C.A.. Exploring plant genome by RNA-indiced gene silencing. Nature 4, 29-38 (2003). 11. Kim, V.N. RNA interference in functional genomic and medicine. J. Korean Med. Sci. 18, 309-318 (2003). 12. Julian Downward.RNA interference. BMJ 2004;328;1245-1248 (2004). 13. Ernie Hood, RNAi: what’s all the noise about gene silencing. Environmental Health Perspectives; vol. 112 – 4; (2004). • Le figure 16,17,18,19,20,21,22 sono tratte dal materiale del workshop internazionale “Gene Silencing”, tenutosi a Villa Gualino, Torino, l’ 11 November 2005. Le immagini sono estrapolate dalle presentazioni di Jozsef Burgyan e Tamas Dalmay. 67 Casi di studio: • Susan J. Lolle, Jennifer L. Victor, Jessica M. Young & Robert E. Pruitt (2005). Genome-wide non-mendelian inheritance of extra-genomic information in Arabidopsis. Nature, vol.434, 505-509. • Ganga Rao Davuluri, Ageeth van Tuinen, Paul D Fraser, Alessandro Manfredonia, Robert Newman, Diane Burgess, David A Brummell, Stephen R King, Joe Palys, John Uhlig, Peter M Bramley, Henk M J Pennings and Chris Bowler (2005). Fruit-specific RNAi-mediated suppression of DET1 enhances carotenoid and flavonoid content in tomatoes. Nature Biotechnology vol.3, n° 7, 890895. Bibliografia citata 1. Abdelgany, A., Wood, M., and Beeson, D. Allele-specific silencing of a pathogenic mutant acetylcholine receptor subunit by RNA interference. Hum. Mol. Genet. 12, 2637-2644 (2003). 2. Ambros, V. The function of animal microRNAs. Nature 431, 350-355 (2004). 3. Angell, S.M., and Balcombe D.C. Consistent gene silencing in transgenic plants expressing a replicating potato virus X RNA. EMBO J. 16, 3675-3684 (1997). 4. Aramayo, R. & Metzenberg, R. L. Meiotic transvection in fungi. Cell 86, 103–113 (1996). 5. Aufsatz, W., Mette, M. F., Matzke, A. J. M. & Matzke, M. The role of MET1 in RNAdirected de novo and maintenance methylation of CG dinucleotides. Plant Mol. Biol. 54, 793–804 (2004). 6. Aufsatz, W., Mette, M. F., van der Winden, J., Matzke, A. J. M. & Matzke, M. RNAdirected DNA methylation in Arabidopsis. Proc. Natl Acad. Sci. USA 99, 16499–16506 (2002). 7. Ausubel, F. et al. Current Protocols in Molecular Biology (Wiley, New York, 1990). 8. Bannister, A. J. et al. Selective recognition of methylated lysine 9 in histone H3 by the HP1 chromo domain. Nature 410, 120–124 (2001). 9. Bao, N., Lye, K.W., and Barton, M.K. MicroRNA binding sites in Arabidopsis class III HD-ZIP mRNAs are required for methylation of the template chromosome. Dev. Cell 7: 653–662 (2004). 68 10. Bartel, D.P. MicroRNAs: genomics, biogenesis, mechanism and function. Cell 116, 281-297 (2004). 11. Baulcombe, D.C. Fast forward genetics based on virusinduced gene silencing. Curr. Opin. Plant Biol. 2, 109–113 (1999). 12. Baulcombe, D.C.. RNA as an initiator of post-transcriptional gene silencing in transgenic plants. Plant Mol Biol, 32: 79-88 (1996). 13. Benian, G., L’Hernault, S. & Morris, M. Additional sequence complexity in the muscle gene, unc-22,and its encoded protein, twitchin, of Caenorhabiditis elegans. Genetics 134, 1097–1104 (1993). 14. Bernstein E, Caudy AA, Hammond SA, and Hannon GJ. Role for a bidentate ribonuclease in the initiation step of RNA interference. Nature 409:363-366 (2001). 15. Billy, E., Brondani, V., Zhang, H., Muller, U., and Filipowicz, W. Specific interference with gene expression induced by long double-stranded RNA in mouse embryonal teratocarcinoma cell lines. Proc. Natl. Acad. Sci. USA 98, 363-366 (2001). 16. Bohnsack, M.T., Czaplinski, K., and Gorlich, D. Exportin 5 is a RanGTP-dependent dsRNA-binding protein that mediates nuclear export of pre-miRNAs. RNA 10: 185-191 (2004). 17. Bourque JE. Antisense strategies for genetic manipulation in plants. Plant Sci. 105: 125-149 (1995). 18. Bosher, J.M., Dufourcq, P., Sookhareea, S. And Labouesse, M. RNA interference can target pre-miRNA: consequences for gene expression in Caernorhabditis elegans operon. Genetics 153, 1245-1256 (1999). 19. Brenner, S. The genetics of Caenorhabditis elegans. Genetics 77, 71–94 (1974). 20. Brummelkamp, T. R., Bernards, R. & Agami, R. A system for stable expression of short interfering RNAs in mammalian cells. Science 296, 550–53 (2002). 21. Brummelkamp, T.R., Bernards, R., and Agami, R. Stable suppression of tumorigenicity by virus-mediated RNA interference. Cancer Cell 2, 243-247 (2002b). 22. Cai, X., Hagedorn, C.H. and Cullen, B.R. Human microRNAs are processed from capped, polyadenylated transcripts that can also function as mRNAs. RNA 10: 19571966 (2004). 23. Cao, X. et al. Role of the DRM and CMT3 methyltransferases in RNA-directed DNA methylation. Curr. Biol. 13, 2212–2217 (2003). 24. Caplen, N.J., Taylor, J.P., Statham, V.S., Tanaka, F.; Fire, A., and Morgan, R.A. Rescue of a polyglutamine-mediated cytotoxicity by double-stranded RNA-mediated RNA interference. Hum. Mol. Genet. 11, 175-184 (2002). 25. Cerutti, L., Mian, N. And Bateman, A. Domains in gene silencing and cell differentiation proteins: the novel PAZ domain and redefinition of the Piwi domain. Trends Biochem. Sci. 25: 481-482 (2000). 69 26. Chen, L., Krause, M., Sepanski, M. & Fire, A. The C. elegans MyoD homolog HLH-1 is essential for proper muscle function and complete morphogenesis. Development 120, 1631–1641 (1994). 27. Chen, X., Liu, J., Cheng, Y. and JIA, D. HEN1 functions pleiotropically in Arabidopsis development and acts in C function in the flower. Development 129: 1085-1094 (2002). 28. Cheng, J.C.,Moore, T.B., and Sakamoto, K.M.. RNA interference and human disease. Mol.Genet. Metab. 80, 121-128 (2003). 29. Chicas, A., Cogoni, C. & Macino, G. RNAi-dependent and RNAi-independent mechanisms contribute to the silencing of RIPed sequences in Neurospora crassa. Nucl. Acids Res. 32, 4237–4243 (2004). 30. Cogoni C, and Macino G. Post-transcriptional gene silencing across kingdoms. Genes Dev 10: 638-643 (2000). 31. Cogoni C, Irelan JT, Schumache, M, Schmidhauser T, Selker EU, and Macino G. Transgene silencing of the al-1 gene in vegetative cells of Neurospora is mediated by a cytoplasmic effector and does not depend on DNA-DNA interactions or DNA methylation. EMBO J 15: 3153-3163 (1996). 32. Colot, V., Maloisel, L. & Rossignol, J. L. Interchromosomal transfer of epigenetic states in Ascobolus: transfer of DNA methylation is mechanistically related to homologous recombination. Cell 86, 855–864 (1996). 33. Covey, S. N., Al-Kaff, N. S., Langara A. & Turner, D. S. Plants combat infection by gene silencing. Nature 385, 781–782 (1997). 34. Dalmay T., R. Horsefield, and TH. Brautenstein. SDE3 encodes an RNA helicase required for post-transcriptional gene silencing in Arabidopsis. EMBO J, 20: 20672077 (2001). 35. Denli, A.M., Tops, B.B., Plasterk, R.H., Ketting, R.F. And Hannon, G.J. Processing of primary microRNAs by the Microprocessor complex. Nature 432: 231-235 (2004). 36. Dorer, D.R., and Henikoff, S. Expansion of trangene repeats cause heterocromatin formation and gene silencing in Drosophila. Cell 77, 993-1002 (1994). 37. Draper, B. W., Mello, C. C., Bowerman, B., Hardin, J. & Priess, J. R. MEX-3 is a KH domain protein that regulates blastomere identity in early C. elegans embryos. Cell 87, 205–216 (1996). 38. Dunoyer, P., and Voinnet, O. The complex interplay between plant viruses and host RNA-silencing pathways. Curr. Op. Plant Biol. 8, 415-423 (2005). 39. Dzitoyeva S, Dimitrijevic N, Manev H. Intra-abdominal injection of double-stranded RNA into anesthetized adult Drosophila triggers RNA interference in the central nervous system. Mol Psychiatry 6(6):665-670 (2001). 40. Ekwall, K. The roles of histone modifications and small RNA in centromere function. Chromosome Res. 12, 535–542 (2004). 41. Elbashir SM, Lendeckel W, and Tuschl T. RNA interference is mediated by 21- and 22-nucleotide RNAs Genes Dev 15(2):188-200 (2001). 70 42. Elbashir, S.M., Harborth, J., Weber, K.,and Tuschl, T. Analysis of gene function in somatic mammalian cells using small interfering RNAs. Methods 26, 199-213 (2001b). 43. Elomaa P., Y. Helariutta, and M. Kotilainen. Transformation of antisense constructs of the chalcone synthase gene superfamily into Gerbera hybrida: differential effect on the expression of family members. Mol Breed, 2: 41-50 (1996). 44. Epstein, H.,Waterston, R. & Brenner, S. A mutant affecting the heavy chain of myosin in C. elegans. J.Mol. Biol. 90, 291–300 (1974). 45. F. Di Serio, H. Schob, and A. Iglesias. Sense and antisense-mediated gene silencing is inhibited by the same viral suppressors and is associated with accumulation of small RNAs. Proc Natl Acad Sci USA, 98: 6506-6510 (2001). 46. Fire, A., Albertson,D., Harrison, S.&Moerman,D. Production of antisenseRNA leads to effective and specific inhibition of gene expression in C. elegans muscle. Development 113, 503–514 (1991). 47. Freitag, M. et al. DNA methylation is independent of RNA interference in Neurospora. Science 304, 1939 (2004). 48. Furner, I.J., Sheikh M.A., and Collet C.E. Gene silencing and homology-dependent gene silencing in Arabidopsis: genetic modifiers and DNA methylation. Genetics 149, 651-662 (1998). 49. Ge, Q., McManus, M.T., Nguyen , T., Shen, C.H., Sharp, P.A., Eisen, H.N, and Chen, J. RNA interference of influenza virus production by directly targeting mRNA for degradation and indirectly inhibiting all viral RNA transcription. Proc. Natl.Acad. Sci. USA 100, 2718-2723 (2003). 50. Gossele, V., Fache, I., Meulewaeter, F., Cornelissen, M. & Metzlaff, M. SVISS a novel transient gene silencing system for gene function discovery and validation in tobacco plants. Plant J. 32 (2002). 51. Gregory, R.I., Yan, K.P., Amuthan, G., Chendrimada, T., Doratotaj, B., Cooch, N. And Shiekhattar, R. The Microprocessor complex mediates the genesis of microRNAs. Nature 432: 235-240 (2004). 52. Grishok A, Pasquinelli AE, Conte D, Li N, Parrish S, Ha I, Baillie DL, Fire A, Ruvkun G, and Mello CC. Genes and mechanisms related to RNA interference regulate expression of the small temporal RNAs that control C. elegans developmental timing. Cell 106:23-34 (2001). 53. Grishok A, Tabar H, and Mello CC. Genetic requirements for inheritance of RNAi in C. elegans. Science 287: 2494-2497 (2000). 54. Guo S, and Kempheus KJ. Par-1, a gene required for establishing polarity in C. elegans embryos, encodes a putative Ser/Thr kinase that is asymmetrically distributed. Cell 81: 611-620 (1995). 55. Guru T. A silence that speaks volumes. Nature 404, 804-808 (2000). 56. Hall, I. M. et al. Establishment and maintenance of a heterochromatin domain. Science 297, 2232–2237 (2002). 71 57. Hamilton AJ, Baulcombe DC. A species of small antisense RNA in posttranscriptional gene silencing in plants. Science 286: 950-952 (1999). 58. Hammond S, Bernstein E, Beach D, and Hannon G. An RNA-directed nuclease mediates post-transcriptional gene silencing in Drosophila cells. Nature, 404: 293-298 (2000). 59. Hammond SM, Caudy AA, Hannon GJ. Post-transcriptional Gene Silencing by Double-stranded RNA. Nature Rev Gen 2: 110-119 (2001). 60. Hannon, G.J. RNA interference. Nature 418, 244-251 (2002). 61. He, L. and Hannon, G.J. MicroRNAs: small RNAs with a big role in gene regulation. Nature Rev. Genet. 5, 522–531 (2004). 62. Hunter CP. Shrinking the Black Box of RNAi. Current Biology 10: R137-R140 (2000). 63. Hutvagner G, and Zamore P.D. RNAi: nature abhors a double-strand. Curr Opin Genetics & Development 12:225-232 (2002). 64. Hutvagner G, McLachlan J, Pasquinelli AE, Balint E, Tuschl T, and Zamore PD. A cellular function for the RNA-interference enzyme Dicer in the maturation of the let-7 small temporal RNA. Science 293:834-838 (2001). 65. Hutvagner, G. and Zamore, P.D. A microRNA in a multipleturnover RNAi enzyme complex. Science 297, 2056–2060 (2002). 66. Ingelbrecht I, Van Houdt H, Van Montagu M, and Depicker A. Posttranscriptional silencing of reporter transgenes in tobacco correlates with DNA methylation. Proc Natl Acad Sci USA 91: 10502-10506 (1994). 67. Izant, J. & Weintraub, H. Inhibition of thymidine kinase gene expression by antisense RNA: a molecular approach to genetic analysis. Cell 36, 1007–1015 (1984). 68. Johansen, L. K. & Carrington, J. C. Silencing on the spot. Induction and suppression of RNA silencing in the Agrobacterium-mediated transient expression system. Plant Physiol. 126, 930–938 (2001). 69. Jones, L., Ratcliff, F. & Baucombe, D. C. RNA-directed transcriptional gene silencing in plants can be inherited independently of the RNA trigger and requires Met1 for maintenance. Curr. Biol. 11, 747–757 (2001). 70. Jorgensen RA, Cluster PD, English J, Que Q, and Napoli CA. Chalcone synthase cosuppression phenotypes in petunia flowers: comparison of sense vs. antisense constructs and single-copy vs. complex T-DNA sequences. Plant Mol Biol 31: 957-973 (1996). 71. Kamath RS, Martinez-Campos M, Zipperlen P, Fraser AG, and Ahringer J. Effectiveness of specific RNA-mediated interference through ingested double-stranded RNA in Caenorhabditis elegans. Genome Biology 2: 2.1-2.10 (2000). 72. Kanno, T. et al. Involvement of putative SNF2 chromatin remodeling protein DRD1 in RNA-directed DNA methylation.Curr. Biol. 14, 810–805 (2004). 72 73. Kawasaki, H. & Taira, K. Short hairpin type of dsRNAs that are controlled by tRNAVal promoter significantly induce RNAimediated gene silencing in the cytoplasm of human cells. Nucleic Acids Res. 31, 700–707 (2003). 74. Kennerdell JR, and Carthew RW. Use of dsRNA-mediated genetic interference to demonstrate that frizzled and frizzled 2 act in the wingless pathway. Cell 95: 1017-1026 (1998). 75. Kennerdell JR, and Carthew RW. Heritable gene silencing in Drosophila using doublestranded RNA. Nature Biotech 18: 896-898 (2000). 76. Ketting RF, Fischer SE, Bernstein E, Sijen T, Hannon GJ, and Plasterk RH. Dicer functions in RNA interference and in synthesis of small RNA involved in developmental timing in C. elegans. Genes Dev 15(20):2654-2659 (2001). 77. Ketting RF, Haverkamp TH, van Luenen HG, and Plasterk RH. Mut-7 of C. elegans, required for transposon silencing and RNA interference, is a homolog of Werner syndrome helicase and RNase D. Cell 99: 133-141 (1999). 78. Kjemtrup, S. et al.Gene silencing from plant DNA carried by a geminivirus. Plant J. 14, 91–100 (1998). 79. Klahre, U., Crete, P., Leuenberger, S. A., Iglesias, V. A. & Meins, F. High molecular weight RNAs and small interfering RNAs induce systemic posttranscriptional gene silencing in plants. Proc. Natl Acad. Sci. USA 99, 11981–11986 (2002). 80. Kurihara, Y. And Watanabe, Y. Arabidopsis micro-RNA biogenesis through Dicer-like 1 protein functions. Proc. Natl. Acad. Sci. USA 101: 12753-12758 (2004). 81. Lachner, M., O’Carroll, D., Rea, S., Mechtler, K. & Jenuwein, T. Methylation of histone H3 lysine 9 creates a binding site for HP1 proteins. Nature 410, 116–120 (2001). 82. Lagos-Quintana M, Rauhut R, Lendeckel W, and Tuschl T. Identification of novel genes coding for small expressed RNAs. Science 294:853-858 (2001). 83. Lau NC, Lim LP, Weinstein EG, and Bartel DP. An abundant class of tiny RNAs with probable regulatory roles in Caenorhabditis elegans. Science 294:858-862 (2001). 84. Lee RC, and Ambros V. An extensive class of small RNAs in Caenorhabditis elegans. Science 294:862-864 (2001). 85. Lee, N. S. et al. Expression of small interfering RNAs targeted against HIV-1 rev transcripts in human cells. Nature Biotechnol. 20, 500–505 (2002). 86. LEE, R.C. and AMBROS, V. An extensive class of small RNAs in Caenorhabditis elegans. Science 294: 862-864 (2001). 87. LEE, R.C., FEINBAUM, R.L. and AMBROS, V. The C. elegans heterochronic gene lin-4 encodes small RNAs with antisense complementarity to lin-14. Cell 75: 843-854 (1993). 88. Lee, Y., Ahn, C., Han, J., Choi, H., Kim, J., Yim, J., Lee, J., Provost, P., Radmark, O., Kim, S. And Kim, V.N. The nuclear RNase III Drosha initiates microRNA processing. Nature 425: 415-419 (2003). 73 89. Lipardi C, Wei Q, and Paterson BM. RNAi as random degradative PCR. siRNA primers convert mRNA into dsRNA that are degraded to generate new siRNAs. Cell 107:297-307 (2001). 90. Liu, Y. L., Schiff, M. & Dinesh-Kumar, S. P. Virus-induced gene silencing in tomato. Plant J. 31, 777–786 (2002). 91. Lu, R., Martin-Hernandez, A.M., Peart J.R., Malcuit I., and Baulcombe, D.. Virusinduced gene silencing in plants. Methods 30, 296-303 (2003). 92. Luff, B., Pawlowski, L., Bender, J. An inverted repeat triggers cytosine methylation of identical sequences in Arabidopsis. Mol. Cell. 3, 505-511 (1999). 93. Lund, A. M. & van Lohuizen, M. Epigenetics and cancer. Genes Dev. 18, 2315–2335 (2004). 94. Manche L, Green SR, Schmedt C, and Mathews MB. (1992). Interactions between double-stranded RNA regulators and the protein kinase DAI. Mol. Cell. Biol. 12:52385248. 95. Matthew, L.. RNAi for plant functional genomics. Comp Funct Genom 5, 240-244 (2004). 96. McManus, M. T., Petersen, C. P., Haines, B. B., Chen, J. & Sharp, P. A. Gene silencing using micro-RNA designed hairpins. RNA 8, 842–850 (2002). 97. Melquist, S. & Bender, J. Transcription from an upstream promoter controls methylation signaling from an inverted repeat of endogenous genes in Arabidopsis. Genes Dev. 17, 2036–2047 (2003). 98. Mette, M. F., Aufsatz, W., van der Winden, J., Matzke, M. A. & Matzke, A. J. M. Transcriptional silencing and promoter methylation triggered by double stranded RNA. EMBO J. 19, 5194–5201 (2000). 99. Meyer, E. & Garnier, O. Non-Mendelian inheritance and homology-dependent effects in ciliates. Adv. Genet. 46, 305–337 (2002). 100. Miller, V.M., Xia, H., Marrs, G.L., Gouvion, C.M., Lee, G., Davidson, B.L., and Paulson, H.L. Allele-specific silencing od dominant disease genes. Proc. Natl. Acad. Sci. USA 100, 7195-7200 (2003). 101. Minks MA, West DK, Benvin S, and Baglioni C. Structural requirements of doublestranded RNA for the activation of 2'-5'-oligo(A) polymerase and protein kinase of interferon-treated HeLa cells. J. Biol. Chem. 254:10180-10183 (1979). 102. Miyagishi, M. & Taira, K. U6 promoter-driven siRNAs with four uridine 3′ overhangs efficiently suppress targeted gene expression in mammalian cells. Nature Biotechnol. 20, 497–500 (2002). 103. Mochizuki, K. & Gorovsky, M. A. Small RNAs in genome rearrangement in Tetrahymena. Curr. Opin. Genet. Dev. 14, 181–187 (2004). 104. Moerman, D. & Baillie, D. Genetic organization in Caenorhabditis elegans: fine structure analysis of the unc-22 gene. Genetics 91, 95–104 (1979). 74 105. Montgomery, M.H., Xu, S., Fire, A. RNAas a target of double-stranded RNA-mediated genetic interference in Caenorhabditis elegans. Proc. Natl. Acad. Sci. USA 95, 1550215507 (1998). 106. Mourrain P., C. Beclin, and T. Elmayan. Arabidopsis SGS2 and SGS3 genes are required for posttranscriptional gene silencing and natural virus resistance. Cell. 101: 533-542 (2000). 107. Muchardt, C. et al. Coordinated methyl and RNA binding is required for heterochromatin localization of mammalian HP1a. EMBO Rep. 3, 975–981 (2002). 108. Napoli C, Lemieux C, and Jorgensen R. (1990) Introduction of a chalcone synthase gene into Petunia results in reversible co-suppression of homologous genes in trans. Plant Cell 2: 279-289. 109. Nellen, W. & Lichtenstein, C. What makes an mRNA anti-sense-itive? Trends Biochem. Sci. 18, 419–423 (1993). 110. Noma, K. et al. RITS acts in cis to promote RNA interference-mediated transcriptional and post-transcriptional silencing. Nature Genet. 36, 1174–1180 (2004). 111. Nykanen A, Haley B, and Zamore PD. ATP requirements and small interfering RNA structure in the RNA interference pathway. Cell 107:309-321 (2001). 112. Paddison PJ, Caudy A, and Hannon GJ. Stable suppression of gene expression by RNAi in mammalian cells. Proc. Natl. Acad. Sci. USA 99(3):1443-1448 (2002). 113. Paddison, P. J., Caudy, A. A., Bernstein, E., Hannon, G. J. & Conklin, D. S. Short hairpin RNAs (shRNAs) induce sequence-specific silencing in mammalian cells. Genes Dev.16, 948–958 (2002). 114. Palauqui JC, Elmayan T, Pollien JM, and Vaucheret H. Systemic acquired silencing: transgene-specific post-transcriptional silencing is transmitted by grafting from silenced stocks to non-silenced scions. EMBO J 16: 4738-4745 (1998). 115. Pal-Bhadra, M., Bhadra, U., and Birchler, J.A.. Cosuppression in Drosophila: gene silencing of alcohol dehydrogenase by white-adhtransgene is polycomb dependent. Cell 90, 479-490 (1997). 116. Pandit, N.N. and Russo, V.E.A.. Reversible inactivation of foreign gene, hph, during asexual cycle in Neurospora crassa trasformants. Mol.Gen. Genet. 234, 412-422 (1992). 117. Paul, C. P., Good, P. D., Winer, I. & Engelke, D. R. Effective expression of small interfering RNA in human cells. Nature Biotechnol. 20, 505–508 (2002). 118. Paule, M. R. & White, R. J. Survey and summary: transcription by RNA polymerases I and III. Nucleic Acids Res. 28, 1283–1298 (2000). 119. Peart, J. R., Cook, G., Feys, B. J., Parker, J. E. & Baulcombe, D. C. An EDS1 orthologue is required for N-mediated resistance against tobacco mosaic virus. Plant J. 29, 569–579 (2002). 120. Pélissier, T. & Wassenegger, M. A DNA target of 30 bp is sufficient for RNA-directed DNA methylation. RNA 6, 55–65 (2000). 75 121. Pélissier, T., Thalmeir, S., Kempe, D., Sänger, H.-L. & Wasseneger, M. Heavy de novo methylation at symmetrical and non-symmetrical sites is a hallmark of RNA-directed DNA methylation. Nucl. Acids Res. 27, 1625–1634 (1999). 122. Pfeffer, S. et al. Identification of virus-encoded microRNAs.Science 304, 734–736 (2004). 123. Proud, C. PKR: a new name and new roles. Trends Biochem. Sci. 20, 241–246 (1995). 124. Que, Q., Jorgensen. R.A. Homology-based control of gene expression patterns in transgenic petunia flowers. Dev. Genet. 22, 100-109 (1998). 125. Ratcliff, F., Martin-Hernandez, A. M. & Baulcombe, D. C. Tobacco rattle virus as a vector for analysis of gene function by silencing. Plant J. 25, 237–245 (2001). 126. Reinhart, B.J., Weinstein, E.G., Rhoades, M.W., Bartel, B. And Bartel, D.P.. miRNAs in plants. Genes Dev. 16: 1616-1626 (2002). 127. Romano, N., and Macino, G. Quelling: transient inactivation of gene expression in Neurospora crassa by trasformation with homologous sequences. Mol. Microbiol. 6, 3343-3353 (1992). 128. Ruiz, M. T., Voinnet, O. & Baulcombe, D. C. Initiation and maintenance of virusinduced gene silencing. Plant Cell 10, 937–946 (1998). 129. Ruvkun G. Glimpses of a tiny RNA world. Science 294:797-799 (2001). 130. Schmid A, Schindelholz B, Zinn K. Combinatorial RNAi: a method for evaluating the functions of gene families in Drosophila. Trends Neurosci 25(2):71-74 (2002). 131. Schramke, V. & Allshire, R. Hairpin RNAs and retrotransposon LTRs effect RNAi and chromatin-based gene silencing. Science 301, 1069–1074 (2003). 132. Schwarz, D. S., Hutvagner, G., Haley, B. & Zamore, P. D. Evidence that siRNAs function as guides, not primers, in the Drosophila and human RNAi pathways. Mol. Cell 10, 537–548 (2002). 133. Seydoux, G. & Fire, A. Soma-germline asymmetry in the distributions of embryonic RNAs in Caenorhabditis elegans. Development 120, 2823–2834 (1994). 134. Sharp PA, and Zamore PD. RNA Interference. Science 287: 2431-2433 (2000). 135. Shiu, P. K., Raju, N. B., Zickler, D. & Metzenberg, R. L. Meiotic silencing by unpaired DNA. Cell 107, 905–916 (2001). 136. Sijen, T. et al. Transcriptional and posttranscriptional gene silencing are mechanistically related. Curr. Biol. 11, 436–440(2001). 137. Stam M., R. deBruin, and R. van Blokland. Distinct features of post-transcriptional gene silencing by antisense transgenes in single copy and inverted T-DNA repeat loci. Plant J, 21: 27-42 (2000). 138. Stark, G.R., Kerr, I.M., Williams, B.R., Silverman R.H., and Schreiber, R.D.. How cells respond to interferons. Annu. Rev. Biochem. 67, 227-264 (1998). 76 139. Sui, G. et al. A DNA vector-based RNAi technology to suppress gene expression in mammalian cells. Proc. Natl Acad. Sci. USA 99, 5515–5520 (2002). 140. SV. Wesley, CA. Helliwell, and NA. Smith. Construct design for efficient, effective, and high-throughput gene silencing in plants. Plant J. 27: 581-590 (2001). 141. Svoboda, P., Stein, P. & Schultz, R. M. RNAi in mouse oocytes and preimplantation embryos: effectiveness of hairpin dsRNA. Biochem. Biophys. Res. Commun. 287, 1099–1104 (2001). 142. Tabara H, Grishok A, and Mello CC. RNAi in C. elegans: soaking in the genome sequence. Science 282: 430-431 (1998). 143. Taller, J., Hirata, Y., Yagishita, N., Kita, M. & Ogata, S. Graft-induced genetic changes and the inheritance of several characteristics in pepper (Capsicum annuum L.). Theor. Appl. Genet. 97, 705–713 (1998). 144. Tavernarakis, N., Wang, S. L., Dorovkov, M., Ryazanov, A. & Driscoll, M. Heritable and inducible genetic interference by double-stranded RNA encoded by transgenes. Nature Genet. 24, 180–183 (2000). 145. Thakur, A. RNA interference revolution. Electronic Journal of Biotechnology, vol.6, n° 1, issue of april 15 (2003). 146. Thomas, C. L., Jones, L., Baulcombe, D. C. & Maule, A. J. Size constraints for targeting post-transcriptional gene silencing and for RNA-directed methylation in Nicotiana benthamiana using a potato virus X vector. Plant J. 25, 417–425 (2001). 147. Timmons L, Court D, and Fire A. Ingestion of bacterially expressed dsRNAs can produce specific and potent genetic interference in Caenorhabditis elegans. Gene 263:103-112 (2001). 148. Timmons, L., and Fire, A. Specific interference by ingested dsRNA. Nature 395: 854 (1998). 149. Van der Krol AR., LA. Mur, and M. Beld. Flavonoid genes in petunia: addition of a limited number of gene copies may lead to a suppression of gene expression. Plant Cell 291-299 (1990). 150. Vaucheret H., C. Beclin, and M. Fagard. Post-transcriptional gene silencing in plants. J Cell Sci, 114: 3083-3091 (2001). 151. Verdel A. et.al RNAi-mediated targeting of heterochromatin by the RITS complex. Science 303, 672–676 (2004). 152. Voinnet, O., Vain, P., Angell, S. & Baulcombe, D. C. Systemic spread of sequencespecific transgene RNA degradation in plants is initiated by localized introduction of ectopic promoterless DNA. Cell 95, 177–187 (1998). 153. Volpe, T. A. et al. Regulation of heterochromatic silencing and histone H3 lysine-9 methylation by RNAi. Science 297, 1833–1837 (2002). 154. Vongs, A., Kakutani, T., Martienssen, R. A. & Richards, E. J. Arabidopsis thaliana DNA methylation mutants. Science 260, 1926–1928 (1993). 77 155. Wall, N.R., and Shi, Y.. Small RNA: can RNA interference be exploited for therapy? Lancet 362, 1401-1403 (2003). 156. Wallrath, L. L. & Elgin, S. C. R. Position effect variegation in Drosophila is associated with an altered chromatin structure. Genes. Dev. 9, 1263–1277 (1995). 157. Wassenegger, M., Heimes, S., Riedel, L. & Sänger, H. RNA-directed de novo methylation of genomic sequences inplants. Cell 76, 567–576 (1994). 158. Weiler, K. S. & Wakimoto, B. T. Heterochromatin and gene expression in Drosophila. Annu. Rev. Genetics 29, 577–605 (1995). 159. Williams, B.R.. PKR: a sentinel kinase for cellular stress. Oncogene 18, 6112-6120 (1999). 160. Worby C.A., Simonson-Leff N., Dixon J.E. RNA interference of gene expression (RNAi) in cultured Drosophila cells. Sci STKE Aug 14, 2001(95):PL1 (2001). 161. Wu, H., Hait, Yang, J.M. Small intefering RNA-inducedsuppression of MDR1 (Pglycoprotein) restores sensitivity to multidrug-resistant cancer cells. Cancer Res. 63, 1515-1519 (2003). 162. Xia, H., Mao, Q., Paulson, H.L., and Davidson, B.L. SiRNA-mediated gene silencing in vitro and in vivo. Nat. Biotechnol. 20, 1006-10 (2002). 163. Yang S, Tutton S, Pierce E, and Yoon K. Specific double-stranded RNA interference in undifferentiated mouse embryonic stem cells. Mol. Cell. Biol. 21(22):7807-7816 (2001). 164. Yang, D., Lu, H. & Erickson, J. W. Evidence that processed small dsRNAs may mediate sequence-specific mRNA degradation during RNAi in Drosophila embryos. Curr. Biol. 10, 1191–1200 (2000). 165. Yi, R., Qin, Y., Macara, I.G. And Cullen, B.R. Exportin-5 mediates thenuclear export of pre-microRNAs and short hairpin RNAs. Genes Dev. 17: 3011-3016 (2003). 166. Yu, J.-Y., DeRuiter, S. L. & Turner, D. L. RNA interference by expression of shortinterfering RNAs and hairpin RNAs in mammalian cells. Proc. Natl Acad. Sci. USA 99, 6047–6052 (2002). 167. Zamore PD, Tuschl T, Sharp PA, and Bartel DP. RNAi: Double-stranded RNA directs the ATP-dependent cleavage of mRNA at 21 to 23 nucleotide intervals. Cell 101: 25-33 (2000). 168. Zamore, P.D.. Ancient pathways programmed by small RNAs. Science 296: 1265-1269 (2002). 169. Zeng, Y. & Cullen, B. R. RNA interference in human cells is restricted to the cytoplasm. RNA 8, 855–860 (2002). 170. Zeng, Y., Yi, R. And Cullen, B.R. Recognition and cleavage of primary microRNA precursors by the nuclear processing enzyme Drosha. EMBO J. 24: 138-148 (2005). 171. Zilberman, D., Cao, X. & Jacobsen, S. E. ARGONAUTE4 control of locus-specific siRNA accumulation and DNA and histone methylation. Science 299, 716–719 (2003). 78
Scaricare