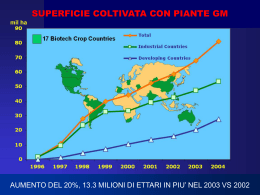
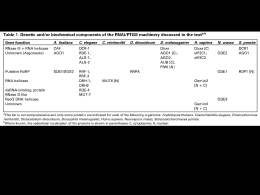
Davide Schiavone Biochimica A.A. 2004-2005 I miRNA NEI MECCANISMI ANTIVIRALI I processi di difesa antivirale operati da RNA sfruttano diversi meccanismi che sono raggruppati sotto il nome di RNA silencing. La prima indicazione del ruolo biologico dell’RNA silencing avvenne in esperimenti di overespressione di transgeni in piante. In tali esperimenti si volevano inserire copie soprannumerarie degli enzimi responsabili della pigmentazione per ottenere piante con fiori intensamente colorati. Cio che inaspettatamente si ottenne furono piante con fiori bianchi. Si comprese in seguito che si erano instaurati dei meccanismi che portavano al silenziamento dei transgeni introdotti e del corrispondente gene endogeno. Una seconda indicazione dell’ esistenza di meccanismi di silenziamento operati da RNA, fu il fatto che piante infettate da virus accumulano vsRNAs (viral short RNAs). Esistono diversi meccanismi tramite cui agisce il silenziamento che si dividono in: silenziamento pre-trascrizionale e silenziamento posttrascrizionale. La maggior parte degli studi sui meccanismi di protezione antivirale operati da RNA sono stati compiuti in piante. I meccanismi antivirali nelle piante Tutti i processi di silenziamento che sono stati individuati nelle piante, hanno la caratteristica comune di essere innescati da dsRNA (double strand RNA). Le fonti primarie di dsRNA variano a seconda del tipo di virus che infetta la pianta. Il caso più comune è rappresentato dai virus a RNA che costituiscono il 90% dei virus delle piante. Tali virus possiedono un genoma ad RNA a singolo filamento e si replicano tramite un intermedio di replicazione a doppio filamento di RNA. Tale dsRNA può essere incorporato dagli enzimi dell’RNA silencing ed innescare il processo di silenziamento. Un’altra fonte di RNA a doppio filamento e costituita dagli hairpin che si formano grazie al ripiegamento di ssRNA virali, sfruttando l’appaiamento di zone omologhe presenti lungo la sequenza. Un discorso analogo può essere fatto per i retrotrasposoni e con i virus a DNA. Il concetto fondamentale e lo stesso, ossia che durante le fasi replicative del virus si vengono a formare degli intermedi di RNA a doppio filamento che possono essere riconosciuti e incorporati dagli enzimi dell’apparato di silenziamento. Fig.1: fonti primarie di dsRNA I pathways antivirali nelle piante Esistono diversi meccanismi di silenziamento che variano a seconda dell’origine del dsRNA. • TGS pathway (transcripional gene silencing): ha luogo nel nucleo ed è solitamente innescato da retrotrasposoni i quali possono produrre dsRNA che sono processati da DCL3 (DICER-like protein 3) a dare siRNA. Un’altra possibilità è che i retrotrasposoni producano ssRNA che vengono utilizzati come stampo da una RNA polimerasi RNAdipendente (RDR2) per produrre dsRNA che vengono a loro volta processati in siRNA. Un’ultima possibilità è che i ssRNA si ripieghino su se stessi a formare hairpin che vengono nuovamente processati per dare siRNA. In tutti e tre i casi il risultato finale è la metilazione del gene target (o del suo promotore) con il conseguente silenziamento trascrizionale. • VIGS pathway (virus-induced gene silencing): il pathway primario ha luogo nel citoplasma in cui DCL2 interagisce con gli stem-loop presenti sull’RNA virale e porta alla formazione di viral small interfering RNA. Questi siRNA di origine virale vengono “srotolati” da una RNA elicasi ed incorporati in RISC che contatta la sequenza target e la degrada clivandola. Esiste un pathway secondario del VIGS in cui i siRNA prodotti nel pathway primario vengono replicati grazie ad una RNA polimerasi, permettendo l’amplificazione del silenziamento. • miRNA pathway: ha origine nel nucleo in cui gli hairpin che si vengono a formare dall’RNA virale sono processati da Dicer a dare dei miRNA che vengono trasportati nel citoplasma da una esportina. Nel citoplasma i frammenti di RNA vengono legati da RISC che degrada le sequenze target. In questo pathway quindi, gli RNA virali danno origine a miRNA i quali vengono però processati come siRNA e come tali agiscono, causando il silenziamento tramite degradazione della sequenza target. I meccanismi tramite i quali si può avere silenziamento genico sono quindi: METILAZIONE e CLIVAGGIO. Fig.2: pathways antivirali nelle piante Il silenziamento è un fenomeno sistemico Una caratteristica molto interessante del sistema di protezione antivirale presente nelle piante è quella di essere in grado di diffondersi da una zona localizzata (ad es.una foglia) all’intera pianta conferendo una resistenza completa contro il virus. Questo fenomeno è stato dimostrato in piante transgeniche per GFP che quando illuminate emettono fluorescenza verde.Iniettando in una foglia di queste piante un costrutto in grado di dare origine a siRNA anti-GFP si osserva una scomparsa della fluorescenza a livello locale indicando che effettivamente si ha la distruzione dell’mRNA codificante per GFP. Con il passare del tempo si osserva però che la fluorescenza scompare anche in altre zone, inizialmente lungo i vasi linfatici ed in seguito in tutta la pianta. Questo avviene grazie ad un meccanismo di amplificazione dei siRNA (siRNA amplification cycle) operato da RNA polimerasi RNAdipendenti (RDR6) e da elicasi (SDE3). I siRNA così amplificati sono in grado di diffondere alle cellule adiacenti tramite dei canali e diffondere il silenziamento all’intera pianta. Questo meccanismo può quindi essere considerato un vero e proprio sistema immunitario GENETICO della pianta in quanto conferisce una protezione contro agenti virali in modo altamente specifico (sequenzaspecifico) e diffuso all’intera pianta. Fig.3: induzione sistemica del silenziamento nelle piante Strategie virali anti-silenziamento Come in tutte le interazioni ospite-parassita, i virus hanno evoluto delle contromosse per sfuggire ai meccanismi di silenziamento operati dalle piante. Queste strategie virali operano in vario modo, ad esempio: • Interferendo con le molecole effettrici: è stata identificata una proteina virale, la proteina P19 in grado di legare i siRNA ed i miRNA non rendendoli disponibili a RISC e bloccando il silenziamento. La cosa sorprendente e che questa proteina funziona con tutti i siRNA/miRNA (basta che abbiano una lunghezza di circa 21 bp) sia nelle piante che in altri organismi come C.elegans e addirittura nell’uomo (come si vedrà più avanti). • Alterando il trascrittoma dell’ospite: alcuni virus sono in grado di far produrre alla pianta delle proteine endogene in quantità molto maggiore rispetto al normale.Tali proteine ad alte concentrazioni si comportano da dominanti-negativi nei confronti di altre proteine del pathway di silenziamento inibendolo. • Producendo miRNA/siRNA difettivi: i virus sono in grado di mutare rapidamente portando alla formazione di hairpin con strutture anomale (es. diverso ripiegamento della sequenza di RNA e formazione di loop in zone differenti) che non vengono riconosciute dall’ apparato di silenziamento. • Evadendo il sistema di silenziamento: alcuni virus adottano una strategia evasiva piuttosto che inibitoria e compiono tutti gli stadi replicativi racchiusi in vescicole. In questo modo le fasi più pericolose per il virus in cui si vengono a formare degli intermedi a dsRNA che possono innescare i processi di silenziamento avvengono in compartimenti isolati. Esiste quindi una continua lotta che vede contrapposti i meccanismi difensivi adottati dalle piante contro i meccanismi evasivi virali. E’importante notare che i meccanismi di RNA silencing di difesa contro i virus presenti nelle piante sono basati sul processo dell’RNA interference. E per quanto riguarda i vertebrati? Meccanismi antivirali analoghi a quelli presenti in piante ed insetti non erano mai stati dimostrati fino all’uscita di un lavoro che dimostra la presenza di un meccanismo di silenziamento mediato da miRNA nelle cellule umane. Proteina inibitoria P19 Alterazione del trascrittoma dell’ospite Produzione di siRNA difettivi La difesa antivirale nei vertebrati (Lecellier et al. A cellular microRNA mediates antiviral defense in human cells SCIENCE 2005 VOL308 557) In questo articolo è riportato lo studio sul virus PFV-1, un retrovirus della famiglia dell’HIV in grado di infettare cellule umane. Ciò che ha attirato l’attenzione dei ricercatori è stata l’osservazione che cellule esprimenti la proteina virale P19 (la proteina in grado di legare i siRNA/miRNA vista in precedenza) accumulano RNA virale. Questo ha suggerito ai ricercatori la presenza di un pathway di siRNA o miRNA operante nelle cellule in grado di limitare la replicazione virale. Per dimostrare l’esistenza di tale meccanismo hanno trasfettato delle cellule wild-type con dei costrutti costituiti da vari frammenti del genoma virale legati al gene reporter GFP. Hanno quindi osservato che i livelli proteici di GFP di uno dei costrutti (GFP-F11) era nettamente più basso, pur non variando la quantità di mRNA. E’ stata quindi ipotizzata la presenza di un meccanismo di silenziamento traduzionale operato da miRNA. La sequenza del costrutto F11 è stata quindi inserita in un programma di predizione computazionale che ha trovato una corrispondenza ad alta probabilità con il microRNA umano miR-32. Il passo successivo è stato quello di andare a vedere se effettivamente il miR-32 è in grado di silenziare la traduzione di GFP legata alla sequenza target del microRNA. E’ stato visto che effettivamente si ottiene il silenziamento della sequenza target ma non della stessa sequenza contenente mutazioni. Dimostrata la presenza e l’efficacia di un miRNA antivirale i ricercatori sono andati a ricercare l’eventuale presenza di una proteina virale anti-silenziamento. Il fatto che i virus delle piante puntualmente sviluppano delle contromosse difensive ha fatto ritenere che lo stesso fenomeno dovesse verificarsi anche nelle cellule di vertebrato. L’attenzione è stata rivolta verso la proteina virale Tas (ritenuta interessante grazie a studi bioinformatici) e la sua efficacia è stata testata in un sistema eterologo: Arabidopsis. Questo tipo di pianta normalmente produce dei semi di colore marrone a causa di un pigmento prodotto dall’enzima Calcone Sintasi. Esiste una linea transgenica di Arabidopsis che esprime un costrutto che da origine ad un siRNA contro la Calcone Sintasi con la conseguente produzione di semi gialli a causa della mancata produzione di pigmento. L’espressione di Tas in tali piante porta alla produzione di semi marroni come nelle piante wild-type, confermando che tale proteina virale è in grado di inibire i pathway di miRNA/siRNA. Conclusioni Questo lavoro ha dimostrato che un meccanismo antivirale basato sul fenomeno dell’RNA silencing è presente anche nei vertebrati e che si tratta quindi di un meccanismo conservato dall’evoluzione. La dimostrazione dell’esistenza di tale meccanismo nelle cellule umane, apre inoltre interessanti prospettive terapeutiche in chiave di terapie antivirali anche se si tratta solo di uno studio preliminare che richiede ulteriori chiarimenti e dimostrazioni. Bibliografia : • • • • • Voinnet Induction and suppression of RNA silencing: insights from viral infection NATURE 2005 Vol.6 , 206-221 Lecellier et al. A cellular MicroRNA mediates antiviral defense in human cells SCIENCE 2005 Vol.308 , 557-560 Waterhouse et al. Gene silencing as an adaptive defence against viruses NATURE 2001 Vol 411, 834-842 Voinnet RNA silencing as a plant immune system against viruses TRENDS in Genetics 2001 Vol.17, 449-459 Bartel MicroRNAs:genomics, biogenesis mechanism, and function Cell 2004 Vol.116, 281-297
Scaricare