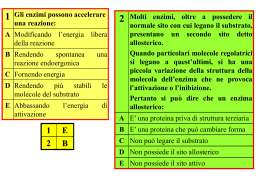
Corso di “Modellistica dei Sistemi Biologici” A.A. 2008/09 Cinetiche di Reazione Docente: ing. Carlo Cosentino Lab. di Biomeccatronica E-mail: [email protected] Tel: 0961-369-4051 URL: http://bioingegneria.unicz.it http://wpage.unina.it/carcosen Università degli Studi Magna Græcia di Catanzaro I anno – II semestre CdL specialistica in Ingegneria Biomedica Corso di Modellistica di Sistemi Biologici – Ing. C. Cosentino – A.A. 2008/09 1 Equilibrio e Velocità di Reazione L’equilibrio è legato alla variazione di energia biochimica libera standard, ∆G’° La velocità della reazione, invece, è determinata dall’energia di attivazione, ∆GS‡→ P 2 Equilibrio di Reazione k1 S → P Si consideri la semplice reazione reversibile S ← P k −1 Essa può essere descritta dal sistema di eq. d [S ] = − k1 [S ] + k −1 [P ] [P] = k1 dt ′ = K eq d [P ] [S ] k−1 = k1 [S ] − k −1 [P ] dt Dalla termodinamica, si ha che la costante di equilibrio ′ ∆G′° = − RT ln K eq R (costante dei gas) = 8.315 J/mol·K T (temperatura assoluta) = 298 K (25 °C) 3 Velocità di Reazione La velocità della reazione è determinata da concentrazione dei singoli reagenti una costante cinetica, in genere indicata con k k → P la velocità di reazione è Ad es. la reazione S V = k [S ] Dalla teoria dello stato di transizione si ha kT − ∆G RT k= e h dove k e h sono la costante di Boltzmann e Planck rispettivamente ‡ 4 Cinetica Enzimatica Gli enzimi sono una tipologia di proteine specializzate nella catalisi delle reazioni I catalizzatori non reagiscono, ma favoriscono la reazione diminuendo la soglia di energia necessaria alla formazione del prodotto Nel caso degli enzimi questo avviene tramite la formazione di un composto enzima-substrato, da cui poi il substrato viene trasformato nel prodotto finale della reazione 5 Ruolo degli Enzimi Gli enzimi giocano un ruolo chiave in tutti i processi biologici Essi hanno un ruolo importante nella regolazione delle vie metaboliche Molte malattie sono causate dalla carenza o assoluta mancanza di enzimi Molti farmaci agiscono interagendo con gli enzimi 6 Enzimi: Funzionamento Le reazioni catalizzate da enzimi avvengono in una ansa chiamata sito attivo in cui si formano condizioni favorevoli alla reazione La molecola che si lega al sito attivo viene chiamata substrato La superficie del sito attivo viene delineata da amminoacidi i cui residui legano il substrato e ne catalizzano la trasformazione 7 Reazione di Michaelis-Menten Il modello base di reazione enzimatica è stato proposto da Michaelis e Menten nel 1913 dove k 1, k -1, k 2 sono costanti positive associate ai tassi di reazione L. Michaelis (1875-1949) La legge di azione di massa ci dice che il tasso di reazione è proporzionale al prodotto della concentrazione dei reagenti A+ B → C k d [C ] = k [A][B ] dt M. Menten (1879-1960) 8 Reazione di Michaelis-Menten Dalla reazione ricaviamo il seguente modello s = −k1es + k −1c, e = −k1es + (k −1 + k 2 )c c = k1es − (k −1 + k 2 )c, p = k 2 c dove abbiamo indicato le concentrazioni delle varie specie come s := [S ], e := [ E ], c := [ES ], p := [P ] e le condizioni iniziali sono s(0)=s0, e(0)=e0, c(0)=0, p(0)=0 Si noti che l’eq. di p è disaccoppiata dalle altre e fornisce t p(t ) = k 2 c(τ )dτ ∫ 0 9 Modello Semplificato La quantità totale di enzima, libero più legato, rimane invariata nel tempo, come si può vedere anche sommando la seconda e terza eq. e + c = 0 ⇒ e(t ) + c(t ) = e0 per cui possiamo derivare e(t) e sostituire, ottenendo il sistema semplificato in due equazioni s = −k1e0 s + (k1s + k −1 )c, c = k1e0 s − (k1s + k −1 + k 2 )c, s (0 ) = s0 c(0 ) = 0 10 Modello Semplificato Tipicamente la formazione iniziale del complesso ES è molto veloce, dopodichè rimane all’equilibrio Ciò si traduce nell’assumere dc/dt ≈ 0, da cui e0 s(t ) c(t ) = s(t ) + K m k 2 e0 s ⇒ s = − s + Km dove la costante positiva k −1 + k 2 Km = k1 è detta costante di Michaelis-Menten 11 Approssimazione di Pseudo-Regime La quantità di enzima si assume tipicamente piccola rispetto a quella di substrato, per cui quest’ultima rimane pressoché invariata durante la formazione del complesso s(0)=s0 Dall’eq. di s otteniamo la soluzione implicita s(t ) + K m ln s (t ) = s0 + K m ln s0 Si noti che l’eq. di c(t) non soddisfa la cond. iniz. c(0)=0, ma l’approssimazione vale in molti casi Esistono due scale temporali, una corrispondente alla formazione del complesso, l’altra relativa alla trasformazione del substrato 12 Validità dell’Approssimazione Per stabilire il range di validità del modello approssimato dobbiamo rispondere a diverse domande Quanto è veloce il transitorio iniziale? Per quali valori di parametri sono sufficienti le approssimazioni di pseudo-regime? Cosa accade se la concentrazione di enzima non è effettivamente piccola rispetto a quella di substrato? 13 Adimensionalizzazione Per rispondere alle domande precedenti dobbiamo innanzitutto adimensionalizzare il sistema, mediante le trasformazioni s(t ) c(t ) , v(τ ) = , τ = k1e0t , u (τ ) = s0 e0 e0 k2 k −1 + k 2 K m , K= , ε= = λ= k1s0 k1s0 s0 s0 Che è una scelta ragionevole se ε <<1, ossia quando l’enzima è presente in quantità molto minore del substrato 14 Adimensionalizzazione Utilizzando le trasformazioni precedenti otteniamo il sistema u = −u + (u + K − λ )v, u (0 ) = 1 ε v = u − (u + K )v, v(0 ) = 0 si noti che K-λ>0 Non è possibile ricavare una soluzione analitica, ma si può abbozzare l’andamento studiando il segno delle derivate al variare di u 15 Stima del Transitorio Sfruttando il fatto che s0 non varia apprezzabilmente durante il transitorio iniziale si può valutare la durata di questo dall’eq. di c c = k1e0 s0 − k1 (s0 + K m )c La costante di tempo associata a questo sistema del primo ordine è 1 tc = k1 (s0 + K m ) Una stima della durata della dinamica di s si ottiene considerando la derivata massima s0 s0 + K m ts ≈ ≈ ds dt max k 2 e0 16 Stima del Transitorio Sulla base delle stime effettuate, la condizione che il transitorio iniziale sia molto veloce rispetto alla dinamica della trasformazione del substrato, ossia tc<<ts si riscrive k 2 e0 k1 (s0 + K m ) 2 << 1 Un’altra condizione per la validità dell’approssimazione è che la deplezione di S durante il transitorio iniziale sia una frazione trascurabile del totale, ossia |∆s/s0|<<1 ε= e0 << 1 s0 + K m La condizione precedente si ottiene considerando una stima per eccesso di ds/dt, derivabile dalla eq. nel modello del 2° ordine (v. lucido 10) ∆s ≤ 1 ds tc = k1e0 s0 ⋅ dt max k1 (s0 + K m ) 17 Condizione di Pseudo-Regime Si noti, tuttavia, che il primo vincolo si può riscrivere come k 2 e0 e0 1 = ⋅ << 1 2 s0 + K m 1 + (k −1 k 2 ) + (s0 k1 k 2 ) k1 (s0 + K m ) Il secondo vincolo risulta, pertanto, più stringente e può essere considerato come condizione di validità dell’approssimazione di pseudoregime Si noti inoltre che, anche se e0/s0=O(1), l’approssimazione rimane valida se Km è grande 18 Parametri Sperimentali Nella pratica sperimentale si misurano due parametri La costante di Michaelis-Menten La velocità massima di reazione Q = [R0 ]max = k 2 e0 k 2 e0 s0 Qs0 R0 = = s0 + K m s0 + K m 19 Substrato Suicida Un processo enzimatico di particolare importanza è quello descritto dal modello di Walsh (1978) dove E, S, P sono rispettivamente enzima, substrato e prodotto, X, Y sono prodotti intermedi, Ei è l’enzima inattivato e le k sono costanti positive Il rapporto r:=k3/k4 è chiamato coefficiente di partizione 20 Substrato Suicida S viene detto substrato suicida ed è capace di legarsi al sito attivo dell’enzima come un comune substrato L’enzima lo converte in un inibitore che inattiva in maniera irreversibile l’enzima stesso I substrati suicidi sono importanti perché forniscono un metodo per inattivare uno specifico enzima L’uso principale è nella somministrazione di farmaci, perché non sono dannosi nella forma comune e solo l’enzima specifico li può convertire nella forma inibitoria (ad es. trattamento della depressione, epilessia, alcuni tumori) 21 Substrato Suicida La cinetica dei substrati suicidi è stata studiata a fondo da Waley (1980) e Tatsunami (1981) Questi studi si concentrano sul meccanismo che permette o meno al substrato di essere interamente trasformato prima che tutto l’enzima sia inattivato Waley ha concluso che questo dipende dal valore r e0 s0 Tatsunami ha proposto come indice il valore (1 + r ) e0 (1 + r ) e0 (1 + r ) e0 s0 s0 < 1 Tutto l’enzima è inattivato s0 > 1 Il substrato viene trasformato interamente 22 Equazioni Cinetiche Applicando la legge di azione di massa s = −k1es + k −1 x e = −k1es + k −1 x + k 3 y x = k1es − k −1 x − k 2 x y = k 2 x − k 3 y − k 4 y ei = k 4 y p = k 3 y e(0) = e0 , s (0) = s0 , x(0) = y (0) = ei (0) = p (0) = 0 23 Modello Ridotto Anche in questo caso si può sfruttare la conservazione della quantità totale di enzima e + x + y + ei = e0 e il fatto che l’eq. di p è disaccoppiata dalle altre s = − k1 (e0 − x − y − ei )s + k −1 x x = k1 (e0 − x − y − ei )s − (k −1 + k 2 )x y = k 2 x − (k 3 + k 4 ) y ei = k 4 y Studieremo il sistema risolvendo numericamente le eq. 24 Fenomeni Cooperativi Nel modello base abbiamo supposto che una molecola di enzima si combini con una sola di substrato Molte proteine hanno più di un sito di legame, ad es. l’emoglobina ha quattro siti per le molecole di ossigeno Una reazione tra un enzima e un substrato si dice cooperativa se una singola molecola di enzima, dopo aver legato una molecola di substrato ad un sito, può legarne un’altra ad un altro sito 25 Effetto Allosterico Una tipologia di reazione cooperativa molto importante si ha quando il legame di un substrato ad un sito può influenzare il legame di altri substrati ad altri siti (enzima allosterico) Un substrato viene detto attivatore o inibitore a seconda che aumenti o diminuisca l’attività di legame in altri siti Se la specie substrato funge anche da modulatore l’interazione si dice omotropica, altrimenti eterotropica 26 Esempio di Reazione Cooperativa Consideriamo ora un semplice esempio di reazione cooperativa in cui un enzima ha due siti di legame Calcoliamo l’approssimazione a pseudo-regime e la funzione di trasformazione del substrato 27 Equazioni Cinetiche Applicando la legge dell’azione di massa otteniamo s = − k1se + (k −1 − k 3 s )c1 + k −3c2 c1 = k1se − (k −1 + k 2 + k 3 s )c1 + (k −3 + k 4 )c2 c2 = k 3 sc1 − (k −3 + k 4 )c2 e = − k1se + (k −1 + k 2 )c1 p = k 2 c1 + k 4 c2 s(0) = s0 , e(0) = e0 , c1 (0) = c2 (0) = p(0) = 0 La conservazione dell’enzima fornisce e + c1 + c2 = e0 28 Modello Ridotto Analogamente ai casi precedenti troviamo il modello ridotto s = −k1e0 s + (k −1 + k1s − k 3 s )c1 + (k1s + k −3 )c2 c1 = k1e0 s − (k −1 + k 2 + k1s + k 3 s )c1 + (k −3 + k 4 − k1s )c2 c2 = k 3 sc1 − (k −3 + k 4 )c2 e adimensionalizziamo usando le relazioni c1 c2 k −1 s , τ = k1e0t , u = , v1 = , v2 = , a1 = k1s0 s0 e0 e0 k3 k e k2 k a2 = , a3 = , a 4 = − 3 , a5 = 4 , ε = 0 k1s0 k1 k1s0 k1s0 s0 29 Modello Adimensionale Sostituendo otteniamo u = −u + (u − a3u + a1 )v1 + (a4 + u )v2 ε v1 = u − (u + a3u + a1 + a2 )v1 + (a4 + a5 − u )v2 ε v2 = a3uv1 − (a4 + a5 )v2 u (0 ) = 1, v1 (0 ) = v2 (0) = 0 Come nei casi precedenti è possibile considerare a regime le eq. relative a v1 e v2, ricavare queste quantità in funzione di u e sostituire nella prima eq., ottenendo u = −u a 2 + a3 a5u (a 4 + a5 )−1 a1 + a 2 + u + a3u (a 4 + a5 ) 2 −1 = −r (u ) < 0 30 Velocità Massima di Reazione Riportando in formato dimensionale troviamo la velocità di reazione di Michaelis-Menten per e0/s0<<1 ds R0 (s0 ) = dt dove t =0 k 2 K m′ + k 4 s0 = e0 s0 K m K m′ + K m′ s0 + s02 k 4 + k −3 k −1 + k 2 Km = , K m′ = k1 k3 sono le costanti di Michaelis-Menten delle due reazioni 31 Curve di Hill La curva risultante può differire da quella di una reazione base, come mostrato in figura 2 s → 0 ⇒ R ∝ s Ad es., per k2=0 si vede subito che 0 0 0 In questo caso l’andamento viene approssimato con una curva di Hill Qs0n R0 (s0 ) = n , n>0 n s0 + K m 32 Curve di Hill Si noti che il numero n non è necessariamente intero, inoltre si definiscono i seguenti casi n>1 cooperazione positiva n<1 cooperazione negativa n=1 cooperazione nulla Alla stessa relazione (ma con n intero) si arriva considerando un modello di enzima che lega contemporaneamente n molecole substrato, ossia E+nS E+nP 33 Autocatalisi Molti processi biologici hanno un meccanismo insito di regolazione mediante retroazione (feedback) In pratica la regolazione si basa sul fatto che il prodotto di una reazione può influenzare la storia futura del processo L’effetto di regolazione è generalmente nonlineare e può essere sia di attivazione che di inibizione nei confronti della reazione In particolare l’autocatalisi è il processo per cui una specie viene utilizzata nella reazione che la produce, ad es. 34 Esempi di Autocatalisi Se la concentrazione della specie A viene mantenuta costantemente al livello a, possiamo scrivere x = k1ax − k −1 x 2 ⇒ k1a x(t ) → x S = k −1 Il sistema ha due punti di equilibrio, x=0 instabile e x=xS stabile La retroazione è fornita dal prodotto stesso, che inibisce la formazione di ulteriore prodotto: l’intensità dell’azione inibente cresce con il quadrato della concentrazione Il meccanismo è analogo a quello studiato nelle popolazioni monospecie 35 Esempi di Autocatalisi Si consideri la reazione e si supponga che a e b vengano mantenuti costanti x = (k1a − k 2 b )x − k −1 x 2 Il sistema ha una biforcazione quando k1a-k2b=0, infatti k 1a-k 2b>0 L’origine è un p. di equilibrio instabile, infatti il tasso di produzione è maggiore di quello di trasformazione k 1a-k 2b<0 L’origine è un p. di equilibrio stabile , infatti il tasso di produzione è minore di quello di trasformazione 36 Esempi di Autocatalisi Un ulteriore esempio di autocatalisi è il modello di oscillatore biologico ideale proposto da Lotka dove la concentrazione di A è mantenuta costante Si noti che le prime due reazioni sono autocatalitiche Applicando la legge dell’azione di massa riotteniamo le equazioni di Lotka-Volterra x = k1ax − k 2 xy y = k 2 xy − k 3 y 37 Grafico di Lineweaver-Burke Il grafico di L-B, detto anche dei doppi reciproci, si ricava invertendo ambo i membri dell’eq. della velocità di reazione 1 K m + [S ] = V0 Vmax [S ] Km 1 1 = + V0 Vmax [S ] Vmax 38 Reazione Uni-Uni Reazione enzimatica unireactant-unireactant E+S k2 k k k 1→ ← ES 3→ ← k4 EP 5→ ← E+P k6 VMr VMf [S ] − r [P] f Km d [P ] K m = [S ] [P] dt 1+ f + r Km Km [P]eq K eq = [S ]eq VMf K Mr = r f VM K M Relazione di Haldane 39 Reazione Bi-Bi Reazioni enzimatiche bi-substrate Vmax d [P ] = S1 S 2 K s K m K mS1 K mS 2 dt + + +1 [S1 ][S 2 ] [S1 ] [S 2 ] Ordered Bi-Bi 40 Reazione Ping-Pong Bi-Bi In questo caso non avviene la formazione di complesso ternario V d [P ] = S1 max S 2 Km Km dt + +1 [S1 ] [S 2 ] N.B. Rispetto al caso precedente c’è un parametro in meno 41 Bi-Bi vs Ping-Pong L’andamento nel tempo è simile La differenza si evince dal comportamento al variare della concentrazione di S2 Bi-Bi Ordinata Ping-Pong 42 Inibizione Enzimatica Inibizione Reversibile Competitiva Mista (non competitiva) Incompetitiva Inibizione Irreversibile e.g. substrato suicida 43 Inibizione Competitiva L’inibitore ed il substrato si legano allo stesso sito Vmax [S ] d [P ] = αK m + [S ] dt α = 1+ [I ] , KI KI = [E ][I ] [EI ] 44 Inibizione Competitiva 45 Inibizione Incompetitiva Siti di legame differenti L’inibitore si lega solo al complesso ES Vmax [S ] d [P ] = dt K m + α ′[S ] α ′ = 1+ [I ] , K I′ K I′ = [ES ][I ] [ESI ] 46 Inibizione Incompetitiva 47 Competizione Mista Siti di legame diversi L’inibitore può legarsi sia a E sia a ES Vmax [S ] d [P ] = dt αK m + α ′[S ] α = 1+ α ′ = 1+ [I ] , KI [I ] , K I′ [E ][I ] [EI ] [ ES ][I ] ′ KI = [ESI ] KI = Se α= α’ l’inibizione viene detta non-competitiva 48 Competizione Mista 49 Dipendenza da altri Fattori Bisogna ricordare che le reazioni enzimatiche sono fortemente dipendenti da altri fattori, e.g. pH e temperatura 50 Modelli Fenomenologici In molti casi reali di interesse non si conosce in maniera dettagliata la lista di reazioni che genera un certo processo biologico Più realisticamente si può ricavare sperimentalmente l’effetto globale al variare di una specie o delle condizioni al contorno In questo caso non si può utilizzare l’approccio visto finora, trasformando direttamente le reazioni in eq. differenziali Il modello, quindi, è costituito da opportuni termini matematici che descrivono i vari fenomeni pur non rappresentandone i meccanismi biochimici di base 51 Esempi di Modelli Fenomenologici Si consideri il seguente modello a − cu b+v v = du − ev u = con a, b, c, d, e costanti positive L’interpretazione biologica di queste eq. è che u attiva v, attraverso un termine du , e entrambe u e v sono degradate in maniera linearmente proporzionale alla loro concentrazione (si parla in questo caso di cinetica del primo ordine) Il termine a/(b+v) porta in conto l’effetto di inibizione esercitato da v su u, infatti il tasso di produzione di u è tanto più piccolo quanto maggiore è la concentrazione di v 52 Esempi di Modelli Fenomenologici Il meccanismo di Thomas (1975) è stato sviluppato per descrivere la reazione dei substrati ossigeno e acido urico in presenza dell’enzima urease u = a − u − ρR(u , v ) v = α (b − v ) − ρR(u , v ) uv R(u , v ) = 1 + u + Ku 2 Effetto di inibizione del substrato 53 Esempi di Modelli Fenomenologici Un ulteriore modello di sistema attivatore (u) - inibitore (v) u = a − bu + ( u2 v 1 + Ku 2 ) v = u 2 − v L’attivatore u è un prodotto autocatalitico, come descritto dal termine u 2/[v(1+Ku 2) ] , ma il tasso di produzione satura al valore 1/Kv per u→∞ L’inibitore v è attivato da u, ma ne inibisce la produzione 54
Scaricare