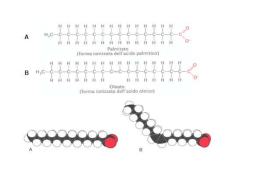
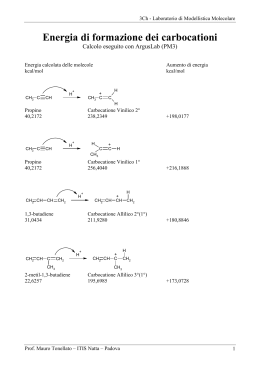
Esercitazione n. 7 - Risonanza. 1. Quale delle strutture di risonanza per ognuna delle seguenti serie contribuisce di più alla descrizione della struttura reale? contributo maggiore a) .. NH2 H .. H + NH2 C O- O b) O- CH2 H + NH2 H H O O + .. CH3-CH-OH .. c) + CH3CH=OH .. Od) CH2 + CH3 CH2 - O C+ CH3 O CH2 CH3 CH2 2. Quale delle strutture di risonanza per ognuna delle seguenti serie contribuisce di meno alla descrizione della struttura reale? contributo minore a) O + N O H3C -O 2+ N O H3C H3C b) H3C C O NH2 H3 C O + N O C O- + NH2 H3C + NH2 C O- 1 3. Quali dei seguenti composti sono stabilizzati per risonanza? Scrivere le strutture corrispondenti: CH3CH2CH3; CH2=CH2; CH3OSO3-; CH3CO2H; CH3-O-CH3; CH2=CH-O-CH3; CH3CN; CH2=CH-CN non ci sono elettroni mobili CH3CH2CH3 CH2=CH2 + CH2 CH2 + CH2 CH2 O- CH3OSO3- 2+ H3C O S O- OO- 2+ H3C O S OOO 2+ H3C O S OO- O + H3C O S O- .. CH3-O-CH .. 3 CH2=CH-O-CH3 CH3CN CH2=CH-CN H3C O S O - OO+ H3C O S O O OH3C O S O O O O+ H3C O S O O- O- OH3C C + O .. H O CH3CO2H O H3C C O .. H H3C C +O H nessuna struttura di risonanza .. CH2=CH-O-CH .. 3 H3C C N : + 2-CH=O-CH3 .. - CH + .. H3C C N: H2C CH C N : H2C + .. CH C N: + CH2 CH C .. N: 2 4. Scrivere le strutture canoniche di risonanza dei seguenti composti: a) acetammide (=etanammide) : O: .. CH3 C NH2 .. : O: .. :O: .. CH3 C NH2 + + CH3 C NH2 + .. CH3 C N : b) acetonitrile (= etanonitrile) CH3 C N : c) 2-butenenitrile + CH C N CH3 CH CH3 CH CH C N O CH3 C CH2 CH3 O CH3 C CH2 CH3 d) butanone e) 3-buten-2-one O CH3 C CH CH2 f) butadiene + O CH3 C CH CH2 CH2 CH + CH CH2 CH2 CH2 CH CH CH2 + g) metil vinil etere O + CH3 C CH CH2 + + CH2 CH CH CH2 CH2 CH CH + CH3 CH CH C N .. CH3 O CH CH2 .. + CH2 CH CH CH2 + CH3 O CH CH2 h) 1-nitropropano + O CH3CH2 CH2 N O 2+ CH3 CH2 CH2 N OO + O - CH3 CH2 CH2 N O i) propanoato di metile O CH3 CH2 C O CH3 O CH3 CH2 C O CH3 + O + CH3 CH2 C O CH3 3 5. Dare il nome ai seguenti composti. Sulla base della regola di Hückel, indicare quali sono aromatici e quali no. Spiegare i motivi della scelta. Regola di Hückel: Anelli monociclici planari, in cui tutti gli atomi dell'anello partecipano con un orbitale p alla formazione degli orbitali molecolari, sono aromatici se hanno negli orbitali p un numero di elettroni pari a (4n + 2) dove n è un numero intero della serie naturale ..- + ciclopropene NO: c’è C sp3 ciclobutadiene NO: 4 elettroni p S catione ciclopropenilio SI’: 2 elettroni p (n = 0) ciclopentadiene NO: c’è C sp3 anione ciclopropenato NO: 4 elettroni p + catione ciclopentadienilio NO: 4 elettroni p O tiaciclopentadiene SI’: 6 elettroni p (n = 1) 4 dei C + 2 di S + catione pirilio SI’: 6 elettroni p (n = 1) cicloeptatriene NO: c’è C sp3 5 dei C + 1 di N :anione cicloeptatrienato NO: 8 elettroni p + catione cicloeptatrienilio SI’: 6 elettroni p (n = 1) NH 1H-azacicloeptatriene NO: 4 elettroni p 6 dei C + 2 di N 4 7. Scrivere le strutture canoniche di risonanza dei seguenti composti: a) benzene b) naftalene c) antracene d) fenantrene 8. Scrivere le strutture di risonanza dei seguenti composti: a) piridina + + N N - N N + N - - b) pirrolo +N H - +N H .. N H +N H - +N H c) anione ciclopentadienato - .. - - - 5 d) catione cicloeptatrienilio + + + + + + + e) 1-naftolo + : OH OH + + OH OH - OH + + + OH OH OH - + OH OH - 6 f) 2-naftolo .. OH - + + OH OH - OH + OH + - + OH + OH OH OH Esercitazione n. 8 - Aspetti generali di reazioni e meccanismi 1. Dare una definizione dei seguenti termini: coordinata di reazione; stadio di una reazione; stato di transizione, reagente radicalico; scissione eterolitica; scissione omolitica; carbocatione; nucleofilo; elettrofilo; reversibilità microscopica; energia libera standard; energia libera di attivazione; costante di velocità; costante di equilibrio; stadio lento; controllo cinetico; controllo termodinamico. coordinata di reazione stadio di una reazione stato di transizione reagente radicalico scissione eterolitica scissione omolitica grandezza che indica il progredire della reazione processo elementare da substrato a prodotto massimo di energia lungo il percorso da reagente a prodotto in ciascuno stadio, caratterizzato da legami parziali Specie con un elettrone spaiato, che utilizza per la formazione di un nuovo legame covalente (con un altro reagente radicalico) rottura di un legame covalente, che lascia i due elettroni su uno degli atomi che formavano il legame rottura di un legame covalente, che lascia un elettrone su ciascuno degli atomi che formavano il legame 7 carbocatione nucleofilo elettrofilo reversibilità microscopica energia libera standard energia libera di attivazione costante di velocità costante di equilibrio stadio lento controllo cinetico controllo termodinamico specie con un C con tre soli legami ed un orbitale vuoto (elettrofilo) specie ricca di elettroni, che partecipa alla formazione di legame con un ORBITALE PIENO (coppia di elettroni n). specie a difetto elettronico, che partecipa alla formazione di legame con un ORBITALE VUOTO principio secondo il quale la variazione dell’energia in funzione della coordinata di reazione segue lo stesso percorso (quello di minima energia) in entrambe le direzioni: da reagente a prodotto e da prodotto a reagente. differenza di energia libera tra reagenti e prodotti differenza di energia libera tra reagenti e stato di transizione grandezza che esprime la reattività di un composto, indipendentemente dalla sua concentrazione (a differenza della velocità di reazione) grandezza che indica il rapporto tra prodotto e reagente all’equilibrio (quando, cioè, la loro concentrazione non cambia più, ma per ogni molecola di substrato che diventa prodotto, ce ne è una di prodotto che torna a substrato Stadio che, in una reazione multistadio, ha l’energia di attivazione più alta Composizione dei prodotti (provenienti da uno stesso substrato) che riflette le rispettive energie di attivazione Composizione dei prodotti (provenienti da uno stesso substrato) che riflette le rispettive energie libere 8 3. Considerando il seguente diagramma dell'energia: stadio lento a) Quale è lo stadio lento di A D? b) Quale è il DG° di C D? c) Quale è il DG di A C? d) Quale è il DG di D C? C D DG° = -30 kcal/mole, -120 kJ/mole A C D C DG =/ = +25 kcal/mole, +100 kJ/mole DG =/ = +40 kcal/mole, +160 kJ/mole 5. A temperatura ambiente una reazione reversibile mette in equilibrio A e B, in rapporto 85:15. Quale è la differenza di energia libera tra A e B? A B K= B A = 15 85 = 0.17 DG° = - RT ln K = - 2.303 RT log 0.17 = + 1 kcal/mole 9 7. Indicare tra le seguenti specie gli elettrofili ed i nucleofili: E BF3 H+ CH2=CH2 CH3O- CN- H2O AlCl3 (CH3)3C+ H2 HBr H+ Ne PH3 NH3 d+ CH3Cl Cu2+ .. .. HO-NH2 H3C C CH3CH2S Br- .. CH3NH2 Hd+ I- H2C O CH Nu Hg2+ 8. Completare le seguenti reazioni, mettendo le frecce curve che indicano la direzione di flusso degli elettroni: a) H .. H N H .. H Br: .. b) H2C HC + H +H O H H + H N H H .. :Br: .. H + H2C CH .. + HOH .. H Br H2C CH 10 9. Ciascuna delle seguenti molecole è un elettrofilo. Individuare l’atomo elettrofilo in ciascun caso e scrivete il prodotto di reazione con un generico nucleofilo Nu-. Elettrofilo: specie a difetto elettronico, che partecipa alla formazione di legame con un ORBITALE VUOTO O + O d+ CH3 d+ H O- O Nu Nu Cl - H3C CH3 O + O + O CH3 S H O Nu + d+ S Cl + CH3 S Nu - Nu-H + H Nu O Cl H H3C O + O CH3 Nu H - H 3C O Nu CH3 O 10. Ciascuna delle seguenti molecole è un nucleofilo. Individuare l’atomo nucleofilo in ciascun caso e scrivete il prodotto di reazione con un generico elettrofilo E+. Nucleofilo: specie ricca di elettroni, che partecipa alla formazione di legame con un ORBITALE PIENO (coppia di elettroni n). H d- H H3C C C :- H3C E+ Al CH3 - O O E+ E+ + O Al S O S - E+ E H H3C CH3 .. + H2N NH2 E H H 3C C C E .. .. H2N NH2 CH3 E S S CH3 11 Esercitazione n. 9 Risonanza magnetica nucleare (NMR) 1. Dare una definizione dei seguenti termini: TMS tetrametilsilano, (CH3)4Si usato come standard per lo 0 della scala di d, sia per 1H che per 13C. ppm parti per milione: per rendere indipendenti dallo strumento i valori dei chemical shifts. d scala in ppm dei chemical shift, cresce da destra (TMS a 0) verso sinistra Segnale di un protone suddiviso in due dall’accoppiamento con UN H su un atomo adiacente. doppietto Segnale di un protone suddiviso in tre dall’accoppiamento con DUE H equivalenti su un atomo adiacente. tripletto area del segnale Area del picco, misurata dall’integratore e indicata da uno scalino su una linea, proporzionale al n° di H che hanno prodotto quel segnale accoppiamento spin-spin chemical shift campo alto suddivisione di un segnale per interazione nuclei magneticamente attivi su atomi adiacenti Spostamento chimico di un segnale (rispetto al TMS) dovuto al diverso campo magnetico “sentito” da nuclei con densità elettronica diversa parte destra dello spettro NMR, dove risuonano i nuclei più schermati multipletto Segnale complesso dovuto all’accoppiamento con protoni adiacenti di tipo diverso quartetto Segnale di un protone suddiviso in quattro dall’accoppiamento con TRE H equivalenti su un atomo adiacente. 2. Quando un campo magnetico molecolare indotto va nella stessa direzione del campo applicato, il nucleo di un protone influenzato da questo campo è schermato o deschermato? E’ spostato verso un campo più alto o più basso? Si trova a destra o a sinistra nello spettro NMR? Se il campo magnetico molecolare indotto va nella stessa direzione del campo applicato, il nucleo RAGGIUNGE PRIMA la combinazione campo/radiofrequenza che lo fa risuonare 12 3. Indicare quante righe ha e in che rapporto sono un multipletto proveniente dalla suddivisione provocata da: a) cinque protoni equivalenti 6, in rapporto 1:5:10:10:5:1 b) sei protoni equivalenti 7, in rapporto 1:6:15:20:15:6:1 c) quattro protoni equivalenti 5, in rapporto 1:4:6:4:1 4. Perché è difficile individuare le righe all’estremità dell’eptupletto con cui risuona un protone adiacente a sei protoni equivalenti? Perché, essendo il rapporto 1:6:15:20:15:6:1, sono molto piccoli e spariscono nel rumore di fondo 5. Se si usa uno strumento a 300 MHz, a quanti Hz a campo più basso del TMS (cioè a sinistra del TMS si trova un segnale con chemical shift 7.5 ppm? ni - nTMS di = n0 x 106 ni 7.5 = 60 x 106 x 106 ni = 450 Hz 6. I due segnali dello spettro 1H NMR dell’1,2-dimetossietano distano dal TMS 288 Hz e 297 Hz quando si usa uno spettrometro a 90 MHz. Quale è il loro chemical shift? Quanti Hz disterebbero dal TMS se lo spettro fosse stato registrato con uno strumento a 100 MHz? E con uno a 400 MHz? H3C O CH2 CH2 O CH3 A dA = B 288 Hz 90 x 106 a 100 MHz 3.20 = 297 Hz 288 Hz x 106 = 3.20 ppm dB = ni - nTMS n0 297 Hz 90 x 106 x 106 x 106 = 3.30 ppm ni ni 100 x di = 106 x 106 = 320 Hz 3.30 = 100 x 106 x 106 = 330 Hz a 400 MHz ni 3.20 = 400 x 106 x 106 = 1280 Hz ni 3.30 = 400 x 106 x 106 = 1320 Hz 13
Scaricare