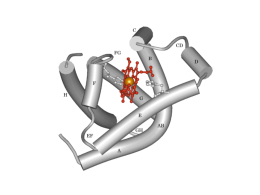
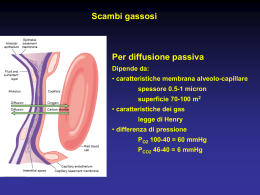
l’emoglobina degli eritrociti è una proteina di trasporto indispensabile per veicolare l’ossigeno e l’anidride carbonica tra i polmoni e i tessuti (Mioglobina, proteina di deposito, presente nelle fibrocellule del miocardio e del muscolo scheletrico, ha la funzione di trasferire l’ossigeno della emoglobina del sangue alla citocromo-ossidasi mitocondriale. Ha infatti una affinità per l’ossigeno superiore a quella dell’emoglobina). gli organismi superiori necessitano di un sistema di trasporto per l’ossigeno, in quanto tale molecola è scarsamente idrosolubile l’emoglobina importante, costante in quindi anche assolve ad una funzione estremamente contribuisce a mantenere il valore di pH condizioni fisio-patologiche, funzionando da sistema tampone L’emoglobina dell’adulto (HbA) è un tetramero costituito da 4 catene a due a due uguali (2a e 2b); ogni subunità porta un gruppo eme (gruppo prostetico contenente un nucleo di Ferro bivalente) Legame dell’ossigeno all’emoglobina Nel sangue intero l’emoglobina è per metà saturata ad una pressione di ossigeno di 26 torr. Le pO2 indicate sono considerate a livello del mare (la pO2 atmosferica a livello del mare è di 151-160 torr): Per un confronto nella figura è riportata la curva di legame dell’ossigeno alla mioglobina. La curva iperbolica tratteggiata si riferisce ad una ipotetica proteina con la stessa p50 dell’emoglobina. La saturazione (Y) è definita come la frazione di siti occupati dall’ossigeno. Y = 0 tutti i siti sono vuoti Y = 1 tutti i siti sono occupati p50 = pressione parziale dell’ossigeno a cui il 50% dei siti sono occupati. p50 per la mioglobina circa 1 torr p50 per l’emoglobina circa 26 torr La mioglobina ha una affinità per l’ossigeno maggiore di quella della emoglobina. La curva di dissociazione dell’ossigeno presenta un andamento iperbolico per la mioglobina e sigmoide per la emoglobina N.B.: Dalle curve prima riportate si desume che se l’emoglobina fosse anch’essa monomerica, cederebbe ai tessuti quantità irrilevanti di ossigeno. Significato fisiologico dell’interazione tra emoglobina e O2 E’ possibile valutare quantitativamente il significato fisiologico della natura sigmoidale della curva di legame dell’emoglobina, o, in altre parole l’importanza fisiologica del fenomeno di cooperatità. L’equazione di Hill : y/(1-y) = (p02/p50)n y = frazione dei siti occupati dall’ossigeno per Y = 1, tutti i siti sono occupati per Y = 0, nessun sito è occupato n = indice di Hill (indica il grado di sigmoidicità della curva ed il grado di cooperatività a p50. n = 1, per la mioglobina (iperbole, nessuna cooperatività) n = 2.8, per la emoglobina (sigmoide, cooperatività) La forma ad S italica è dovuta interdipendenza funzionale dei suoi 4 emi. alla Il primo eme si combina lentamente con l’ossigeno, il secondo per influenza del primo (già ossigenato) si combina più velocemente e così via (effetto cooperativo). Tale modalità è caratteristica della quaternaria e costituisce un esempio di allosterica. struttura regolazione l’ossigeno si lega agli atomi di ferro bivalenti (normalmente lo stato di ossidazione del ferro non cambia, la metaemoglobina trivalente, formatasi per ossidazione del nucleo di ferro, non è in grado di trasportare O2) l’eme ha una struttura tetrapirrolica, il ferro centrale crea 4 legami di coordinazione con gli atomi di azoto dell’anello tetrapirrolico, uno con un residuo istidinico della globina e un sesto legame di coordinazione avviene con la molecola dell’ossigeno (ossiemoglobina) struttura dell’eme l’emoglobina è stata la prima proteina di cui sono stati osservati effetti allosterici (modificazioni strutturali) questa può infatti assumere 2 conformazioni, la forma R (“relaxed” o rilassata) e la forma T (“tense” o tesa); il passaggio dall’una all’altra forma è data da interazioni elettrostatiche che dipendono dalla presenza o l’assenza di legami fra l’eme e la molecola di ossigeno Durante il legame dell’emoglobina con l’ossigeno si ha una riduzione della lunghezza nel legame ad idrogeno fra le subunità a e b, determinando così 2 conformazioni possibili, la forma R (relaxed, rilassata) o ossiHb e la forma T (tense, tesa) o deossiHb Le interazioni tra le singole subunità possono essere perturbate dal legame del tetramero con l’ossigeno, causando una modificazione conformazionale Movimenti dell’eme e dell’elica F durante la transizione T R nell’emoglobina. Nella forma T (in blu) il Fe è 0.6 Å al di fuori del piano dell’eme, che assume una forma a cupola, con il Fe al centro. Quando l’emoglobina assume la forma R (in rosso), il Fe si muove verso il piano dell’eme e la porfirina diventa planare. In questa posizione il Fe lega saldamente una molecola di ossigeno. L’His F8 e l’elica F sono costrette a seguire il movimento del Fe MODELLO DI PERUTZ aumentando la pressione parziale dell’ossigeno, un numero sempre più crescente di molecole assume forma R, più affine all’ossigeno; la cooperatività tra le subunità, e quindi anche l’affinità verso l’ossigeno, cresce all’aumentare della pressione parziale dell’ossigeno altri effettori allosterici possono influenzare l’equilibrio fra le 2 forme Legami salini tra le subunità nella deossiemoglobina. Questi legami elettrostatici non covalenti vengono spezzati durante l’ossigenazione l’emoglobina partecipa al trasporto dell’anidride carbonica dai tessuti ai polmoni; circa il 90% della CO2 non viene trasportata come tale ma viene prima convertita in ione bicarbonato HCO3-, molto più solubile nei polmoni lo ione HCO3- viene riconvertito in CO2 che viene eliminata con l’espirazione i 2 processi sono rispettivamente accoppiati alla deossigenazione e all’ossigenazione dell’emoglobina (HbH, HbO2) a questi 2 processi interviene anche l’anidrasi carbonica, presente negli eritrociti, che permette l’interconversione tra acido carbonico in CO2 e viceversa Effettori allosterici dell’emoglobina (modificazioni strutturali) • ossigeno: effettore positivo (omotropico) • H+: effettore negativo (effetto Bohr) H-Hb + O2 HbO2 + H+ •2,3-bis-fosfoglicerato: effettore negativo Hb-2,3-BPG + 4 O2 • CO2: effettore negativo CO2 + +H3N-globina Hb(O2)4 + 2,3 - BPG -OOCHN-globina + 2H+ la CO2 è un prodotto del metabolismo aerobico e deve essere trasportato ai polmoni per essere rilasciato dal nostro organismo la maggior parte della CO2 viene convertita in bicarbonato, HCO3-, mediante l’azione dell’anidrasi carbonica e quindi rilasciato nel plasma CO2 + H2O H2CO3 HCO3- + H+ la restante CO2 si lega reversibilmente all’emoglobina attraverso la formazione di un legame carbamidico con gli a-amino gruppi della porzione N-terminale dei polipeptidi della globina CO2 + +H3N-globina -OOCHN-globina + 2H+ L’effetto Bohr non è altro che il rilascio di ossigeno da parte dell’emoglobina che si osserva quando la concentrazione di ioni H+ aumenta (il pH diminuisce). L’effetto Bohr è fisiologicamente importante, in quanto i tessuti che stanno ossidando grandi quantità di sostanze nutrienti, e che di conseguenza hanno bisogno di grandi quantità di ossigeno, generano ioni H+, rilasciando CO2 nel sangue: CO2 + H2O H2CO3 HCO3- + H+ Facilitando il rilascio di ossigeno, questi ioni H+ consentono il deposito di O2 extra in quei tessuti che stanno consumando molto attivamente Emoglobina e trasporto di CO2 L'emoglobina partecipa anche al trasporto del biossido di carbonio (CO2) dai tessuti ai polmoni. Circa il 90% della CO2 non viene trasportata come tale, ma viene trasformata in idrogenocarbonato (HCO3-) molto più solubile in acqua. Nei polmoni l'idrogenocarbonato viene ritrasformato in CO2 che viene eliminato con l'espirazione. I due processi - la formazione di HCO3- nei tessuti e la liberazione di CO2 nei polmoni - sono rispettivamente accoppiati alla deossigenazione e all'ossigenazione dell'emoglobina. La deossiemoglobina è una base marcatamente più forte dell'ossiemoglobina e lega quindi protoni (circa 0,7 H+ per tetramero) favorendo così nei capillari dei tessuti la formazione di HCO3- da CO2. segue Partecipa al processo anche l'anidrasi carbonica, presente in alte concentrazioni negli eritrociti. L'HCO3- formato viene rilasciato per la maggior parte nel plasma in cambio di Cl- e con il plasma va ai polmoni dove le reazioni descritte avvengono in direzione opposta: la deossiemoglobina viene ossigenata e cede protoni che spostano l'equilibrio HCO3-/H2CO3 e favoriscono così il rilascio di CO2. Una piccola parte di CO2 (circa il 5%) viene trasportata, legata covalentemente con l'emoglobina, come carbammino-Hb (non riportato). Si calcola che i meccanismi descritti siano responsabili per il 60% del trasporto di CO2. gli ioni H+ producono uno spostamento verso destra della curva di saturazione dell’ossigeno (effetto Bohr) Nei capillari dei tessuti extrapolmonari, gli eritrociti trasformano in HCO3- la CO2 prodotta dal metabolismo dei tessuti; l’HCO3- così prodotto esce dagli eritrociti per scambio con il Cl-. Nei capillari polmonari, l’ HCO3- penetra negli eritrociti per scambio con il Cl-. Dentro gli eritrociti, l’ HCO3- viene trasformato in CO2, che quindi diffonde fuori dagli eritrociti e viene espirata Effetto tampone dell’emoglobina Il 2,3-BPG deriva dall’ 1,3-BPG, un intermedio della glicolisi eritrocitaria ogni molecola di 2,3-BPG lega ciascuna molecola di emoglobina; la sua concentrazione nell’eritrocita è quasi identica a quella dell’emoglobina un incremento del 2,3-BPG stabilizza la forma T (deossiHb) e quindi favorisce il rilascio di O2 un incremento di 2,3-BPG interviene in risposta a ipossia tissutale (dovuta a: anemia, disfunzione polmonare, fumo di sigarette, elevate altitudini) in assenza di effettori allosterici, nel caso di emoglobina purificata, la curva di saturazione di questa proteina tende ad assumere un andamento simile a quello della mioglobina. In definitiva, quindi, gli effettori negativi risultano di fondamentale importanza per il rilascio dell’ossigeno. La mioglobina, presente nelle fibre muscolari, ha un’affinità verso l’ossigeno maggiore rispetto all’emoglobina, l’andamento della curva non è sigmoidale in quanto l’affinità non è influenzata da effettori allosterici come BPG e H+ Il paradosso fetale Il feto deve ottenere ossigeno dal sangue materno attraverso la placenta. Lo scambio può avvenire grazie al fatto che il sangue fetale presenta un’affinità maggiore rispetto al sangue della madre Come è possibile? Il sangue fetale contiene un tipo di emoglobina differente rispetto a quella dell’adulto (HbA), l’HbF infatti è costituita da un tetramero di tipo a2g2 . La subunità g differisce rispetto alla b-globina in quanto presenta un residuo neutro di serina al posto del residuo carico His143. Questa differenza fa si che l’HbF è estremamente meno affine al 2,3-BPG (effettore allosterico negativo) rispetto all’HbA, di conseguenza l’HbF lega l’ossigeno con maggiore affinità Le sindromi talassemiche Sono la conseguenza di anormalità o non-funzionamento dei geni per la codifica delle globine, l’insufficiente sintesi dei diversi tipi di globina porta ad un’anemia emolitica. La severità del danno è funzione dei numeri di geni mutati. Si distinguono 2 tipi di talassemia: b-talassemia – bassi livelli (b+) o completa assenza (b0) di bglobina. Si può verificare un’overproduzione compensatoria di HbF (a2g2) a-talassemia – bassi livelli di a-globina. Questa forma risulta essere più complicata poiché vengono coinvolti 2 tipi di geni che codificano per l’a-globina. Le vie compensatorie determinano la produzione di 2 tipi di emoglobina, l’HbH (b4) e l’Hb di Bart (g4) che non esibiscono transizioni allosteriche, effetto Bohr, inoltre queste rimangono sempre nello stato R Anemia falciforme L’anemia falciforme è una patologia ereditabile; manifestazioni comuni: anemia emolitica e dolore ricorrente basi biochimiche: mutazione puntiforme del gene per la bglobina, il residuo di Glu6 risulta essere sostituito da una Val (valina) Lo scambio di questo aminoacido riduce la solubilità, promuove la polimerizzazione di molecole di emoglobina di tipo S deossigenata (HbS) Spettro dei genotipi: anemia falciforme (HbSS) – quadro clinico severo anemia falciforme di tipo lieve (HbAS) – minori problemi clinici anemia falciforme – b+talassemia – coesistenza delle 2 varianti di emoglobina con quadro clinico davvero complicato La severità della patologia dipende dalla quantità di HbA e di HbF presenti
Scaricare