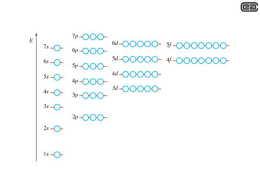
A.A 2010-2011 G. Cambi - M. Piccinini - N. Semprini - S. Zucchelli Eq. di Schrödinger - indipendente dal tempo - in coordinate polari sferiche 2 (r ) U (r ) (r ) E (r ) 2 2 2m x r sin cos y r sin sin z r cos 2m 2 (r , , ) U (r ) (r , , ) E (r , , ) 2 2 2 1 2 1 1 1 2 2 2 2 2 r 2 sin 2 x y z r r r r sin sin 2 2 le variabili angolari compaiono solo in un termine percio’ ricerco le soluzioni nella forma: (r , , ) R(r )Y ( , ) 1 2 1 2 1 1 2 r R(r )Y ( , ) 2 R ( r ) Y ( , ) U (r ) R(r )Y ( , ) E R(r )Y ( , ) sin R(r )Y ( , ) 2 2 2m r r r r sin sin 2 Y ( , ) 2 R( r ) 2 R( r ) ossia r R ( r ) sin Y ( , ) Y ( , ) (U (r ) E )R(r )Y (, ) 0 2 2 2 2 2m r 2 r r r sin r sin 2 dividendo per R(r )Y ( , ) e moltiplicando per 2mr 2 2 si ottiene : 1 2 2mr 2 1 1 2 R(r ) Y ( , ) 2 (U (r ) E ) 0 r sin Y ( , ) 2 2 R ( r ) r r Y ( , )sin Y ( , )sin A.A 2010-2011 G. Cambi - M. Piccinini - N. Semprini - S. Zucchelli 2 1 2 1 1 Y ( , ) 1 2Y ( , ) 2mr r R ( r ) ( U ( r ) E ) (sin ) 0 2 2 2 R ( r ) r r Y ( , ) sin sin riarrangiando i termini: dato che il primo termine, che dipende solo da r, e’ indipendente dal secondo, che dipende solamente da e , affinche’ l’equazione sia sempre verificata bisogna che i due termini siano entrambi costanti, posto che la costante valga l(l+1) , dove l e’ un intero, si dovra’ avere 2 1 2 2mr r R ( r ) (U (r ) E ) l (l 1) 2 R(r ) r r e 1 Y ( , ) 1 2Y ( , ) (sin ) 2 l (l 1) Y ( , ) sin sin 2 1 parte radiale parte angolare Y ( , ) 2Y ( , ) (sin ) l (l 1)Y ( , ) sin 2 per quanto riguarda la parte angolare si ha: sin 2 tenteremo di nuovo di operare sulla parte angolare separando le variabili, del tipo Y ( , ) G ( ) F ( ) dividendo per sostituendo si ottiene G( ) F ( ) si ha ossia ipotizzando una soluzione G( ) F ( ) 2G( ) F ( ) sin (sin ) l (l 1)G( ) F ( ) sin 2 0 2 1 G( ) 1 2 F ( ) 2 sin (sin ) l (l 1)sin 0 G( ) F ( ) 2 poiche il primo termine, che dipende solo da , e’ indipendente dal secondo, che dipende solamente da , sara’ possibile utilizzare le derivate normali: quindi 1 d dG( ) 1 d 2 F ( ) 2 ) l (l 1)sin 0 sin (sin G( ) d d F ( ) d 2 affinche’ l’equazione sia sempre verificata bisogna che i due termini siano entrambi costanti, dove m e’ un intero, si dovra’ avere 1 d dG ( ) (sin ) l (l 1)sin 2 m 2 sin G ( ) d d e posto che la costante assuma il valore m2 , e d 2 F ( ) m2 2 F ( ) d 1 A.A 2010-2011 G. Cambi - M. Piccinini - N. Semprini - S. Zucchelli d F ( ) m2 F ( ) 2 d 2 le soluzioni dell’equazione sono F ( ) Aeim e F ( ) Aeim ma di solito si ingloba la costante come fattore moltiplicativo nella funzione G () e sempre per convenzione si assume come soluzione F ( ) eim consentendo poi ad m di assumere anche valori negativi dato che l’angolo azimutale ha periodicita’ di 2p e dato che dopo un avanzamento di 2p si torna allo stesso punto dello spazio imporremo la condizione che ossia e im ( 2p ) e im vale a dire m 0, 1, 2, .... nello specifico e im 2p 1 F ( 2p ) F ( ) cio’ comporta che il numero quantico m debba in effetti essere un intero e, limitandosi a questo contesto, m non avrebbe limite superiore nota bene: questa non e’ una supposizione scontata a priori infatti esistono grandezze fisiche che non ritornano nella stessa identica condizione dopo una rotazione di 360 gradi. Es. spinori o come esempio classico il cameriere ed il piatto che ruota id quindi per essere corretti occorrerebbe moltiplicare per una fase tipo e id ossia affermare che F ( 2p ) e F ( ) le soluzioni a 1 d dG ( ) (sin ) l (l 1)sin 2 m 2 ossia della sin G ( ) d d sin d dG ( ) (sin ) (l (l 1)sin 2 m2 )G ( ) 0 d d m sono G ( ) APl (cos ) m dove i Plm sono le funzioni associate di Legendre definite come Pl ( x) (1 x ) m 2 2 m d Pl ( x) dx m 1 d l ( x 2 1)l mentre i Pl(x) sono i polinomi di Legendre che e’ consuetudine definire, usando la formula di Rodrigues, come Pl ( x) l 2 l! dxl da notare come : • affinche’ la formulazione dei polinomi di Legendre nella forma di Rodrigues abbia senso il numero quantico l deve essere un numero intero positivo o nullo quindi l 0, 1, 2, ... • dalla definizione delle funzioni associate di Legendre risulta che deve essere m intero ed |m| ≤ l quindi per ogni valore assegnato di l sono possibili ( 2l+1) valori per m con m l , (l +1),.. 1, 0, 1, ... (+l 1), l A.A 2010-2011 G. Cambi - M. Piccinini - N. Semprini - S. Zucchelli Parte radiale 2 1 2 2mr r R ( r ) ( U ( r ) E ) l (l 1) 2 R(r ) r r d 2 dR(r ) 2mr 2 r 2 (U (r ) E ) l (l 1) R(r ) dr dr 1 dove si e’passati dalle derivate parziali a quelle normali visto che R dipende solo dalla variabile radiale r o anche, riarrangiando i termini : d 2 dR(r ) 2mr 2 r 2 (U (r ) E ) R(r ) l (l 1) R(r ) dr dr u (r ) rR(r ) equazione che puo’ essere semplificata se poniamo: da questa condizione ne deriva che R (r ) dR(r ) dr u (r ) r du (r ) dr 1 (r du (r ) u (r )) 2 r2 dr r e applicando regola di derivazione del prodotto di funzioni otteniamo u (r ) r inoltre d 2 dR(r ) d 1 du (r ) d du d du (r ) du (r ) du (r ) d 2u (r ) du (r ) d 2u (r ) (r ) (r 2 ( 2 (r u (r ))) (r u (r )) (r ) r r dr dr dr r dr dr dr dr dr dr dr 2 dr dr 2 dr dunque la ossia d 2 dR(r ) 2mr 2 r 2 (U (r ) E ) R(r ) l (l 1) R(r ) dr dr d 2u (r ) 2mr 2 u (r ) u(r ) ( U ( r ) E ) l ( l 1) 2 2 2 2 diviene d 2u (r ) 2mr 2 u (r ) u (r ) r ( U ( r ) E ) l ( l 1) 2 dr 2 r r infine, semplificando il termine r2 d 2 u ( r ) 2m u (r ) ( U ( r ) E ) u ( r ) l ( l 1) 2 2 2 A.A 2010-2011 G. Cambi - M. Piccinini - N. Semprini - S. Zucchelli 2 d 2u ( r ) l (l 1) U ( r ) e, riarrangiando i termini si ottiene la u (r ) E u (r ) 2 2m dr 2 2 m r 2 equazione che diviene equivalente alla equazione di Shroedinger indipendente dal tempo in una dimensione ossia alla dove d 2 V E 2m dr 2 2 l (l 1) 2m r 2 2 l (l 1) e’ detto centrifugo in quanto tende ad allontanare dall’origine del centro di forza 2 2m r Veff U (r ) il termine a patto di sostituire al potenziale V un potenziale efficace Veff 2 Atomo idrogenoide : potenziale coulombiano le soluzioni all’equazione 1 d 2 dR(r ) l (l 1) (r ) 2m r 2 dr dr r2 2 2 e2 R(r ) R(r ) ER(r ) 4 p r o sono i polinomi di Laguerre: come conseguenza affinche’ si abbia convergenza dei polinomi di Laguerre il numero quantico l puo’ assumere al massimo il valore n-1 A.A 2010-2011 G. Cambi - M. Piccinini - N. Semprini - S. Zucchelli quindi per un generico valore del numero quantico n l 0, 1, 2, ... (n 1) il numero quantico l puo’ assumere gli n valori ma per ciascun valore di l vi sono 2l 1 valori possibili per il numero quantico m n 1 e la degenerazione di un livello energetico En associato al numero quantico n sara’ pari a quindi E1 degenerazione = 1 n 1, l 0, m 0 E2 degenerazione = 4 (2l 1) n l 0 E3 degenerazione = 9 n 2, l 0, m 0 n 3, l 0, m 0 n 2, l 1, m 1 n 3, l 1, m 1 n 2, l 1, m 0 n 3, l 1, m 0 n 2, l 1, m 1 n 3, l 1, m 1 n 3, l 2, m 2 n 3, l 2, m 1 n 3, l 2, m 0 tenuto conto dello spin degli elettroni e del principio di esclusione di Pauli cio’ spiega la capienza in elettroni dei vari livelli energetici dell’atomo idrogenoide E1 degenerazione = 1 numero di elettroni possibili = 2 E2 degenerazione = 4 numero di elettroni possibili = 8 E3 degenerazione = 9 numero di elettroni possibili = 18 n 3, l 2, m 1 n 3, l 2, m 2 2 A.A 2010-2011 G. Cambi - M. Piccinini - N. Semprini - S. Zucchelli in conclusione le funzioni d’onda dell’atomo di idrogeno, propriamente normalizzate, sono r 2 (n l 1)! na 2r 2l 1 2r m n ,l , m ( r , , ) e Ln l 1 Yl ( , ) 3 na 2 n (( n l )!) na na 3 dove gliL p q p dp ( x) (1) Lq ( x) p dx p l sono i polinomi associati di Laguerre d q x q (e x ) sono i polinomi di Laguerre e Lq ( x) e q dx x le Yl m ( , ) 4p 0 2 ed a me2 sono le armoniche sferiche e’ il raggio di Bohr a 0.529 10 10 m A.A 2010-2011 G. Cambi - M. Piccinini - N. Semprini - S. Zucchelli partendo soltanto dalla degenerazioni dei livelli energetici e dal principio di esclusione di Pauli si puo’ tentare di costruire la tavola periodica degli elementi idrogeno 1 elettrone n=1 l=0 m=0 s = -1/2 elio 2 elettroni n=1 n=1 l=0 l=0 m=0 m=0 s = -1/2 s = +1/2 3 elettroni n=1 n=1 n=2 l=0 l=0 l=0 m=0 m=0 m=0 s = -1/2 s = +1/2 s = +1/2 litio ma se n = 2 sia l = 0 che l =1 sono stati possibili ed hanno la stessa energia quindi perche’ non occupare prima lo stato con l = 1 ? la risposta e’ che non si puo’ ignorare la repulsione coulombiana tra gli elettroni la presenza del termine centrifugo fa si’ che il valore del raggio medio ad n fissato aumenti in funzione del numero quantico l o, detto in altri termini, fa si’ che gli elettroni tendano in media ad allontanarsi maggiormente dal centro di forza all’aumentare del numero quantico l a parita’ di numero quantico n piu’ lontano dal nucleo e’ l’elettrone piu’ assume rilevanza l’effetto di schermatura o “screening” degli elettroni piu’ interni che fa si’ che piu’ e’ lontano l’elettrone minore carica efficace percepisce dunque tenendo conto della repulsione degli elettroni lo stato con l = 0 e’ quello piu’ strettamente legato al nucleo, ossia e’ quello che ha l’energia minore e l’energia, a parita’ di n, aumenta all’aumentare di l A.A 2010-2011 G. Cambi - M. Piccinini - N. Semprini - S. Zucchelli Determinare nell’atomo di idrogeno quale sia il valore piu’ probabile di r negli stati caratterizzati dai numeri quantici n e dal massimo numero quantico orbitale possibile nell’ atomo di idrogeno P(r) e’ la densita’ di probabilita’ radiale ossia P(r)dr e’ la probabilita’ di trovare l’elettrone ad una distanza compresa tra r e r + dr dal nucleo. il numero quantico l puo’ assumere al massimo valore n-1, quindi lmax= n - 1 Rn ,l n 1 r e l r na r n 1 e r na o a 2 0.529 A 2 c me c dove e’ il raggio di Bohr e e’ la “massa ridotta” del sistema protone elettrone u R r e u rR me m p me m p me m me (1 e ) me me mp 1 mp n 1 u r r e r na r e n r na Prob(r [r,r dr]) un2,l n 1 r 2 n e quindi 2r na un ,l n 1 r n e r na A.A 2010-2011 G. Cambi - M. Piccinini - N. Semprini - S. Zucchelli P dP d 2 n na 2 2 n na 2 n 1 na (r e ) 2nr e r e 0 r dr dr na 2r raccogliendo a fattor comune 2r 2r 2 n 1 ed 2r e 2r na si ha 2r 2 n 1 e 2r na 1 r0 escludendo le soluzioni a zero e all’ infinito resta da risolvere la n na equazione che ha per soluzione : 1 (n r ) 0 na r n2a la probabilita’ e’ massima in corrispondenza di quegli rn tali per cui : ossia in corrispondenza delle orbite dell’atomo di Borh rn n 2 a
Scaricare