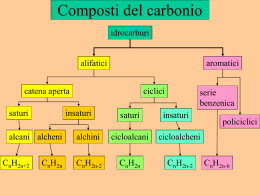
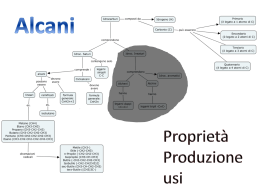
IDROCARBURI SATURI SILSIS VIII ciclo Paola Morandi, y04546 IDROCARBURO SATURO H C massimo numero di H possibile Sono composti organici formati solo da carbonio e idrogeno Contengono solo legami semplici C-H Hanno formula generale CnH2n+2 Il carbonio presenta ibridazione sp3 in cui n è un qualsiasi numero intero IDROCARBURI SATURI: ALCANI E CICLOALCANI Classificazione degli IDROCARBURI ALIFATICI A CATENA APERTA SATURI ALCANI INSATURI AROMATICI A CATENA CHIUSA SATURI INSATURI CICLOALCANI ALCANO: termine di derivazione araba. Noti anche come PARAFFINE (dal latino parum affinis, poco affini) a causa della loro scarsa reattività. IBRIDAZIONE DEL CARBONIO Configurazione elettronica nello stato fondamentale Promozione di un elettrone nell’orbitale 2p vuoto 4 orbitali sp3, con geometria tetraedrica METANO MODI DI RAPPRESENTAZIONE Struttura di Lewis METANO Modello tridimensionale a scheletro: la linea in neretto emerge dal piano del foglio, quella tratteggiata penetra al di sotto del piano del foglio, quella continua giace sul piano del foglio Modello a sfere e bastoncini CH4 C4H10 Butano Formula condensata NOMENCLATURA IUPAC La nomenclatura IUPAC stabilisce le seguenti regole per la denominazione di un alcano: Individuare la catena più lunga di atomi di carbonio; tale catena costituirà la base del nome in funzione del numero di atomi di carbonio che possiede (3: propano, 4: butano, 5: pentano, 6: esano, 7: eptano, 8: ottano, etc...) 5 atomi: PENTANO Numerare gli atomi della catena sequenzialmente partendo da una delle estremità, in modo che gli atomi che recano ramificazioni abbiano i numeri più bassi possibile da sinistra a destra: 2,2,4 --> ok da destra a sinistra: 2,4,4 --> no Nominare le ramificazioni in modo analogo alla catena principale, sostituendo il suffisso -ano con il suffisso -il (pertanto 1: metil, 2:etil, 3: propil, etc...) Raggruppare le ramificazioni in ordine alfabetico e, qualora ne compaia più di una di un tipo nella formula, indicarne la molteplicità tramite l'opportuno prefisso (di- tritetra-, etc...) 3 gruppi CH3: tri-metil- Il nome è costituito dall'elenco delle ramificazioni precedute dal numero di ogni atomo della catena principale che le ospita, seguito dal nome della catena principale 2,2,4-trimetilpentano GRUPPI ALCHILICI gruppo alchilico è il gruppo funzionale corrispondente ad un alcano privo di un atomo di idrogeno. il nome del gruppo alchilico è simile a quello dell'alcano da cui deriva, salvo la sostituzione del suffisso -ano con il suffisso –ile. Vengono utilizzati per dare il nome ad alcani ramificati. CICLOALCANI CnH2n Sono idrocarburi alifatici con forma ciclica Il nome deriva dall’alcano corrispondente, preceduto dal prefisso ciclo- La costituzione del ciclo fa diminuire di due unità gli atomi di H PROPANO: C3H8 CICLOPROPANO: C3H6 ISOMERIA: isomeri costituzionali Si verifica quando un idrocarburo ha C = 4 o C 4 Due isomeri costituzionali (o strutturali) hanno la stessa formula molecolare ma struttura diversa (diversa connettività di legame) Hanno proprietà fisiche diverse Sono molecole DIVERSE ! Tipi di atomi di carbonio Isomeri conformazionali O conformeri Un alcano può esistere in diverse conformazioni Le diverse conformazioni derivano dalla rotazione intorno ai legami sigma C-C, che portano in posizione diversa i sostituenti Due possibili conformazioni dell’ETANO SONO LA STESSA MOLECOLA ! Due conformazioni “limite” dell’etano: CONFORMAZIONE SFALSATA: Epot minima (minore ingombro sterico) Gli isomeri conformazionali si differenziano solo per il loro contenuto energetico La conformazione sfalsata è più stabile CONFORMAZIONE ECLISSATA: Epot massima E per i cicloalcani ? ciclobutano ciclopentano H2C H2C H2 C C H2 CH2 CH2 cicloesano Se fosse planare sarebbe tensionato (120° contro 109.5°) In realtà assume una forma ripiegata È il ciclo più comune in natura Conformazioni del cicloesano Conformazione a SEDIA: sfalsata favorita dal punto di vista energetico Conformazione a BARCA: eclissata sfavorita dal punto di vista energetico SONO LA STESSA MOLECOLA ! FORZE INTERMOLECOLARI LEGAME C-C non polare LEGAME C-H solo debolmente polare I legami sono, inoltre, disposti in modo simmetrico Prima conseguenza Gli alcani sono molecole APOLARI Gli alcani, e gli idrocarburi in generale, possono fare solo forze di dispersione tra dipoli temporanei Seconda conseguenza Gli alcani sono molecole INERTI Non hanno reattività da elettrofili/nucleofili PROPRIETÁ CHIMICO-FISICHE Punti di ebollizione/fusione e densità relativamente bassi DIPENDONO DALLA DIMENSIONE E DALLA FORMA DELLE MOLECOLE Nel caso di isomeri costituzionali: le molecole lineari hanno e.p. maggiore rispetto a quelle ramificate (per maggiore superficie di contatto) I cicloalcani hanno e.p. più alto rispetto a quello dei corrispondenti alcani (a causa della loro simmetria e della rotazione più impedita) NON SONO SOLUBILI IN SOLVENTI POLARI (es. H2O) REATTIVITÀ Sono praticamente INERTI Ottimi solventi nelle reazioni di sintesi organica Due reazioni principali: 1) COMBUSTIONE 2) ALOGENAZIONE RADICALICA Essendo inerti, sono necessari luce e/o calore per innescare le reazioni Sono entrambe reazioni radicaliche a catena: vengono innescate dalla formazione di un radicale per azione del calore o della luce NB ricordiamo che un RADICALE è un atomo (o un gruppo di atomi) con un e- spaiato REAZIONE DI COMBUSTIONE (ossidazione) CnH2n+2 + eccesso O2 fiamma nCO2 + (n+1) H2O + calore Reazione fortemente esotermica FONTI NATURALI: IL PETROLIO PETROLIO (dal greco πέτρα–roccia e έλαιο–olio): liquido infiammabile, che si trova in alcuni punti degli strati superiori della crosta terrestre. È una MISTURA DI VARI IDROCARBURI, IN PREVALENZA ALCANI, ma con variazioni nella composizione e nelle proprietà. È prodotto dalla decomposizione anaerobica di materiale organico. GPL I componenti idrocarburici del petrolio vengono in gran parte separati per distillazione frazionata. Oltre al petrolio, altra fonte naturale di alcani è il GAS NATURALE (di cui principale componente è il metano) Carburante motori diesel BIOLOGIA: ACIDI GRASSI E DERIVATI ACIDO GRASSO TRIGLICERIDE CATENE IDROCARBURICHE (parte idrofobica della molecola) FOSFOLIPIDE Trigliceridi: metabolismo energetico Elevato contenuto energetico (composti ridotti e anidri) Trigliceridi 9 kcal/g Carboidrati/proteine 4 kcal/g Via metabolica: -ossidazione degli acidi grassi Fosfolipidi: componenti delle membrane biologiche In soluzione acquosa Micella Doppio strato BIOLOGIA: SISTEMI POLICICLICI Ciclopentanoperidrofenantrene = sistema tetraciclico di atomi di carbonio STEROIDI: gruppo di composti molto diffusi in natura (comprende il colesterolo e gli ormoni sessuali). formula di struttura degli steroidi: gli atomi di carbonio numerati dal 18 in su possono essere assenti Fra i farmaci cardiocinetici spiccano alcune sostanze estratte dai fiori della digitale. I derivati attivi sono principalmente due: la digossina e la digitossina. digossina LABORATORIO Riconoscimento di alcani, (acidi e ammine): saggio di solubilità ? Combustione del metano e altro http://www.itchiavari.org/chimica/lab/index.html
Scaricare