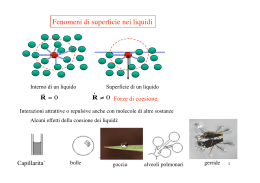
TORINO 21-05-2006 Ortocheratologia Update. Corso di aggiornamento sulla correzione ortocheratologica con lenti a contatto e gestione della comunicazione con l’ametrope. Proprietà dei fluidi e dinamica a piccola scala Prof. Marina SERIO Dipartimento di Fisica Generale Amedeo Avogadro Argomenti • Modello principale dell’interazione lentecornea • Proprietà dei fluidi – Viscosità – Lubrificazione – Tensione superficiale MODELLO FISICO - Forze agenti - Proprietà dei materiali biologici su cui agiscono le forze Cos’è una forza dal punto di vista fisico? La forza è una interazione che varia la velocità di un corpo. Una forza e’ definita da tre quantità: la grandezza o intensità la direzione lungo cui agisce il verso nel quale agisce VARIABILE VETTORIALE Per i fluidi: Dato che i fluidi non hanno forma propria (nel caso dei gas, non hanno nemmeno un volume proprio), occorre tenere conto della superficie su cui agisce la forza COMPRESSIONE TENSIONE FORZA TANGENZIALE STRESS (sforzo) pressione F A stress tangenziale Lo stress produce una deformazione del corpo su cui agisce la forza Se, dopo aver tolto la forza applicata, il corpo ritorna nelle condizioni iniziali, si dice che si sta operando in regime di elasticità. Il massimo valore di stress applicabile in regime di elasticità è chiamato Modulo di Young FORZE AGENTI • Gravità (trascurabile) • Forza esercitata dalla palpebra/lente (positiva - compressione) • Forze viscoelastiche nello strato lacrimale (squeeze film pressure) • Tensione superficiale ai margini della lente e della palpebra (negativa - tensione) Materiali biologici • Liquido lacrimale – Fluido essenzialmente assimilabile all’acqua (viscosità, tensione superficiale) • Epitelio corneale – Strati cellulari che possono essere compressi e soggetti a movimento (fluido newtoniano) • Cornea – Sostanza viscoelastica BILANCIO DELLE FORZE La palpebra esercita una forza compressiva sulla lente, che si avvicina all’occhio. A sua volta la forza compressiva viene trasmessa dalla lente allo strato lacrimale sottostante Il film lacrimale, distribuito in modo non uniforme sulla superficie corneale, “sfoga” l’azione compressiva ai bordi della lente Forza negativa (tensione - pull) dove e’ spesso Forza positiva (compressione - push) dove e’ sottile La forza compressiva non uniforme esercitata sull’epitelio provoca uno stress tangenziale alla superficie corneale una “redistribuzione” della materia epiteliare (il cui volume deve conservarsi) fino al raggiungimento dell’equilibrio. Il risultato è l’assottigliamento epiteliare in centro e l’inspessimento nelle zone periferiche, con una variazione di forma. Situazione di quasi equilibrio movimento della lente sull’occhio Lenti più curve (raggio minore) esercitano nella zona centrale una forza negativa (tensione) che tende a rendere più curva la cornea Necessaria precisa valutazione dell’eccentricità VISCOSITA’ DI UN FLUIDO • Coefficiente di viscosità • Dipendenza dalla temperatura 1 dy F dy f dv A dv e 1 T Coefficiente di Viscosità Sostanza Viscosità (*10-3) Pa.s Sangue intero 3.015 Plasma 1.81 Siero 1.88 Bile 1.27 Urina 1.07 Acqua 1.00 Fluidi Newtoniani e non-Newtoniani flusso Newtoniano: la velocità di flusso aumenta linearmente con l'aumentare della forza applicata. Esempi: acqua, glicerina, cloroformio, sciroppi semplici, soluzioni saline, alcool etilico, benzene,gasolio flusso plastico: per lo scorrimento è necessario che la forza applicata superi un valore minimo. Poi, dopo un certo valore della forza, F, il comportamento del sistema diventa lineare. Esempi: sospensioni con particelle flocculate, pomate, pasta dentifricia, gelatine, ketchup Fluidi Newtoniani e non-Newtoniani flusso pseudoplastico: lo scorrimento inizia anche per azione di forze modeste, e la velocità di flusso aumenta con l'aumentare della forza applicata flusso dilatante: lo scorrimento inizia anche per azione di forze modeste, e la velocità di flusso diminuisce con l'aumentare della forza applicata. Esempi: sabbia e sabbie mobili, composti zuccherini, burro d’arachidi, dispersioni liquide di gomme arabiche o sintetiche. Esempi: sangue, vernici, brillantina melassa, sapone, emulsioni, inchiostro, amidi, pasta di legno per la carta Fluidi Tissotropici e Reopressici Sostanza tissotropica: il grafico riporta il comportamento di un fluido la cui curva di ritorno evidenzia un aumento di fluidità, e la struttura iniziale ha maggiore valore limite di scorrimento. Sostanza reopressica: il grafico riporta il comportamento di un fluido la cui curva di ritorno evidenzia una diminuzione di fluidità, ma la struttura iniziale ha un minore valore limite di scorrimento. LUBRIFICAZIONE La lubrificazione ha lo scopo di ridurre l’attrito tra due superfici e il consumo del materiale di cui sono composte. Ha anche il compito di trasportare via il calore sviluppato per attrito e proteggere le superfici qualora sia presente adsorbimento Il film fluido tra le superfici deve avere uno spessore maggiore delle dimensioni delle asperità delle superfici. Deve essere abbastanza viscoso per mantenere separate le superfici su tempi lunghi, ma non troppo per non smorzare il moto delle superfici NUMERO DI SOMMERFELD Il numero di Sommerfeld è un numero adimensionale che caratterizza l’aumento o la diminuzione del fattore di attrito S v NL = viscosità v = velocità superfici N = forza normale (di moto) L = dimensione tipica S << 1 aumenta il fattore di attrito D l 2r h0 Forza propulsiva = Forza viscosa l p 8v 2 r Pmax D D 2 V 2 C h0 h0 1 2 h0 h h0 D4 Squeeze film force F PA C V 1 2 h 3 0 Forze di coesione molecolare Forze di coesione molecolare Tensione superficiale F l alcool etilico (20°C) glicerina (20°C) acqua (20°C) acqua (100°C) film lacrimale (37°C) L L 2ls 2A =0.0223 Nm-1 =0.0631 Nm-1 =0.0728 Nm-1 =0.0589 Nm-1 =0.0460 Nm-1 Lamine in un telaio cubico. Lamine fra due Le lamine non si anelli unite da una dispongono sulle facce del lamina in comune cubo, ma si uniscono fra loro. Lamina tuboidale fra due anelli, ottenuta rompendo la lamina in comune. Lenti a contatto perforate Tensione superficiale e regno animale Pond skaters BAGNABILITA’ Relazione di Young cos sa sl la sa solido aria sl solido liquido la liquido aria PARZIALE MASSIMA SCARSA NULLA Sostanze tensioattive Se si aggiunge un soluto ad un liquido si puo’ variare la tensione superficiale di quest’ultimo in funzione della concentrazione c del soluto. Le molecole del soluto formano uno strato sottilissimo che, per essere efficace deve ricoprire integralmente la superficie del liquido. Le sostanze che influenzano la tensione superficiale vengono chiamate tensioattive. Equazione di Gibbs c 1 RT lnc Tensioattive (si dispongono sulla superficie) Tensioinattive (si dispongono all’interno) Indifferenti iniz c > 0 c < 0 c = 0 fin iniz > fin iniz < fin iniz = fin Addizionando sodio laurilsolfato (SLS, pm = 288) diminuisce la tensione superficiale dell’acqua, che non regge piu’ il peso dell’insetto. Le concentrazioni molari sono per i tre fotogrammi rispettivamente 0, 0.003M e 0.004M CAPILLARITA’ L'elevata intensità delle forze di adesione del liquido con le pareti del capillare, costringe il livello sopra il pelo libero dell'acqua L'elevata intensità delle forze di coesione del liquido, costringe il livello sotto il pelo libero dell'acqua Altezza del liquido in un capillare Eguagliando la forza verticale F dovuta alla tensione superficiale del liquido, al peso della colonna di liquido, si ricava l’altezza raggiunta dal liquido nel capillare 2 cos h gr Se = 90º, cos = 0 Se < 90º, cos > 0 Se > 90º, cos < 0 h=0 h>0 h<0 L’altezza e’ proporzionale alla tensione superficiale e inversamente proporzionale al raggio r del capillare I fenomeni capillari producono risultati contrari al principio dei vasi comunicanti. Esempio: salita della linfa vegetale negli xilemi degli alberi (fino a 30 cm) OSMOSI L’osmosi (dal greco osmòs = spinta) è il fenomeno che si verifica fra due soluzioni a diversa concentrazione, separate da una membrana semipermeabile. La diversa concentrazione spinge le sostanze a diffondersi nella zona a minore concentrazione, ma la membrana impedisce il passaggio di molecole di soluto. In natura sono molto diffuse le membrane semipermeabili: con esse si instaura il passaggio del solo solvente dalla soluzione meno concentrata (ipotonica) alla soluzione più concentrata (ipertonica), che tende a portare alla stessa concentrazione le due soluzioni. Equazione di Van’t Hoff QuickTime™ e un de com press ore TIFF (No n compre sso) so no n ece ssari per vi sual izza re qu est'imm agin e. cRT QuickTime™ e un de com press ore TIFF (No n compre sso) so no n ece ssari per vi sual izza re qu est'imm agin e. QuickTime™ e un de com press ore TIFF (No n compre sso) so no n ece ssari per vi sual izza re qu est'imm agin e. Le figure mostrano cosa può accadere quando le cellule animali o vegetali vengono introdotte in una soluzione acquosa. Cellule vegetali Cellule animali Se la soluzione è isotonica rispetto alla cellula, la concentrazione del soluto sarà la stessa ad entrambi i lati della membrana quindi l' acqua si muoverà in entrambe le direzioni in modo uniforme Una soluzione ipertonica ha una maggiore quantità di soluto, e il movimento netto dell 'acqua verso l' esterno della cellula causa il suo raggrinzimento. Una soluzione ipotonica ha una minore concentrazione di soluto, e il movimento netto dell 'acqua avverrà verso l' interno della cellula causando un rigonfiamento o la lisi. Alcuni esempi di osmosi: 1) Terapia Orale di Re-idratazione (ORT) per casi di diarrea nei paesi in via di sviluppo 2) Bevande con integratori salini utilizzate dagli sportivi 3) Scambio di nutrienti ed ossigeno attraverso la parete dei vasi capillari sanguigni 4) Scambio di ioni attraverso la membrane delle cellule nervose (impulsi nervosi, potenziali di azione, etc.) 5) Il fenomeno dell’osmosi inversa, che permette ad alcuni tipi di piante (mangrovie, etc.) di vivere vicino ad acque salate.
Scaricare