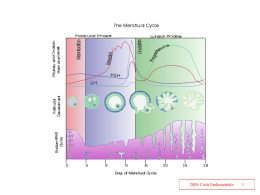
L’imaging ecografico ha reso obsoleta l’isteroscopia diagnostica in età postmenopausale? Manuela Guerrini U.O. Ginecologia e Fisiopatologia della Riproduzione Umana Azienda ospedaliera S. Orsola – Malpighi - Bologna Indicazioni cliniche per la valutazione delle patologie endometriali 1.Pazienti in post-menopausa con AUB 2.Pazienti in post-menopausa asintomatiche (screening, riscontro occasionale) 3.Pazienti in post-menopausa in terapia con tamoxifene PERDITA EMATICA ANOMALA Definizione in postmenopausa sanguinamento genitale che si presenta dopo almeno 12 mesi di amenorrea (WHO Technical Report Series,1996 Incidenza in postmenopausa 4-10% (Disaia,2002; The Writing group for the Postmenopausal Estrogen/Progestin intervention Trial,1996) •20-60% dei consulti specialistici ginecologici •25% degli interventi chirurgici maggiori (Awwad JT,1993; Spencer CP. 1997; Shwayder JM. 2000; Van Dongen H,2007) AUB in POSTMENOPAUSA CAUSE PREVALENZA Bronz L. Ultrasound Obstet Gynecol 1997 Atrofia 60-70% Polipi, miomi, iperplasia, adenomiosi Carcinoma endometriale 20-40% 10% Choo YC. Obstet.Gynecol.1985 Osmers R. Lancet 1990 Karlsson B. Am.J.Obstet.Gynecol.1995 PROCEDURE DIAGNOSTICHE •Metodiche di sampling endometriale alla cieca (D&C, VABRA, Pipelle,…) •Ecografia transvaginale (TVS) •Sonoisterografia (SHG) •Isteroscopia +/- sampling endometriale office Pazienti in post-menopausa con AUB Approccio storico dei ginecologi verso il sanguinamento uterino anomalo in post-menopausa “ Carcinoma endometriale fino a prova contraria” (Goldstein, 2009) Il Ca. endometriale si presenta con sanguinamento genitale nell’ 80-95% dei casi (Smith-Bindman, 2004) Per tale motivo tali pazienti devono essere sottoposte a metodiche diagnostiche di approfondimento Quale metodica offre il miglior rapporto costo/beneficio? TVS SHG Isteroscopia office Pazienti in post-menopausa con AUB Standard of Care TVS come screening iniziale (Smith-Bindman,1998; Dubinsky,2004; ACOG 2000; Society of Radiologists in US-sponsored Consensus Conference, 2001) Second Step SHG (Timmerman 2009; Goldstein 2009; Dubinsky 2004) Iteroscopia +/- bx (Smith-Bindman,1998; ACOG 2000; Society of Radiologists in US-sponsored Consensus Conference, 2001) Pazienti in post-menopausa con AUB • A partire dalla fine degli anni ’80 sono stati pubblicati numerosi studi che hanno valutato lo spessore endometriale come variabile ecografica predittiva del carcinoma dell’endometrio. • Sono stati proposti cut off variabili tra 3 e 10 mm Quale cut off? Esistono altre caratteristiche ecografiche utili? Pazienti in post-menopausa con AUB: quale cut off? Autore Cut-off N° pz Tipo pz Falsi negativi (mm) Nasri 1989 Goldstein 1990 Granberg 1991 Varner 1991 Karlsson 1995 ≤5 ≤5 ≤5 ≤4 ≤4 93 30 205 80 1138 AUB AUB AUB Asint/AUB AUB-HRT/noHRT 0 0 0 1 0 Ferrazzi 1996 Guner 1996 Granberg 1997 Smith-Bindman 1998 (review) ≤4 ≤4 ≤4 ≤5 930 289 1110 5892 2 0 0 4% Briley 1998 Mateos 1999 Garuti 1999 Gull 2000 Epstein e Valentin 2001 Gull 2003 ≤5 ≤5 ≤4 ≤4 ≤4 <4 182 168 419 163 97 394 AUB Asint/AUB AUB HRT/noHRT Asint/AUB AUB AUB AUB AUB AUB AUB 0 (3 iperplasie) ? ? 1 0 0 (follow up 10 aa) Pazienti in post-menopausa con AUB Quale cut off? Quindi Rischio di EC nella popolazione sopra a 50 anni < 1/1000 (SEER 2000) 1-14% Rischio di EC in paziente con AUB (Hawwa 1970; Gramberg 1991; Rose 1996;Goldstein 2009) Rischio di EC in pazienti con AUB Con spessore endometriale ≤4 0,1-1% Con spessore endoemtriale ≥5 4,6-20% (Smith_bindman 2004; Jurkovic 2005; Goldstein 2009) Pazienti in post-menopausa con AUB Quale cut off? • Uno spessore endometriale ≤4 mm è fortemente predittivo di atrofia endometriale • Con rima endometriale ≤4 mm non è consigliabile eseguire ISC e biopsia, in considerazione del basso rischio di EC e dell’alto tasso di fallimento della biopsia (assenza di materiale o materiale insufficiente per diagnosi) Con un cut-off ≤4 mm FN 0,25-0,50% Con un cut off ≤5 mm FN 4% (Goldstein 2009) (Smith-Bindman 1998) • Usando un cut-off ≤4 mm si può ridurre la necessità di diagnostica invasiva per il 31-70% dei casi (Granberg 1991; Osmers 1990; Ferrazzi 1996) Pazienti in post-menopausa con AUB: Fattori di rischio per EC •Età •Obesità •Nulliparità •Diabete mellito •Ipertensione arteriosa •Esposizione estrogenica •Tamoxifene •Menarca precoce/menopausa tardiva •S. di Linch (HNPCC) N.B. HRT non è un fattore di rischio accertato Pazienti in post-menopausa con AUB: Fattori di rischio 930 pazienti cut off di 4 mm •sensibilità per EC 98% •NPV per EC 99% •LHR per EC 0.05 age age 80 70 60 Post-test 50 1 0,9 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 0 40 80 70 60 bmi = 35 bmi = 27 bmi = 20 Prevalence Pre-test 50 Con rima endometriale ≤ 4 mm la probabilità di EC non è influenzata da età e BMI e diventa paragonabile a quella della popolazione generale con spessore endometriale ≤ 4 mm 1 0,9 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 0 40 Età e BMI sono gli unici fattori che sono risultati significativi in un analisi multivariata Prevalence •LHR per atrofia 7.1 HRT E SPESSORE ENDOMETRIALE Terapia ormonale continua combinata non altera in maniera significativa lo spessore endometriale quindi non c’è un cut off ecografico diverso. L’ecografia può essere eseguita in qualsiasi momento del ciclo Terapia ormonale sequenziale Vanno valutate allo stesso modo delle pazienti in età fertile, subito dopo il termine del sanguinamento (5-10° gg del ciclo) L’ecografia transvaginale è più accurata nelle pazienti che non assumono HRT rispetto alle pazienti in HRT Sensibilità comparabile Specificità inferiore nelle pazienti in HRT (Smith-Bindman 1998) Pazienti in post-menopausa con AUB Altre caratteristiche ecografiche utili • La valutazione dell’ecostruttura endometriale (omogeneità versus disomogeneità) aumenta accuratezza, specificità e NPV della TVS. Quindi è utile una valutazione quantitativa e qualitativa. (Sousa 2001; Dubinsky 2004) • Uno studio del 2006 afferma che ecostruttura endometriale disomogenea presenza di profili endometriali irregolari presenza di architettura vascolare irregolare al power doppler sono predittivi di EC. (Epstein e Valentin 2006) Pazienti in post-menopausa con AUB Altre caratteristiche ecografiche utili • Uno studio del 2007 ha preso in considerazione diverse caratteristiche ecografiche che possono essere predittive di EC (ecostruttura disomogenea, margini endometriali irregolari, cisti endometriali, iper/ipo/isoecogenicità, linee iperecogene endometriali, tipo di vascolarizzazione al power doppler) e dopo analisi multivariata: ecostruttura disomogenea dell’endometrio il fattore più predittivo di EC La valutazione delle caratteristiche doppler aumenta di poco la capacità diagnostica con TVS. (Opolskiene 2007) • Il problema di tutte le altre variabili ecografiche è la loro riproducibilità tra i diversi operatori. Lo spessore endometriale è la variabile più riproducibile ed è quindi la prima da prendere in considerazione Metodica della TVS • La TVS non permette di ottenere materiale per una diagnosi istologica, pertanto la misura dello spessore endometriale deve essere accurata e ben documentata Scansione longitudinale (in coronale lo spessore viene sovrastimato) Rima endometriale visualizzata lungo tutto il suo decorso comprendendo il cc Misura in corrispondenza del fondo della cavità Se c’è fluido in cavità va misurato lo spessore delle due emirime • Valutare l’ecostruttura endometriale per escludere patologie focali (polipi e miomi sottomucosi) e diffuse • Per escludere patologie focali non è sufficiente ottenere una scansione longitudinale mediana, bisogna ottenere multiple scansioni longitudinali bidimensionali da un angolo tubarico all’altro oppure una ricostruzione 3D della cavità • Valutare i confini endometrio-miometriali • L’utilizzo del power doppler può aggiungere delle informazioni (“feeding vessel” di polipo endometriale, vascolarizzazione periferica di mioma sottomucoso, architettura vascolare irregolare nelle patologie diffuse) Metodica della TVS Bright edge B-Mode Feeding vessel Power Doppler Fallimento della TVS In circa il 5-10% dei casi la rima endometriale non è valutabile (Goldtsein 1994; Ferrazzi 1996; Dubisky 2004) Probabilmente attualmente questa percentuale è inferiore dato il miglioramento della tecnologia CAUSE: •Fibromatosi/adenomiosi uterina (distorsione dei profili, profili sfumati) (Van den Bosch 2007, Goldsetin 2009; Dubinsky 2004) •Utero in asse (Non AVF/non RVF) •Precedente chirurgia sull’utero •Obesità (Goldstein 2009) (Goldstein 2009) (Goldstein 2009) N.B. Se l’endometrio non è chiaramente visualizzabile in tutta la sua estensione e se i confini con il miometrio sono sfumati l’ecografia TV non è sufficiente Esame di II livello raccomandato (ISC/SIS) Pazienti in post-menopausa con AUB ECOGRAFIA TV ≤4 mm ATROFIA NON DIAGNOSTICA NO > 4 mm SONOHYSTEROGRAPHY/HYSTEROSCOPY La sonoisterografia ha un’accuratezza diagnostica comparabile a quella dell’isteroscopia Non può completamente rimpiazzare l’isteroscopia ma può ridurre il numero di procedure invasive SHG: che tipo di ispessimento? Focale Diffuso Pazienti in post-menopausa con AUB ECOGRAFIA TV ≤4 mm ATROFIA NON DIAGNOSTICA NO > 4 mm SONOISTEROGRAFIA/ISTEROSCOPIA Lesione diffusa Biopsia office Lesione focale Isteroscopia operativa Pazienti in post-menopausa con AUB: analisi dei costi La biopsia endometriale di routine senza valutazione ecografica preliminare può portare a rischi inutili, disconfort e costi per la paziente. L’approccio basato sulla biopsia endometriale sarebbe vantaggioso se la biopsia avesse una sensibilità > del 94% per le patologie benigne o se il Ca dell’endometrio avesse una prevalenza del 31% nelle donne con AUB (Dubinsky 2004) La strategia diagnostica basata sulla TVS con cut off di 5 mm è la meno costosa TVS cut off 5 mm £ 11.470 TVS cut off 4 mm/Biopsia endometriale £ 30.000 Le strategie combinate (TVS+ISC+EB/TVS+ISC/ISC+EB) non hanno un miglior rapporto costo beneficio Pazienti in post-menopausa ASINTOMATICHE CONSIDERAZIONI: - Non esiste un razionale scientifico per lo screening ecografico delle patologie endometriali. Per proporre tale screening bisognerebbe avere dati certi sulla riduzione di mortalità e morbilità per EC. (Gull 1996; Jurkovic 2005; Goldstein 2009) - L’utilizzo della TVS nelle pazienti in post-menopausa è sempre più diffuso per vari motivi (Es: Follow up ecografico di cisti ovariche semplici, miomi uterini etc.). Sempre più frequente è il riscontro occasionale di endometrio ispessito. (Goldstein 2009) - Non esiste un cut off certo. Sono stati proposti cut off variabili da 5 a 11 mm. (Jurkovic 2005) - Non esistono studi prospettici che abbiano valutato qual è il significato dell’aumento delle spessore endometriale in tali pazienti. (Goldstein 2009) - Non c’è evidenza che vi sia un’ indicazione a sottoporre a biopsia endometriale le pazienti asintomatiche in postmenopausa con ispessimento endometriale. La decisione va valutata caso per caso. (Goldstein 2009) • 123 pazienti con endometrio sospetto alla eco TV, senza sanguinamento vaginale • 190 pazienti con k endometrio diagnosticato dopo sanguinamento • Confronto fra sopravvivenza nei due gruppi • Analisi dei costi economici Correlazione fra disease-free survival e bleeding time Conclusioni • Nessuna differenza in termini di stadio e sopravvivenza fra pazienti con k endometriale scoperto per caso e coloro con sanguinamento della durata < 8 settimane • Screening ecografico associato a interventi non necessari: – Morbilità iatrogena – Ridotta qualità di vita di pazienti anziane – Alti costi sanitari Pazienti in post-menopausa ASINTOMATICHE Tuttavia l’interpretazione e la gestione di un riscontro occasionale di ispessimento endometriale è utile e non è standardizzata. Pazienti in post-menopausa ASINTOMATICHE Dato il basso rischio di EC nelle pazienti in post-menopausa è inutile uno screening ecografico Cut off Rischio di EC Pazienti positive allo screening Detection rate di EC asintomatico > 11 6.7 0.25 % 87 % >10 5.8 0.39 % 89 % >8 (Osmers 1989) 2.1 1% TAMOXIFENE • SERM (Modulatore Selettivo dei Recettori per Estrogeni) • Effetti antiestrogenici sul seno • Effetti estrogenici su osso, endometrio, vagina INDICAZIONI FARMACOLOGICHE • Terapia adiuvante del cancro mammario (20 mg/die per 5 anni) • Terapia delle metastasi • Chemioprofilassi in donne ad alto rischio EFFETTI SULL’ UTERO Aspetti istologici • Ipertrofia/iperplasia dello stroma endometriale (frequente) • Iperplasia dell’epitelio ghiandolare (più raro) • Formazione cisti subendometriali (frequente) • Adenomiosi uterina (frequente) Aumento di incidenza di K endometrio pari a 2-5 volte quella dei controlli (1.6/1000 donne/anno rispetto a 0.7/1000/anno) INCIDENZA COMPLESSIVA DI PATOLOGIA ENDOMETRIALE (A 5 ANNI) • Circa il 30% delle pazienti sviluppano qualche patologia endometriale – 20-29% polipi endometriali – 5-15% iperplasia non atipica – 1-5% iperplasia atipica – <1% nuovi casi di k endometrio Vosse et al., 2002 Garuti et al., 2006 Spessore endometriale DURATA DEGLI EFFETTI SULL’ENDOMETRIO Crescita media di 0.75 mm per anno Diminuzione media di 1.27 mm per anno 5 anni Fishman et al., 2006 QUALE STRATEGIA DI SCREENING UTILIZZARE? • Non esiste uno screening universalmente accettato nelle pazienti asintomatiche. • Nessun controllo nelle pazienti asintomatiche (ACOG Committee Opinion No. 336, Obstet Gynecol June 2006) • Avvisare la paziente del rischio di sviluppare K endometriale • Screening nelle pazienti con AUB o precedente patologia endometriale • Screening annuale/biennale/triennale QUALE METODICA DIAGNOSTICA? • Isteroscopia diagnostica ? • Biopsia endometriale ? • Citologia endometriale ? • Ecografia Transvaginale ? DIFFICOLTA’ TECNICHE DELLA TVS Confini endometriomiometriali sfumati Presenza di cisti subendometriali Presenza di adenomiosi Incertezza nel posizionamento dei calipers media di tre misure PERFORMANCE DEI DIVERSI CUT-OFFs Duffy (2005) > 3 mm > 5 mm Vosse (2002) > 8 mm Garuti (1999) > 3 mm > 7 mm Salmaggi (1997) > 5 mm Haller (1996) > 4 mm Sens (%) Spec (%) PPV (%) NPV (%) 78.3 34.8 56.0 79.6 15.1 14.6 96.3 92.4 95.1 70 64 --- 95.1 83.8 54.8 81.3 63.7 79.4 ----- 90.9 72 90.9 95.8 45.5 71.9 88.2 ECOGRAFIA TRANSVAGINALE • Molto sensibile ma poco specifica • Deve essere completata da test più specifici • Quale cut-off impiegare? • Se ≥5 mm procedure invasive in > 50% delle pazienti • Se ≥8 mm procedure invasive in circa 20% delle pazienti CUT-OFF ed ESITO ISTOLOGICO % positive % atrofia cistica % atipie e K • > 5 mm 50 41 1-3 • > 8 mm 10-20 30 10 PROTOCOLLO DI GESTIONE VALUTAZIONE ECOGRAFICA A TEMPO ZERO NORMALE SCREENING TRIENNALE (cut-off≥8 mm) ANORMALE SONOISTEROGRAFIA/ISTEROSCOPIA RISOLUZIONE PATOLOGIA ENDOMETRIALE SCREENING ANNUALE (cut-off≥8 mm) Per concludere: l’imaging ecografico ha reso obsoleta l’isteroscopia diagnostica in età post-menopausale? NO …ma La TVS insieme alla SHG può ridurre la necessità di ricorrere all’ isteroscopia L’isteroscopia va considerato un esame diagnostico di II livello L’ecografia TV presenta numerosi vantaggi: poco costosa, poco invasiva, non dolorosa, non comporta complicanze, raramente non diagnostica, con elevata sensibilità diagnostica …Grazie PATOLOGIE UTERINE IN POSTMENOPAUSA • Patologie organiche focali benigne (polipi endometriali, miomi uterini) • Iperplasia endometriale e Ca Endometrio • Ca Cervice Abnormal uterine bleeding (AUB) PROCEDURE DIAGNOSTICHE •Metodiche di sampling endometriale alla cieca (D&C, VABRA, Pipelle,…) •Ecografia transvaginale (TVS) •Sonoisterografia (SHG) •Isteroscopia +/- sampling endometriale office METODICHE DI SAMPLING ENDOMETRIALE ALLA CIECA 1)D&C • utilizzato a partire dalla seconda metà del XIX secolo • Viene eseguito in Anestesia generale durante ricovero • comporta circa un 10% di falsi negativi (più spesso per patologie focali come polipi e miomi) (Word 1958) METODICHE DI SAMPLING ENDOMETRIALE ALLA CIECA 2) Vacuum Suction Curettage devices (Vabra, Pipelle, etc) • Pipelle sarebbe ugualmente efficace, più sottile, di plastica e quindi meno doloroso e meno costoso del sistema VABRA (Kaunitz, 1988) • Il sampling endometriale alla cieca ambulatoriale può essere causa di disconfort, non è eseguibile (ad es. per stenosi del CC) in una quota del 2-28% dei casi può essere poco accurata soprattutto in caso di patologie focali (es. Polipi) (Smith-Bindman, 1998) • La sensibilità della pipelle per il carcinoma endometriale (EC) è variabile da 68 a 97,5% a seconda delle casistiche con una quota di FN del 2-32% (Kaunitz, 1988; Stovall, 1991; Zorlu, 1994; Ferry, 1993; Guido, 1995) Risultati istologici • 123 pazienti asintomatiche • 16 casi K endometrio (13%) • 5 casi iperplasia atipica (4%) • 16 casi iperplasia non atipica (13%) • 61 casi polipi (50%) • 23 casi atrofia endometriale (19%) • 1 caso mioma (0.8%) • 1 caso metastasi da k mammario (0.8%) PREMESSE • Quale % di donne hanno patologie endometriali prima di cominciare la terapia? • Qual è la probabilità di sviluppare patologie endometriali ogni anno e al termine della terapia? • Gli effetti sull’endometrio regrediscono alla cessazione della terapia? • Quale è l’accuratezza della metodica di indagine che scegliamo? PREVALENZA DI PATOLOGIA ENDOMETRIALE PRIMA DELL’INIZIO DELLA TERAPIA 146 pazienti sottoposte a TVS prima della terapia 44 (30%) pazienti avevano endometrio > 4 mm 31 (21%) pazienti avevano patologie endometriali, di cui: 2.7% iperplasie atipiche o K endometriale 18.3% polipi e iperplasie non atipiche Garuti et al., 2006 INCIDENZA DI PATOLOGIA ENDOMETRIALE/ANNO • Significativa solo dopo almeno sei mesi • 5 nuovi casi di patologia endometriale per 100 donne ogni anno di terapia • Correlazione lineare con dose e tempo Vosse et al., 2002
Scaricare