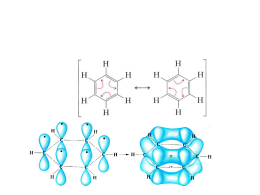
• • • • Effetto Batocromo Effetto Ipsocromo Effetto Auxocromo Effetto solvente. Mauro Sabella RED SHIFT e- Vedremo sperimentalmente come il gruppo CH3- condiziona la lunghezza d’onda di massima Assorbanza. Analizzeremo all’UV 3 campioni contenenti BTX in fase vapore. 268 nm 274 nm toluene Xilene benzene 261 nm Ma come possiamo giustificare tale fenomeno? • Grazie all’effetto della iperconiugazione, gli elettroni σ dei legami C-H alchilici partecipano alla risonanza dell’anello ampliando l’effetto della delocalizzazione elettronica. Ciò porta ad un abbassamento dei dislivelli energetici fra orbitali agevolando le transizioni elettroniche π→π*. EFFETTO IPSOCROMO BLUE SHIFT e- anilina Ione anilinio 256,5 nm anilinio 288,5 anilina benzene 261 nm • Ciò avviene perché nelle vicinanze del cromoforo (benzene) è legato un gruppo detto ipsocromo–NH3+ • In ambiente acido l’anilina si protona e diventa ione aniliio impegnando il doppietto di non legame dell’azoto il quale non potrà partecipare alla delocalizzazione degli elettroni del benzene • Possiamo concludere che più aumenta l’acidità minore sarà la lunghezza d’onda AUXOCROMO • Si tratta di un fenomeno conseguente alla presenza di un gruppo funzionale saturo legato al cromoforo. Come nel red shift anche qua avremo lo spostamento della λMAX ma anche di ε. Questa caratteristica è data da atomi o gruppi con doppietti di non legame. (Alogeni, -NH2, OH, CN) • Bibliografia: – COZZI-PROTTI-RUARO • Mauro Sabella – www.smauro.it – http://flippedlaboratory.wikispaces.com/
Scaricare