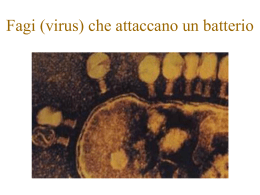
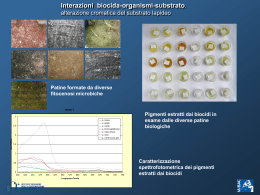
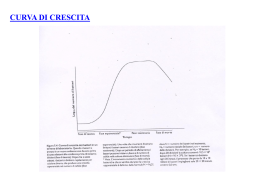
PROGETTO NAZIONALE COLLEZIONE DI MICRORGANISMI DI INTERESSE AGRARIO, INDUSTRIALE ED AMBIENTALE COLMIA Manuale d’uso Edizione curata da: Marina Barba, Alessandra Belisario, Laura Luongo PETRA 21 (1)), 1-84 - COLMIA (Manuale d’uso) Hanno collaborato alla stesura del d manuale i segu uenti autori: ● Collezion ne di microrgan nismi di intereesse fitopatologgico (CRA-PAV V) Marina Baarba, Alessandra Belisario, Franccesco Faggioli, A Angela Gallelli, SteS fania Loreeti, Laura Luongoo, Laura Tomasso oli ● Collezion ne di lieviti e baatteri di interesse enologico (CRA-ENO) Manuela Cersosimo, C Antonnella Costantini, Emilia Garcia-M Moruno, Enrico VauVa dano ● Funghi del d suolo (CRA A-CIN): Francesco Caputo, Alessanndro Lazzari, Luissa M. Manici ● Collezion ne di microrgaanismi di interresse industrialle nella preparrazione dellle olive da men nsa (CRA-OLII) Barbara Laanza, Paolo Marffisi, Francesca Ru ussi ● Microrgaanismi entomoo-patogeni e Collezione C di b batteri diazotroofi liberi in suoli s di interessse agrario (CR RA-ABP) Maurizio Castaldini, C Marceello Pagliai, Pietrro Rumine ● Collezion ne di microrgaanismi patogen ni del tabacco e delle principali colture errbacee dell’Itaalia meridionalle(CRA-CAT) Rosa Caiaazzo, Ernesto Lahhoz ● Collezion ne di microrganismi di inteeresse lattiero--caseario (CR RAFLC) Barbara Bonvini, B Domeniico Carminati, Maria M Emanuela Fornasari, Giorggio Giraffa, Liia Rossetti, Miriaam Zago ● Microrgaanismi utili dell suolo (funghi e batteri) (CR RA-RPS) Anna Beneedetti, Stefano Mocali M ● Collezion ne di Rizobi azoto fissatori (C CRA-ORT) Massimo Zaccardelli Z Le schede descrittiive dei microrgaanismi di interesse agraario, industriale ed ambientale soono consultabili sul sitoo: www.colmia.itt Indice Introduzione ............................................................................................................ 5 1 L’origine delle collezioni di microrganismi: l’erbario ....................................... 9 2 Microrganismi di interesse agro-industriale ..................................................... 11 2.1 Premessa ................................................................................................... 11 2.2 Pre-trattamento del campione ................................................................... 11 2.2.1 Latte e derivati ............................................................................... 12 2.2.2 Vino e mosto ................................................................................... 13 2.2.3 Olive .............................................................................................. 13 2.3 Coltivazione .............................................................................................. 13 2.3.1 Ricerca di batteri lattici nel latte e derivati ................................... 13 2.3.2 Ricerca di batteri lattici e lieviti nel vino e nel mosto ................... 15 2.3.3 Ricerca di batteri e miceti delle olive e delle salamoie .................. 16 2.4 Isolamento e purificazione ........................................................................ 17 2.4.1 Conservazione intermedia (o temporanea) e rivitalizzazione ........ 18 2.4.1.1 Protocollo ......................................................................... 18 2.4.2 Rivitalizzazione .............................................................................. 18 2.5 Identificazione e caratterizzazione ............................................................ 19 2.5.1 Identificazione ............................................................................... 20 2.5.2 Caratterizzazione ........................................................................... 22 2.5.3 La gestione dei dati ........................................................................ 23 2.6 Conservazione prolungata ......................................................................... 24 Bibliografia ............................................................................................... 25 3 Microrganismi fitopatogeni ............................................................................... 26 3.1 3.2 3.3 3.4 3.5 3.6 3.7 3.8 3.9 3.10 3.11 3.12 3.13 Premessa ................................................................................................... 26 Isolamento di funghi fitopatogeni ............................................................. 27 Isolamento di batteri fitopatogeni ............................................................. 30 Mantenimento in vivo di virus e viroidi .................................................... 31 Purificazione delle colture di funghi e oomiceti ....................................... 34 Purificazione e preparazione delle colture di batteri ................................. 35 Purificazione di virus e viroidi .................................................................. 36 Identificazione e caratterizzazione di funghi ed oomiceti ......................... 38 Identificazione e caratterizzazione di batteri ............................................. 42 Identificazione e caratterizzazione di virus e viroidi ................................. 46 Conservazione di funghi ed oomiceti ........................................................ 50 Conservazione di batteri ............................................................................ 54 Conservazione di virus e viroidi ............................................................... 57 Bibliografia ............................................................................................... 58 3 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) 4 Microrganismi entomopatogeni ......................................................................... 61 4.1 4.2 4.3 4.4 4.5 4.6 4.7 Premessa .................................................................................................... 61 Campionamento ......................................................................................... 63 Isolamento .................................................................................................. 64 Purificazione .............................................................................................. 65 Identificazione ............................................................................................ 66 Caratterizzazione ........................................................................................ 67 Conservazione ............................................................................................ 68 Bibliografia ................................................................................................ 70 5 Microrganismi utili del suolo ............................................................................. 71 5.1 5.2 5.3 5.4 5.5 Premessa .................................................................................................... 71 Isolamento .................................................................................................. 72 Riconoscimento dei microrganismi coltivabili ........................................... 79 Conservazione ............................................................................................ 80 Microrganismi non coltivabili: isolamento e conservazione ...................... 81 Bibliografia ................................................................................................ 83 4 Collezione di microrganismi di interesse agrario, industriale ed ambientale INTRODUZIONE La necessità di mantenere in vita i microrganismi per studiarli o utilizzarli in tempi successivi ha costituito argomento di interesse già dalla metà dell’Ottocento. Con lo sviluppo delle tecniche di coltivazione in purezza su substrati artificiali si è arrivati a conseguire l’isolamento dei microrganismi e il loro mantenimento come ceppi individuali. Grazie a questo traguardo iniziarono a sorgere le collezioni di microrganismi, inizialmente riguardanti piccole raccolte di isolati ad uso esclusivo e personale di singoli ricercatori. Successivamente, alcune di queste collezioni sono cresciute a tal punto da richiedere una organizzazione del personale e finanziamenti appositi. Il fine principale di queste collezioni è la conservazione di microrganismi che hanno importanza attuale o potenziale. Esistono in diversi Paesi del mondo collezioni microbiche di utilità generale. Le più prestigiose sono quelle del Centraalbureau voor Schimmelcultures di Utrecht in Olanda, del C.A.B. International Mycological Institute in Gran Bretagna e dell’American Type Culture Collection nel Maryland negli Stati Uniti d’America. Le collezioni di microrganismi consentono di disporre di fonti di variabilità genetica di sicura caratterizzazione in quanto preventivamente identificate e studiate a livello morfo-funzionale. Pertanto, le collezioni di microrganismi hanno l’obiettivo di fornire materiale biologicamente attivo, fenotipicamente e/o genotipicamente caratterizzato, sul quale fondare le attività di ricerca in termini produttivi, comparativi e cognitivi. Allo stato attuale, inoltre, le moderne collezioni forniscono importanti servizi supplementari a quelli precedentemente esposti, che prevedono la preventiva conoscenza di ulteriori proprietà dei ceppi. In Italia il Ministero delle Politiche Agricole Alimentari e Forestali (MiPAAF) ha finanziato un progetto nazionale “Collezione di microrganismi di interesse agrario, industriale ed ambientale” (COLMIA) per mantenere le collezioni presenti nei diversi Istituti del Consiglio per la Ricerca e la Sperimentazione in Agricoltura (C.R.A.), frutto di ricerche finanziate da organismi pubblici o privati. Al Progetto afferiscono nove strutture di ricerca distribuite sul territorio nazionale e coinvolte, a vario titolo, nello studio di popolazioni microbiche di particolare rilevanza economica nei seguenti settori d’interesse: Microrganismi di interesse agroindustriale e alimentare Tre Istituzioni del C.R.A. gestiscono e conservano lieviti e batteri d’interesse alimentare. In particolare: • C.R.A. - Centro di ricerca per le colture foraggere e lattiero-casearie - Lodi, • C.R.A. - Centro di ricerca per l’enologia - Asti, • C.R.A. - Centro di ricerca per l’olivicoltura e l’industria olearia - Pescara. 5 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Microrganismi fitopatogeni Due strutture di ricerca collaborano all’isolamento, caratterizzazione e conservazione di microrganismi agenti di gravi malattie delle piante agrarie. Vengono conservati funghi, oomiceti, batteri, virus e viroidi isolati e caratterizzati da: • C.R.A. - Centro di ricerca per la patologia vegetale - Roma, • C.R.A. - Unità di ricerca per le colture alternative al tabacco - Scafati. Microrganismi entomopatogeni Tra i microrganismi maggiormente impiegati in metodologie di lotta biologica per la difesa delle colture da insetti fitofagi o vettori, sono essenzialmente annoverati funghi e batteri. La collezione di questi microrganismi è curata da: • C.R.A. - Centro di ricerca per l’agrobiologia e la pedologia - Firenze. Microrganismi utili del suolo Batteri e funghi tellurici che concorrono a definire la qualità e la salute di un suolo sono caratterizzati e conservati nella collezione grazie al contributo delle seguenti strutture: • C.R.A. - Centro di ricerca per lo studio delle relazioni tra pianta e suolo - Roma, • C.R.A. - Centro di ricerca per l’agrobiologia e la pedologia - Firenze, • C.R.A. - Centro di ricerca per le colture industriali - Bologna. La collezione è interattiva tra i partecipanti e consultabile dagli utenti, contiene informazioni sull’identificazione del microrganismo, sulle sue caratteristiche biologiche, colturali e genetiche, sulle diverse modalità di conservazione e sulla eventuale disponibilità ad essere inviato a istituzioni diverse. L’elenco dei microrganismi inseriti nella banca dati, è consultabile via internet sul sito: http://www.colmia.it. Le collezioni che afferiscono ad ogni singola Unità di Ricerca sono conservate in situ e periodicamente aggiornate ed ampliate dalle diverse strutture di ricerca, rispettando alcune linee guida precedentemente concordate che prevedono: • il continuo ampliamento della collezione con l’acquisizione di nuovi microrganismi di interesse agrario, industriale o ambientale; • la caratterizzazione e valutazione dell’attività di tali microrganismi; • la valutazione dei metodi di conservazione migliori per ciascun isolato, tali da garantire il mantenimento dei parametri biometrici, fisiologici e biochimici. La collezione COLMIA si avvale di personale qualificato, esperto della tassonomia e dei caratteri distintivi dei microrganismi in essa conservati ed in grado di 6 Collezione di microrganismi di interesse agrario, industriale ed ambientale individuare e, volta per volta, selezionare specifici metodi di mantenimento per funghi, lieviti, batteri, virus, viroidi al fine di minimizzare il rischio di variabilità genetica, cui i diversi isolati potrebbero andare soggetti. La costituzione di questa collezione scaturisce dall’attività di ricerca che le varie Istituzioni partecipanti svolgono negli specifici settori di competenza. Ogni Istituzione competente deve decidere quali siano i microrganismi idonei ad essere inclusi nella collezione, in quanto adeguatamente caratterizzati, qualificanti e rappresentativi di una biodiversità nell’ambito della popolazione di appartenenza. 1. Identificazione: le metodologie adottate variano a seconda della tipologia del microrganismo in esame e riguardano lo studio dei caratteri colturali, morfologici, biochimici, genomici, sierologici, ecc. Sulla base dei parametri osservati il microrganismo è schedato e classificato; 2. caratterizzazione: i microrganismi di particolare interesse sono sottoposti ad analisi sia fenotipiche, sia molecolari, volte a una loro migliore identificazione e biotipizzazione. Queste analisi possono riguardare la valutazione di profili genotipici (es: mini e microsatelliti; RAPD-PCR), o di attività enzimatiche di interesse industriale, il sequenziamento totale o parziale del genoma o di porzioni del genoma, l’eventuale valutazione di aspetti di sicurezza (es. antibiotico-resistenza), ecc. Poiché le caratteristiche da associare ai singoli ceppi sono diverse fra microbi agroalimentari, entomo-fito patogeni e tellurici, sono all’uopo concordati protocolli di caratterizzazione standard fra le singole Unità afferenti ai tre sottoprogetti; 3. conservazione: le modalità di conservazione variano a seconda del microrganismo. Più in generale, gli isolati sono mantenuti su substrati agarizzati, in acqua distillata sterile, su carta, in azoto liquido, in olio minerale oppure liofilizzati. Un caso a parte è quello di alcuni patogeni sistemici quali viroidi e fitoplasmi che, non essendo coltivabili in vitro, devono essere mantenuti in planta; 4. informatizzazione dei risultati: riguarda sia l’organizzazione delle informazioni interne alle singole collezioni, sia quelle relative ai microrganismi che si intendono inserire nella collezione, che sono organizzate in maniera interattiva: ogni UO ha una chiave d’accesso che consente l’aggiornamento a distanza del data base; 5. costituzione della banca dati: le schede descrittive dei microrganismi sono raccolte in una banca dati utilizzando un programma appositamente studiato. La banca dati è suddivisa in tre settori riguardanti: • microrganismi di interesse agroindustriale e alimentare • microrganismi entomo-fito patogeni • microrganismi utili del suolo. Questo manuale contiene alcune brevi informazioni sulle caratteristiche chimico-fisiche e biologiche dei diversi microrganismi presenti nella collezione e sul loro utilizzo nel settore agrario, industriale ed ambientale, nonché alcune indicazioni 7 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) sulle modalità di campionamento, coltivazione, isolamento, caratterizzazione e conservazione utilizzate da tutti coloro che concorrono al mantenimento e alla gestione della collezione COLMIA. Questo manuale può rappresentare una base d’informazione per tutti coloro che sono interessati alla conservazione di microrganismi. 8 Collezione di microrganismi di interesse agrario, industriale ed ambientale 1 L’ORIGINE DELLE COLLEZIONI DI MICRORGANISMI: L’ERBARIO La prima forma di collezione di organismi vegetali, nei quali originariamente venivano compresi anche i funghi, è rappresentata dall’erbario. Solo recentemente Whittaker (1969) ha assegnato ai funghi un regno separato dai vegetali all’interno degli organismi eucarioti. La costituzione del V Regno, quello dei funghi, non ha, comunque, avuto alcuna influenza nel continuare a conservare e collezionare campioni vegetali portanti le strutture fungine idonee per la determinazione tassonomica. L’erbario ha un origine antica si può far risalire all’epoca romana del IV secolo d.C. con Apuleio. Il più antico Erbario, tuttora conservato, è una copia del sec. VI del trattato De materia medica attribuito a Pedanio Dioscoride che come l’Herbarium attribuito ad Apuleio Barbaro si diffuse ampiamente nel Medioevo, in particolare nei centri monastici. Infatti, in epoca medievale gli erbari erano orientati principalmente alla catalogazione delle erbe medicinali per il riconoscimento dei semplici utilizzati nella medicina. Spesso queste raccolte portano ancora il nome dello studioso che ne è stato l’artefice. A partire dal sec. XV ai campioni di erbario essiccati (exsiccata) si è accompagnata la raffigurazione dei campioni stessi eseguita a mano libera oppure a stampa. Fino all’800 gli erbari hanno avuto, quasi esclusivamente, carattere personale, in quanto ogni studioso costituiva il proprio erbario o con finalità comparative per facilitare il riconoscimento delle specie vegetali o come catalogazione della flora presente in determinati ambienti. Un esempio prestigioso, conservato Fig. 1.1 – Sintomi di presso il CRA-PAV, è l’“Erbario di funghi agrumicoli” di Ottone Penzig, studioso tedesco naturalizzato italiano e Cladosporium compactum su foglia di Citrus limonum. assistente del Saccardo (da Fig. 1.1 a Fig. 1.4). Un Erbario costituisce il supporto scientifico di base per le ricerche in numerosi settori della Biologia, incluse Botanica e Micologia. In particolare è indispensabile per studi di: tassonomia, sistematica, fitogeografia, ecologia, genetica, morfologia e anatomia ed anche per studi evolutivi che riguardano l’adattamento di una specie nel tempo e nello spazio. I campioni di erbario sono infatti la testimonianza della realtà biologica vegetale presente in un territorio e relativa al periodo in cui è stato effettuato il prelievo. Ogni campione è accuratamente essiccato (utilizzando opportune presse e materiali assorbenti) e successivamente posto sul foglio di erbario. Questo è dotato di una etichetta recante: nome scientifico dell'entità, località di raccolta, nome del raccoglitore e data di raccolta, nome del determinatore (se diverso da quello del raccoglitore). I campioni di erbario così ottenuti sono raggruppati secondo l'ordine gerarchico naturale (famiglia, genere, specie), sistemati in cartelle e alloggiati 9 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Fig. 1.2 – Sintomi di Colletotrichum gloeosporioides su foglia di Citrus limonum. Fig. 1.3 – Sintomi di Fusarium dimerum su legno di Citrus medica. Fig. 1.4 – Scheda dell’Erbario di funghi agrumicoli di Ottone Penzig. in adatti armadi chiusi e in ambiente asciutto. Una opportuna totale disinfestazione dei locali adibiti ad erbario deve essere periodicamente effettuata. Con l’avvento del nuovo millennio, si sta assistendo ad una ulteriore evoluzione delle finalità annesse all’erbario che sono quelle di documentare nel modo più completo la diversità botanica di uno specifico territorio, fissarne una fotografia che potrà nel futuro servire da riferimento per verificare comparse e scomparse di specie, seguire l’evoluzione dell’ambiente dal punto di vista botanico, ma anche molecolare, potendo disporre comunque di campioni che, sebbene non vitali, possono ancora fornire informazioni utili sul proprio genoma in termini comparativi ed evolutivi. L’erbario del Centro di Ricerca per la patologia vegetale (CRA-PAV), ex Istituto Sperimentale per la Patologia Vegetale (ISPaVe), è censito nell’Index Herbariorum con la sigla ROPV. Annovera al suo interno circa 8000 campioni (exsiccata), tra questi si ricordano: Erbario di funghi agrumicoli di Penzig Herbarium Mycologicum Romanicum Mycotheca Italica (di Saccardo) Erbario Crittogamico Italiano (di Anzi, Arcangeli, Carestia, Passerini, Spegazzini) I funghi parassiti delle piante coltivate o utili (di Cavara, Briosi, Pollacci). 10 Collezione di microrganismi di interesse agrario, industriale ed ambientale 2 MICRORGANISMI DI INTERESSE AGRO-INDUSTRIALE 2.1 PREMESSA L’Italia è ricca di produzioni alimentari tipiche, ottenute con metodologie tradizionali, molte delle quali hanno ottenuto il riconoscimento di marchi DOP o IGP. Fra esse sono inclusi prodotti fermentati (come i formaggi, le olive da tavola e i vini), la cui produzione è spesso fortemente frammentata e fa riferimento a tecnologie tradizionali. Un ruolo essenziale nel determinare questa straordinaria diversità di prodotti alimentari tipici è svolto dai microrganismi. La presenza di differenti quantità e tipi di microrganismi negli alimenti ha in genere implicazioni di carattere igienico e nutrizionale, che risultano sostanziali nel definire la qualità dei prodotti stessi. In relazione al tipo di alimento, la presenza dei microrganismi può essere considerata funzionale, dannosa o ininfluente in base a molteplici aspetti di natura ecologica e fisiologica. Fra i microrganismi utili di interesse alimentare, lieviti e batteri (per lo più lattici) sono di fondamentale importanza nella trasformazione e conservazione di molti prodotti fermentati. Essi rivestono un ruolo essenziale nelle produzioni agroalimentari, in virtù soprattutto delle loro proprietà di interesse tecnologico, che sono determinanti nel definire le caratteristiche qualitative dell’alimento. Molte specie microbiche hanno, inoltre, un notevole valore commerciale poiché sono impiegate come colture starter in svariati alimenti fermentati. Infine, alcune specie possiedono una serie di proprietà biologiche, ritenute utili da un punto di vista applicativo per alimenti probiotici o funzionali. Pertanto, lo studio delle proprietà biochimiche e biologiche dei microrganismi di interesse alimentare è importante non solo per meglio comprendere tutte le variabili da cui dipendono le caratteristiche dell’alimento, ma anche, e soprattutto, per controllare tali variabili al fine di ottenere un prodotto rispondente alle esigenze del mercato. Per rispondere a questi obiettivi, sono essenziali la caratterizzazione e la conservazione del germoplasma microbico di origine alimentare, che assumono un’importanza crescente in relazione alla necessità di valorizzare le risorse biologiche per migliorare la qualità e la sicurezza dei prodotti. Nei paragrafi successivi sono brevemente descritte le principali tecniche attualmente adottate per l’isolamento, la coltivazione e la caratterizzazione di microbi alimentari, con particolare riguardo agli aspetti tassonomici ed eco-fisiologici ad essi associati. 2.2 PRE-TRATTAMENTO DEL CAMPIONE Nel caso degli alimenti, il pre-trattamento del campione è una tappa essenziale dell’analisi microbiologica, soprattutto se si tratta di matrici solide o semi-solide (mosti, formaggi, olive). L’eterogeneità fisica e la complessità chimico-fisica che contraddistinguono questi prodotti determinano una distribuzione irregolare dei mi- 11 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) crorganismi, i quali in relazione alle loro caratteristiche, colonizzano selettivamente alcune parti del prodotto, più favorevoli al loro sviluppo. Pertanto, nella scelta del tipo di trattamento da adottare al campione (es. tipo e volumi di diluente, omogeneizzazioni, eventuali pre-trattamenti enzimatici), è necessario valutare: a) lo stato fisico della matrice; b) le caratteristiche chimico-fisiche (pH, Aw, redox, presenza e organizzazione dello stato grasso e della matrice proteica) e microbiologiche (natura e proprietà di microrganismi da ricercare) dell’alimento. 2.2.1 Latte e derivati Campioni liquidi • Prelevare con una pipetta sterile con incertezza di misura pari al ± 5% almeno 10 ml di campione, e porli in una beuta sterile. • Aggiungere diluente (soluzione di Ringer) in quantità necessaria a raggiungere un rapporto 1:10 (es. 10 ml in 90 ml), corrispondente alla diluizione -1. • Miscelare accuratamente usando un’altra pipetta o agitatore tipo Vortex. Campioni solidi • Omogeneizzare con omogeneizzatore tipo Stomacher. • Determinare il peso del sacchetto. • Pesare almeno 10 g di campione nel sacchetto con un’incertezza di misura non superiore al ± 5%. • Aggiungere 90 ml di diluente (sodio citrato), corrispondente alla diluizione -1. • Omogeneizzare per 1 o 2 minuti. Diluenti • Soluzione di Ringer Composizione Quantità • KCl • NaCI • CaCl2 • NaHCO3 • acqua distillata 0,105 g 2,25 g 0,06 g 0,05 g 1000 ml • Soluzione di sodio citrato Composizione Quantità • citrato trisodico • acqua distillata 20 g 1000 ml 12 Collezione di microrganismi di interesse agrario, industriale ed ambientale 2.2.2 Vino e mosto Campioni liquidi • Prelevare con una pipetta sterile con incertezza di misura pari al ± 5% almeno 10 ml di campione, e porli in un contenitore sterile. • Mantenere a 4 °C e seminare in piastra, su specifico terreno di coltura, entro 48 h, eventualmente diluendo in acqua peptonata o soluzione fisiologica, a seconda dei campioni (mosto, mosto in fermentazione, vino). 2.2.3 Olive Campioni liquidi: salamoie • Mescolare accuratamente la salamoia con una bacchetta di vetro sterile. • Prelevare un’aliquota della salamoia con una pipetta sterile. • Eseguire diluizioni seriali con acqua distillata sterile, agitando con pipetta automatica e miscelando con Vortex. Campioni solidi: olive e foglie a) carposfera e filloplano • Preparare una beuta con 450 ml di acqua peptonata (peptone di soia 4,5 g, NaCl 2,25 g, 450 ml di acqua distillata) e sterilizzarla in autoclave (121°C per 15 min). • Pesare ca. 50 g di olive intere o foglie e aggiungerle all’acqua peptonata. • Incubare a 30° C per 24 h in agitazione termica. • Prelevare 1 ml di acqua peptonata con pipetta sterile ed eseguire diluizioni seriali in acqua distillata sterile, agitando con pipetta automatica e miscelando con Vortex. b) polpa • Omogeneizzare 10 g di pasta di olive con 90 ml di acqua sterile (1:10). • Prelevare 1 ml di omogeneizzato con pipetta sterile ed eseguire diluizioni seriali in acqua distillata sterile, agitando con pipetta automatica e miscelando con Vortex. 2.3 COLTIVAZIONE 2.3.1 Ricerca di batteri lattici nel latte e derivati Esiste attualmente un’ampia gamma di terreni e condizioni colturali utili per una coltivazione e quantificazione dei batteri lattici. La scelta dipende da svariati fattori, fra i quali i più importanti sono la matrice del campione (latte, siero di latte, 13 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) latti fermentati, formaggi, ecc.), il tipo di batteri lattici e il grado di selettività desiderata. Occorre, infatti, ricordare che i batteri lattici in quanto tali non hanno una connotazione tassonomica precisa, perché comprendono entità specifiche e sub specifiche riferibili a diversi generi (Lactobacillus, Streptococcus, Lactococcus, Leuconostoc, Pediococcus, Enterococcus) con caratteristiche tassonomiche e fisiologiche alquanto differenti. Le conte sono generalmente espresse in “unità formanti colonie” (UFC)/g o ml di prodotto. Per consentire una facile individuazione della morfologia delle colonie ed un agevole isolamento, è buona prassi distribuire con una spatola od ansa la patina di campione, pre-trattato e opportunamente diluito, sulla superficie delle piastre. La Tab. 2.1 elenca i principali terreni (agarizzati) e le condizioni colturali applicate nell’analisi di prodotti caseari. I terreni più adatti per l’isolamento dei batteri lattici (LAB) con caratteristiche idonee per l’uso come innesti acidificanti (Starter LAB) sono: 7, 8, 9. Il terreno 10 viene usato per il recupero di batteri adattati al siero di latte (es. i lactobacilli ritrovabili nelle colture naturali nel siero, o sieroinnesti Fig. 2.1). Gli altri terreni possono essere utili per una caratterizzazione complessiva della cenosi lattica (2 e 5) nella quale si possono trovare batteri lattici che intervengono nei processi di maturazione (Non Starter LAB). Gli enterococchi, anche se non lattici, sono caratteristici dei prodotti a base di latte crudo e possono anch’essi avere un ruolo nei processi di maturazione dei formaggi. TABELLA 2.1 – Principali terreni agarizzati e relative condizioni di coltivazione. 1 Pediococchi: MRS + 5% NaCl + 50 ppm vancomicina 30°C per 3/4 gg 2 Leuconostoc: MSE 21°C per 4 gg 3 Lattici citrato fermentanti: MRS + 2% Ca citrato 30°C per 48 ore 4 Enterococchi: KAA 42°C per 24/48 ore 5 Lattobacilli mesofili eterofermentanti: FH medium 30°C per 3 gg (anaerobiosi) 6 Lattobacilli mesofili totali: MRS 25°C per 48 ore (anaerobiosi) 7 Lattobacilli termofili: MRS (pH 5.4) 42°C per 48 ore (anaerobiosi) 8 Lattococchi: M17 25°C per 48 ore 9 Streptococchi termofili: M17 42°C per 48 ore 10 Lattobacilli termofili da innesti: Siero Agar 42°C per 48 ore (anaerobiosi) NB: Per metodi e modalità di preparazione si rimanda alle schede dei singoli fornitori. Per la coltivazione in brodo, si utilizzano gli stessi terreni non agarizzati e l’incubazione è in genere protratta per sole 24 h alle temperature indicate. 14 Collezione di microrganismi di interesse agrario, industriale ed ambientale Fig. 2.1 – Esempio di microflora lattica, colorata con sistema BacLightTM, di siero-innesti per formaggio Grana Padano. Cellule rosse: non vitali; verdi: vitali. 2.3.2 Ricerca di batteri lattici e lieviti nel vino e nel mosto Batteri lattici I batteri lattici, fondamentali per la realizzazione della fermentazione malolattica, possono anche essere considerati microrganismi dannosi se il loro sviluppo nei vini non è adeguatamente controllato. Fra essi le specie appartenenti a Pediococcus e Lactobacillus sono ritenute le più insidiose, in quanto in grado di utilizzare gli zuccheri residui con intorbidamenti e precipitazioni nel prodotto in bottiglia. Un discorso a parte meritano gli enococchi (Oenococcus spp.), i principali agenti della fermentazione malolattica, ritenuta fondamentale in quasi tutti i tipi di vino, in modo particolare nei vini rossi, per la definizione delle proprietà finali del prodotto. Per il loro isolamento a partire da mosto o vino, si utilizzano terreni selettivi (MRS o MLO in presenza di actidione, per inibire la crescita dei lieviti). La Tab. 2.2 elenca i principali terreni (agarizzati) e le condizioni colturali applicate nell’analisi di questi tre gruppi di batteri lattici. TABELLA 2.2 – Principali terreni agarizzati e relative condizioni di coltivazione dei batteri lattici nel vino e nel mosto. Pediococchi: MRS (pH 5,7) 30°C per 3/4 gg Enococchi MLO 30°C per 5 gg Enococchi: MRS pH 4,8 + 10% Tomato juice 30°C per 5 gg Lattobacilli MRS (pH 5,7) 30°C per 2 gg 15 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Lieviti I lieviti sono gli agenti delle fermentazioni alcoliche e, pertanto, sono i più importanti degli “starter” per la produzione di vini, birra e altre bevande alcoliche. Fra i lieviti di interesse enologico, i più importanti sono quelli del genere Saccharomyces, che portano a termine la fermentazione alcoolica. Per il loro isolamento a partire da mosto o vino, si utilizzano terreni selettivi in presenza di ampicillina, che consente di inibire la crescita batterica. I Brettanomyces sono lieviti contaminanti che, alterandone le qualità organolettiche, deprezzano il vino dal punto di vista commerciale. Il loro studio è particolarmente importante poiché molto diffusi in cantina e di difficile isolamento e identificazione. Per il loro isolamento a partire da vino, si utilizzano terreni selettivi in presenza di ampicillina, per inibire la crescita batterica, e di actidione, per inibire la crescita degli altri lieviti. La Tab. 2.3 elenca i principali terreni di crescita e le condizioni colturali applicate nell’analisi di questi lieviti. TABELLA 2.3 – Principali terreni agarizzati e relative condizioni di coltivazione dei lieviti agenti delle fermentazioni alcoliche. Saccharomyces e non Saccharomyces YEPGA 25°C per 2 gg Brettanomyces YEPGA + 2% CaCO3 30°C per 5 gg 2.3.3 Ricerca di batteri e miceti delle olive e delle salamoie I microrganismi associati alle fermentazioni delle olive da tavola sono moltissimi, con ruoli positivi o negativi a seconda del gruppo considerato. Fra essi si annoverano non solo i batteri lattici che, analogamente alle fermentazioni casearie, svolgono quasi sempre un ruolo positivo come “starter” (specialmente Lactobacillus spp.), ma anche lieviti, muffe, batteri coliformi e stafilococchi, indici questi ultimi due dello stato igienico delle produzioni. La Tab. 2.4 espone metodi di conta in terreni agarizzati e le condizioni di coltivazione di questi microrganismi su olive e salamoie. 2.4 ISOLAMENTO E PURIFICAZIONE Questa è una tappa essenziale di tutti gli studi di microbiologia ed è volta all’individuazione di singoli ceppi o biotipi (“isolamento”), segregandoli da una popolazione complessa (“purificazione”). Il protocollo che segue concerne l’isolamento 16 Collezione di microrganismi di interesse agrario, industriale ed ambientale TABELLA 2.4 – Principali terreni e relative condizioni di coltivazione di microrganismi in olive e salamoie. Lattobacilli: MRS 30°C per 2 gg; anaerobiosi Eumiceti totali: MEA 30°C per 2 gg; Eumiceti totali : Rose-Bengal Chloranphenicol 30°C per 2 gg Enterococchi: Mac Conckey 37°C per 1 g *Coliformi: Brillant Green Bile broth 37°C per 1 g Clostridi/stafilococchi: SPS 37°C per 1 g, anaerobiosi * Conta in brodo mediante MPN (in provetta con campanelle Durham). NB: Per metodi e modalità di preparazione si rimanda alle schede dei singoli fornitori. Per la coltivazione in brodo, si utilizzano gli stessi terreni non agarizzati e l’incubazione è in genere protratta per sole 24 h alle temperature indicate. e la purificazione a partire da una moltitudine di colonie diverse accresciute in terreno agarizzato, che è il procedimento più frequente. Le piastre agarizzate con le colonie microbiche derivano in genere da indagini volte alla individuazione o quantificazione di specie o gruppi microbici da diverse matrici. Dopo la semina e l’incubazione alle condizioni standard di crescita, si individuano le piastre aventi dalle 50 alle 100 colonie, prelevandone almeno il 10% in base a eventuali differenze morfologiche (forma, colore, consistenza, dimensione e margini). Ogni colonia (a cui è stato dato un numero) viene, quindi, trapiantata in provette contenenti un substrato liquido oppure “spatolata” con un’ansa (“streaking”) su substrato solido in piastra (Fig. 2.2a). a) b) Fig. 2.2 – a) Spatolamento su substrato solido in piastra; b) crescita di colonie isolate. Provette o piastre vengono quindi incubate a opportune temperature. In genere, microrganismi presunti mesofili (da piastre incubate a 25-30°C) vengono incubati a 30°C mentre ceppi presunti termofili (da piastre a 37-42°C) vengono incubati a 37°C. 17 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Dopo la crescita, valutabile per intorbidamento del brodo o per sviluppo di colonie tipiche ben separate su substrato solido (Fig. 2b), si eseguono una serie (1-2) di strisci di purificazione con lo scopo di ottenere una piastra in cui è presente una sola morfologia delle colonie. A questo punto, si isolano 1-2 colonie ben separate prelevandole con un ago o un’ansa e si coltivano in mezzo liquido. In caso di pleomorfismo di colonia, è consigliabile eseguire ancora 1-2 strisci in piastra; se le diverse morfologie non si risolvono, si reputa che il pleomorfismo sia un carattere distintivo del ceppo in esame. La coltura liquida purificata, dopo una verifica della purezza mediante osservazione microscopica, viene temporaneamente conservata (conservazione intermedia), in attesa di ulteriori saggi (identificazione, caratterizzazione). 2.4.1 Conservazione intermedia (o temporanea) e rivitalizzazione Questa tipologia di conservazione ha lo scopo di mantenere in stato di purezza e vitalità i microrganismi. In questa fase, si definisce “isolato” un microrganismo che è stato sottoposto a isolamento e purificazione secondo i protocolli descritti in precedenza. Per praticità, può rendersi necessario che gli isolati vengano conservati anche per periodi prolungati, in attesa di successivi procedimenti (identificazione; caratterizzazione fenotipica e genotipica). Si definisce “ceppo” o “biotipo” un isolato che è stato assegnato ad un taxon. Gli isolati da identificare o caratterizzare (nonché i ceppi già identificati) sono preventivamente rivitalizzati mediante i seguenti protocolli standard. 2.4.1.1 Protocollo Preparare 2-3 criotubi sterili (da 1 o 2 ml) contenenti glicerolo sterile (15% concentrazione finale) e aggiungere un’opportuna aliquota di coltura pura in fase esponenziale di crescita. L’aggiunta di glicerolo come crioprotettore consente la conservazione anche prolungata delle cellule a bassa temperatura, mantenendone la vitalità. I criotubi vengono conservati a -80°C. Il surgelamento dovrebbe essere immediato, meglio se in azoto liquido. 2.4.2. Rivitalizzazione Si parte dal ceppo o dall’isolato surgelato (-80°C). Si lascia sciogliere il contenuto del criotubo e si preleva un’aliquota di coltura, che viene trasferita su terreno 18 Collezione di microrganismi di interesse agrario, industriale ed ambientale specifico (2-10%); quindi si incuba per tutta la notte alla temperatura di crescita ottimale. Dopo l’intorbidamento del substrato, la purezza della coltura ottenuta viene controllata mediante striscio con un’ansa su terreno agarizzato. Infine, si procede al controllo morfologico delle colonie e alla verifica della loro purezza mediante osservazione al microscopio di aliquote stemperate in acqua sterile. Le colonie devono essere tutte uguali; qualora ci fosse più di una morfologia o più di un morfotipo cellulare, indici entrambi di probabile inquinamento, è necessario ripurificare il ceppo (vedi 2.4). Verificata la purezza del ceppo o dell’isolato, si procede al ripristino dello stock in glicerolo per la conservazione a -80° C; nel contempo, viene seminato terreno di coltura fresco (inoculo 2%, crescita durante la notte) per ottenere la coltura con cui proseguire per i procedimenti di identificazione e caratterizzazione. Nel corso di questa analisi, la coltura può essere conservata a +4°C per qualche settimana. 2.5 IDENTIFICAZIONE E CARATTERIZZAZIONE Identificazione e caratterizzazione sono tappe essenziali nella gestione e mantenimento di una collezione di microrganismi. L’identificazione è assolutamente necessaria qualora la collezione non si ponga come unico obiettivo il mantenimento del germoplasma. Il protocollo di identificazione molecolare è piuttosto identico, nei suoi passaggi essenziali, per i diversi organismi, con qualche piccola significativa differenza (es. sequenza del primer e cicli termici in caso di identificazione mediante PCR) in relazione al taxon considerato. La caratterizzazione è qui intesa invece nella sua accezione più ampia e comprende una serie di informazioni biologiche, eco-fisiologiche e molecolari le quali, essendo spesso il risultato di precedenti sperimentazioni, non sono necessariamente omogenee. L’identificazione consente l’assegnazione di un organismo ad un taxon e, pertanto, è un’informazione necessaria alla definizione stessa di ceppo microbico. A tal riguardo, vi sono vari gradi di identificazione: • identificazione preliminare, o presuntiva: consente una prima assegnazione di un isolato a determinati gruppi tassonomici (es. famiglia o genere); • identificazione specifica: definisce in modo univoco l’appartenenza di un ceppo a una determinata specie; • identificazione sub-specifica (taxa sub specifici: sottospecie, varietà, forma, biotipo, razza); • tipizzazione intra-specifica: ad esempio marker tassonomici ceppo-specifici. Vi sono vari gradi di caratterizzazione: fenotipica, genotipica, biochimica, ecofisiologica, tecnologica. Di fatto, essa comprende tutte le informazioni biologi- 19 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) che relative alla collezione. La completezza dipende dalla storia del ceppo, ovvero dalla tipologia di studio e sperimentazione del microrganismo. 2.5.1 Identificazione Identificazione preliminare L’identificazione preliminare comprende l’accertamento di alcune caratteristiche morfologiche, fisiologiche e biochimiche “di base”, utili per l’assegnazione preliminare di un isolato ad un taxon. Le caratteristiche più comunemente accertate sono: • morfologia cellulare, colorazione di Gram e motilità (mediante microscopia ottica o microscopio elettronico; Fig. 2.3); • intervalli di temperatura e pH ottimali per la crescita; • presenza di catalasi; • NH3 da arginina; • CO2 da glucosio. a) b) c) Fig. 2.3 – Immagini al microscopio elettronico di microrganismi di interesse alimentare: a) lattobacilli all’interno di formaggio Grana maturo; b) Lactobacillus plantarum presente nel mesocarpo di olive da tavola fermentate; c) lievito Saccharomyces cerevisiae. Identificazione specifica Comprende analisi fenotipica o genotipica, profili chemiotassonomici e proprietà fisiologiche e biochimiche. In alcuni casi (es. eumiceti) la semplice analisi morfologica è talora sufficiente per l’identificazione tassonomica su base morfologica. All’opposto, i ceppi microbici isolati da “habitat naturali”, o da prodotti alimentari tipici, a causa delle pressioni selettive ambientali e tecnologiche cui sono sottoposti, mostrano marcate differenze fenotipiche rispetto ai ceppi “tipo” delle specie, oppure spiccata variabilità intra-specifica. Ciò significa che è possibile ritrovare, con elevata frequenza, diversi biotipi o biovarianti adattati a particolari nicchie ecologiche, che hanno subito un’evoluzione tale da determinare piccoli o grandi cambiamenti sia nel fenotipo, sia nel genotipo. Pertanto, il ricorso a un singolo criterio i- 20 Collezione di microrganismi di interesse agrario, industriale ed ambientale dentificativo non è sempre sufficiente a catalogare in modo corretto e univoco un microrganismo. Al fine di ottenere una risposta più sicura, attualmente si applicano procedimenti polifasici, comprendenti cioè una o più tecniche appartenenti alle diverse categorie identificative secondo protocolli dettati più dall’esperienza personale o dalla dotazione del singolo laboratorio, che dall’esistenza di schemi univoci di riferimento. Per i microrganismi di origine casearia, olearia ed enologica si applicano, fra gli altri, i seguenti metodi di identificazione fenotipica o chemotassonomica: • profilo fermentativo degli zuccheri mediante gallerie API (API System; Fig. 2.4); • assimilazione degli zuccheri (solo lieviti); • profilo delle proteine di parete (solo batteri), e i seguenti principali metodi molecolari: • • • • • PCR specie-specifica; sequenza completa o parziale del gene 16S rRNA (per batteri); sequenza del gene 26S rRNA (per lieviti); Multi Locus Sequence Typing (MLST); RFLP di genoma totale, del gene 16S RNA (mediante separazione dei frammenti e ibridazione, o ribotyping; per batteri) e di geni metabolici; • RFLP delle regioni intergeniche ITS (per lieviti) • REA-PFGE. Fig. 2.4 – Identificazione di lattobacilli con sistema 50 CHL (APY System). Tipizzazione Molteplici sono i sistemi di tipizzazione infra-specifica. Fra quelli fenotipici, i più utilizzati sono la lisotipia (o fagotipia), la batteriocinotipia e l’antibiogramma men- 21 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) tre, fra quelli molecolari, i più applicati nei nostri laboratori sono: • PCR multiplex di microsatelliti (per l’identificazione intraspecifica di Saccharomyces cerevisiae); • RAPD-PCR; • Pulsed Field Gel Electrophoresis (PFGE); • Polimorfismo di sequenza di geni tassonomici (es. 16S RNA) o metabolici (ßgalattosidasi, lattosio permeasi, etc.). 2.5.2 Caratterizzazione I saggi da applicare per la caratterizzazione intraspecifica dei ceppi sono virtualmente moltissimi e, in genere, riguardano proprietà relative alla possibile applicazione tecnologica dei microrganismi (caratteri pro-tecnologici). Essi, evidentemente, differiscono a seconda della tipologia di alimento e di coltura (coltura starter; coltura funzionale; coltura protettiva) e all’impiego finale del microrganismo. Le più importanti determinazioni applicate nell’ambito della Collezione sono le seguenti: Batteri di origine casearia I principali saggi applicati a ceppi di origine casearia: • attività enzimatiche generiche e specifiche (attività proteolitica e peptidolitica nel latte o nei substrati sintetici; attività glutammato deidrogenasica); • attività acidificante (curva di pH ) nel latte e siero di latte (Fig. 2.5); • potere acidificante (% acido lattico prodotto) nel latte; Fig. 2.5 – Curve di acidificazione di lattobacilli nel siero di latte. • sensibilità al batteriofago (saggio in micropiastre); 22 Collezione di microrganismi di interesse agrario, industriale ed ambientale • saggio della lisogenia (presenza di profago integrato nel genoma, attraverso induzione colturale con mitomicina C); • ricerca di proprietà di interesse probiotico per un’applicazione in prodotti funzionali da matrice casearia (adesione a cellule eucariotiche; resistenza a condizioni che simulano l’acidità gastrica; resistenza alla bile; deconiugazione dei sali biliari; degradazione del colesterolo, antibiotico-resistenza). Batteri di origine olearia I principali test applicati a ceppi di origine olearia: • • • • • attività enzimatiche specifiche (attività β-glucosidasica; attività esterasica); tolleranza a diverse concentrazioni di NaCl; potere acidificante (% ac. lattico); tolleranza ai fenoli; attività oleuropeinolitica, mediante semina di MRS broth arricchito di oleuropeina e dosaggio mediante analisi GC o HPLC dei prodotti di degradazione; • produzione di batteriocine attive nei confronti di germi patogeni. Batteri di origine vinaria I principali saggi applicati a ceppi di origine vinaria: • capacità di portare a termine la “fermentazione malolattica” (produzione di acido lattico e diminuzione di acido malico, mediante HPLC); • attività amminoacido-decarbossilasica e produzione di ammine biogene (mediante PCR, TLC ed HPLC); • interesse industriale nel settore enologico (mediante analisi sensoriale dei prodotti finiti). Lieviti di origine vinaria I principali saggi applicati a ceppi di origine vinaria: • capacità fermentativa, attività fermentativa (produzione di CO2 e determinazione dell’alcool); • “fattore killer”; • resistenza alla SO2 e produzione di H2S (mediante terreno Biggy); • produzione di acidità volatile (distillazione in corrente di vapore e titolazione); • attività enzimatiche specifiche (glicosidasica, riduzione del geraniolo a citronellolo, mediante GC); • interesse industriale nel settore enologico (mediante GC dei composti aromatici ed analisi sensoriale dei prodotti finiti). 23 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) 2.5.3 La gestione dei dati Lo sviluppo delle tecnologie informatiche ha contribuito al miglioramento della capacità di interpretazione ed elaborazione dei dati microbiologici. Molti laboratori e, in generale, tutte le collezioni microbiche internazionali che offrono anche servizi di tipo diagnostico, basano tutta la fase di confronto, gestione e incremento dei “database” su particolari software (es. APILAB Plus, Gel CompareTM, BioNumericsTM) in grado non solo di elaborare dati provenienti da una sola tecnica di indagine, ma di “fondere”, con opportune tecniche di normalizzazione e aggregazione e con il ricorso a opportuni algoritmi matematici, dati provenienti da metodi anche molto differenti fra loro, come profili elettroforetici, sequenze, informazioni fenotipiche sia binarie, sia continue. L’acquisizione di un software di elaborazione, che in genere presenta costi elevati e necessita di competenze specifiche per un efficace utilizzo, non è strettamente necessaria se si lavora con un centinaio di ceppi con una singola tecnica identificativa, mentre è insostituibile per la gestione di dati polifasici relativi a ceppo teche o collezioni microbiche, per confrontare nuovi isolati con ceppi di collezione, per mantenere la “memoria” biologica di gruppi microbici, o per valutare l’evoluzione di popolazioni in ecosistemi. Attualmente, sia APILAB Plus che GelComparTM/ BioNumericsTM sono disponibili presso CRA-FLC, CRA-ENO e CRA-OLI, unitamente a database genotipici (in genere di profili RAPD-PCR) di svariate centinaia di ceppi appartenenti alle rispettive collezioni. È in corso inoltre un utile scambio di informazioni al fine di armonizzare i protocolli di tipizzazione da adottare all’interno delle tre Unità, che consentirà un confronto affidabile fra profili di biotipi provenienti da ciascuna sotto-collezione. 2.6 CONSERVAZIONE PROLUNGATA Questa fase ha lo scopo di mantenere uno stato prolungato di vitalità microbica e, nel contempo, la massima stabilità biologica. Quest’ultimo aspetto è particolarmente importante in considerazione del fatto che in questa fase transitano nella collezione ceppi già identificati e spesso in avanzata fase di caratterizzazione. Pertanto, le proprietà ritenute di interesse e che determinano la necessità di mantenere in vita un determinato microrganismo, devono essere garantite nel corso del tempo, soprattutto qualora si renda necessario rivitalizzare il ceppo per studi successivi o fornirlo a unità esterne, che è uno dei servizi essenziali per qualsiasi collezione microbica. Le tecniche non differiscono significativamente da quelle adottate per la conservazione temporanea: congelamento o surgelazione della coltura, a cui si affianca anche la liofilizzazione. Il doppio “stock” dà maggiori garanzie qualora insorgano problemi di natura tecnica (malfunzionamento di congelatori; inquinamenti; sconge- 24 Collezione di microrganismi di interesse agrario, industriale ed ambientale lamenti). Inoltre, il liofilizzato è di gran lunga il sistema più pratico ed efficace utilizzato anche dalle grandi collezioni per la fornitura dei ceppi ad altre Unità. Presso il CRA-FLC, i batteri (circa 2500) sono tutti conservati a -80°C in miscela di glicerolo; inoltre, i ceppi ritenuti più importanti della collezione (circa un migliaio) sono conservati anche in forma liofilizzata (fialette mantenute a +4°C). Presso il CRA-OLI, i batteri e i lieviti (circa 300) sono tutti conservati a 80°C in miscela di glicerolo; inoltre, i batteri lattici presenti nella collezione sono conservati anche in forma liofilizzata (fialette mantenute a +4°C). Presso il CRA-ENO, i lieviti (circa 1200) ed i batteri (circa 300) sono tutti conservati a -80°C in miscela di glicerolo; alcuni ceppi di lievito (circa 30) sono conservati anche in forma liofilizzata (fialette mantenute a +4°C). Inoltre le tre Unità si stanno attrezzando al fine di giungere a una duplicazione delle rispettive ceppoteche nei diversi laboratori, al fine di salvaguardare ulteriormente la conservazione dei microrganismi. Per esempio, già da 5 anni è presente una copia presso il CRA-FLC di molti lieviti di interesse enologico provenienti dal CRA-ENO. Le collaborazioni scientifiche in atto fra i tre Centri stanno ulteriormente favorendo questo processo di integrazione fra le ceppoteche. Bibliografia ATLAS R.M., 2006. Handbook of microbiological media for the examination of food. CRC Press, Taylor & Francis Group, Boca Raton, USA. COLLINS C.H., P.M. LYNE, J.M. GRANGE, 1989. Microbiological methods. Butterworth & Co, Inghilterrra. CORRIEU G., F.M. LUQUET, 2008. Bactéries lactiques - De la genetique aux ferments. Lavoiser, Paris, Francia JAY J.M., M.J. LOESSNER, D.A. GOLDEN, 2009. Microbiologia degli alimenti. Springer-Verlag Italia, Milano. 25 Collezione di microrganismi di interesse agrario, industriale ed ambientale 3 MICRORGANISMI FITOPATOGENI 3.1 PREMESSA Come per le altre collezioni, anche per quella dei microrganismi fitopatogeni la funzione essenziale è quella di preservare la biodiversità. È importante, dunque, non solo annoverare diverse specie, ma anche conservare molti isolati della stessa specie patogena per assicurare la variabilità all’interno di una popolazione in termini di virulenza, di produzione di metaboliti e/o tossine, di resistenza a fitofarmaci, ecc. I patogeni delle piante comprendono una varietà di microrganismi quali funghi, oomiceti, batteri e fitoplasmi, come pure di entità infettive come virus e viroidi. I funghi fitopatogeni che vengono conservati nella collezione sono organismi eucarioti generalmente microscopici, filamentosi, che si riproducono mediante spore. Sono eterotrofi e rappresentano i maggiori organismi decompositori di sostanze organiche. Sono note più di 10.000 specie fungine responsabili di malattie delle piante. Alcune di esse sono parassiti obbligati o biotrofi e sono in grado di vivere e riprodursi solo sull’ ospite; altre, considerate saprofite o necrotrofi, colonizzano le piante ospiti per una parte del loro ciclo vitale, ma sono in grado di accrescersi su materiale organico non vivente e di crescere su terreni di Fig. 3.1 – Colonia fungina di Altercoltura artificiali (Fig. 3.1). naria alternata, fungo mitosporico. Gli Oomiceti sono organismi filamentosi (Fig. 3.2), molto simili ai funghi, ma con la parete cellulare composta da cellulosa anziché da chitina, hanno forme di diffusione mediante zoospore biflagellate e riproduzione sessuata mediante oospore. Le analisi molecolari hanno mostrato che questi organismi sono correlati alle diatomee e alle alghe brune e sono stati inclusi nel regno degli Stramenopila o Chromista. Gli oomiceti hanno evoluto uno stile di vita simile a quello fungino e comprendono speFig. 3.2 – Micelio, sfiancamenti ifali e cie fitopatogene che causano appassimento, sporangi di Phytophthora. morie e marciumi di piante erbacee e arboree. Appartenenti all’ordine Pythiales abbiamo i generi Phytophthora e Pythium, ai quali appartengono importanti patogeni non obbligati. 26 Collezione di microrganismi di interesse agrario, industriale ed ambientale I batteri fitopatogeni comprendono specie Gram positive e Gram negative; sono organismi procarioti, unicellulari, asporigeni, provvisti di parete e membrana citoplasmatica, caratterizzati dall’assenza di un nucleo e di mitocondri e dalla presenza di poche strutture cellulari. Le cellule batteriche possono presentare una forma bastoncellare o rotonda ed essere provvisti di microfibrille, flagelli, pili o fimbrie. Alcuni (Corinebatteri) hanno cellule con forme irregolari. Gli Attinomiceti (o Attinobatteri) sono Gram positivi e formano strutture filamentose. I batteri si moltiplicano per scissione binaria. Sono noti circa 26 generi di batteri responsabili di fitopatie, cui afferiscono almeno 180 specie riconosciute, tra le quali quelle incluse nei generi Xanthomonas, Pseudomonas, Erwinia, Ralstonia, Agrobacterium. Ad eccezione di quelli cosiddetti esigenti per fonti nutrizionali (“fastidious”), difficili da coltivare in vitro (es. Xylella), i batteri fitopatogeni sono saprofiti facoltativi e possono crescere su terreni di coltura artificiali. I virus delle piante sono patogeni sistemici composti da un genoma generalmente a RNA, o più raramente a DNA, sia a singolo (ss) sia a doppio (ds) filamento, e da un involucro proteico detto capside. Il virus, una volta penetrato nella cellula vegetale, dà inizio alla sua replicazione utilizzando la maggior parte dei componenti cellulari dell’ospite. Il virus è comunque capace di produrre alcune proteine funzionali come una RNA polimerasi RNA dipendente e proteine strutturali che formano i capsidi virali. Attualmente vi sono centinaia di virus responsabili di malattie delle piante, classificati in 14 famiglie e 50 generi. I viroidi sono organismi sistemici composti solo da una molecola di RNA a singolo filamento circolare di 300-400 nucleotidi di lunghezza, che non codifica per alcuna proteina. L’acido nucleico non è ricoperto da un capside proteico, non viene degradato dagli enzimi cellulari grazie alla sua circolarità e alle caratteristiche strutture secondarie molto complesse che esso assume. I viroidi ad oggi conosciuti sono circa 30, classificati in 2 famiglie e 15 generi. Gli organismi fitopatogeni sono talora difficili da isolare ed identificare. Normalmente, la loro identificazione si basa su tecniche diverse che vanno dallo studio delle caratteristiche morfologiche e biologiche, all’impiego di metodi biochimici ed immunologici ed anche di metodi molecolari quali l’ibridazione, reazione a catena della polimerasi (PCR), ovvero Real time-PCR. Di seguito sono riportati i principali protocolli di analisi che riguardano: isolamento, identificazione, caratterizzazione e conservazione di funghi, batteri, virus e viroidi fitopatogeni. 3.2 ISOLAMENTO DI FUNGHI FITOPATOGENI L’isolamento avviene attraverso metodi di laboratorio che differiscono in relazione alla matrice di origine. In particolare: 27 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Isolamento da ospite vegetale Se il fungo sporula sul tessuto ospite, si può ottenere una coltura pura prelevando i conidi, le spore o altri propaguli dal tessuto e trasferendoli su un idoneo substrato di crescita agarizzato. Se non sono visibili fruttificazioni sull’ospite, il campione viene lavato sotto acqua corrente, disinfettato con NaClO o H2O2 o con altri disinfettanti e lasciato asciugare sotto cappa. Una volta asciutto, al margine della zona lesionata vengono prelevate piccole porzioni di tessuto che sono poi poste su idoneo substrato di crescita (tab. 3.1), al quale possono essere aggiunti antibiotici (es. penicillina o ampicillina (100 mg/l) per sfavorire la crescita di eventuali contaminanti batterici. In alternativa, i frammenti prelevati vengono blandamente sterilizzati con una soluzione di ipoclorito di sodio all’1% per 1 minuto, quindi risciacquati con acqua distillata sterile. Una volta asciutti, vengono posti su substrato agarizzato in piastre. La disinfezione superficiale dei frammenti di tessuto ospite può anche essere eseguita per flambazione, passando velocemente sulla fiamma frammenti di tessuto corticale/legnoso prelevati al margine di lesioni prodotte su organi legnosi di piante arboree o arbustive. Isolamento da terreno I funghi presenti nel terreno possono essere isolati con la tecnica delle diluizioni. Si lascia asciugare il terreno in ambiente ben areato. Una volta che il terreno si è asciugato, si setaccia in modo da ottenere una polvere abbastanza fine. Si prelevano 3 differenti quantità di terreno (0,5-1-2 g) che vengono disperse in altrettante provette contenenti 100 ml di acqua distillata sterile e agar tecnico (0,05%). Il campione è posto ad agitare per circa 20 min, quindi 1 ml della sospensione viene distribuito tale e quale in piastre contenenti agar-acqua; dalla sospensione madre vengono fatte diluizioni seriali (generalmente 10-1, 10-2, 10-3) che sono poi distribuite anch’esse su agar-acqua ovvero su terreni di coltura molto poveri (es. Czapeck dox agar) (Fig. 3.3). Per ciascuna diluizione si effettuano almeno 3 repliche. Dopo 5-6 giorni di incubazione a 20-25°C si sceglierà la concentrazione migliore (ossia quella in cui sono visibili non più di 30-40 colonie distribuite sulla piastra). Dalle colonie vengono quindi effetFig. 3.3 – Micelio fungino su agar-acqua. tuati i trasferimenti su PDA. 28 Collezione di microrganismi di interesse agrario, industriale ed ambientale TABELLA 3.1 – Principali terreni agarizzati impiegati per l’isolamento e la crescita di funghi fitopatogeni. AGAR-ACQUA 20 g agar 1litro di acqua distillata AGAR PATATE DESTROSIO (PDA) 39 g agar patate destrosio 1 litro di acqua distillata AGAR FARINA DI MAIS (CMA) 17g agar farina di mais 1litro di acqua distillata AGAR-CAROTA 200g carote (preferibilmente biologiche) 20g agar 1litro di acqua distillata AGAR ESTRATTO DI MALTO 20g estratto di malto 20 g di agar 1 litro di acqua distillata AGAR AVENA 30g avena 20g agar 1 litro di acqua distillata CZAPECK DOX AGAR 33,36 g di Czapeck 20 agar 1 litro di acqua distillata V8 A 200 ml V8 15 g agar 2 g CaCO3 1 litro di acqua distillata AGAR CON CAROTA A PEZZI (CPA) 50 g carota a pezzi 22 g agar 1 litro di acqua distillata KOMADA AGAR 1 g K2HPO4 0,5 g KCl 0,5 g MgSO4.7H2O 0,01g FeNa EDTA 2 g L-Asparagina 20 g D-Galattosio 15 g Agar 1 litro di acqua distillata “Baiting” ovvero uso di esche per l’isolamento La tecnica del “baiting” è utilizzata spesso per l’isolamento di Oomiceti, in particolare per isolare specie di Phytophthora dal terreno o dalle radici di piante deperienti. Questa tecnica permette di aumentare la possibilità di isolamento di questi patogeni notoriamente difficoltoso anche in presenza di sintomi conclamati e di sfavorire lo sviluppo di contaminanti. Nel caso più comune di un campione di terreno, questo viene ripartito in più contenitori (es. 3-5 bicchierini o vaschette), avendo cura di integrare il terreno anche con frammenti di radici. Ai campioni viene aggiunta acqua distillata sulla cui superficie vengono poste foglie di azalea o camelia o quercia (o altro opportuno materiale vegetale). I campioni vengono incubati a temperatura ambiente, lontano da luce di- 29 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) retta, fino alla comparsa dei sintomi sulle foglie (solitamente 3-5 giorni) che non devono essere a diretto contatto con il terreno o con le radici. Le foglie sono, quindi, tagliate alle estremità, risciacquate con acqua distillata, l’acqua in eccesso viene fatta asciugare e le foglie vengono ridotte in piccole porzioni (3x3 mm) e messe in piastre con substrato selettivo (Tab. 3.2). Le piastre vengono incubate al buio a temperatura ambiente ovvero in termostato a circa 20-25°C. Le colonie che si sono sviluppate sono successivamente trasferite su substrati di crescita come PDA, CMA, CPA, V8A (Tab. 3.1) per l’identificazione. TABELLA 3.2. - Principali substrati selettivi per le specie di Phytophthora. CARBHy 17 g agar farina di mais (CMA) 10 mg pimaricina 250 mg ampicillina 10 mg rifampicina 15 mg benomyl 50 mg imexazolo 1 litro di acqua distillata N.B. Il terreno di coltura va conservato al buio in frigorifero e utilizzato possibilmente entro 7 giorni. P10VP 17 g agar farina di mais (CMA) 10 mg pimaricina 200 mg vancomicina 100 mg PNCB 50 mg imexazolo N.B. Il terreno di coltura va conservato al buio in frigorifero e utilizzato possibilmente entro 7 giorni. La pimaricina è fotolabile, risente delle alte temperature e perde buona parte della sua efficacia dopo 7 giorni. 3.3 ISOLAMENTO DI BATTERI FITOPATOGENI Due sono le tecniche più comunemente utilizzate: la macerazione e l’immersione in acqua o tamponi sterili. Macerazione Per isolare i batteri dai tessuti vegetali, piccole porzioni di tessuto (2-3 × 2-3 mm) al margine del sintomo vengono prelevate con bisturi sterile e macerate dentro mortai (Fig. 3.4) contenenti 1-3 ml di acqua distillata o tampone fosfato (Tab. 3.3) sterili. Il tessuto finemente triturato così ottenuto si lascia decantare per circa 20 minuti. Successivamente, vengono allestite tre diluizio- 30 Fig. 3.4 – Macerazione di tessuto vegetale per l’isolamento di batteri. Collezione di microrganismi di interesse agrario, industriale ed ambientale ni seriali decimali. Aliquote (100 µl) di tali sospensioni, compreso il ‘tal quale’, vengono distribuite uniformemente, mediante apposite anse ad ‘L’, in piastre contenenti il terreno di crescita (Tab. 3.4). Le piastre vengono poste in termostato a temperatura compresa tra 25°C e 28°C. Immersione in acqua o tamponi sterili Un’altra tecnica di isolamento è l’immersione di piccole porzione di tessuti, allo stadio iniziale del sintomo, in 1.5 ml di acqua distillata o tampone fosfato o soluzione fisiologica (Tab. 3.3) sterili. Dopo aver lasciato il tessuto per 30-45 minuti in immersione, aliquote (100 µl) della sospensione e delle diluizioni decimali vengono strisciate su piastre di substrati idonei (Tab. 3.4). TABELLA 3.3 – Tamponi utilizzati in fase di isolamento. Tampone fosfato pH 7,0 4,26 g Na2HPO4 2,72 g KH2PO4 1 litro di acqua distillata Soluzione fisiologica 0,85 g NaCl /1 litro di acqua distillata TABELLA 3.4 – Principali terreni agarizzati impiegati per l’isolamento o per la crescita dei batteri fitopatogeni. Nutrient agar (NA) 28 g di nutrient agar 1 litro di acqua distillata Nutrient agar + saccarosio al 5% (NSA) 28 g di nutrient agar 50 g saccarosio 1 litro di acqua distillata Mezzo B di King (KB) 10 g proteose peptone 1,5 g K2HPO4 1,5 g MgSO4 10 ml glicerina 15 g bacto-agar 1 litro di acqua distillata YDC 20 g glucosio 10 g estratto di lievito 20 g CaCO3 17 g bacto-agar 1 litro di acqua distillata 3.4 MANTENIMENTO IN VIVO DI VIRUS E VIROIDI A differenza di funghi e batteri, non è mai possibile ottenere una coltura pura di virus e viroidi vegetali, in quanto parassiti obbligati endocellulari. 31 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) È possibile tuttavia il mantenimento in vivo, ossia il trasferimento del virus o viroide dal campione vegetale ad indicatori erbacei o arborei; cioè a specie di piante anche spontanee, che possono essere agevolmente allevate in serra, a rapido accrescimento e che rispondono con una sintomatologia specifica e costante all’infezione di virus e viroidi diversi. La possibilità di utilizzare indicatori ha per fondamento l’assunto che una della proprietà comuni a tutti i virus e viroidi è quella di essere trasmissibili per succo o per innesto (patogeni generalizzati o sistemici). Una buona parte di essi può essere trasmessa meccanicamente sugli indicatori, ma per altri è necessario far ricorso a vettori o a innesto. Sono note serie più o meno standard di ospiti vegetali atti alla identificazione ed al mantenimento in vivo della maggior parte dei virus e viroidi. Spesso si tratta di specie erbacee spontanee o di essenze arbustive o legnose impiegate come portainnesti ma, in un saggio biologico, questa gamma di ospiti dovrebbe sempre includere la specie da cui l’entità infettiva è stata isolata in natura al fine di mantenere le stesse condizioni cellulari che assicurino il mantenimento delle caratteristiche biologiche e molecolari del virus o viroide da tenere in collezione. In genere la trasmissione meccanica o per succo comporta lo strofinamento con un dito o con una spatola, sulla superficie fogliare delle piante di saggio, previamente cosparsa di polvere abrasiva (celite o carborundum), del succo estratto da porzioni di tessuto infetto, triturato in un mortaio in presenza di opportune soluzioni tampone (Fig. 3.5) che si oppongono a variazioni di pH dell’estratto cellulare (in genere un tampone fosfato) o all’azione di enzimi (ribonucleasi, polifenolossidasi) presenti nel succo cellulare e in grado di inibire l’infettività dei virus. a) b) Fig. 3.5. – Macerazione di un campione vegetale e inoculazione meccanica del succo su pianta indicatrice. Per la trasmissione per innesto si utilizza preferenzialmente l’innesto a scaglia o “chip budding”. Questo tipo di innesto si applica in particolare alla piante arboree, in luogo di quello alla maiorchina. Lo scudetto, una gemma fornita di una porzione di legno, deve avere uno spessore nella parte inferiore, di circa 3 mm e 32 Collezione di microrganismi di interesse agrario, industriale ed ambientale una lunghezza di 2-3 cm. Il taglio nel portainnesto deve consentire l'incastro dello scudetto alla base (Fig. 3.6). Dopo una settimana dall’innesto la pianta viene cimata, e dopo 10 giorni va tagliata poco sopra la gemma innestata, per favorire il manifestarsi dei sintomi. Fig. 3.6 – Innesto di tipo “chip budding” sul portainnesto/indicatore GF 305 (pesco). Bisogna tenere conto di diversi fattori che possono influenzare la valutazione del risultato del saggio: • Controlli: è bene includere sempre da 3 a 5 indicatori della stessa specie vegetale da utilizzare come controllo negativo. • Presenza di inibitori: i succhi cellulari di alcune specie contengono potenti inibitori che impediscono il trasferimento dell’infezione per inoculazione per succo. Ad esempio, il succo di una specie da saggio comunemente usata (Chenopodium quinoa) contiene alcuni di questi inibitori. È bene, quindi, inoculare per ultimi gli individui di questa specie, onde evitare il trasferimento degli inibitori nell’estratto adoperato per l’inoculazione. Per lo stesso motivo, le piante vengono sciacquate con acqua dopo lo strofinamento con il succo infetto. • Tempi di risposta: sono più o meno noti e caratteristici per la specie o il gruppo virale (5-10 giorni per le lesioni locali, 14-20 giorni per l’infezione sistemica) (Fig. 3.7). Nel caso di marze e talee è frequente il ricorso alla forzatura, con temperatura ed umidità elevate, per accelerare la comparsa di sintomi. Fig. 3.7 – Risposte sintomatologiche (a sinistra) e sistemiche (a destra) su tabacchi utilizzati come piante indicatrici per trasmissione di virus e mantenimento in vivo. • Età e stadio vegetativo dell’indicatore. • Condizioni di allevamento: costituiscono uno dei punti più critici per l’esecuzione del saggio. Proprio per questo motivo le piante indicatrici vengono coltiva- 33 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) te in ambienti controllati, generalmente serre termo-condizionate o fitotroni, in cui la temperatura, l’illuminazione e l’umidità sono impostate per garantire la replicazione dei virus e dei viroidi (Fig. 3.8). Fig. 3.8 – Gli ambienti di serra per il mantenimento in vivo degli agenti virali e viroidali sono dotati di controllo termo-igrometrico e fotoperiodo. 3.5 PURIFICAZIONE DELLE COLTURE DI FUNGHI E OOMICETI La formazione di organi di moltiplicazione o riproduzione di molti funghi è favorita da un’incubazione a temperature di circa 22-25°C con luce alternata (es. fotoperiodo di 12 h di luce). Per eliminare eventuali contaminazioni da batteri si possono prelevare piccole porzioni di micelio da colonie provenienti da un primo isolamento da tessuto ospite o comunque da infezione naturale e trasferirle su terreno di coltura addizionato con antibiotici solitamente streptomicina o ampicillina (100 mg/l) oppure può essere preparato del PDA acidificato aggiungendo 10 ml/l di acido lattico al 25% da conservare al buio dal momento che l’acido lattico è fotolabile. L’identificazione e lo studio, sia di tipo tradizionale sia molecolare, di un microrganismo fungino o di un oomicete, normalmente viene effettuato su isolati portati in purezza, ossia su colonie provenienti da un solo propagulo (conidio, sporangio, ifa, spora, ecc.). Per avere colture monosporiche, dalle colonie ottenute da isolamento diretto, si prelevano frammenti di micelio e si trasferiscono su idoneo substrato di crescita che ne favorisca la sporificazione incubandoli in idonee condizioni di temperatura e luce. Quando il fungo è sufficientemente cresciuto una piccola porzione sporificante viene prelevata, trasferita in una provetta contenente acqua distillata sterile, agitata per diffondere e separare i propaguli nel mezzo liquido e versata su una piastra contenente agar-acqua (1,2%). La sospensione viene, quindi, distribuita in modo da coprire uniformemente l’intera piastra e lasciata 10-20 minuti a riposare. Successivamente, si elimina l’eccesso di acqua e si mette ad incubare per una notte a tempe- 34 Collezione di microrganismi di interesse agrario, industriale ed ambientale ratura ambiente (Fig. 3.9). Dalla piastra con le spore o i conidi germinati, operando al microscopio ottico, si taglia un quadrato o un triangolo di agar intorno al singolo propagulo germinato (la germinazione è indice di vitalità) che si preleva con una lancetta e si trasferisce in una piastra contenente substrato di crescita. Fig. 3.9 – Sequenza di operazioni per ottenere una sospensione conidica distribuita in piastra di agar-acqua, dalla quale si effettueranno i tagli per l’ottenimento di colonie monoconidiche. Esistono numerosi substrati di coltura per l’accrescimento dei funghi. Bisogna tenere presente che i funghi crescono meglio su substrati ricchi di carboidrati, ma per lunghe conservazioni, un terreno particolarmente ricco può ridurre la sporificazione nonché la vitalità stessa dell’isolato. Molti funghi crescono bene su PDA, che essendo un terreno particolarmente ricco, favorisce la crescita del micelio, ma non la sporificazione del fungo, inoltre è sconsigliato come substrato per la conservazione dei funghi, poiché può causare mutazioni nel fungo stesso. L’agar-carota come altri substrati poco ricchi, invece, è un terreno che favorisce la formazione di spore ed è generalmente consigliato per la conservazione. Similmente all’agar-carota può essere utilizzato l’agar farina di mais (CMA). Per alcune specie di Phytophthora si possono effettuare colture monosporangiche inducendo la produzione di sporangi su PCA o utilizzando altri mezzi che inducono la sporificazione (vedi paragrafo 3.8). Nel caso di organismi che non formano propaguli, è necessario effettuare una coltura monoifale. Si preleva una porzione del micelio dalle piastre d’isolamento, lo si mette su agar-acqua (1,2%) e si incuba al buio a 22-25°C. In questo caso bisogna ricorrere a substrati poveri, che permettono una crescita lassa dell’organismo (ife ben distanziate le une dalle altre) per favorire il prelievo. Quando sono chiaramente distinguibili le ife, si taglia una porzione di una singola ifa, che viene trasferita in piastra su un idoneo substrato di crescita. 3.6 PURIFICAZIONE E PREPARAZIONE DELLE COLTURE DI BATTERI L’isolamento su terreno di coltura determina l’accrescimento di colture miste di specie batteriche saprofite e specie fitopatogene (Fig. 3.10). Al fine di iden- 35 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) tificare le colonie batteriche fitopatogene è necessario ottenerle in coltura pura. Le singole colonie vengono trasferite con apposite anse dalla piastra di isolamento a una nuova piastra contenente il terreno di coltura (Fig. 3.11). Il terreno di crescita batterica può essere un substrato generico quale l’agar nutritivo (NA), oppure un substrato che metta in evidenza determinate caratteristiche della specie, come il terreno B di King, che permette di evidenziare la presenza di colonie fluorescenti, o l’NSA sul quale è possibile rilevare caratteristiche colonie a forma convessa (cosiddette levaniformi). Fig. 3.10 – Coltura mista di batteri su piastra dopo incubazione per 48 ore a 26-28 °C. Fig. 3.11 – Coltura pura di Pseudomonas syringae. 3.7 PURIFICAZIONE DI VIRUS E VIROIDI I virus e viroidi vegetali non sono organismi coltivabili, quindi è possibile ottenere solamente o una purificazione delle particelle virali (virioni), non applicabile ai viroidi in quanto privi di rivestimento proteico, o una purificazione degli acidi nucleici virali o viroidali, sia mediante estrazione della doppia elica di RNA (dsRNA), sia mediante estrazione dell’acido nucleico nella sua forma originaria (ssRNA, ssDNA, dsDNA). Purificazione dei virioni È possibile ottenere la purificazione delle particelle nucleo-proteiche virali integre e infettive mediante protocolli che prevedono l’utilizzo di solventi per la chiarificazione del materiale vegetale (100-200 g circa di foglie inoculate di pianta indicatrice) e cicli di centrifugazione differenziale e ultracentrifugazione isopicnica su gradienti (Fig. 3.12). Le caratteristiche bio-chimiche delle diverse specie virali richiedono l’utilizzo di tamponi di estrazione e cicli di centrifugazione specifici. 36 Collezione di microrganismi di interesse agrario, industriale ed ambientale Fig. 3.12 – Ultracentrifuga per cicli ad alta velocità necessari alla sedimentazione in “pellet” delle particelle virali e per la sedimentazione su gradienti. Estrazione della doppia elica di RNA (dsRNA) È il primo approccio molecolare alla diagnosi virologica. La tecnica consiste nell’isolare, da un estratto di acidi nucleici totali di un campione di tessuto, RNA bicatenari (dsRNA) prodotti dalla replicazione virale. Per isolare il dsRNA sono necessarie grandi quantità di tessuto polverizzato con azoto liquido. Nel caso di possibile infezione da virus, è necessario partire da 30 g di tessuto. Dopo il passaggio in un tampone di estrazione composto fondamentalmente da fenolo, l’acido nucleico proveniente dai tessuti della pianta viene messo in contatto con una soluzione a base di cellulosa che cattura gli acidi nucleici e non i residui cellulari. Lavaggi con etanolo consentono la successiva eluizione selettiva degli acidi nucleici. Per quanto riguarda i virus, l’isolamento del RNA avviene grazie ad una serie di digestioni enzimatiche, la prima con DNasi, la seconda con la proteinasi K, a cui segue una seconda pulizia con fenolo e una precipitazione alcolica dell’acido nucleico. Il risultato si visualizza grazie ad una corsa elettroforetica su gel di acrilamide. Per quanto riguarda i viroidi, il protocollo di estrazione dell’acido nucleico a singola elica (ssRNA) è più rapido e prevede l’utilizzo di soli 5 g di materiale verde. Per l’isolamento dell’RNA viroidale si sfrutta la circolarità dell’acido nucleico del viroide. Questa caratteristica, infatti, rende l’RNA del viroide unico a confronto con il contenuto di acidi nucleici del tessuto vegetale. L’RNA viroidale si isola con una doppia corsa elettroforetica su gel di acrilamide, la prima di tipo normale, la seconda con un gel denaturante in cui tutti gli RNA lineari vengono persi nella corsa e si trattengono solo quelli circolari. L’isolamento di dsRNA virali dalla pianta permette di stabilire la presenza di un’infezione virale ma non di identificare l’agente infettante responsabile. Al contrario, nel caso dei viroidi è possibile anche la caratterizzazione, sia sulla base del peso molecolare del viroide, sia con un saggio di tipo Northern blot (vedi ibridazione molecolare). 37 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) 3.8 IDENTIFICAZIONE E CARATTERIZZAZIONE DI FUNGHI ED OOMICETI L’identificazione di un fungo è innanzitutto effettuata osservando al microscopio ottico le caratteristiche morfologiche dell’isolato, il che permette una prima assegnazione a determinati gruppi tassonomici (es.: genere). La prima osservazione al microscopio comprende anche la tipologia di micelio, che per la maggior parte dei funghi è settato, con l’eccezione dei Zigomiceti (es. Mucor mucedo, Rhyzopus) il cui micelio è cenocitico (senza setti) e nastriforme. Anche gli Oomiceti (es. Phytophthora, Pythium) presentano un micelio cenocitico. Segue un’identificazione della specie, che può essere effettuata sia mediante osservazione al microscopio ottico (talora anche al microscopio elettronico), sia utilizzando altri metodi, ad esempio molecolari. È buona norma accompagnare le tecniche molecolari, ove possibile, ad una descrizione morfologica (es. morfologia della colonia, tipologia dei conidi e della conidiogenesi). Per quelle specie che producono solo micelio, l’attribuzione ad una determinata specie può avvenire con metodi molecolari in associazione ad informazioni morfo-colturali. Caratterizzazione morfologica Morfologia della colonia L’aspetto della colonia in piastra a volte può essere osservato su substrati specifici, che vengono indicati per quel particolare genere, es. PDA o Komada per Fusarium oppure substrati contenenti particolari sostanze. Alcuni caratteri morfologici, come ad esempio il micelio fioccoso, compatto, stellato, a rosetta, il margine della colonia intero o frastagliato, nonchè il colore delle colonie possono essere aspetti indicativi o caratteristici per l’identificazione della specie (Fig. 3.13). Fig. 3.13 – Colonie di Fusarium lateritium dal tipico colore aranciato ad accrescimento compatto. Parametri ambientali, quali temperatura e luce, sono fattori fondamentali per la crescita dei funghi e possono giocare un ruolo importante anche per la determinazione della specie. I funghi cosiddetti imperfetti o mitosporici sono così definiti perché si presentano nelle forme di moltiplicazione agamica. Essi però fanno quasi sempre parte di un ciclo che comprende la riproduzione (“for- 38 Collezione di microrganismi di interesse agrario, industriale ed ambientale ma perfetta”) e la formazione di organi come aschi (Ascomiceti), basidi (Basidiomiceti), oospore (Oomiceti). Le strutture moltiplicative comprendono le cellule conidiogene, i conidiofori, gli acervuli, i picnidi, gli sporodochi, i sinnemi o coremi, gli sclerozi, ecc. che possono essere osservate al microscopio ottico e utilizzate nell’identificazione. Delle spore o dei conidi vanno rilevate la morfologia e le dimensioni (Fig. 3.14). Per gli Oomiceti le strutture più importanti per l’identificazione, oltre alle caratteristiche delle colonie e del micelio sono quelle degli sporangi e rami sporangiofori implicati nella moltiplicazione e dei gametangi (anteridi e oogoni) implicati nella riproduzione (Fig. 3.15). Fig. 3.14 – Macroconidi di Fusarium (a sinistra) e conidio muriforme di Alternaria alternata (a destra). Fig. 3.15 – Sporangio papillato (a sinistra) e gametangi (a destra) di Phytophthora cactorum. Di seguito si descrivono alcune tecniche comunemente utilizzate per favorire la formazione di strutture moltiplicative di alcuni funghi e oomiceti. 39 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Induzione della formazione di sporodochi di Fusarium • CLA (carnation leaf agar) = Per ottenere agar-foglie di garofano, si pongono 1 o 2 frammenti di foglia di garofano (precedentemente sterilizzati) in piastre Petri e si versa lentamente l’agar acqua al 2% (Fisher et al., 1982). Si pongono porzioni di micelio in piastre di CLA (Fig. 3.16) in prossimità dei frammenti delle foglie di garofano. Le piastre vengono incubate a 25°C sotto luce nera o luce di Wood (ultravioletto vicino-nUV) ovvero a luce bianca alternata (12 h di luce) in termostato con un intervallo termico di 20-25°C a seconda della specie di Fusarium. Fig. 3.16 – Sporodochi di Fusarium prodotti su CLA. Induzione della sporificazione di Pyrenochaeta • Il micelio cresciuto su PDA acidificato viene trasferito su agar acqua e incubato per 3 giorni al buio, poi trasferito su 2xV8 agar (V8 con doppia concentrazione) e incubato con un fotoperiodo di 18 h o ad illuminazione continua a 21°C. Normalmente la formazione di strutture riproduttive avviene dopo 3-4 settimane (Shishkoff, 1992). Induzione della produzione di sporangi di Phytophthora • Soluzione di Petri. Si pongono dei piccoli tasselli di micelio (10 x 10 mm) nella soluzione di Petri (Tab. 3.5) e si incubano a 12-20°C alla luce bianca continua. Dopo 3-4 giorni, la soluzione viene sostituita con acqua distillata e gli sporangi si osservano nell’arco delle 24 h al binoculare o preparando vetrini da osservare al microscopio ottico. TABELLA 3.5. - Soluzione di Petri. Reagente Quantità Ca(NO3)2 0,4 g . MgSO4 7H2O 0,15 g KH2PO4 0,15 g KCl 0,06 g Acqua 1 litro 40 Collezione di microrganismi di interesse agrario, industriale ed ambientale • Semi di peperone. Si utilizzano semi di peperone sani e freschi, vengono lavati in acqua corrente per circa 1 ora, risciacquati in acqua distillata sterile e fatti asciugare su carta bibula sotto cappa. Successivamente si pongono circa venti semi su una colonia di Phytophthora di circa 5-6 gg e si incuba a temperatura ambiente e illuminazione naturale per 24 ore. I semi vengono, quindi, trasferiti su agar acqua e coperti con un velo di acqua di fosso. Dopo 48 ore si può osservare al binoculare la formazione di sporangi. • Filtrato di terreno non sterilizzato. Si pone un quadratino di micelio (1×1 cm) in una piastra Petri contenente un soluzione ottenuta da estratto di terreno o filtrato di terreno. Dopo circa 5-7 giorni di incubazione a temperatura ambiente e luce continua si possono osservare gli sporangi. Il filtrato di terreno viene preparato miscelando 200 g di terriccio e 500 ml di acqua deionizzata e lasciando in agitazione per 30-60 minuti. La sospensione viene, successivamente, filtrata con carta bibula. Caratterizzazione intraspecifica Alcuni organismi fitopatogeni possono presentare una specificità nei confronti di un determinato ospite o gruppo di specie ospiti affini. Questo carattere può non essere accompagnato da differenze morfologiche, vale a dire che la caratterizzazione morfologica permette la definizione di un organismo fino al rango di specie, mentre raggruppamenti subspecifici possono essere identificati ricorrendo a tecniche di differenziazione patogenetica. La caratterizzazione intraspecifica può includere la conoscenza dei gruppi di anastomosi (AG) per Rhizoctonia (Parmeter et al., 1969) oppure dei gruppi di compatibilità vegetativa (VCGs) per Fusarium (Puhalla, 1985) e Sclerotinia (Schafer et al., 2006). A tale scopo, gli isolati da caratterizzare sono appaiati in coltura duale con gli isolati cosiddetti “tester” dei vari gruppi di anastomosi o dei diversi VCGs. Dall’analisi micro e macroscopica di avvenuta plasmogamia, si può assegnare l’isolato ad un particolare gruppo intraspecifico. Le cosiddette “forme speciali” sono raggruppamenti sub-specifici che risultano morfologicamente indistinguibili, ma differiscono per la patogenicità verso una specie ospite o un gruppo di specie ospiti. Anche le “razze fisiologiche” sono in grado di infettare un gruppo o singole varietà od ibridi. Per la distinzione di forme speciali ovvero di razze all’interno di una forma speciale è necessario inoculare, su ospiti o serie di ospiti o varietà specifiche (dette “differenziali”), gli isolati fungini. In base alla reazione sintomatica sulle diverse entità genetiche, l’isolato viene associato ad una data forma speciale o ad una determinata razza. Caratterizzazione molecolare Numerosi protocolli molecolari sono utilizzati a scopo diagnostico per la determinazione di specie fungine. I metodi utilizzati si basano sull’impiego della PCR 41 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) (reazione a catena della polimerasi) e di marcatori molecolari, specifici se esistenti, o universali come gli ITS (internal transcribed spacer) del DNA ribosomale, nello specifico ITS6 e ITS4 per gli oomiceti, ITS5 e ITS4 per i funghi filamentosi, oppure geni di proteine che contengono sequenze altamente conservate come il fattore di elongazione (TEF1-alfa), la calmodulina, la beta-tubulina, poligalatturonasi, gli istoni (H3 e H4) (tab. 3.6). Il fattore di elongazione permette, in alcuni casi, di identificare fino a livello di forma speciale. Di recente introduzione per la diagnosi anche quantitativa (es. quantità di inoculo presente) di funghi ed oomiceti è la tecnica della “real-time PCR”, basata sull’utilizzo di oligonucleotidi marcati con opportuni fluorofori, la quale registra il livello di fluorescenza liberato durante l’amplificazione in relazione al numero di cicli della PCR. Il sistema TaqMan®, in particolare viene utilizzato come metodo di diagnosi anche verso organismi da quarantena ed è impiegato, ad esempio, per il rilevamento di Phytophthora ramorum (Hayden et al., 2006). TABELLA 3.6. Principali primer utilizzati attraverso l’analisi di sequenza nella identificazione di funghi e oomiceti. PRIMER SEQUENZA ITS 6 (White et al., 1990) 5’ GAAGGTGAAGTCGTAACAAGG 3’ ITS 5 (White et al., 1990) 5’ GGAAGTAAAAGTCGTAACAAGG 3’ ITS 4 (White et al., 1990) 5’ TCCTCCGCTTATTGATATGC 3’ Fattore di elongazione (TEF-1alfa) (O’Donnell et al., 1988) EF1= 5’ ATGGGTAAGGA(A/G)GACAAGAC 3’ EF2=5’ GGA(G/A)GTACCAGT(G/C)ATCATGTT 3’ Calmodulina (Carbone e Kohn, 1999) Cal F= 5’ GAGTTCAAGGAGGCCTTCTCCC3’ Cal R= 5’CATCTTTCTGGCCATCATGG 3’ Beta-tubulina (O’Donnell e Cigelnik, 1997) T1=5’ AACATGCGTGAGATTGTAAGT 3’ T2=5’ TAGTGACCCTTGGCCCAGTTG 3’ Istone 3 (H3) (Glass e Donaldson, 1995) H3-1a= 5’ ACTAAGCAGACCGCCCGCAGG 3’ H3-1b= 5’ GCGGGCGAGCTGGATGTCCTT 3’ Istone 4 (H4) (Glass e Donaldson, 1995) H4-1a= 5’ GCTATCCGCCGTCTCGCT 3’ H4-1b= 5’ GGTACGGCCCTGGCGCTT 3’ Poligalatturonasi (Marek et al., 2003) PEF=5’ATCGGCTGCGGATTGAAAG3' PER= 5'AGTCACGGGTTTGGAGGGA3' 3.9 IDENTIFICAZIONE E CARATTERIZZAZIONE DI BATTERI Caratterizzazione morfologica La morfologia di una colonia, ovvero l’attenta osservazione della forma, colore, elevazione, superficie, margine, consistenza, ed odore delle colonie, può sugge- 42 Collezione di microrganismi di interesse agrario, industriale ed ambientale rire, indicativamente, il genere a cui appartiene l’isolato. Inoltre, è necessario eseguire osservazioni al microscopio ottico in contrasto di fase delle cellule batteriche per accertare la loro forma e aggregazione, nonché per verificare se siano Gram-positive o Gram-negative. Caratterizzazione biochimica e nutrizionale Mediante l’esecuzione dei saggi biochimici è possibile verificare se un isolato batterico possiede determinati enzimi in grado di metabolizzare particolari composti organici. La presenza dei vari enzimi può essere rilevata in diversi modi, secondo la loro specifica attività. Per esempio, l’azione della levanosaccarasi su saccarosio provoca la polimerizzazione del fruttosio che viene escreto dalla cellula in grande quantità, determinando la formazione di colonie levaniformi, tipica di alcune Pseudomonadi e di Erwinia amylovora. La produzione di enzimi pectinolitici, da parte di specie di Pseudomonas o Pectobacterium agenti di marciume, viene messa in evidenza ponendo su fettine di patata la colonia batterica che ne provoca il rammollimento (attività pectinolitica su patata). L’attività di altri enzimi viene rilevata mediante l’aggiunta nel terreno di crescita del substrato dell’enzima e di un indicatore di pH (qualora la reazione catalizzata dall’enzima provochi una variazione di pH) che determina un cambiamento del colore del mezzo di coltura, che testimonia la presenza dell’enzima (es. arginina deidrolasi). Talvolta, in seguito alla reazione enzimatica, si formano dei prodotti che rendono scuro il mezzo di coltura (es. idrolisi dell’esculina, dell’arbutina, della tirosina) (Fig. 3.17). È possibile, inoltre, eseguire saggi nutrizionali per verificare se un batterio è capace di utilizzare un determinato composto organico (carboidrato, aminoacido, acido organico) come unica fonte di energia. Tali saggi vengono di solito eseguiti inoculando il batterio indagato in un substrato minimo contenente una sola fonte di carbonio o azoto, in presenza di un indicatore di pH. Se il batterio è in grado di utilizzare la fonte saggiata per la crescita, si avrà una variazione del pH e di conseguenza, un Fig. 3.17 – Saggio di idrolisi delcambiamento del colore del mezzo. Sono, l’arbutina per l’identificazione di Pseudoinoltre, disponibili dei sistemi che permettomonas syringae pv. syringae. no di verificare contemporaneamente la capacità di un isolato di utilizzare diversi composti organici. Il sistema API 150, formato da 150 microtubi seriali contenenti vari composti organici e un indicatore di pH, permette di saggiare la capacità di un ceppo batterico di usare come unica fonte di energia uno o più dei 49 carboidrati, 49 aminoacidi e 49 acidi organici diversi. Il Biolog è un sistema analogo con il quale è possibile saggiare l’assimilazione di 95 composti organici diversi mediante un lettore ottico collegato a un computer che registra i risultati ottenuti e li confronta con una banca dati relativa a batteri fitopatogeni noti. 43 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Caratterizzazione fisiologica Al fine di identificare una specie batterica può essere utile rilevare alcune caratteristiche fisiologiche, come la crescita a diverse temperature (es. 4°C o 37°C), la tolleranza a diverse concentrazioni di NaCl (es. 2,5 e 7%) o di sali di tetrazolio, la capacità di produrre tossine o la capacità, caratteristica tipica di Pseudomonas syringae pv. syringae, di produrre proteine che catalizzano la formazione di nuclei di ghiaccio. Caratterizzazione sierologica Le analisi sierologiche possono fornire ulteriori informazioni per l’identificazione delle specie batteriche, sono, inoltre, affidabili, rapide e abbastanza sensibili. Esse si basano sulla disponibilità di anticorpi specifici, ovvero proteine di difesa, dette immunoglobuline, prodotte dagli animali (mammiferi) quando vengono introdotte nel loro corpo sostanze, chiamate antigeni, quali possono essere le cellule batteriche o parti di esse. La reazione antigene-anticorpo può avvenire anche all’esterno del corpo dell’animale, ovvero in vitro, e può essere resa visibile in vari modi a secondo della tecnica impiegata. Una tecnica sierologica maggiormente utilizzata nella diagnosi batterica è l’immunofluorescenza: gli anticorpi vengono coniugati con un composto chimico, di solito isotiocianato di fluorescina, che emette fluorescenza sotto la luce ultravioletta. L’anticorpo coniugato, quindi, riconosce e si lega all’antigene specifico, rappresentato in questo caso da una porzione superficiale della parete della cellule batterica. I preparati, sia l’estratto vegetale infetto, sia la sospensione batterica, vanno posti su idonei vetrini, e dopo la colorazione di immunofluorescenza, sono osservati al microscopio ottico fornito di lampada epifluorescente a vapori di mercurio. Qualora la reazione risulti positiva, i batteri in esame risulteranno fluorescenti al microscopio. Un’altra tecnica sierologica impiegata è l’ELISA (Enzyme-Linked Immunosorbent Assay). Tale metodo viene eseguito in apposite piastre di polistirene contenenti 96 pozzetti, nei quali, al preparato in esame, viene aggiunto l’anticorpo specifico coniugato con un enzima (fosfatasi alcalina), in presenza del suo substrato (p-nitrofenil-fosfato). In seguito alla reazione antigene-anticorpo e alla conseguente reazione enzimatica, i campioni positivi, che rimangono legati ai pozzetti, assumono una caratteristica colorazione gialla. Caratterizzazione molecolare Allo scopo di identificare e caratterizzare le specie batteriche fitopatogene, sono di grande utilità le tecniche molecolari, in quanto specifiche, sensibili e affidabili, le quali danno risultati in tempi più brevi rispetto ai saggi tradizionali. La maggior parte dei protocolli molecolari si avvalgono dell’amplificazione, mediante PCR (reazione a catena della polimerasi), di sequenze specifiche del genoma batterico. Il prodotto di questa amplificazione può essere un unico “amplicone” di una determinata dimensione, che individua una determinata specie batterica. 44 Collezione di microrganismi di interesse agrario, industriale ed ambientale Diversi protocolli diagnostici, utilizzati in fitobatteriologia, si basano sull’amplificazione di specifici geni coinvolti nell’espressione della risposta di ipersensibilità o di patogenicità, appartenenti al cluster genico hrp (hypersensitive response and pathogenicity). Ad esempio, i geni hrpW e hrpL sono stati utilizzati come bersaglio per il rilevamento, rispettivamente, di Pseudomonas avellanae (Loreti e Gallelli, 2002) e di Pseudomonas syringae pv. papulans (Kerkoud et al., 2002). Alternativamente, possono essere utilizzati come bersagli “target” per l’identificazione geni codificanti per prodotti di virulenza. Ceppi di Pseudomonas syringae pv. syringae possono essere identificati per la presenza di un frammento del gene syrB coinvolto nella produzione di tossine (Sorensen et al., 1998); l’amplificazione specifica del gene pel, codificante l’enzima pectato liasi, permette di identificare alcune sottospecie appartenenti al genere Pectobacterium (Darrasse et al., 1994). Altri “primer”, disegnati sulle sequenze dei geni ribosomiali (16S, 23S, 5S), sono utilizzati sia a scopo diagnostico, sia in studi di tassonomia batterica. Inoltre, sono disponibili dei primer universali che, amplificando delle sequenze geniche ripetute e conservate, generano dei profili elettroforetici, formati da frammenti di DNA di diverso peso molecolare. Le sequenze caratteristiche presenti nei batteri fitopatogeni appartengono a tre famiglie: REP (Repetitive Extragenic Palindromic), ERIC (Enterobacterial Repetetive Intergenic) e l’elemento BOX (tab. 3.7). Il confronto dei profili elettroforetici di diversi ceppi batterici, eventualmente elaborati mediante analisi statistiche, può fornire informazioni sia per l’identificazione della specie, sia per stabilire relazioni tassonomiche tra i vari ceppi. Di recente introduzione per la diagnosi di fitobatteri la “real-time PCR”, basata sull’utilizzo di oligonucleotidi marcati con opportuni fluorofori, registra il livello di fluorescenza liberato durante l’amplificazione proporzionalmente al numero di cicli della PCR. Il sistema TaqMan®, in particolare, è stato utilizzato per il rilevamento di Clavibacter michiganensis subsp. sepedonicus e Ralstonia solanacearum in tuberi di patata (Shaad et al., 1999; Ozakman et al., 2003). TABELLA 3.7 – Primer universali per l’ottenimento di profili molecolari utili per l’identificazione di batteri. Primer Sequenza REP 5’ IIIICGICGICATCIGGC 3’ 5’ ICGICTTACIGGCCTAC 3’ (Higgins et al., 1982; Versalovic et al., 1991) ERIC 5’ ATGTAAGCTCCTGGGGATTCAC 3’ 5’ AAGTAAGTGACTGGGTGAGCG 3’ (Hulton et al., 1991) BOX 5’ CTACGGCAAGGCGACGCTGACG 3’ ( Versalovic et al., 1994) 45 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) 3.10 IDENTIFICAZIONE E CARATTERIZZAZIONE DI VIRUS E VIROIDI La caratterizzazione di un virus o di un viroide può avvenire grazie all’uso di diverse tecniche. Per quanto riguarda i virus si possono usare sia i saggi sierologici, sia quelli molecolari, mentre per i viroidi possono essere utilizzati solo saggi molecolari. La caratterizzazione ceppo-specifica dei virus può essere perseguita sierologicamente utilizzando un anticorpo monoclonale in grado di legarsi ad epitopi caratteristici del capside di un solo ceppo virale. Se si intende, invece, utilizzare l’amplificazione genica per identificare e caratterizzare un virus, si può procedere con un attento disegno di primer specifici che consentano di distinguere la specie all’interno di un genere tassonomico o di un ceppo nell’ambito della stessa specie virale. Spesso, però, le differenze nucleotidiche nei genomi di due ceppi sono troppo esigue per essere in grado di discriminare l’appartenenza con il solo uso di primer specifici. Si può ricorrere, allora, al sequenziamento di una porzione di genoma, oppure si può ricorrere a tagli con enzimi di restrizione sui prodotti di amplificazione che, a seconda della sequenza nucleotidica, danno un “motivo” di segmenti diversi consentendo, quindi, tramite il confronto di essi, di risalire al ceppo di origine della sequenza (polimorfismo da lunghezza dei frammenti di restrizione, RFLP). Molto importante nella caratterizzazione del virus è la scelta della porzione del genoma da analizzare. Le differenze maggiori all’interno dei ceppi si trovano in genere sui geni che codificano per la proteina capsidica, mentre, se si tenta di fare una discriminazione per famiglie, può essere più utile lavorare su geni più conservati come l’RNA polimerasi RNA dipendente. Per quanto riguarda i viroidi, la caratterizzazione avviene quasi esclusivamente mediante sequenziamento di tutta la sequenza nucleotidica del genoma, che, essendo molto piccola, rende molto efficace lo studio dei diversi polimorfismi. Saggio sierologico Base della diagnosi sierologica è la capacità degli anticorpi prodotti dal sistema immunitario di organismi animali di reagire in vitro ed in maniera specifica con quegli stessi antigeni che ne hanno stimolato la formazione. Da molti anni l’ELISA (Enzyme Linked Immune Sorbent Assay) è il metodo immunoenzimatico più comunemente usato per la diagnosi delle malattie virali delle piante. L’ELISA è un saggio su fase solida in cui un anticorpo specifico agisce in successione, prima intrappolando e poi rilevando la presenza dell’antigene bersaglio (particella virale) mediante l’impiego di un enzima (ad es. fosfatasi alcalina) capace di produrre il viraggio di colore di un opportuno substrato. Per l’individuazione e la caratterizzazione di isolati virali è possibile utilizzare sia l’ELISA diretta, sia quella indiretta. 46 Collezione di microrganismi di interesse agrario, industriale ed ambientale Le fasi schematiche di un protocollo di ELISA diretta (DAS-ELISA) possono essere riassunte come segue (Clark e Adams, 1997): • • • • • • • • • • • Sensibilizzazione della piastra con le IgG specifiche (100-200ml) Incubazione a 37°C per 2-3 ore Lavaggio con tampone specifico Caricamento del campione estratto in tampone (100-200ml) Incubazione a 4°C O/N Lavaggio con tampone specifico Caricamento delle IgG coniugate con un enzima (100-200ml) Incubazione a 37°C per 2-3 ore Lavaggio con tampone specifico Viene caricato il substrato dell’enzima Si osserva il viraggio del colore del substrato tramite lettore (Fig. 3.18). Fig. 3.18 – Reazione colorimetrica in piastra ELISA, la cui assorbanza si misura con appositi lettori. Per l’ELISA indiretta (TAS-ELISA) lo schema è fondamentalmente analogo, ma il primo reattivo (anticorpo intrappolante) è un anticorpo prodotto in un animale (es. capra/topo/pollo), cui viene fatta seguire l’azione di un anticorpo specifico per lo stesso antigene (virus) ma prodotto in un animale diverso (es. coniglio) la cui presenza viene rilevata mediante un terzo tipo di anticorpo coniugato con l’enzima, specifico per il secondo (in questo caso anti-coniglio) e definito “coniugato universale”. Il metodo TAS-ELISA (Lommel et al.,1982) presenta due vantaggi: • risolve il problema della minor reattività degli anticorpi coniugati rispetto a quelli nativi verso uno stesso antigene, • usando un “coniugato universale” supera la necessità di preparare tanti coniugati per quanti sono i sieri che si prevede di impiegare. Per entrambi i metodi l’intensità del colore che si ottiene dopo il viraggio dipende dalla concentrazione dell’antigene. L’ELISA è un metodo di diagnosi indicato 47 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) per saggiare un elevato numero di campioni, ma presenta una sensibilità da 100 a 10.000 volte inferiore al saggio molecolare. Saggi molecolari Come per i funghi e i batteri, anche per virus e viroidi sono stati messi a punto numerosi protocolli molecolari (Makkouk e Kumari, 2006) ai fini diagnostici e di caratterizzazione per i virus e viroidi vegetali; in particolare sono stati sviluppati sia protocolli di ibridazione molecolare sia di amplificazione genica. Entrambi questi protocolli necessitano della conoscenza, anche parziale, della sequenza nucleotidica del genoma del patogeno che si intende identificare, in quanto il disegno dei primer per l’amplificazione genica e delle sonde per l’ibridazione molecolare sono subordinati alla presenza di sequenze nucleotidiche complete o parziali in banca dati. Ibridazione molecolare L’ibridazione molecolare si basa sull’interazione tra le basi azotate che compongono gli acidi nucleici, che consente il riconoscimento specifico di un determinato bersaglio (“target”) molecolare grazie all’utilizzo di una sonda (“probe”) opportunamente prodotta. Esistono diverse possibilità nella realizzazione di un protocollo di ibridazione molecolare: • Il modo in cui la molecola bersaglio è immobilizzata su un supporto solido • Il tipo di molecola scelta come sonda (cDNA o cRNA) • Il tipo di marcatura scelta (chimica o radioattiva). La preparazione del campione target può essere effettuata in molti modi, in genere l’acido nucleico target viene immobilizzato su un supporto tipo nitrocellulosa o membrana di nylon (Meinkoth e Wahl, 1984). Si può utilizzare direttamente il succo di un campione vegetale, imprimendo una parte del tessuto sul supporto solido oppure possono essere applicati sulla membrana direttamente gli estratti di acidi nucleici ottenuti dal trattamento dei tessuti vegetali. Una volta preparato e opportunamente attivato, il supporto solido viene messo in contatto con la sonda, in genere diluita in una soluzione detta di ibridazione. L’evidenziazione dell’avvenuta ibridazione si ottiene mediante esposizione di una lastra radiografica su cui compaiono delle macchie scure in corrispondenza dei campioni infetti (Fig. 3.19). Nel caso dei virus la scelta della sequenza da usare come sonda si basa sul tipo di utilizzazione della tecnica; sequenze molto conservate all’interno dei genomi virali possono essere utili nella produzione di sonde genere- o famiglia-specifiche; zone del genoma più variabili possono essere utilizzate in una sorta di caratterizzazione ceppo-specifica. 48 Collezione di microrganismi di interesse agrario, industriale ed ambientale Fig. 3.19 – Fasi operative per l’ibridazione con impronta di tessuto e risultato finale. Nel caso dei viroidi generalmente viene usata tutta la sequenza genomica completa come sonda. La sonda può essere prodotta come RNA o DNA marcato a singolo filamento complementare al target o DNA marcato a doppio filamento; in questo caso è opportuno denaturare la sonda prima di utilizzarla. Ad oggi il sistema più utilizzato è la marcatura con UTP-digossigenato. Questo metodo è allo stesso tempo sicuro (non sono presenti composti radioattivi) e molto sensibile. Amplificazione genica Prima di poter effettuare l’amplificazione genica è necessario estrarre l’acido nucleico totale (mediante kit commerciali) dal campione vegetale costituito da foglie, nervature, tessuto sottocorticale, frutto, ecc., a seconda del patogeno. L’RNA viroidale viene generalmente ottenuto mediante estrazione di tipo fenolico o su matrice silicea di acidi nucleici. Ormai da anni la tecnica della PCR (reazione a catena della polimerasi) (Seal e Coates, 1998) è diventata di uso comune con diverse metodologie e varianti che si basano tutte sulla replicazione esponenziale (amplificazione) di un segmento specifico di DNA in presenza di polimerasi stabili (Taq) ed inneschi di reazione sintetizzati specificatamente sul RNA/DNA bersaglio del virus o viroide che si vuole identificare. Tutti i viroidi e la maggior parte dei virus vegetali hanno un genoma formato da RNA. In questo caso è prima necessario procedere alla sintesi di un fila- 49 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) mento di DNA complementare (cDNA) mediante una retro-trascrizione, per mezzo di un enzima di retro-trascrittasi (AMV o MMLV), utilizzando come innesco un primer specifico complementare alla sequenza target o primer randomizzati. Successivamente si può procedere all’amplificazione genica vera e propria, mediante oligo specifici (sia complementari sia omologhi) a seconda del virus o viroide. Il risultato di un’amplificazione in PCR può essere visualizzato mediante elettroforesi in gel di agarosio ad una concentrazione del 1-1,5% (Fig. 3.20). Fig. 3.20 – I prodotti di amplificazione genica si visualizzano in elettroforesi. 3.11 CONSERVAZIONE DI FUNGHI E OOMICETI Esistono diversi metodi di conservazione dei funghi e degli oomiceti. La scelta è suggerita dalle caratteristiche delle singole specie. È consigliabile, comunque, conservare ogni isolato utilizzando almeno due metodi (Fig. 3.21). Fig. 3.21 – Differenti metodi di conservazione di funghi. Solo i funghi saprotrofi e necrotrofi possono essere conservati in collezione, in quanto quelli biotrofi possono vivere unicamente sui tessuti delle piante ospiti in quanto parassiti obbligati. 50 Collezione di microrganismi di interesse agrario, industriale ed ambientale Solitamente, vengono sottoposte a conservazione colture monoconidiche/monosporiche oppure colture monoifali nel caso di funghi che non sporificano in piastra. Qui di seguito vengono illustrati alcuni metodi comunemente utilizzati per la conservazione di tali organismi. Tubi con terreno agarizzato solidificato (a becco di flauto) Una piccola porzione di una coltura fungina viene prelevata con un’ansa o ago sterile e trasferita in tubo contenente un substrato di crescita agarizzato. Esistono diversi substrati che possono adattarsi alle esigenze delle specie fungine. Tra i più utilizzati vi è l’agar-farina di mais (CMA), l’agar-carota e l’estratto di carote e patate. Una volta trasferiti in tubo, gli isolati vengono incubati al buio ad una temperatura solitamente compresa tra i 20 e 25°C. Raggiunto lo sviluppo di circa 2 cm di raggio, gli isolati fungini vengono trasferiti in frigorifero per la conservazione a 5-8°C. Rivitalizzazione: si preleva una piccola porzione di micelio della coltura cresciuta in tubo, e si trasferisce in piastra con terreno di coltura. Il metodo della conservazione in tubo non è indicato per il mantenimento a lungo termine. Vantaggi: è un metodo economico e non richiede una strumentazione particolare, inoltre la rivitalizzazione è facile. Svantaggi: può indurre variabilità genetica, perdita di patogenicità o di caratteristiche biochimiche, fisiologiche e morfologiche. Si possono facilmente avere contaminazioni anche da acari. Olio minerale L’olio minerale viene sterilizzato a 121°C per 15 min con due passaggi successivi a distanza di 24 ore. Le colture cresciute in tubo a becco di flauto contenente substrato agarizzato vengono coperte con uno strato di olio minerale sterilizzato e conservate a 5-8°C, assicurandosi che tutto il micelio sia coperto dallo strato di olio minerale per 1 cm oltre il margine del substrato stesso. Rivitalizzazione: si preleva una piccola porzione di micelio della coltura cresciuta in tubo e la si poggia su un supporto sterile (es: una piastra Petri) cercando di eliminare quanto più possibile l’olio minerale, quindi si trasferisce su piastra con terreno di crescita. Generalmente è necessario effettuare un secondo trasferimento. Vantaggi: l’olio minerale assicura una più lunga conservazione delle colonie, diminuendo il disseccamento dell’agar e una protezione da eventuali contaminazioni da 51 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) acari. È un metodo economico e non richiede particolari attrezzature, inoltre assicura una lunga vitalità a molte specie di funghi ed oomiceti, sebbene sia più laborioso del precedente metodo e possa presentare contaminazioni da specie di Penicillium ed altri funghi ubiquitari. Acqua Porzioni di micelio fungino (circa 5 x 5 mm) vengono messe in provette contenenti acqua distillata sterile e conservate a temperatura ambiente o a 5-8°C per i funghi e a 10°C per gli oomiceti. Il metodo è particolarmente indicato per questi ultimi. Rivitalizzazione: si prelevano uno o più tasselli che possono essere anche suddivisi che vengono posati su terreno di coltura. Vantaggi: il metodo assicura una buona vitalità, è indicato soprattutto per organismi filamentosi che non sono in grado di sopravvivere con altri metodi di conservazione (es. Pythium e Phytophthora). È un metodo economico, non richiede particolari attrezzature e preserva da contaminazioni da acari. Silica-gel È un metodo indicato per funghi che sporificano in coltura. Le provette in vetro vengono riempite con granuli di silica-gel e sterilizzate a secco per 3 ore a 180°C. Si pipettano 2 ml di una sospensione al 10% di latte scremato (sterilizzato per 10 min a 115-120°C) nella piastra in cui è cresciuto il fungo; quindi si aggiungono 2 ml di acqua distillata sterile. Dopo accurato mescolamento, si pipetta pochissimo liquido contenente i propaguli fungini nella provetta, ovvero Eppendorf da 1,5 ml, con il silica-gel. I funghi in silica-gel vanno conservati a 5°C. Rivitalizzazione: alcuni cristalli di silica-gel vengono messi in piastre Petri contenenti PDA o altro substrato. Si aggiungono 0,5-1ml di acqua distillata sterile per lavare i cristalli e si incuba a 20-25°C per 24-48 ore. Vantaggi: è un metodo economico, semplice e non richiede particolari attrezzature. Le colture si mantengono stabili per molti anni. Svantaggi: non è applicabile agli oomiceti, o a funghi che presentano spore con una struttura complessa, c’è inoltre la possibilità di introdurre contaminanti. 52 Collezione di microrganismi di interesse agrario, industriale ed ambientale Liofilizzazione Viene preparata una sospensione contenente il 10% di latte scremato in polvere e il 5% di inositolo, sterilizzata a 115°C per 10 min. I tubi per la liofilizzazione vengono sterilizzati a 180°C per 3 ore. Si pipettano 2 ml di sospensione di latte-inositolo nella piastra in cui è cresciuto il fungo, si spande bene la soluzione e si pipetta nei tubi da liofilizzazione. I tubi vanno tenuti preventivamente per 24 ore a -80°C, successivamente si procede con la liofilizzazione vera e propria. Dopo tale procedimento, i campioni vengono conservati a 5°C. Rivitalizzazione: si apre il tubo contenente il fungo liofilizzato e si aggiunge 1 ml di acqua distillata sterile, si attende 20-30 min quindi si inocula su PDA o altro substrato e si incuba a 20-25°C. Vantaggi: il metodo protegge da contaminanti ed assicura una lunga vitalità delle colture. Svantaggi: alcuni isolati fungini non sopravvivono al processo di liofilizzazione o possono verificarsi danni genetici. Il processo di liofilizzazione è inoltre un processo complesso e richiede elevati costi per le attrezzature, nonché personale esperto. Azoto liquido Nella piastra contenente il fungo si versa una aliquota di glicerolo al 10% (sterilizzato a 121°C per 10 min) o di dimetilsolfossido (DMSO) al 10% (non sterilizzato). Si spande la soluzione e si gratta delicatamente la superficie della coltura. Con una pipetta si preleva la mistura e la si mette nelle provette per azoto liquido. Le provette vanno tenute per 20-30 min a -80°C e successivamente immerse in azoto liquido in appositi contenitori. Rivitalizzazione: si prende la provetta dall’azoto liquido, si lascia per alcuni minuti a 37°C, quindi si versa il contenuto in piastra con PDA o altro substrato e si incuba a 20-25°C. Vantaggi: le colture sono mantenute in condizioni controllate, per lunghi periodi e sono esenti da possibili contaminazioni esterne. La maggior parte dei funghi sopravvivono bene a questo tipo di conservazione. Svantaggi: è un metodo dispendioso, per le necessarie attrezzature e per personale addestrato. Inoltre è richiesto un continuo rifornimento di azoto liquido per rimboccare il contenitore dell’azoto. 53 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Essiccazione su carta da filtro Un disco di carta da filtro (n. 1 Qualitative, Whatman, UK), sterilizzato in stufa a 180°C per 3 ore, del diametro di 70 mm è posto al centro di una piastra Petri di 90 mm di diametro contenente PDA o altro substrato. Dal margine di una coltura in attiva crescita (circa 7 giorni) vengono tagliati dei quadratini di 9 mm2 e posti al bordo della carta da filtro (circa 4 colonie per piastra), il tutto viene poi incubato a 20-25°C al buio. Quando il filtro è completamente coperto dal micelio del fungo, si pone ad essiccare. Questo avviene prelevando delicatamente il filtro che viene messo all’interno di una piastra Petri sterile di 90 mm di diametro vuota la quale, successivamente, viene posta in un essiccatore a campana collegato ad una pompa da vuoto. L’essiccatore contiene silica-gel preventivamente sterilizzato in stufa per 3 ore a 180°C. Quando le colonie fungine sul filtro appaiono completamente essiccate (2448 ore), il filtro viene rimossa dalla piastra operando in condizioni di sterilità (sotto cappa) e, molto velocemente, viene tagliato in piccole strisce, a loro volta ritagliate in quadratini (circa 3 x 3 mm) che vengono stoccati in contenitori di vetro sterili della capacità di 10 ml. I contenitori, ben chiusi, sono posti immediatamente in freezer a -20°C. Rivitalizzazione: quadratini dell’isolato fungino vengono prelevati e messi su piastre con PDA o altro substrato; le piastre vengono incubate a 20-25°C al buio. Vantaggi: è un metodo che permette di conservare molti isolati in poco spazio. È relativamente economico. Svantaggi: il processo di essiccazione va seguito costantemente per individuare il momento giusto per fermare il processo, poiché una eccessiva essiccazione provoca la morte del fungo. 3.12 CONSERVAZIONE DI BATTERI Esistono diversi metodi per mantenere in purezza i ceppi batterici, che differiscono tra di loro per la durata del periodo di conservazione. Quest’ultimo, tuttavia, non dipende solo dal metodo utilizzato, ma anche dalle caratteristiche della specie. Quando si procede alla conservazione di un ceppo è opportuno ottenere la coltura batterica da conservare da una singola colonia pura, ciò al fine di assicurare il mantenimento di una coltura geneticamente uniforme. 54 Collezione di microrganismi di interesse agrario, industriale ed ambientale Terreno nutritivo Quando occorre conservare degli isolati batterici per un periodo di tempo di 2-4 settimane, le colonie possono essere strisciate in piastre o, alternativamente, in tubi contenenti agar nutritivo (NA) con l’aggiunta dello 0,1 % di glucosio e fatte crescere in termostato per 24/48 ore a 25°-28°C. Gli isolati vengono poi conservati a circa 5°C. Rivitalizzazione: si preleva con l’apposita ansa una colonia batterica mantenuta in piastra o tubo e si striscia su un substrato di crescita. Vantaggi: è un metodo economico che non richiede una strumentazione particolare. Svantaggi: vi può essere pericolo di variabilità genetica, perdita di patogenicità o di caratteristiche biochimiche, fisiologiche e morfologiche. Vi può essere un rischio di inquinamento. Acqua Si prepara una sospensione batterica alla concentrazione di 1 x 108 u.f.c./ml (unità formanti colonie/ml), da colture cresciute per 24/48 ore su agar nutritivo, si versa in un tubo contenente acqua distillata sterile e si conserva a 5°-10°C. Il tempo di conservazione è molto variabile e dipende dalle caratteristiche della specie. Rivitalizzazione: si agita bene il tubo, si prelevano 100 µl della sospensione batterica e si distribuiscono uniformemente su un substrato di crescita. Vantaggi: è un metodo economico che non richiede una strumentazione particolare. Svantaggi: il metodo presenta il rischio di contaminazione dei tubi; è consigliabile solo per conservazione di breve durata. Conservazione a -80°C Le colonie batteriche cresciute su NA per 24-48 h vengono sospese in 10-20 ml di brodo nutritivo (NB) e fatte crescere con agitazione (200 rpm) per 24-48 h alla temperatura ottimale per la specie da conservare. Si aggiunge poi un volume di glicerolo fino a raggiungere la concentrazione del 15-20 %. Si suddivide la sospensione batterica così ottenuta in aliquote da 1 ml in tubi sterili. Per favorire un graduale congelamento, si pongono i tubi a -20°C per trenta minuti e poi si trasferiscono a 80°C. Questo tipo di conservazione permette di mantenere gli isolati batterici per tempi più lunghi (1-2 anni). 55 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Rivitalizzazione: si prelevano i tubi dal congelatore, si preleva dalla superficie un po’ di sospensione batterica congelata e si sospende in brodo nutritivo o si distribuisce su terreno di coltura. Per non compromettere la vitalità della restante coltura, occorre evitare di farla scongelare durante il prelievo. Vantaggi: permette di mantenere i batteri per tempi relativamente lunghi. Svantaggi: occorre un’adeguata strumentazione (congelatore a -80°C, gruppo elettrogeno). Essiccazione su carta da filtro Preparare tubi sterili contenenti 0,5 ml di soluzione acquosa di peptone al 5% più gelatina al 3%, e 0,5 ml di soluzione di glucosio all’8%. In tali tubi risospendere le colonie batteriche cresciute per 48 ore su terreno di coltura. Versare con pipette sterili la sospensione su strisce (5 mm x 30 mm) di carta Whatman n °1, fino a completa imbibizione. Porre le strisce di carta imbibite su un supporto metallico o di vetro e appoggiare tale supporto su un foglio di carta da filtro disposto sopra uno strato di silica gel essiccato dentro capsule Petri di vetro. Deporre le capsule in un essiccatore per 3-5 giorni. Dopo l’essiccazione conservare le strisce avvolte in fogli di alluminio riposti in contenitori di vetro con silica gel come indicatore di umidità. Tutto il materiale utilizzato deve essere sterile. Rivitalizzazione: le strisce di carta vengono poste su piastre contenenti l’opportuno terreno di crescita. Vantaggi: è un metodo che permette di conservare molti isolati in poco spazio. Svantaggi: il processo di essiccazione è lungo. Liofilizzazione Questo metodo permette di conservare i batteri per lunghi periodi, oltre 10 anni, fino anche a 50 anni a seconda della specie batterica, senza alterare le loro caratteristiche. Dopo 24-48 ore di crescita su NA una singola colonia della coltura batterica pura viene prelevata, risospesa in una soluzione acquosa di saccarosio (7%) e peptone (7%) e incubata per 25-48 ore alla temperatura ottimale. La sospensione batterica viene suddivisa in aliquote da 2 ml in flaconcini da penicillina (da 10 ml) sterili o, alternativamente, possono essere utilizzate fiale monouso. Le colture vengono, quindi, mantenute per 24 ore a -80°C. Successivamente, si procede con l’essiccazione, sotto vuoto, nel liofilizzatore. I batteri liofilizzati sono conservati a 5°C (Fig. 3.22). 56 Collezione di microrganismi di interesse agrario, industriale ed ambientale Fig. 3.22 – Colture liofilizzate di batteri per il mantenimento a lungo termine. Rivitalizzazione: i batteri liofilizzati assumono un aspetto polverulento. Per renderli vitali si aggiunge un’aliquota di brodo nutritivo o acqua distillata sterile e, una volta disciolta completamente la polvere, si trasferiscono 100 µl della sospensione in una piastra contenente l’opportuno terreno di crescita, distribuendo uniformemente il liquido su tutta la piastra con l’apposita ansa. Vantaggi: è un metodo sicuro per mantenere a lungo gli isolati proteggendoli dai contaminanti. Svantaggi: occorre un’adeguata apparecchiatura (congelatore a -80°C, liofilizzatore). 3.13 CONSERVAZIONE DI VIRUS E VIROIDI A differenza di funghi e batteri, non è mai possibile ottenere una coltura pura di virus e viroidi vegetali da conservare in collezione. È possibile tuttavia il mantenimento in vivo, ossia il trasferimento del virus o viroide dal campione vegetale ad indicatori erbacei o arborei, che possono essere agevolmente allevati in serra. Questo sistema di conservazione in vivo è estremamente oneroso, richiede esperienza e disponibilità di strutture di mantenimento specifiche. Generalmente si preferisce, quando le proprietà fisico-chimiche del virus lo consentono, conservare gli isolati virali direttamente nelle matrici vegetali trovate infette (foglie, frutti, bacche, tessuto sottocorticale) oppure macerate in azoto liquido. I campioni opportunamente etichettati possono essere conservati tal quali a -20°C ovvero, per periodi molto più lunghi, a -80° C. In caso di necessità, è possibile macerare il campione congelato, sospeso in un opportuno tampone di macerazione, e inoculare il succo ottenuto su piante ospiti erbacee per consentire la replicazione ed il rinnovamento delle particelle virali. Nel caso di virus che temono la conservazione a freddo o che sono particolarmente instabili è possibile procedere ad una loro purificazione partendo da tessuto infetto. I virioni purificati vengono conservati in apposite provette a -20°C in presenza di glicerolo al 30-50%. Gli isolati viroidali sono, invece, conservati sotto forma di RNA sospeso in etanolo. Un’altra tecnica di conservazione di agenti virali o viroidali è la disidratazione o la liofilizzazione di tessuti infetti. Per il primo sistema di conservazione, le ma- 57 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) trici vegetali infette vengono sminuzzate e poste su carta da filtro all’interno di una capsula Petri contenete granuli di calcio cloruro. Le capsule vengono chiuse ermeticamente e conservate a 4°C. Dopo alcuni mesi i tessuti disidratati, vengono trasferiti in idonei contenitori chiusi e conservati a basse temperature (4°C). La liofilizzazione (“freeze-drying”), la tecnica maggiormente diffusa, prevede un primo passaggio di congelamento dei tessuti (-20°C) o dell’estratto di succo grezzo e, successivamente, la disidratazione spinta sotto vuoto (48-36 ore) nel liofilizzatore. Per la scelta del metodo di conservazione si deve tenere conto delle caratteristiche fisiche-chimiche dei virioni e delle finalità lavorative. Ad esempio, alcuni virus, in particolare quelli filamentosi, subisco con il congelamento a -20°C alterazioni nella struttura proteica terziaria del capside e nei legami genoma/capside per cui il materiale spesso non mantiene le capacità infettive o le caratteristiche strutturali per una sicura identificazione sierologica. Bibliografia CARBONE I., L.M. KOHN, 1999. A method for designing primer sets for speciation studies in filamentous ascomycetes. Mycologia, 91(3), 553-556. CLARK M.F., A.N. ADAMS, 1977. Characteristics of the microplate method of enzymelinked immunosorbent assay for the detection of plant viruses. Journal of General Virology 34(3), 475-483. DARRASSE A., S. PRIOU, A. KOTOUJANSKY, Y. BERTHEAU, 1994. PCR and Restriction Fragment Lenght Polymorphism of a pel gene as a tool to identify Erwinia carotovora in relation to potato diseases. Applied and Environmental Microbiology, 60, 1437-1443. FISHER N.L., L.W. BURGESS, T.A. TOUSSON, 1982. Carnation leaves as a substrate and for preserving cultures of Fusarium species. Phytopathology, 72(1), 151-153. GLASS N.L., G. DONALDSON, 1995. Development of Primer Sets Designed for Use with the PCR to Amplify Conserved Genes from Filamentous Ascomycetes. Applied and Environmental Microbiology, 61(4), 1323-1330. HAYDEN K.J., IVORS K., WILKINSON C., GARBELOTTO M., 2006. TaqMan real-time chemistry for Phytophthora ramorum detection and quantification, with comparison of diagnostic methods. Phytopathology 96, 846-54. HIGGINS C.F., G.F.L. AMES, W.M. BARNES, J.M. CLEMENT, M. HOFNUNG, 1982. A novel intercistronic regulatory element of prokaryotic operons. Nature, 298, 760-762. HULTON C.S.J., C.F. HIGGINS, P.M. SHARP, 1991. Eric sequences - a novel family of repetitive elements in the genomes of Esherichia coli, Salmonella tyophimurium and other enterobacteria. Molecular Microbiology, 59, 825-834. 58 Collezione di microrganismi di interesse agrario, industriale ed ambientale KERKOUD M., C. MANCEAU, J.P. PAULIN, 2002. Rapid diagnosis of Pseudomonas syringae pv. papulans, the causal agent of blister spot of apple, by polymerase chain reaction using specifically designed hrpL gene primers. Phytopathology, 92, 1077-1083. LOMMEL S.A., A.H. MCCAIN, T.J. MORRIS, 1982. Evaluation of indirect enzymelinked immunosorbent assay for the detection of plant viruses. Phytopathology, 72, 1018-1022. LORETI S., A. GALLELLI, 2002. Rapid and specific detection of virulent Pseudomonas avellanae strains by PCR amplification. European Journal of Plant Pathology, 108, 237-244. MAKKOUK K.M., S.G. KUMARI, 2006. Molecular diagnosis of plant viruses. Arab Journal of Plant Protection, 24(2), 138-135. MAREK P., T. ANNAMALAI, K.VENKITANAYANAN, 2003. Detection of Penicillium expansum by polymerase chain reaction. Int. Food Microbiol, 89, 139-144. MEINKOTH J., G. WAHL, 1984. Hybridization of nucleic acids immobilized on solid supports. Analytical Biochemistry, 138, 267-284. O’DONNEL K., E. CIGELNIK, 1997. Two divergent intragenomic rDNA ITS2 types within a monophyletic lineage of the fungus Fusarium are nonorthologus. Mol. Phylogenet. Evol. 7, 103-116. O’DONNELL K., H.C. KISTLER, E. CIGELNIK, R.C. PLOETZ, 1988. Multiple evolutionary origins of the fungus causing Panama disease of banana: Concordant evidence from nuclear and mithocondrial gene genealogies. Proceedings of the National Academy of Sciences of the United States of America, 95, 2044-2049. OZAKMAN M., N.W. SHAAD, 2003. A Real-Time BIO-PCR assays for detection of Ralstonia solanacearum race 3, biovar 2 in asymptomatic potato tubers. Canadian Journal of Plant Pathology, 25, 232-239. PARMETER J.R. JR, R.T. SHERWOOD, W.D. PLATT, 1969. Anastomosis grouping among isolates of Thanatephorus cucumeris. Phytopathology 59, 1270-1278. PUHALLA J.E., 1985. Classification of strains of Fusarium oxysporum on the basis of vegetative compatibility. Canadian Journal of Botany, 63,179-183. SCHAFER M.R., M.L. KOHN, 2006. An optimized method for mycelial compatibility testing in Sclerotinia sclerotiorum. Mycologia, 98 (4), 593-597. SEAL S., D. COATES, 1998. Detection and Quantification of Plant Viruses by PCR. Methods in Molecular Biology, 81, 469-485. SHAAD N.W., Y. BERTHIER-SHAAD, A. SECHLER, D. KNORR, 1999. Detection of Clavibacter michiganensis subsp. sepedonicus in potato tubers by BIO-PCR and an automated Real-Time fluorescence detection system. Plant Disease, 83, 1095-1100. SHISHKOFF N., 1992. Pyrenochaeta in Methods for Research on Soilborne Phytopathogenic Fungi. Eds. Singleton L.L., Mihail J.D. and Rush C.M., APS Press St. Paul, Minnesota, pp. 153-156. 59 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) SORENSEN K.N., K.H. KIM, J.Y. TAKEMOTO, 1998. PCR detection of cyclic lipodepsinonapeptide-producing Pseudomonas syringae pv. syringae and similarity of strains. Applied and Environmental Microbiology, 64, 226-230. VERSALOVIC J., M. SCHNEIDER, F.J. DE BRUIJN, J.R. LUPSKI, 1994. Genomic fingerprinting of bacteria using repetitive sequence-based polymerase chain reaction. Methods in Molecular and Cellular Biology, 5, 25-40. WHITE T.J., T. BURNS, S. LEE, J. TAYLOR, 1990. Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics. PCR Protocols: A guide to methods and Applications. M.A. Innis, D.H. Gelfang, J.J. Sninsky, e T.J. White, eds. Accademic Press, Inc., San Diego, CA, 315-322. WHITTAKER R.H. 1969. New concepts in kingdoms of organisms. Science, 163, 150160. 60 Collezione di microrganismi di interesse agrario, industriale ed ambientale 4 MICRORGANISMI ENTOMOPATOGENI 4.1 PREMESSA I microrganismi entomopatogeni sono naturalmente presenti in natura e dotati della capacità di esercitare azione antagonista (parassitismo, competizione, ecc.) verso le popolazioni di artropodi o di nematodi appartenenti a interi ordini, famiglie, generi o specie. Fra gli artropodi da combattere con la lotta biologica, particolare interesse è rivolto agli insetti fitofagi che sono in grado di danneggiare coltivazioni agrarie e forestali. Fra i microrganismi maggiormente impiegati nei sistemi di lotta biologica sono da ricordare alcuni batteri e funghi. Essi possono trovare ampia applicazione in interventi di difesa basati sul principio delle strategie a basso impatto ambientale, della biosostenibilità, del mantenimento della biodiversità. Tali principi sono alla base dell’importanza di una collezione di microrganismi intesa come una “riserva” di variabilità genetica in termini di virulenza, spettro d’azione, capacità di produrre metaboliti ecc. alle diverse esigenze di difesa delle varie colture. Tra i microrganismi attualmente di maggiore importanza per la lotta biologica si ricordano i seguenti. Batteri Bacillus thuringiensis Si tratta di un batterio sporigeno e tossigeno, molto studiato, che ha trovato la più ampia utilizzazione in ambito forestale oltre che in contesti agrari e urbani. Questa specie è diffusa ovunque, nel terreno, sulla vegetazione, su insetti morti. In coltura, su substrati idonei, forma di norma colonie di colore bianco-crema con superficie e contorni corrugati (Fig. 4.1). Del batterio sono attualmente conosciute diverse sottospecie, tra le quali si ricordano le ssp. kurstaki, ssp. tenebrionis, ssp. aizawai, ssp. israelensis. Ognuna di esse è caratterizzata da una attività prevalente nei confronti di determiFig. 4.1 – Coltura di Bacillus thunati gruppi di insetti. ringiensis su substrato agarizzato. 61 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Funghi Beauveria bassiana Tra i miceti entomopatogeni B. bassiana è estesamente impiegato nella difesa microbiologica contro artropodi dannosi in campo agro-forestale. Ubiquitario, vive nel terreno, sulla vegetazione, sugli insetti morti dai quali può essere isolato. Caratterizzato da micelio bianco, tendente al giallo-crema con l’invecchiamento, assume spesso un aspetto polverulento per l’abbondante produzione di conidi (variabile con gli isolati) (Fig. 4.2). Ha capacità di controllo su un ampio spettro di artropodi. Fig. 4.2 – Coltura di Beauveria bassiana su substrato agarizzato. Metarhizium anisopliae In coltura artificiale forma colonie inizialmente di colore bianco che in seguito virano al verde oliva (Fig. 4.3). Fig. 4.3 – Coltura di Metarhizium anisopliae su substrato. È caratterizzato da conidi di forma allungata e privi di setti, di colore verde, riuniti in catene. Il micete è assai diffuso nel terreno ed è in grado di attaccare, secondo il ceppo, un’ampia gamma di insetti fra cui ortotteri, emitteri, lepidotteri e coleotteri. Paecilomyces spp. Le specie di questo genere di funghi hanno ampia diffusione in natura e formano colonie dalla colorazione variabile dal grigio al crema al viola. Alcune specie risultano variamente adatte per applicazioni di lotta biologica contro larve di lepidotteri e coleotteri e anche nei confronti di alcuni nematodi (Fig. 4.4). 62 Fig. 4.4 – Coltura di Paecilomyces lilacinus su substrato agarizzato. Collezione di microrganismi di interesse agrario, industriale ed ambientale Verticillium lecanii Il micete è rinvenibile su numerosi substrati fra cui diversi artropodi. Caratterizzato da micelio di colore bianco, può trovare applicazione soprattutto in serra per la lotta biologica contro emitteri (afidi, aleurodidi, ecc.) e lepidotteri (Fig. 4.5). Può risultare attivo anche nei confronti di acari e nematodi. Fig. 4.5 – Coltura di Verticillium lecanii su substrato agarizzato. 4.2 CAMPIONAMENTO Il campionamento costituisce il punto di partenza per l’ottenimento di isolati o ceppi di microrganismi (batteri e funghi) entomopatogeni e prevede la ricerca di matrici diverse in funzione dell’obiettivo proposto. Solitamente si procede al prelievo dei campioni per lo più in ambiente naturale come i boschi, le foreste e il pieno campo, ma anche nelle colture protette. I materiali più frequentemente presi in esame sono il terreno, parti di vegetale (cortecce, rami, foglie, semi ecc.) (Fig. 4.6), corpi di insetti morti (Fig. 4.7) ma, in relazione a particolari esigenze, altre fonti di prelievo possono essere l’acqua o l’aria. Fig. 4.6 – Prelievo di campioni di corteccia Le tecniche di prelievo dei camFig. 4.7 – Corpo di insetto (Rhynchophorus pioni sono quelle consuete in ambito ferrugineus) morto naturalmente ad opera di un micete agro-forestale (per es. uso di attrezzi, entomopatogeno (Beauveria bassiana). sacchetti e contenitori sterili, raccolta di quantità adeguate di terreno a diverse profondità in vicinanza delle piante, scelta di porzioni vegetali, ricerca di artropodi morti in contesti particolari, ecc.) dove si devono sempre considerare le condizioni ambientali così come gli obbiettivi specifici. 63 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) 4.3 ISOLAMENTO L’isolamento dei microrganismi entomopatogeni avviene attraverso metodologie di laboratorio che differiscono in relazione all’organismo cercato ed al substrato di partenza. Isolamento da terreno Partendo da campioni di terreno, possono essere adottate diverse tecniche. Per quanto riguarda i batteri, possono essere fatte sospensioni dei terreni in acqua sterile a diluizioni progressive che, in quantità dell’ordine di circa 1 ml, possono essere distribuite in piastra su substrati selettivi specifici. Nel caso dei miceti, oltre a quanto indicato per i batteri, può essere usata la tecnica del “baiting” consistente nell’immissione nella Fig. 4.8 – Impiego di insetti-esca (Galleria massa del campione di suolo di un certo mellonella) per l’isolamento di funghi entomopatonumero di insetti-esca (per esempio lar- geni. ve del lepidottero Galleria mellonella), aventi lo scopo di attirare sul proprio corpo il micelio di funghi entomopatogeni eventualmente presenti (Fig. 4.8). Isolamento da materiale vegetale L’isolamento da parti di vegetali comporta invece la scelta del materiale campionato e il taglio dei campioni. • Per quanto riguarda la ricerca di batteri, una tecnica che sembra dare buoni risultati consiste nel lavaggio delle superfici vegetali (foglie, corteccia, ecc.) con acqua sterile + Tween 80 e nella raccolta del percolato da utilizzare, a varie diluizioni, in coltura su mezzo agarizzato come agar nutritivo (NA). • Per quanto riguarda la ricerca di funghi, si può procedere con i “lavaggi” come per i batteri oppure, con l’uso di substrati selettivi e con tecniche particolari, a partire direttamente dai tessuti vegetali come nel caso dell’isolamento di funghi endofiti. 64 Collezione di microrganismi di interesse agrario, industriale ed ambientale Isolamento dal corpo di artropodi L’ottenimento di microrganismi dal corpo di un artropode inizia generalmente con la disinfezione esterna dell’esemplare con una soluzione di ipoclorito di sodio al 5% o più in generale con sostanza disinfettante seguita da ripetuti lavaggi in acqua sterile. • Nel caso della ricerca di batteri, si può procedere alla dissezione in sterilità del corpo dell’insetto secondo linee longitudinali. Aperto il corpo si può procedere al recupero del liquido dell’emocele mediante capillari, alla sua diluizione in acqua sterile o soluzione di Ringer ed all’immissione in piastra su mezzo agarizzato come NA o BHIA (Brain-Heart Infusion Agar). Altro metodo di isolamento consiste nel prelevare piccole porzioni di tessuto interno, immergerle in acqua sterile o soluzione di Ringer, triturarle e formare una sospensione da “strisciare” in piastra su uno dei mezzi di coltura precedentemente indicati. • Nel caso, invece, di isolamento di funghi, si favorisce (con l’impiego di camere umide) l’emersione all’esterno del corpo dell’insetto del micelio fungino e delle fruttificazioni. Quindi si procede al prelievo di una piccola porzione del micete, alla sua semina in piastra su substrato di coltura ed all’incubazione in ambiente termostatato. 4.4 PURIFICAZIONE Una volta ottenuto l’isolato, è spesso necessario procedere alla sua purificazione in quanto non è infrequente trovarsi di fronte alla sgradita presenza di più microrganismi in antagonismo o in coabitazione sul terreno di coltura. Il ricorso ripetuto all’impiego di substrati selettivi, abbinato, per esempio, ad una incubazione a temperature adatte allo sviluppo dell’organismo desiderato, facilita l’esclusione di alcuni microrganismi caratterizzati da una crescita notevolmente più rapida. Inoltre, l’inquinamento da batteri in una coltura fungina può essere generalmente controllato con l’aggiunta di antibiotici (come il solfato di streptomicina). Fra i numerosi terreni di coltura usati per i funghi occorre distinguere fra quelli adatti all’isolamento o al mantenimento e quelli più idonei a favorire la produzione di propaguli. Fra i primi si ricorda il PDA, ampiamente usato per l’isolamento di una gran quantità di specie, ma non particolarmente adatto per la loro conservazione in quanto può favorire, in seguito a ripetuti trasferimenti, mutazioni indesiderate. Altro mezzo di coltura assai utilizzato per l’isolamento di diversi funghi entomopatogeni è SDA+Y (Sabouraud Dextrose Agar + Yeast extract) che ne favorisce l’accrescimento. Fra i substrati che inducono la sporificazione, invece, si ricorda in particolare SMA+Y (Sabouraud Maltose Agar + Yeast extract). Il mantenimento in collezione dei microrganismi fungini richiede spesso, proprio per una questione di purezza dell’isolato, l’ottenimento di colture monosporiche descritte in dettaglio al paragrafo 3.5. 65 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) 4.5 IDENTIFICAZIONE L’identificazione del microrganismo richiede innanzitutto la conoscenza della sua morfologia. In linea di massima è relativamente semplice giungere alla definizione del genere (per es. mediante chiavi di identificazione) mentre più ardua risulta la determinazione specifica. In alcuni casi è indispensabile ricorrere all’identificazione da parte di esperti. Nel caso delle specie di microrganismi entomopatogeni, esse sono in numero limitato. D’altra parte, l’ampia variabilità intraspecifica comporta un approfondito ed esteso lavoro di caratterizzazione dei singoli ceppi. Batteri La morfologia della colonia batterica in coltura artificiale fornisce le prime indicazioni utili all’identificazione. Le colonie di B. thuringiensis si presentano generalmente traslucide, di colore biancastro-crema chiaro, con superficie corrugata e contorni irregolari. L’osservazione al microscopio ottico, specialmente in contrasto di fase, consente di mettere in evidenza la dimensione e la morfologia della cellula batterica, la presenza o meno delle forme di resistenza del batterio (endospore) e le eventuali formazioni cristalline (corpo parasporale). Per esempio, B. thuringiensis è caratterizzato da un’endospora di forma ellittica accompagnata da uno o più cristalli di Fig. 4.9 – Endospora (S) e cristalli (C) di B. forma variabile (Fig. 4.9) con la sottothuringiensis. specie bipiramidale, cubica, sferoidale, amorfa, ecc. Metodologie di identificazione più approfondite si basano su saggi sierologici (antigeni flagellari) o, più recentemente, sull’analisi dei geni codificanti per protossine del cristallo (geni cry) mediante reazione a catena della polimerasi (PCR). Funghi Uno dei primi passi da effettuare per l’identificazione di un micete è costituito dall’osservazione morfologica della colonia fungina in coltura artificiale. Anche per i miceti l’osservazione al microscopio ottico consente di mettere in evidenza dimensione e morfologia delle strutture vegetative e riproduttive. Nel 66 Collezione di microrganismi di interesse agrario, industriale ed ambientale caso dei funghi entomopatogeni anamorfi (i più diffusi ed utilizzati nella lotta biologica), hanno rilevanza sistematica i conidiofori, le cellule conidiogene (es. fialidi) e i conidi (Fig. 4.10). Nei funghi “perfetti”, teleomorfi, può essere indicativa la morfologia delle strutture riproduttive. È questo il caso degli Ascomiceti, come quelli appartenenti al genere Cordyceps, che presentano vistose formazioni osservabili ad occhio nudo (Fig. 4.11). Fig. 4.10 – Cellu- Fig. 4.11 – Vistose strutture riproduttive le conidiogene e conidi di (genere Cordyceps) emergenti dal corpo dell’insetto Paecilomyces sp. ospite. L’identificazione specifica può essere ottenuta sia con parametri morfologici e colturali sia con l’ausilio di tecniche molecolari basate sulla PCR con l’uso di marcatori molecolari specifici o generici. 4.6 CARATTERIZZAZIONE Accertata l’identità del microrganismo, diventa importante procedere alla sua caratterizzazione. Come è noto, esistono metodologie diverse aventi diversa finalità. Per esempio, accanto ad una caratterizzazione genetica (analisi del DNA) possono essere effettuati: • saggi fisiologici di sviluppo in vitro (velocità di accrescimento, produzione di spore o conidi, ecc.); • analisi dei metaboliti; • saggi di patogenicità su insetti bersaglio (artropodi in stadi di sviluppo diversi, in condizioni ambientali diverse, ecc.). 67 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) 4.7 CONSERVAZIONE La buona conservazione dei microrganismi è condizione indispensabile per il loro impiego nella lotta microbiologica. Tramite la conservazione si intende raggiungere lo scopo di mantenere il più possibile inalterate nel tempo le caratteristiche del microrganismo stesso e di poterne disporre in maniera pronta e facilmente utilizzabile. Fra i metodi saggiati e messi in atto, la conservazione tradizionale in tubo su substrato agarizzato è quella di più rapida manualità per assicurare in breve tempo i trapianti. Di fatto, essa può riservare sorprese sgradite per quanto riguarda il mantenimento delle caratteristiche degli isolati che, come è noto, possono andar soggetti a mutazioni indesiderate (proprio anche a seguito di frequenti trapianti). Per ovviare a ciò si può ricorrere alla crioconservazione di batteri e miceti a basse e bassissime temperature o di inglobamento in “pellets” di alginato di sodio. Questi metodi consentono di mantenere gli isolati per periodi relativamente lunghi (superiori ad un anno). Un metodo di conservazione sovente praticato è quello della liofilizzazione, che permette di raggiungere lunghi periodi e di restringere radicalmente le dimensioni delle collezioni. Più dettagliatamente: Conservazione in tubo su substrato agarizzato (tubi a becco di flauto) Dagli isolamenti ottenuti in purezza si preleva una minima quantità della coltura e la si trasferisce in tubo sterile contenente un substrato agarizzato adatto al batterio o al fungo entomopatogeno. I terreni di coltura sono quelli precedentemente indicati: prevalentemente NA per i batteri ovvero PDA, MA (agar malto), SDA+Y o SMA+Y per i funghi. I tubi vengono quindi posti in termostato al buio a 28-30°C nel caso di batteri ed a 20-25°C nel caso di funghi fino al raggiungimento di uno sviluppo ottimale. A sviluppo avvenuto, vengono conservati in frigorifero a circa 4°C. Al momento dell’impiego i ceppi vengono “rivitalizzati” mediante trasferimento in piastra su substrato agarizzato adatto (per i batteri si usa generalmente NA mentre per i funghi PDA o MA). Il metodo di conservazione e utilizzazione dei microrganismi risulta piuttosto semplice in normali condizioni di laboratorio senza disponibilità di strumentazioni sofisticate. Come si è detto in precedenza, però, sussiste il rischio di alterazione di alcune peculiarità del ceppo come la patogenicità. Conservazione a basse temperature (crioconservazione) La tecnologia del freddo è molto promettente anche per la conservazione di numerosi microrganismi entomopatogeni. È in fase di verifica la possibilità di conservare a temperature ultrabasse (-140°C) in glicerolato alcuni isolati di B. thuringiensis. 68 Collezione di microrganismi di interesse agrario, industriale ed ambientale Risultati promettenti sono stati ottenuti conservando a basse temperature alcuni miceti (B. bassiana) allevati in tubo su substrato agarizzato. Dopo 3 anni di conservazione, infatti, le colonie sono risultate ancora vitali. Conservazione in “pellets” di alginato di sodio La conservazione di batteri e funghi in formulazioni di alginato di sodio può essere consigliata, non tanto per la lunga durata, quanto per quelle occasioni in cui si renda necessaria, per esempio, la distribuzione dei microrganismi entomopatogeni in substrati come il terreno, contro insetti elateridi o nottue. Per grandi linee, il metodo di incapsulamento in “pellets” di alginato consiste nella preparazione di una sospensione del microrganismo alla concentrazione desiderata da unire, in un imbuto gocciolatore, ad una sospensione di sodio-alginato 1,33% + caolino lavato 1%. Mantenendo in continua lenta agitazione, si procede a far gocciolare il materiale in calciocloruro 0,25M, anch’esso tenuto in leggero movimento circolare. I “pellets” che man mano si formano vengono prelevati, asciugati all’aria, in cappa sterile e quindi introdotti in tubi o altri contenitori sterili (Fig. 4.12). Fig. 4.12 – “Pellets” di alginato in preparazione. La conservazione può essere fatta in frigo a 4°C oppure semplicemente a temperatura ambiente. La conservazione è di lunga durata (oltre l’anno). Inoltre, il metodo risulta di pratica attuazione e non richiede attrezzature costose o particolarmente sofisticate. Conservazione per liofilizzazione La liofilizzazione è un processo che implica la disponibilità di attrezzature specifiche e piuttosto costose. In laboratorio, il procedimento si attua a partire da quantità adeguate di materiale batterico o fungino che è stato coltivato su adatti substrati di coltura. Per quanto riguarda i batteri, si procede all’inoculo di piastre Petri contenenti substrato agarizzato NA. A sviluppo ottimale si procede alla “raccolta” della colonia mediante una spatola sterile (si può anche far uso di microsfere di vetro sterilizzate da fare scorrere sulla colonia batterica dopo aggiunta di piccole quantità di acqua sterile) ed alla sua immissione, in aliquote determinate, in contenitori sterili come provette Eppendorf o piccole fiale o ampolle di vetro da sigillare. 69 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Per quanto si riferisce ai funghi, le piastre contengono substrati specifici come PDA o MA oppure, nel caso di B. bassiana, SDA+Y, sui quali è posto un disco di cellophane sterilizzato. In tal modo, la produzione di micelio e conidi, favorita dal mezzo selettivo, avviene al di sopra del cellophane e la raccolta è semplificata ed esclude la presenza di residui di agar. Come per i batteri, il materiale viene introdotto, nelle quantità volute, in contenitori sterili e sottoposto a liofilizzazione. L’operazione di liofilizzazione viene, di solito, protratta per circa 48 ore. La conservazione dei liofilizzati è effettuata in frigorifero a temperatura di 4°C oppure in congelatore a -20°C. L’utilizzazione dei liofilizzati avviene mediante prelievo del microrganismo liofilizzato e il suo reinoculo, a secco o dopo sospensione in acqua sterile, su substrato agarizzato in piastre Petri. Per i batteri si impiega prevalentemente il terreno di coltura NA; per i funghi si usa PDA oppure MA o SDA+Y (per miceti del genere Beauveria). Le piastre sono poste in ambiente termostatato (a 28-30°C per i batteri ed a 20-25°C per i funghi) per il tempo necessario ad un buono sviluppo del microrganismo: da alcuni giorni per i batteri come B. thuringiensis a 10-15 giorni per i miceti come B. bassiana. Come si è accennato, la liofilizzazione consente lunghi periodi di conservazione, permette la conservazione di un gran numero di ceppi in poco spazio e ne rende agevole il trasporto e la manipolazione. Bibliografia BUTT T. M., C.W. JACKSON, N. MAGAN, 2001. Fungi as biocontrol agents. Progress, problems and potential. Butt T.M., C.W. Jackson, N. Magan, (Eds.). CABI Publishing, 390. DESEÖ KOVÁCS K.V., L. ROVESTI, 1992. Lotta microbiologica contro i fitofagi. Teoria e pratica. Edagricole, Bologna, 296. POINAR JR. G.O., G.M. THOMAS, 1978. Diagnostic manual for the identification of insect pathogens. Plenum Press, New York and London, 218. SAMSON R.A., H.C. EVANS, J.P. LATGÉ, 1988. Atlas of entomopathogenic fungi. Springer-Verlag, Berlin Heidelberg New York London Paris Tokyo, 187. 70 Collezione di microrganismi di interesse agrario, industriale ed ambientale 5 MICRORGANISMI DEL SUOLO 5.1 PREMESSA Il suolo è l’ambiente naturale, costituito da materiali minerali ed organici, che sulla superficie della Terra garantisce la vita agli organismi viventi. Recentemente è stato definito “la zona critica” della terra meritando un’attenzione particolare grazie al suo ruolo chiave negli equilibri ambientali, a sostegno dell’intera vita del nostro pianeta. Mantenere in collezione i microrganismi del suolo rappresenta una necessità irrinunciabile soprattutto nel caso di studi ambientali per comprendere quali pressioni realmente possano intervenire da parte dell’uomo o di eventi ambientali sul suolo, quali i cambiamenti climatici, la deforestazione, le colture OGM (Lynch et al., 2004) o la stessa agricoltura intensiva (Mocali et al., 2008). Alcuni ceppi microbici o fungini possono essere utilizzati come biomarcatori e, quindi, fungere da eccellenti bioindicatori ambientali. Il suolo rappresenta una miniera di geni perlopiù inesplorata e dallo studio e dalla caratterizzazione dei microrganismi ivi presenti è possibile individuarne sia le funzioni ecologiche (Nannipieri et al., 2003) sia le potenziali applicazioni in molti processi biotecnologici, che spaziano dalla bioenergia alla biofertilizzazione, dal biorecupero alla biodegradazione, ecc. Oggi si è in grado, attraverso appropriati indicatori microbiologici, biochimici e molecolari, di definire la qualità e la salute di un suolo (Bloem et al., 2006), prevederne ed arginarne processi di degradazione, fino alla desertificazione, nonché calibrare correttamente gli interventi di fertilizzazione con una gestione integrata delle sostanze nutritive, sulla base della conoscenza del ciclo e del bilancio dei diversi elementi, quali ad esempio l’azoto. Su questo principio si possono basare tutti gli studi che rientrano nel tema della metagenomica del suolo. Realizzare una collezione di microrganismi del suolo risulta più complesso della raccolta in collezione di altri microrganismi di interesse agrario, in quanto è noto dalla bibliografia che solo l’1% dei microrganismi che vivono nel suolo sono coltivabili e quindi isolabili, caratterizzabili e conservabili in collezione. Di seguito sono descritte le modalità per la messa in collezione di batteri e funghi tellurici, inoltre vengono anche descritti elementi necessari a fornire una base per l’inserimento nella collezione dei microorganismi non colturabili come genoma del suolo, nella prospettiva della creazione di un database per il metagenoma suolo degli ambienti italiani. 5.2 ISOLAMENTO L’isolamento dei microrganismi del terreno avviene attraverso metodi di laboratorio che differiscono in relazione alle caratteristiche dei microrganismi stessi. 71 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) La preparazione del campione di suolo Il campione può essere prelevato con sgorbie, trivelle, pale o campionatori a martellamento con cilindro o pistone, facendo attenzione a mantenere il più possibile il campione integro. Per ciascun sito di prelievo, viene generalmente compilata una apposita scheda (Tab. 5.1). La scheda dovrebbe fornire al potenziale utente della collezione informazioni utili alla collocazione del microrganismo nell’ambiente di raccolta, al fine di consentire comparazioni ovvero rappresentare uno strumento di riferimento. La registrazione dei dati generali costituisce l’elemento base per l’ identificazione del campione e dovrà seguire un criterio concordato ed omologato con un protocollo dettagliato e specifico da raccogliere in una piccola guida. In questa parte dovranno essere annotate l’oggetto, il numero e il nome dei campioni, la data del rilievo, il nome del rilevatore e la località con le relative coordinate GPS. Molto importante sarà anche l’accuratezza della descrizione del sito considerando come importanti caratteristiche ad esempio l’esposizione ai venti, la pendenza del suolo, la rocciosità e la quota sul livello del mare. Risulterà anche fondamentale per l’interpretazione dei dati raccolti la registrazione di alcuni elementi come la profondità del prelievo, la presenza di falda, l’umidità e la presenza di radici, nonché i principali dati climatici. Infine per meglio caratterizzare l’organismo studiato sarà necessario specificare l’uso del suolo come ad esempio la coltura in atto e la gestione colturale abituale, se forestale (specificare la specie o la consociazione), prato-pascolo, incolto o altro (fruizione turistica, riserva naturale, giardino pubblico, ecc), nonché la vicinanza a centri urbani, strade e autostrade, siti industriali, ferrovie, ecc. Ogni informazione utile a ricostruire l’evolversi dell’ecosistema. Ad esempio sarebbe interessante conoscere, nel caso si considerasse un terreno incolto, se e da quanto tempo è incolto oppure se precedentemente hanno insistito coltivazioni, boschi, ecc., nonché il colore del suolo, la presenza di croste superficiali, l’affioramento di materiali particolari come metalli, plastiche, laterizi, residui organici di vario genere, ecc. Al fine di costituire un campione medio rappresentativo, il campionamento viene effettuato in maniera randomizzata lungo un percorso a X o a W che non tenga conto delle zone anomale e dei bordi della parcella, prelevando almeno 5 sottocampioni (Allievi et al., 2003). Il campione di terreno viene, quindi, liberato dai residui colturali superficiali presenti. È necessario utilizzare guanti monouso, in modo da non provocare contaminazione con microrganismi estranei, e si utilizzano per la raccolta del campione sacchetti sterili di almeno 2 litri di capacità qualora si vogliano riunire subito i sottocampioni. La profondità del prelievo è di norma compresa tra 0 e 20 cm, anche se condizioni particolari della parcella (ad es. aratura) o particolari tipi di terreno (ad es. suolo con copertura forestale) possono richiedere diverse profondità o la suddivisione di una profondità in diversi campioni in relazioni ai diversi strati; per informazioni 72 Collezione di microrganismi di interesse agrario, industriale ed ambientale TABELLA 5.1 – Scheda di campionamento. Dati generali Oggetto: Campione n. Rilevatore: Data del rilievo: Località: °N Coordinate GPS della stazione °E Descrizione del sito Esposizione Quota s.l.m. Temperature dell’aria (media mensile) Precipitazioni (media mensile) Piovose: Nevose: Descrizione del suolo Profondità del prelievo (cm) Granulometria Caratteristiche chimico- pH fisiche e biologiche Sostanza organica N tot C/N Respirazione basale Dosaggio biomassa microbica Ogni altro elemento utile alla caratterizzazione del suolo (CSC, metalli pesanti, elementi della fertilità, parametri biochimici, indice di compattazione, pF, ritenzione capillare, ecc.) Vicinanza di centri urbani, industriali, autostrade, ecc. Tipo di vegetazione e copertura (%) Prato Alto fusto Colture Uso del suolo (agricolo, pascolo, riserva naturale, ecc.) Descrizione della superficie del terreno al momento del prelievo 73 Altro PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) più dettagliate su questo punto si rimanda al “Manuale di Metodi di Analisi Microbiologica del suolo” della SISS. Per il “bulk soil” (cioè per il terreno non permeato dalle radici) si campiona a debita distanza dalla vegetazione. Per la rizosfera si preleva un pane di terra contenente la pianta con la massima parte dell’apparato radicale, nel caso di pianta erbacea, mentre nel caso di piante arboree si effettuano prelievi di suolo ad una distanza dalla pianta e ad una profondità che variano a seconda dello sviluppo radicale della specie studiata. Una volta prelevato, il campione si mantiene a 4°C attraverso un contenitore da trasporto refrigerato fino all’arrivo in laboratorio, preferibilmente entro la giornata stessa del prelievo. Isolamento di funghi e batteri Per la valutazione dei funghi e dei batteri colturabili, si mette il suolo, parzialmente sminuzzato, a seccare all’aria in vasche di materiale inerte (Fig. 5.1) in luogo buio e areato per non più di 5-6 giorni. I campioni vengono poi setacciati con vagli con pori di dimensione di 2-4 o più mm, a seconda delle esigenze. Fig. 5.1 – I campioni di suolo posti ad essiccare in vasi di plastica al buio e in luogo areato. Nel caso dell’isolamento di batteri dalla rizosfera, si rimuove il pane di terra dalle radici e si preleva l’apparato radicale della pianta con il suolo adeso per uno 74 Collezione di microrganismi di interesse agrario, industriale ed ambientale spessore non superiore ai 2 mm; si recupera il suolo tramite sbattimento, in agitatore orbitale a 200 oscillazioni min-1 per 30 minuti, di 5 g di radici spezzettate in frammenti di 1 cm ca., + suolo, in presenza di 25 ml di tampone fosfato salino PBS pH 7,4; si eliminano le radici e si recupera il suolo rizosferico con una centrifugazione a 5.000 rpm per 15 minuti a RT (temperatura ambiente) in varie Eppendorf. Isolamento delle comunità dei batteri azotofissatori aerobi Vengono utilizzati i seguenti metodi: 1. Metodo di coltura diretta da suolo (indicato per Azotobacter): • Una piccola aliquota di suolo (30-50 g), vagliato come precedentemente indicato, viene impastato con una quantità pari all’ 1% di Na-piruvato e acqua sterile in un mortaio di porcellana; • L’impasto viene trasferito in capsule Petri con una spatola sterile, avendo cura di “lisciare” convenientemente la superficie dell’impasto, che non deve toccare il coperchio della piastra al fine di evitare condizioni di anaerobiosi. Dopo incubazione a 30°C per 3-7 giorni si evidenziano le colonie di Azotobacter, di aspetto lucido e consistenza viscosa a causa della sintesi di esopolisaccaridi (Fig. 5.2). Fig. 5.2 – A sinistra: colonie di Azotobacter dall’aspetto lucido e viscoso. A destra: ingrandimento 1000x di un campione prelevato da una colonia in cui si osservano cisti (cellule ovali, chiare) e cellule vegetative (bacilli, scuri). Per gli isolamenti viene adottato il metodo secondo Beijerinck per le Azotobacteriaceae (Beijerinck, 1901): • 20 ml di brodo nutritivo vengono distribuiti in beute da 100 ml sterilizzate, inoculate con 0,3-0,5 g di terreno e incubate per 2-7 giorni a 30°C. 75 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) • Prelevato il film caratteristico della crescita di questi batteri e diluito in 10 ml di acqua sterile, 100 µl di questa diluizione vengono ulteriormente diluiti in provette Eppendorf contenenti 1,9 ml di acqua sterile, fino a raggiungere la quinta diluizione; 100 µl di ciascuna diluizione vengono strisciati su piastre contenenti il terreno di coltura ed incubate a 30°C. Questo ulteriore passaggio in un mezzo solido privo di azoto si rende necessario per allontanare gli eventuali ceppi contaminanti, la cui crescita in mezzo liquido, avvertibile dal forte odore di butirrato, può essere resa possibile dall’azoto fissato prodotto da Azotobacter. • Allo sviluppo delle colonie, queste ultime vengono strisciate su capsule Petri di 10 cm di diametro con terreno RM (Newton et al., 1953) e incubate per 24 h a 30°C. I substrati utilizzati sono quelli originali di Beijerinck 1901, riportati nei testi di microbiologia. 2. Isolamento su substrati solidi o semisolidi • Gli isolamenti si ottengono a partire da 10 g di suolo vagliato, messo ad agitare in beute di vetro sterili da 250 ml contenenti 90 ml di tampone fosfato pH 7,2 (0,8 g K2HPO4 + 0,2 g KH2PO4) per 30 minuti in shaker orizzontale oscillatorio a 120 rpm. Questa sospensione viene considerata una diluizione 10-1. Vengono poi effettuate successive diluizioni seriali in tampone fosfato e 100 µl delle diluizioni 10-3, 10-4 e 10-5 vengono strisciati su substrati solidi o inoculati in 4,9 ml di substrato semisolido. • I substrati solidi sono realizzati con l’aggiunta di 15 g/l di Agar mentre per i semisolidi vengono aggiunti 5 g/l di Agar. Fra i substrati più usati si ricordano: - Substrato di Rennie (Rennie, 1981) generale per Diazotrofi liberi aerobi. - Substrato Nfb (Krieg e Döbereiner, 1984) per le specie di Azospirillum. Isolamento delle comunità dei rizobi I rizobi sono batteri capaci di instaurare una simbiosi mutualistica con le radici di piante leguminose, in quanto i batteri si riforniscono dei carboidrati prodotti dalla pianta mediante fotosintesi, mentre le piante si riforniscono di azoto assimilabile (ammoniaca) prodotto dai batteri per riduzione dell’azoto atmosferico (azoto molecolare). Questi batteri sono presenti in tutti i terreni e la loro capacità di adattamento a condizioni estreme (es. terreni salini, terreni semidesertici, ecc.) rende gli studi su questa specie batterica molto interessanti. Particolare attenzione viene data alla selezione e all’impiego di ceppi dotati di maggiore efficienza azotofissatrice (Zhang et al., 2001; Zaccardelli et al., 2002). L’isolamento dei rizobi avviene generalmente dai tubercoli radicali. In caso di isolamento diretto dal suolo, campioni rappresentativi di terreno vengono prelevati e posti in vasi all’interno dei quali vengono successivamente seminati semi di le- 76 Collezione di microrganismi di interesse agrario, industriale ed ambientale guminose, opportunamente disinfettati in superficie. Quando le piante hanno raggiunto un sufficiente sviluppo, si procede alla raccolta dei tubercoli. In caso di isolamento dei rizobi da campioni di seme, questi ultimi vengono posti direttamente in vasi contenenti agriperlite sterile e, dalle piante che si sviluppano, vengono prelevati i tubercoli per l’isolamento. Operativamente, l’isolamento dai tubercoli radicali avviene come segue: • ogni singolo tubercolo o gruppo di tubercoli viene disinfettato in superficie con soluzione acquosa sterile contenente il 2% circa di ipoclorito di sodio, per un tempo di 2 minuti; • dopo lavaggio con acqua bidistillata sterile (SDDW) per 2-3 volte, il tubercolo viene schiacciato in tubi Eppendorf sterili in presenza di 200 μl di SDDW; • l’omogenato ottenuto viene strisciato, con un’ansa, su piastre di YEM-agar (composizione per litro: mannitolo 7,5 g; KH2PO4 0,5 g; MgSO4 0,2 g; NaCl 0,1 g; estratto di lievito 0,4 g; pH 7,2) e incubato a 28 °C per 4-6 giorni; • da ognuna delle piastre di isolamento viene prelevata e purificata, per almeno due volte, una singola colonia; • avvenuto l’isolamento in purezza, si procede alla conservazione dei ceppi. Le comunità fungine colturabili del suolo Le comunità fungine dei suoli hanno caratteristiche molto diverse e non possono essere valutate con un solo metodo (Burgess et al., 1988; Gams, 2007). Si riportano di seguito i metodi utilizzati per 2 comunità fungine, individuate come rappresentative per lo studio dei suoli agrari. Per valutare le comunità dei funghi colturabili del suolo con il metodo delle diluzione seriali (Dhingra e Sinclair, 1985) su agar acqua, si parte dai campioni essiccati all’aria, come descritto nel punto precedente sulla preparazione dei campioni. Il suolo così preparato viene vagliato con setaccio a 4 mm. Appena il campione di suolo è pronto si procede alla valutazione delle comunità fungine. Si prepara la soluzione madre 10-1 a partire da 3 g di suolo in tubi Falcon di 40 ml agitando alla massima velocità con vortex per 1 min. Dalla soluzione 10-1 si ottengono le diluizione successive 10-2, 10-3, da cui si preleva 1 ml che viene aggiunto a 49 ml di agar acqua raffreddato a 40 °C, addizionato con 200 mg/l di streptomicina fosfato e 2 g/l Oxgal. La soluzione di suolo in agar acqua ottenuta viene distribuita in più piastre Petri in modo da creare un film sottilissimo di suolo incluso in agar che viene incubato a 24°C per 3 giorni. La diluizione più rappresentativa viene scelta per la conta del numero di propaguli espressi per grammo di suolo. Per la valutazione qualitativa le colonie fungine vengono classificate in funzione della forma. Almeno 30 colonie per forma vengono trasferite da agar acqua ad un substrato nutritivo come PDA per: 1) verificare la corrispondenza della specie con il simbolo di identificazione; 2) per la successiva identificazione. 77 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) I funghi endofiti Per la valutazione dei funghi con comportamento endofita, la raccolta dei campioni di suolo avviene con i criteri generali di raccolta del suolo precedentemente indicati. Tuttavia, in questo caso vengono raccolti almeno 5 kg di suolo per campione, che vengono parzialmente asciugati all’aria in ambiente fresco e sminuzzati grossolanamente a mano o con piccoli attrezzi. In funzione della specie ospite oggetto di studio, il suolo viene distribuito in vasi di 8-10 cm di diametro o in contenitori multifori con diametro minimo di 5 cm. Per le colture da seme, le piantine ottenute in sterilità vengono trapiantate nei vasi con il suolo campione, per le piante da frutto si possono utilizzare piantine micro propagate. Coltivando le piantine per 2 mesi in serra, si ottiene una buona colonizzazione radicale del campione. Dopo questa fase, le radici vengono delicatamente liberate dai residui di suolo, lavate sotto acqua corrente per almeno 10 minuti, disinfettate con una soluzione di ipoclorito di sodio all’1% per 1 minuto, risciacquate con acqua sterile e asciugate sotto cappa per almeno 15 minuti. Un numero predefinito di espianti (30-50 mm) delle radici viene posto su agar acqua e incubato per 4-5 giorni. Le colonie che partono dai singoli espianti vengono trasferite in substrato nutritivo (PDA) e incubate per almeno una settimana; le colonie risultanti vengono sottoposte a identificazione. 5.3 RICONOSCIMENTO DEI MICRORGANISMI COLTIVABILI Riconoscimento dei funghi Il riconoscimento delle specie fungine viene svolto sulla base delle comuni chiavi tassonomiche, come per il genere Fusarium ci si riferisce a Nelson et al. (1983). In alcuni casi, a conferma del riconoscimento tassonomico, viene condotta l’estrazione del DNA da micelio con l’utilizzo di Kit specifici. Il DNA estratto viene amplificato, con primer specifici della regione 18S o ITS di rDNA secondo il metodo descritto da Manici e Bonora (2007), e sequenziato. L’isolato viene successivamente riconosciuto per comparazione con altri isolati eventualmente già presenti nel database delle sequenze nucleotidiche in GenBank (Lane, 1991). Riconoscimento dei batteri azotofizzatori aerobi L’identificazione dei batteri azotofissatori liberi isolati dal suolo viene eseguita per via molecolare attraverso: • il sequenziamento del gene per il 16S rDNA; 78 Collezione di microrganismi di interesse agrario, industriale ed ambientale • il sequenziamento di una porzione del gene nifH per la nitrogenasi reduttasi, gene specifico dei batteri azotofissatori liberi. A partire dal DNA genomico, estratto dalle cellule batteriche attraverso il metodo detto del CTAB, la porzione del 16S rDNA viene amplificata utilizzando primers specifici (P0 e P6) e, successivamente, sequenziata. Riconoscimento dei rizobi Il riconoscimento dei rizobi può essere eseguito adottando mezzi biologici, biochimici o molecolari. L’ identificazione con mezzi biologici consiste nell’ eseguire saggi di nodulazione su una o più specie di leguminose al fine di individuare la specie ed, eventualmente, la sottospecie di appartenenza del rizobio isolato. Questi saggi di nodulazione vengono eseguiti ricorrendo all’allevamento di piantine in vasi contenenti agriperlite sterile; le piantine vengono ottenute dalla germinazione di semi preventivamente disinfettati con soluzione di ipoclorito di sodio al 2% e inoculati con il ceppo batterico da identificare. Dopo circa 1-2 mesi di crescita, vengono eseguiti i rilievi sulle radici per verificare la presenza o meno di tubercoli (Fig. 5.3). Fig. 5.3 – Noduli radicali prodotti da rizobio. Il saggio di nodulazione presenta lo svantaggio di richiedere molto tempo, ma fornisce indicazioni in merito all’ efficienza azotofissatrice dei ceppi. L’ identificazione con mezzi biochimici si basa sul profilo catabolico mostrato dal ceppo batterico da identificare, cioè dalla capacità o meno di utilizzare una serie di specifici composti organici. Un sistema biochimico di identificazione semplice da utilizzare e che dà risposta in un paio di giorni è il BIOLOG. Questo sistema utilizza delle piastre, molto simili a quelle impiegate nei saggi ELISA, nelle quali i 96 pozzetti contengono specifici substrati che, se catabolizzati dallo specifico ceppo da identificare, assumono una colorazione violacea (Fig. 5.4). 79 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) Fig. 5.4 – Sistema di identificazione BIOLOG. Il profilo indicato dalla colorazione dei pozzetti corrisponde ad un determinato ceppo batterico. I metodi molecolari di identificazione dei rizobi si basano, come per la maggior parte dei batteri, sulla reazione a catena della polimerasi (PCR). Primer specifici per i geni nodABC sono stati disegnati per Rhizobium leguminosarum biovar viciae (Zhang et al., 2001). Questo protocollo di PCR è sicuramente molto valido ma, purtroppo, permette l’identificazione soltanto di questa sottospecie. Diversi altri metodi molecolari, universalmente usati per la caratterizzazione e l’identificazione dei batteri, sono stati adottati anche per i rizobi. Tra essi si ricordano l’amplificazione del 16S rDNA, seguita dall’analisi di restrizione (ARDRA) o dal sequenziamento; l’amplificazione di specifici geni implicati nell’azotofissazione, seguita dalla restrizione o dal sequenziamento, ecc. Tuttavia, questi metodi sono abbastanza laboriosi nell’interpretazione dei risultati e, pertanto, non molto adatti ad essere applicati nell’identificazione routinaria. 5.4 CONSERVAZIONE Funghi tellurici I funghi colturabili del suolo possono essere conservati con vari metodi a seconda delle loro caratteristiche: • Tutti gli isolati possono essere conservati come porzioni di micelio o spore concentrate in azoto liquido (-180 °C), previo congelamento lento a -80°C per 2-3 giorni, in acqua contenente Dimethylsulfoxide al 10%. • Molti Ascomiceti, Oomiceti (Chromista) e Zigomiceti possono essere mantenuti in collezione in acqua sterile (10 ml) contenuta in provette di plastica da 15 ml, in frigorifero a 4°C. • Pochi isolati, come colonie su substrato nutritivo (Potato Sucrose Agar) a 6-8°C, in provette di vetro con tappo a vite in silicato. Per tutte le modalità di conservazione vengono seguite le indicazioni descritte da Smith e Onions (1994). 80 Collezione di microrganismi di interesse agrario, industriale ed ambientale Batteri azotofissatori liberi I ceppi isolati sono mantenuti in collezione attraverso la preparazione di glicerolati conservati a -80°C. Per questo sistema di conservazione, 1 ml di coltura del ceppo, coltivato su un substrato liquido di tipo massimo (es: RM, Trypticase Soy Broth (MacFaddin, 1985); PY (Grove e Randall, 1955) viene aggiunto, in una provetta sterile per criogenia da 2 ml con tappo a vite, ad 1 ml di glicerolo 80% (w/v) in modo da ottenere una soluzione al 40% (w/v) finale in glicerolo. La provetta si agita energicamente per mescolare il glicerolo con la coltura e si conserva a –80°C. Rizobi La conservazione dei rizobi avviene secondo le modalità generalmente adottate per tutti i batteri coltivabili aerobi. Per periodi relativamente brevi (diversi mesi) i rizobi possono essere conservati in tubi di YEM-agar posti in frigorifero (4°C). Per garantire la conservazione degli isolati per lunghi periodi (diversi anni) si ricorre alla preparazione di liofilizzati oppure, più semplicemente, alla crioconservazione a – 80°C. In questo caso le sospensioni batteriche vengono concentrate (almeno 109 C.F.U/ml) in YEM-brodo addizionato con il 20% di glicerolo. Vista l’elevata variabilità dei rizobi dal punto di vista genetico, della specificità dell’ospite e dell’efficienza azotofissatrice, è di estrema importanza conservare un numero molto elevato di ceppi affinchè sia ben rappresentata la biodiversità di questi simbionti. Pertanto, al fine di ridurre i tempi e i costi della conservazione, è anche possibile crioconservare a –80°C direttamente i tubercoli, senza ricorrere all’isolamento dei rizobi. 5.5 MICRORGANISMI NON COLTIVABILI: ISOLAMENTO E CONSERVAZIONE Studi relativi alla composizione e diversità delle comunità microbiche del suolo sono molto difficili da compiere a causa della grande difficoltà che si incontra nell’isolamento e successiva coltivazione dei diversi microrganismi. Come accennato in precedenza, solo l’1% dell’intera popolazione microbica del suolo è coltivabile, la restante parte non lo è. È questa la ragione per la quale sono stati proposti metodi biochimici di caratterizzazione delle attività metaboliche che si svolgono nel suolo, al fine di ottenere un dato sulla composizione e sull’attività microbica in maniera dedotta. È altrettanto noto però che alle stesse funzioni concorrono organismi diversi (ridondanza funzionale). Per ovviare alla difficoltà di non poter studiare l’intera popolazione microbica in vitro gli studiosi si sono orientati all’utilizzazione di metodi di biologia mole- 81 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) colare che non richiedono l’isolamento e la coltura dei microrganismi (Ausubel, 1987). Essi si basano sull’estrazione dal suolo del DNA totale, dall’osservazione del quale poter poi dedurre eventuali alterazioni in termini di richness (numero di specie presenti) ed eveness (quantità relativa di ciascuna specie). Per l’estrazione di DNA da suolo, il suolo essiccato e vagliato a 2 mm viene conservato a -20°C o a temperature inferiori. L’estrazione del DNA viene svolta con l’utilizzo dei kit per estrazione di DNA da suolo, utilizzando le istruzioni della ditta fornitrice. Il DNA estratto viene amplificato con primer specifici per il 16S rDNA e gli amplificati vengono clonati direttamente o previa separazione mediante Denaturing Gradient Gel Electrophoresis (DGGE) (Fig. 5.5). Fig. 5.5 – Immagine di una Denaturing Gradient Gel Electrophoresis (DGGE) in cui si possono effettuare valutazioni sia in termini di “richness” (numero di bande), sia di “eveness” (intensità delle bande). I frammenti provenienti dalla scelta casuale dei cloni o dalle bande elettroforetiche più significative vengono sequenziati, come descritto in Castaldini et al., (2005); la collocazione tassonomica degli organismi viene poi eseguita per comparazione con il database di sequenze nucleotidiche disponibile nel web (es. GenBank). Conservazione del genoma del suolo Parallelamente alla conservazione in collezione di singoli isolati microbici, possono essere conservati suoli campione con l’intero materiale genetico, detto “metagenoma”, per un database nazionale di campioni ambientali provenienti da siti di elevato valore agronomico o naturalistico. 82 Collezione di microrganismi di interesse agrario, industriale ed ambientale Bibliografia ALLIEVI L., A. BENEDETTI, F. PINZARI, 2003. Campionamento, preparazione e conservazione. Manuale dei metodi di Analisi Microbiologica del suolo” coord. Nannipieri P. e Picci G., Franco Angeli ed. AUSUBEL F.M., 1987. Current protocols in molecular biology, section 2.4.2. Wiley, NewYork, N.Y. BEIJERINCK M.W., 1901. Proceedings of the Koninklijke Nederlandse Akademie van Wetenschappen, 3, 586-595. BLOEM J., D. HOPKINS, A. BENEDETTI, 2006. Microbial Methods for assessing soil quality. CABI Publishing. Bloem J., Hopkins D., Benedetti A., Eds. BURGESS L.W, C.M. LIDDELL, B.A. SUMMERELL, 1988. Laboratory Manual for Fusarium research. 2nd Ed. CASTALDINI M., A. TURRINI, C. SBRANA, A. BENEDETTI, M. MARCHIONNI, S. MOCALI, A. FABIANI, S. LANDI, F. SANTOMASSIMO, B. PIETRANGELI, M.P. NUTI, N. MICLAUS, G. GIOVANETTI, 2005. Impact of Bt corn on rhizospheric and soil eubacterial communities and on beneficial mycorrhizal symbiosis in experimental microcosms. Applied and Environmental Microbiology, 71(11), 6719-6729. DHINGRA O.D., J.B. SINCLAIR, 1985. Basic Plant Pathology Methods. CRC press 355. GAMS W., 2007. Biodiversity of soil-inhabiting fungi. Biodiversity Conservation 16, 69-72. GROVE D.C., W.A. RANDALL, 1955. Assay methods of antibiotics. Medical Encyclopedia, Inc. New York, N.Y. LANE D.J., 1991. 16S/23S rRNA sequencing, 115-175. In E. Stackebrandt and M. Goodfellow (ed.), Nucleic acid techniques in bacterial systematics. JohnWiley & Sons, Chicester, United Kingdom. LYNCH J.M., A. BENEDETTI, H. INSAM, M. NUTI, K. SMALLA, V. TORSVIK, P. NANNIPIERI, 2004. Microbial diversity in soil: ecological theories, the contribution of molecular techniques and the impact of transgenic plants and transgenic microorganisms. Biology and Fertility of Soils, 40(6), 363-385. MACFADDIN, 1985. Media for isolation-cultivation-identification-maintenance of medical bacteria, vol.1. Williams & Wilkins, Baltimore, Md. MANICI L.M., P. BONORA, 2007. Molecular genetic variability of Italian binucleate Rhizoctonia spp. isolates from strawberry. European Journal of Plant Pathology, 118, 31-42. MOCALI S., D. PAFFETTI, G. EMILIANI, A. BENEDETTI, R. FANI, 2008. Diversity and dynamics of microbial communities isolated from soils treated with fumigant agents. Biology and Fertility of Soils, 44, 557-569. NANNIPIERI P., J. ASCHER, M.T. CECCHERINI, L. LANDI, G. PIETRAMELLARA, G. RENELLA, 2003. Microbial diversity and soil functions. European Journal of Soil Science, 54, 655-670. 83 PETRA 21 (1), 1-84 - COLMIA (Manuale d’uso) NELSON P.E., T.A. TOUSSON, W.F.O. MARASAS, 1983. Fusarium Species. An Illustrated Manual for Identification. Pennsylvania, PA: The Pennsylvania State University Press. 190. NEWTON J.W., P.W. WILSON, R.H. BURRIS, 1953. Direct demonstration of ammonia as an intermediate in nitrogen fixation by Azotobacter. Journal of Biological Chemestry, 204, 445-451. RENNIE R. 1981. A single medium for the isolation of acetylene-reducing (dinitrogen-fixing) bacteria from soils. Canadian Journal of Microbiology, 27, 8-14. SMITH D., A.H.S. ONIONS, 1994. The Preservation and Maintainance of Living Fungi. IMI technical handbooks No. 2 CABI Publishing 2nd Revised edition. ZACCARDELLI M., A. DEL GALDO, M. PARISI, I. GIORDANO, 2002. Caratterizzazione molecolare di isolati di Rhizobium leguminosarum biovar viciae e loro impiego, in pieno campo, per il miglioramento produttivo del pisello proteico. Agroindustria, 1 (3), 153-158. ZHANG X.X., B. KOISIER, B. PRIEFER, 2001. Genetic diversity of indigenous Rhizobium leguminosarum bv. viciae isolates nodulating two different host plants during soil restoration with alfalfa. Molecular Ecology, 10, 2297-2305. 84
Scaricare