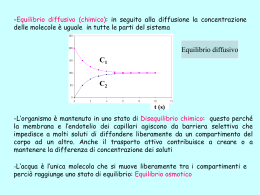
Chimica e laboratorio Solubilità e proprietà colligative Classi quarte Docente: Luciano Canu Anno Scolastico 2008/2009 Prerequisiti Conoscere il concetto di energia Energia cinetica Energia potenziale Unità di misura dell’energia Conoscere i legami chimici primari e secondari Sapere che a ciascun tipo di legame è associata una energia di legame Conoscere i passaggi di stato e le energie associate Sapere cosa è la mole Saper descrivere gli stati della materia Conoscere le caratteristiche dei diversi tipi di sostanze 2 Obiettivi Comprendere e saper descrivere i meccanismi di solubilizzazione di sostanze diverse 3 Soluzioni liquide Sistemi omogenei in cui un soluto è sciolto in un solvente Miscuglio formato da almeno due componenti diversi con proprietà, fisiche e chimiche costanti in ogni suo punto Le proprietà di una soluzione dipendono dai componenti, dalla loro concentrazione e sono, in genere, diverse da quelle dei componenti puri Soluti Liquidi Aeriforme Solido 4 Soluto e solvente In genere si distinguono Solvente, liquido e/o in maggiore quantità Soluto, minore quantità Si interpreta il fenomeno come se il soluto si disperda uniformemente nel solvente 5 Terminologia sulle concentrazioni Esistono dei termini qualitativi per indicare le concentrazioni delle soluzioni Diluita (quando contiene “poco” soluto) Concentrata (quando contiene “molto” soluto) Un altro termine è più preciso Satura (contiene la massima quantità di soluto) Viene chiamato anche punto di saturazione Quantità di solvente Temperatura 6 Solubilità È la quantità massima in grammi di una sostanza che può essere disciolta in 100 grammi di solvente ad una specifica temperatura 7 Solubilità (qualitativo) Dipende dalla sostanza (soluto) Temperatura Pressione (nei solidi non influisce) g di soluto in 100 g di H2O Di diverse sostanze In diverse condizioni Solidi (sostanze ioniche) in acqua (solventi polari) KNO3 NaNO3 NH4Cl NaCl Ce2(SO4)3 8 T Gas in acqua (solventi polari) Dipende dal tipo di gas (soluto) Dipende dalla temperatura Aumentando la temperatura diminuisce la solubilità del gas Dipende dalla pressione Aumentando la pressione g di soluto in 100 g di H2O Solubilità (qualitativo) NH3 O2 del gas sul liquido aumenta la solubilità 9 T Interpretazione del fenomeno Nei due componenti A e B puri della soluzione ci sono le normali interazioni A---A B…B Quando si forma la soluzione queste interazioni vengono, in parte, sostituite da interazioni A~~B Quando due sostanze possono formare una soluzione? Quando il sistema può raggiungere un livello di energia più basso (maggiore stabilità) 10 Solubilizzazione + Composti ionici Le molecole d’acqua si orientano sulla superficie del solido ionici L’acqua cerca di penetrare nel reticolo ionico scalzando gli ioni Gli ioni separati sono schermati da un certo numero di molecole d’acqua Il fenomeno viene definito idratazione (solvatazione) - + + - + - + - + + + - + - +Solido - ionico - + - + - + + - + + +- - + 11 Solubilizzazione Sostanze molecolari si sciolgono in acqua per Formazione di legami idrogeno Interazioni dipolo-dipolo Tutte le sostanze che possiedono gruppi OH si sciolgono in acqua formando legami idrogeno Gruppo OH Etanolo Glucosio H H O H C C H H etanolo H O H H 12 Glucosio in acqua GLUCOSIO H O + H 13 Elettroliti Tutte le sostanze che si dissociano in ioni quando sono poste in un liquido sono denominate appunto elettroliti Sali solubili (composti ionici) Acidi (composti covalenti polari) Basi (composti covalenti polari) Elettroliti possono essere Forti, dissociazione ionica completa Conducono molto bene la corrente Deboli, dissociazione ionica parziale Conducono parzialmente la corrente 14 dissociazione Dissociazione di composti ionici NaCl(s) + Na (aq) + Cl (aq) NH4Cl(s) NH4+(aq) + Cl-(aq) Al2(SO4)3(s) 2Al3+(aq) + 3SO42-(aq) 15 Verifica scritta Domande e risposte Domanda n° 5 – Le soluzioni Le soluzioni. Descrivi le soluzioni liquido-liquido e quelle solido-liquido. Spiega qual è la terminologia che si utilizza nel campo delle soluzioni, indica tutti i termini specialistici e ciascuna definizione. Indica che tipi di sostanze si sciolgono in acqua e per quale motivo. Spiega cosa si intende per solvatazione e idratazione. Una soluzione è un sistema omogeneo in cui tutte le particelle dei componenti sono mischiate tra loro così intimamente che Non è possibile separarle con metodi semplici, di tipo meccanico; sono necessari sistemi fisici o chimico-fisici Spesso uno dei due componenti deve essere sacrificato durante la separazione Non è possibile individuare con facilità i componenti del sistema Il sistema presenta la stessa composizione con qualunque tipo di campionatura 17 Domanda n° 5 – Le soluzioni [2] Le soluzioni possono avvenire perché un certo componente dimostra affinità elettrostatica con l’altro Cioè si formano interazioni tra le due sostanze; tali interazioni sono simili ed altrettanto vantaggiose (se non di più) di quelle tra due individui della stessa specie Una soluzione è formata da almeno due componenti Solvente, è generalmente liquido ed in quantità maggiore Soluto, è il componente meno preponderante 18 Domanda n° 5 – Le soluzioni [3] Le soluzioni possono essere definite Diluite, se il soluto non è in quantità eccessive Concentrata, se il soluto è presente in concentrazioni elevate ma è possibile scioglierne ancora Satura quando la soluzione contiene la più alta quantità di soluto per quella temperatura La solvatazione (idratazione) è Un fenomeno in cui tutte le particelle di un solido o di un liquido (ioni o molecole polari) sono circondate (coordinate) da un certo numero di molecole di solvente (acqua) che scherma e mantiene disperso il soluto 19
Scaricare