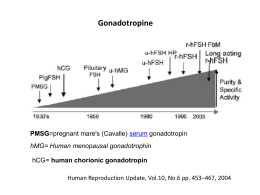
1. Ormone stimolante il follicolo: identificazione della molecola, struttura, meccanismo d’azione, attività sull’ovaio Antonio Stanziano, Filippo M. Boscia SOMMARIO DEL CAPITOLO 1.1 Cenni storici sull’identificazione della molecola 3 1.2 Struttura della molecola 4 1.2.1 Struttura e gruppi glicosidici delle subunità dell’FSH 1.3 Metabolismo e escrezione 1.4 Regolazione della biosintesi e della secrezione 5 5 6 1.4.1 Controllo ipotalamico 6 1.4.2 Feedback degli steroidi gonadici 6 1.4.3 Sistema attivina-inibina-follistatina 6 1.5 Il recettore 6 1.5.1 Vie di trasduzione del segnale del recettore gonadotropinico: i secondi messaggeri 1.5.2 Desensibilizzazione 1.6 Funzione dell’ormone follicolo-stimolante 1.6.1 Sviluppo follicolare Bibliografia 6 7 7 7 9 1.1 Cenni storici sull’identificazione della molecola I primi passi verso l’utilizzazione clinica delle gonadotropine si compirono alla metà degli anni ‘20, quando Zondek e Smith, separatamente ma quasi simultaneamente, scoprirono che la funzione gonadica era controllata dalla ghiandola ipofisaria. Zondek dimostrò che il trapianto dell’ipofisi anteriore causava un rapido sviluppo degli organi sessuali in animali prepuberi. Più o meno nello stesso periodo, Smith e il suo gruppo dimostrarono che l’ipofisectomia causava un arresto della maturazione sessuale in animali prepuberi e una rapida regressione dei caratteri sessuali in animali adulti (1). Durante gli anni ‘30 e ‘40, furono ricavati estratti di gonadotropine da differenti tessuti e/o liquidi biologici animali; questi estratti furono somministrati a esseri umani per stimolare la funzione ovarica. Tuttavia ci si rese conto immediatamente che questi preparati rivestivano un’importanza clinica molto limitata in quanto le gonadotropine dei non primati causavano negli umani una rapida risposta immunologica che neutralizzava il loro effetto terapeutico (1). Questo indirizzò gli sforzi dei ricercatori verso tentativi di isolamento delle gonadotropine da tessuti umani. Ricerche intensive in questo campo furono eseguite contemporaneamente in Italia, Inghilterra, Scozia, Svizzera e Svezia. Alla fine degli anni ‘50 e agli inizi degli anni ‘60, questi tentativi furono coronati dal successo. All’Università di Uppsala, Gemzell e i suoi collaboratori riportarono nel 1958 il primo successo nell’induzione dell’ovulazione utilizzando gonadotropine ipofisarie umane (hPG) e nel 1960 il primo caso di gravidanza (2, 3). Indicativamente nello stesso periodo, Bettendorf riuscì a estrarre un potente agente gonadotropinico dall’ipofisi umana e riferì sulla prima esperienza clinica con quest’ormone (4). Lunenfeld e il suo gruppo, lavorando con estratti urinari di gonadotropine umane menopausali (hMG), ottennero l’ovulazione e la gravidanza in donne anovulatorie. I loro risultati furono riportati in occasione di vari convegni scientifici e medici a partire dal 1959, Parte I. Fisiologia dell’ormone stimolante il follicolo 3 4 furono pubblicati nel 1963 e tuttora rappresentano un modello per le terapie di induzione dell’ovulazione (5). Nel 1964 Donini e collaboratori riuscirono a estrarre e a purificare una gonadotropina ad azione simile all’ormone follicolo-stimolante (FSH) e luteinizzante (LH) dalle urine di donne in menopausa. In seguito, s’intrapresero studi clinici su vasta scala in nume rosi centri in tutto il mondo e i relativi risultati furono riportati in letteratura. Rivestivano particolare importanza le relazioni di Bettendorf e Gemzell che riuscirono a indurre l’ovulazione e la gravidanza in donne ipofisectomizzate (6, 7). L’introduzione di dosaggi ormonali rapidi e affidabili e, più tardi, la disponibilità di sonde a ultrasuoni in grado di visualizzare e misurare i follicoli ovarici, resero accurato e obiettivo il monitoraggio della terapia con gonadotropine e migliorarono i risultati del trattamento. Negli anni ‘80, i programmi di fecondazione in vitro (FIV) eseguiti su vasta scala, si avvalsero dei principi e dell’esperienza maturata con l’induzione dell’ovulazione nelle pazienti anovulatorie e arricchirono di nuove e importanti intuizioni la comprensione del meccanismo di stimolazione ovarica con gonadotropine. L’FSH estratto dall’urina umana e impiegato come alternativa all’hMG, divenne disponibile in commercio verso la fine degli anni ‘80 (8, 9). Grazie alla tecnologia del DNA ricombinante e alle tecniche altamente sofisticate delle colture cellulari, vengono oggi preparate gonadotropine con DNA ricombinante. Ciò che attualmente richiederebbe 200 milioni di litri di urine viene prodotto sfruttando l’ingegneria gene- tica in terreni di coltura chimicamente definiti, contenenti solo una piccola frazione di quel volume (10) (Tabella 1.1). 1.2 Struttura della molecola L’FSH è una glicoproteina eterodimerica di 35–45 KD, composta da due diverse subunità proteiche (α: 92 AA; β: 111 AA) unite da legame non covalente. All’aminoacido asparagina (Asn) in posizione 52 e 78 della subunità α si legano due strutture glucidiche, mentre nella subunità β le due catene glucidiche sono legate all’Asn in posizione 7 e 24. La subunità β caratterizza la specificità d’azione dell’FSH mentre la subunità α è presente anche nell’LH, nell’hCG e nell’ormone che stimola la tiroide (TSH). Le due subunità sono tra loro articolate da una porzione della subunità β (denominata seat belt) che si avvolge attorno alla subunità α e che svolge un ruolo primario nel legame recettore-ormone (Figura 1.1) (12). Le informazioni sul metabolismo degli ormoni gonadotropi sono scarse. È stato dimostrato che preparati purificati di hFSH, iniettati per endovena negli esseri umani, hanno emivite sieriche di 180-240 minuti. È stato stabilito che la clearance metabolica media (MCR) dell’hFSH nelle donne è di 14 mL/min e che solo il 3–10% della produzione giornaliera di FSH e LH viene escreto nelle urine in una forma biologicamente attiva, ma riflette la percentuale di secrezione gonadotropa in condizioni fisiologiche e patologiche (12–14). Tabella 1.1 Tappe fondamentali nello sviluppo della terapia con gonadotropine. Anni ’20 e ’30 1. Scoperta del principio gonadotropo che controlla la funzione ovarica. Anni ’30 e ’40 2. Ulteriori informazioni sulla fisiologia dell’asse ipotalamo-ipofisi-ovaio. 3. Estrazione di gonadotropine da fonti animali e da urine di donna gravida Anni ’50 4. Estrazione di gonadotropine da ipofisi umane e da urine di donne in postclimaterio. Anni ’60 5. Estrazione su vasta scala e processo di purificazione delle gonadotropine umane. 6. Studi clinici sull’induzione dell’ovulazione utilizzando l’hPG e l’hMG. 7. Introduzione di dosaggi ormonali veloci e affidabili per il monitoraggio della terapia. Anni ’70 8. Impiego clinico su vasta scala delle gonadotropine nelle pazienti infertili. 9. Introduzione dell’ecografia per il monitoraggio della terapia di induzione dell’ovulazione. Anni ’80 10. Terapia di superovulazione controllata impiegata nei programmi FIVET Anni ’90 11. Impiego clinico di FSH urinario altamente purificato (FSH-u, 1993) e produzione con tecniche di ingegneria genetica di FSH ricombinante (FSH-r, 1995). Parte I. Fisiologia dell’ormone stimolante il follicolo Figura 1.1 Ormone stimolante il follicolo. Mod da (11). di acido sialico accorciano notevolmente l’emivita della molecola con effetto minimo sulla capacità di agire a livello recettoriale. Il risultato è che le attività biologica dell’FSH umano privato di acido sialico è molto ridotta in vivo, ma è conservata in vitro sui recettori di membrana e sulle cellule bersaglio isolate. Inoltre, la rimozione dei gruppi dei carboidrati legati all’azoto riduce notevolmente la capacità di attivare le cellule bersaglio nei testicoli e nelle ovaie ma incide solo minimamente sul suo legame con i siti recettonali. Per esempio, l’FSH perde virtualmente la sua capacità di stimolare l’attività dell’adenilato-ciclasi, pur mantenendo un’alta affinità di legame per i recettori delle gonadi dopo la rimozione quasi totale dei loro gruppi di oligosaccaridi legati all’azoto. Come già anticipato, l’FSH deglicossilato può agire in vitro come antagonista competitivo dell’azione degli ormoni glicoproteici per quanto riguarda la produzione di adenosin monofosfato ciclico (cAMP) e di altri secondi messaggeri e, in misura minore, per la produzione di ormoni steroidei (16–19). 1.2.1 Struttura e gruppi glicosidici delle subunità dell’FSH 1.3 Metabolismo e escrezione Le subunità dell’FSH presentano dei residui di carboidrati, con due gruppi di oligosaccaridi sulla subunità α (Asn 52 e Asn 78) e β (Asn 13 e Asn 30). I principali gruppi glicosidici sono associati all’Asn o aminate, come per esempio la N-acetilglucosamina accoppiata a specifici residui di Asn a livello apoproteico. Il contenuto di zucchero dell’FSH supera di poco il 16%. I residui monosaccaridici includono la N-acetilglucosamina, il mannosio, il galattosio, il fucosio, la glucosarnina, la N-acetilgalattosamina e l’acido sialico. Ogni oligosaccaride è suddiviso in ramificazioni sia in modo biantennare che triantennare ed è marcatamente eterogeneo nelle ramificazioni periferiche, le quali terminano spesso con acido sialico e fucosio e occasionalmente con il galattosio (12–14). Da uno studio sull’eterogeneità dei residui glicosidici dell’FSH e sulla sintesi principale dell’ormone, è emerso che ci sono modelli di glicosilazione specifici sia per i tessuti che per l’ormone stesso (15). Alla luce di ciò, un recente lavoro suggerisce come una serie di glicosiltransfensferasi specifiche tissutali siano situate all’interno delle cellule gonadotrope e svolgano la funzione di mediare la sintesi di questi differenti gruppi di carboidrati (16). Nell’FSH sono localizzati 5 residui di acido sialico e le variazioni nei punti isoelettrici (pIs) vanno da 4,5 a 5 in relazione alla differente composizione dei residui di carboidrati. La rimozione enzimatica dei residui terminali Le proprietà molecolari dell’FSH circolanti sono generalmente simili a quelle dell’ormone estratto dall’ipofisi. La gonadotrina plasmatica mostra piccole differenze nelle dimensioni da quella ipofisaria, ma non c’è alcuna prova convincente dell’esistenza di un pre-ormone più grande o di una forma attiva più piccola di FSH. Sono stati osservati sottili variazioni nelle proprietà della forma circolante e ipofisaria negli animali dopo modificazioni del feedback steroideo della gonade sull’ipofisi. Ad esempio nel ratto, il trattamento con androgeni aumenta l’attività biologica dell’FSH ipofisario relativamente alla sua immunoreattività e riduce la velocità di eliminazione di FSH dal circolo. Nella scimmia rhesus, l’ovariectomia è seguita da cambiamenti nelle proprietà della molecola, mostrando un leggero incremento della dimensione e un rallentamento della eliminazione dal circolo. Le aumentate dimensioni dell’FSH ipofisario vengono rinormalizzate dalla terapia sostitutiva con estrogeni negli animali castrati. È probabile che questi cambiamenti qualitativi regolati dagli estrogeni dipendano dall’alterazione nella composizione dei carboidrati e, in modo specifico, dalla quantità di residui di acido sialico contenuti nella struttura. Il contenuto di acido sialico ha un effetto marcato sulla velocità di eliminazione dal circolo e influenza anche la dimensione molecolare come determinato dall’analisi di filtrazione (14). 1. Ormone stimolante il follicolo: identificazione della molecola, struttura, meccanismo d’azione, attività sull’ovaio 5 6 1.4 Regolazione della biosintesi e della secrezione Nel ciclo riproduttivo, la biosintesi e la secrezione dell’FSH sono strettamente regolate. L’espressione del mRNA specifico e l’increzione di FSH sono modulate da fattori ipotalamici (dall’ormone rilasciante la gonadotropina (GnRH) in particolare), fattori intraipofisari (principalmente i peptidi attivina e follistatina) e dal feedback gonadico (ormoni sia peptidici sia steroidei). I livelli di modulazione possono essere diversi, includendo: 1. alterazioni nella velocità di trascrizione, 2. stabilizzazione dell’mRNA, 3. aumentata sintesi delle subunità delle proteine, 4. modificazioni post-traduzionali come la glicosilazione 5. cambiamenti nel numero di cellule gonadotrope. In base allo stato riproduttivo, gli estrogeni possono aumentare o diminuire l’espressione del gene delle gonadotropine (21). 1.4.3 Sistema attivina-inibina-follistatina Negli ultimi dieci anni sono stati isolati dal fluido follicolare tre fattori proteici, inibina, attivina e follistatina, così definiti sulla base dei loro effetti selettivi sull’espressione del gene dell’FSH. Come suggerito dai loro nomi, l’inibina riduce e l’attivina stimola la funzione della cellula gonadotropa. Anche la follistatina sopprime l’espressione del gene FSH con una potenza di circa un terzo rispetto all’inibina (22). 1.5 Il recettore 1.4.1 Controllo ipotalamico Il controllo ipotalamico dell’espressione dell’FSH si ha in primo luogo attraverso l’azione del GnRH che è normalmente rilasciato in maniera pulsatile, piuttosto che continuo. Durante l’infusione di GnRH si ha un unico progressivo innalzamento di FSH plasmatico. L’assenza di una risposta precoce dell’FSH potrebbe riflettere la mancanza di scorte di FSH stesso, immediatamente disponibili, in forma di granuli all’interno delle cellule gonadotrope, oppure la necessità di avere stimoli da fattori esclusivamente specifici per l’FSH. Una frequenza ottimale degli stimoli pulsatili di GnRH sull’ipofisi è essenziale per mantenere normali i livelli plasmatici di FSH e per far sì che la sua concentrazione circolante si abbassi quando la frequenza dei “picchi” di GnRH è troppo bassa ma anche quando lo stimolo del GnRH è troppo frequente o addirittura continuo (20). 1.4.2 Feedback degli steroidi gonadici La biosintesi e la secrezione di FSH è modulata da due sistemi di feedback gonadici: il sistema degli steroidi gonadici e il sistema attivina-inibina-follistatina. Le azioni di questi due sistemi si sovrappongono all’azione stimolatoria del GnRH pulsatile. Dal momento che la gonadectomia porta ad un rapido aumento nei livelli della gonadotropina nel siero, l’effetto generale di questi sistemi può essere visto come inibitorio. Parte I. Fisiologia dell’ormone stimolante il follicolo Il recettore per l’FSH è caratterizzato da un esteso dominio extracellulare con una regione ricca in leucina e multipli siti potenziali di glicosilazione. È codificato da un gene lungo più di 85 chilobasi, contiene 10 esoni, 9 dei quali codificano per il dominio extracellulare (23). È localizzato sulla membrana plasmatica delle cellule della granulosa e della teca (nell’ovaio) e delle cellule del Sertoli e del Leydig (nel testicolo) (24). Esso contiene 678 aminoacidi e la sua attivazione coinvolge il sistema dell’adenilatociclasi nel regolare sia la steroidogenesi che la gametogenesi (25). Il meccanismo d’azione delle gonadotropine nell’ovaio è analogo a quella nel testicolo. L’interazione fra recettore e ormone porta a un cambiamento nella conformazione del recettore stesso, che a sua volta attiva un sistema segnale accoppiato alla proteina G e associato alla membrana. È interessante notare che il legame e l’attivazione del recettore con la trasduzione del segnale intracellulare sono momenti distinti che possono essere separati sperimentalmente e potrebbero essere influenzati in modo differente in condizioni patologiche. 1.5.1 Vie di trasduzione del segnale del recettore gonadotropinico: i secondi messaggeri Il recettore dell’FSH è accoppiato a un sottogruppo di proteine regolatrici che legano il guanosintrifosfato (GTP) o proteine G, che attivano il sistema della protein-chinasi A (PKA). Le proteine G sono eterotrimeri formate da una subunità a (Gsa) stimolatoria dotata di attività GTPasica, associata ad un complesso formato da una catena b e da una catena g. L’interazione della gonadotropina con il suo recettore porta all’attivazione del recettore stesso, presumibilmente attraverso l’induzione di cambiamenti conformazionali nella struttura recettoriale. La formazione del complesso gonadotropina-recettore determina la sostituzione del guanosindifosfato legato alla subunità a con il GTP, il che porta alla dissociazione della subunità a della proteina G dal complesso b. La subunità a libera, quindi, lega l’adenilato-ciclasi che converte l’adenosina trifosfato (ATP) in cAMP, incrementando i valori intracellulari dello stesso che attivano quindi la PKA. La PKA modula la funzione di una grande varietà di proteine intracellulari, attraverso la fosforilazione di specifici residui di serina e treonina. Mentre la maggior parte dei dati indica il cAMP come il principale mediatore dell’azione dell’FSH, recenti evidenze suggeriscono che potrebbe anche essere coinvolta la via della protein-chinasi C (PKC). In questa via, una differente proteina G è legata al recettore gonadotropinico. L’attivazione di questo complesso (Gq) attiva la fosfolipasi C che scinde i fosfolipidi di membrana per produrre inositolo 1, 4, 5 trifosfato (IP3) e 1, 2 diacilglicerolo (DAG). L’IP3 determina il rilascio di calcio sequestrato nello spazio intracellulare incrementando quindi i livelli di calcio citosolico; il DAG attiva la protein-chinasi C. Quindi, il recettore può stimolare entrambe le vie della protein-chinasi A e C (Figura 1.2) (26–28). Figura 1.2 L’interazione con il recettore attiva percorsi multipli di traduzione del segnale. AC ATP Gs bg Gg PLCb PI-4,5P2 bg cAMP DAG PKA PKC P Proteina Via de cAMP Mod da (28). InsP3 P Proteina Via de DAG/PKC Ca2+ 1.5.2 Desensibilizzazione In aggiunta all’attivazione cellulare, il legame dell’ormone al suo recettore dà vita anche a un processo chiamato desensibilizzazione che riduce la sensibilità cellulare a stimolazioni ripetute o continue. La desensibilizzazione omologa è ottenuta con un meccanismo veloce, chiamato “disaccoppiamento” che avviene in pochi minuti, oppure attraverso un processo più lento chiamato down regulation. Nel “disaccoppiamento” le modificazioni recettoriali, post-traduzionali, si traducono in una ridotta attività senza modificazioni nel numero dei recettori. Mentre le modificazioni esatte non sono state ancora delucidate, si sa che il “disaccoppiamento” richiede la presenza della regione C terminale del recettore (intracellulare). La down regulation è ottenuta attraverso un aumento della frequenza di internalizzazione recettoriale e accumulo lisosomiale che risulta in un’aumentata velocità di degradazione. Nella seconda fase della down regulation, che avviene dopo tre o quattro ore, la biosintesi recettoriale si riduce (26, 27). 1.6 Funzione dell’ormone follicolo-stimolante L’FSH, come suggerito dal nome, è il principale promotore dello sviluppo e maturazione del follicolo. Il normale sviluppo follicolare e la steroidogenesi richiedono una sequenza ben definita di modificazioni ormonali. L’abilità dell’FSH di controllare la crescita e la differenziazione follicolare dipende dalla sua capacità di determinare molteplici effetti simultaneamente. Esperimenti compiuti in vivo su roditori suggeriscono che l’FSH è in grado di aumentare il numero dei propri recettori nelle cellule della granulosa. Mentre l’estradiolo da solo non sembra avere effetto sulla distribuzione, sul numero e sull’affinità dei recettori per l’FSH sulle cellule della granulosa è stato dimostrato che gli estrogeni in sinergia con l’FSH incrementano il numero totale dei recettori per l’FSH presenti sulle cellule della granulosa (29). 1.6.1 Sviluppo follicolare La follicologenesi rappresenta un meccanismo fisiologico dagli aspetti molteplici, non completamente cono- 1. Ormone stimolante il follicolo: identificazione della molecola, struttura, meccanismo d’azione, attività sull’ovaio 7 8 sciuti e di difficile indagine. A differenza di quanto si è per lungo tempo creduto, la follicologenesi, nel suo insieme, si è rivelata sempre più un processo dinamico e lineare, assimilabile forse alla stessa gametogenesi maschile e dotata, comunque, di ritmi e frequenze certamente più intensi della cadenza dei cicli estrali. In generale, possiamo distinguere una follicologenesi basale (gonadotropino-indipendente), praticamente continua e una follicologenesi tonica (gonadotropino-dipendente) più o meno intermittente, alla quale accedono solo follicoli di definite dimensioni (di classe 5, diametro >4 mm) (30). Questi ultimi, a loro volta, si differenzieranno in follicoli destinati a regressione più o meno precoce e follicoli evolutivi (dominanti ovulatori e dominanti anovulatori). Secondo tale opinione, i follicoli di classe 5 della fase luteinica tardiva costituiscono la coorte da cui i follicoli destinati a ovulare nel ciclo successivo saranno reclutati. Nella fase gonadotropino-indipendente, le cellule della teca interna del follicolo acquisiscono recettori per l’LH, mentre le cellule della granulosa conseguono recettori per l’FSH. In tal modo, diventano capaci di rispondere a una stimolazione gonadotropa e di sintetizzare estrogeni. I follicoli primordiali si formano quasi con certezza senza l’influenza della stimolazione gonadotropinica. Questo primo periodo della follicologenesi è ancora in parte sconosciuto, ed è sotto il controllo di fattori intraovarici ed intrafollicolari. Il secondo periodo dello sviluppo follicolare dipende essenzialmente dalle gonadotropine ipofisarie. Nel complesso meccanismo dello sviluppo follicolare, un ruolo importante sembra essere svolto dai neurotrasmettitori contenuti nei nervi ovarici. Le strutture nervose dell’apparato genitale femminile di molti mammiferi contengono, oltre ai neurotrasmettitori tradizionali, acetilcolina e noradrenalina o norepinefrina (NE), neuropeptidi ritenuti trasmettitori e/o modulatori dell’impulso nervoso; in particolare, la NE e il peptide intestinale vasoattivo (VIP) promuovono l’accrescimento follicolare, inducendo la formazione dei recettori per l’FSH sui follicoli neoformati. I neurotrasmettitori agiscono sulla steroidogenesi ovarica, mentre entrambi stimolano la secrezione di progesterone e di androgeni; soltanto il VIP stimola la produzione di estradiolo (31). La crescita gonadotropino-dipendente, è esponenziale con un incremento di circa 160 volte del patrimonio delle cellule della granulosa e risulta in un aumento delle dimensioni del follicolo, da 5 a 20 mm di diametro. Il follicolo, perciò, è disposto in modo da trascorrere circa Parte I. Fisiologia dell’ormone stimolante il follicolo 5 giorni in ognuna delle rimanenti classi follicolari (da 6 a 8) prima dell’ovulazione. È durante questo periodo che la selezione follicolare e la dominanza vengono portate a termine. Nella fase follicolare precoce, l’FSH stimola l’attività aromatasica delle cellule della granulosa, determinando un incremento della concentrazione degli estrogeni follicolari (32). L’incremento degli estrogeni fa aumentare la captazione follicolare dell’FSH e perciò aumenta la sensibilità del follicolo all’azione dell’FSH. Dalla fase follicolare intermedia, un follicolo (probabilmente per puro caso) ha prodotto quantità relativamente più elevate di estrogeni degli altri follicoli appartenenti alla stessa coorte (Figura 1.3). La produzione di estrogeni da parte del follicolo dominante è responsabile dell’asimmetria nella concentrazione estrogenica, osservata nella vena effluente ovarica dal 5° al 7° giorno della fase follicolare. L’aumentata formazione dell’antro e l’acquisizione dei recettori per l’LH devono essere anticipate. Il follicolo dominante, perciò, si trova in un’ordinata sequenza di eventi in cui l’FSH e gli estrogeni stimolano la crescita, la formazione dell’antro e la comparsa dei recettori per l’LH. Il drammatico aumento nella produzione di estrogeni da parte del follicolo dominante, durante la seconda metà della fase follicolare è associato a una caduta dei livelli circolanti di FSH. Di conseguenza, i follicoli non dominanti della stessa coorte non riescono a crescere. Questi follicoli sono caratterizzati da una ridotta sintesi di estrogeni così come da elevate concentrazioni di androgeni intrafollicolari e da una ridotta sensibilità all’FSH. Ci sono cambiamenti tecali associati allo sviluppo del follicolo dominante. Infatti, dal 7° giorno del ciclo, il follicolo destinato a ovulare è circondato dalla teca che selettivamente risponde di più all’LH della teca degli altri follicoli, appartenenti alla stessa coorte in via di sviluppo. Dal 9° giorno della fase follicolare, la vascolarizzazione della teca del follicolo dominante è raddoppiata rispetto a quella degli altri follicoli e questo facilita l’aumentato rilascio di LH e lipoproteine a bassa densità (LDL) alla teca e di FSH alle cellule della granulosa (30, 33). Si suppone che il follicolo dominante produca una proteina in grado di inibire l’aromatasi dei follicoli ipsilaterali adiacenti più piccoli e un effetto simile si osserva nell’ovaio controlaterale. Il follicolo dominante allora esercita un ruolo attivo nel creare le condizioni più favorevoli per se stesso. Altri ritengono che la comparsa del follicolo dominante sia una conseguenza dell’arresto della crescita degli elementi più piccoli della coorte follicolare. Secondo questo punto di vista, la relativa incapacità di crescere degli elementi non dominanti della coorte non Figura 1.3 Fase di crescita follicolare gonadotropino-dipendente (esponenziale): conversione dalla classe 1 fino a follicolo di classe 5, M: mesi; Gn: gonadotropine; LH: ormone luteinizzante; FSH: ormone follicolo-stimolante. CLASSE 1 CLASSE 2 CLASSE 3 CLASSE 4 CLASSE 5 gio rni Fase di crescita tonica 1-2 10 Diametro follicolare (mm) 2-5 0,5-0,9 0,2-0,4 25 giorni i Fase di crescita dipendente dalle gonadotropine iorn 15 g Antrale precoce i iorn 20 g 0,15 Preantrale LH Ovulo Ovulo M 1° ciclo Ovulo M 2° ciclo FSH Ovulo M 3° ciclo Mod da (30). riflette un effetto attivo sulla parte del follicolo dominante, ma piuttosto riflette un ambiente endocrino in via di deterioramento, dove solo il follicolo dominante sopravvive. Questo effetto differenziale potrebbe rispecchiare la relativa incapacità dei follicoli più piccoli di sopravvivere alla caduta dei livelli di FSH che avvengono nella fase follicolare intermedia, probabilmente in risposta all’incremento del feedback negativo ovarico. Ancora di più, l’amplificata risposta all’FSH sembra essere associata al marcato incremento nell’indice mitotico delle cellule della granulosa in via di sviluppo. Queste conclusioni sono in accordo con le osservazioni in cui si è dimostrato che le cellule della granulosa dei follicoli più grandi sono significativamente più sensibili all’FSH, per ciò che concerne l’attività aromatasica, in confronto ai follicoli più piccoli (34). L’FSH regola anche la produzione cellulare di inibina durante la fase follicolare. Quando la maturazione follicolare progredisce, inizia la produzione di progesterone nelle cellule della granulosa, sotto l’influenza della secrezione dell’LH pre-ovulatorio. Questo concetto è supportato dai risultati ottenuti in donne con deficit di gonadotropine trattate con FSH umano ricombinante. Mentre in queste donne si osserva una precoce crescita follicolare e bassi livelli di produzione di estrogeni, gli alti livelli di estrogeni richiesti per l’induzione del picco di LH e la maturazione finale del follicolo, non sono mai raggiunti. Quindi, sebbene sia richiesto solo l’FSH per la follicologenesi precoce, una completa steroidogenesi ovarica è dipendente dall’LH (35–37). Bibliografia 1. Alberda Ath, Gan RA, Vemer HM, eds. Pioneers in vitro fertilization. Carnforth: Parthenon Publishing. 1993. 2. Gemzell CA, Diczfalusy E, Tillinger KG. Clincal effect of human pituitary follicle stimulating hormone (FSH). J Clin Endocrinol 18: 1333–1348, 1958. 3. Gemzell CA, Diczfalusy E, Tillinger KG. Human pituitary follicle-stimulating hormone. Clinical effect of a partly purified preparation. Ciba Foundation Colloquia Endocrinol 13: 191–198, 1960. 4. Bettendorf G. Ovarian stimulation in hypophysectomized patients by human gonadotropins. Proc. 5 World Congress on Fertility and Sterility. Excerpta 133: 53–54, 1966. 5. Lunenfeid B. Treatment of anovulating by human gonadotropins. Int J Gynecol Obstet 1: 153 –158, 1963. 6. Bettendorf G. Ovarian stimulation in hypophysectomized 1. Ormone stimolante il follicolo: identificazione della molecola, struttura, meccanismo d’azione, attività sull’ovaio 9 10 patients by human gonadotropins. Proc. 5° World Congress on Fertility and Sterility. Excerpta 133: 53–57, 1966. 7. Gemzell CA. Induction of ovulation in patients foliowing removal of pituitary adenoma. Am J Obstet Gynecol 117: 955–961, 1973. 8. Couzinet B, Lestrat N, Brailly S, et al. Stimulation of ovarian follicular maturation with pure follicle stimulating hormone in women with gonadotropin deficiency. J Clin Endocrinol Metab 66: 552–556, 1988. 9. Devroy P, Naaktgeboren N, Traey E, et al. Hormonal evaluation of failed ovarian stimulation in an in vitro fertilization program. IV World Conference on In Vitro Fertilization, Melbourne, Abstract p 6, Australia 1985. 10. Devroy P, Van Steirteghem A, Mannaerts B, Coelingh Bennink H. Successful in-vitro fertilization and embryo transfer after treatment with recombinant human FSH. Lancet 339: 1170, 1992. 11. Lapthorn AJ, Harris DC, Littlejohn A, et al. Crystal structure of human chorionic gonadotropin. Nature 369: 455–461, 1994. 12. Pierce JG, Parsons TE. Glycoprotein hormones: Structure and function. Annual Rev Biochem 50: 465–495, 1981. 13. Ryan RI, Charlesworth MC, McCormick DJ, et al. The glycoprotein hormones: Recent studies of structure-function relationships. FASEB J 12: 2661–2669, 1988. 14. Gharib SD, Wierman ME, Shupnik MA, et al. Molecular biology of the pituitary gonadotropins. Endocr Rev 11: 177–199, 1990. 15. Baenziger JU. Regarding the glycoprotein hormones and their sulphated oligosaccharides (Letter). Glycobiology 5: 459, 1995. 16. Parsons TF, Pierce JG. Free a-like material from bovine pituitaries: Removal of its O-linked oligosaccharide permits combination with lutropin b. J Biol Chem 259: 2662–2666, 1984. 17. Chen H-C, Shimohigashi Y, Dufau ML, et al. Characterization and biological properties of chemically deglycosylated human chorionic gonadotropin. J Biol Chem 257: 14446– 14452, 1982. 18. Ulloa-Aguirre A, Midgley AR Jr, Beitins IZ, et al. Folliclestimulating isohormones: Characterization and physiological relevance. Endocr Rev 16: 765–787, 1995. 19. Matzuk MM, Boime I. Mutagenesis and gene transfer define site specific roles of the gonadotropin oligosaccharides. Biol Reprod 40: 48–53, 1989. 20. Hayflick JS, Adelman JP, Seeburg PH. The complete nucleotide sequence of the human gonadotropin-releasing hormone gene. Nucleic Acids Res 17: 6403–6404, 1989. 21. Gharib SD, Wierman ME, Badger TM, et al. Sex steroid hormone regulation of follicle-stimulating hormone subunit mes- Parte I. Fisiologia dell’ormone stimolante il follicolo senger ribonucleic acid (mRNA) levels in the rat. J Clin Invest 80: 294–299, 1987. 22. Dye RB, Rabinovici J, Jaffe RB. Inhibin and activin in reproductive biology. Obstet Gynecol Surv 47: 173- 185, 1992. 23. Hu ZZ, Tsai-Morris CH, Buczko E, et al. Hormonal regulation of LH receptor mRNA and expression in the rat ovary. FEBS Lett 274: 181-184, 1990. 24. Yamoto M, Shima K, Nakano R. Gonadotropin receptors in human ovarian follicles and corpora lutea throughout the menstrual cycle. Horm Res 37: 5-11, 1992. 25. Minegishi T, Nakamura K, Takakura Y, et al. Cloning and sequencing of human FSH receptor cDNA. Biochem Biophys Res Commun 175: 1125-1130, 1991. 26. Segaloff DB, Ascoli M. The lutropin/choriogonadotropin receptor… 4 years later. Endocr Rev 14: 324-347, 1993. 27. Alberts B, Bray D, Lewis J, et al. Cell signaling. In The Molecular Biology of the Cell. New York, Garland Publishing, p681, 1984. 28. Davis JS. Mechanisms of hormone action: Luteinizing hormone receptors and second-messenger pathways. Curr Opin Obstet Gynecol 6: 254-261, 1994. 29. Tilly JL, LaPolt PS, Hsueh AJ. Hormonal regulation of follicle-stimulating hormone receptor messenger ribonucleic acid levels in cultured rat granulosa cells. Endocrinology 130: 1296-1302, 1992. 30. Gougeon A. Dynamics of follicular growth in the human: A model from preliminary results. Hum Reprod 1: 81-87, 1986. 31. Mayerhofer A, Dissen G.A., Costa M.E., Ojeda S.R. A role for neurotransmitters in early follicular development: induction of functional follicle-stimulating hormone receptors in newly formed follicles of the rat ovary. Endocrinology 138: 3320-3329, 1997. 32. Peters H, Byskov AG, Himelstein-Braw R, Faber M. Follicular growth: The basic event of the mouse and human ovary. J Reprod Fertil 45: 559, 1975. 33. Savard K, Marsh JM, Rice BF. Gonadotropins and ovarian steroidogenesis. Recent Prog Horm Res 21: 285-365, 1965. 34. Palumbo A, Yeh J. Apoptosis as a basic mechanism in the ovarian cycle: Follicular atresia and luteal regression. J Soc Gynecol Invest 2: 565-573, 1995. 35. Payne RW, Hellbaum AA. The effect of estrogens on the ovary of the hypophysectomized rat. Endocrinology 57: 193199, 1955. 36. Rao MC, Midgley AR Jr, Richards JS. Hormonal regulation of ovarian cellular proliferation. Cell, 14: 71-78, 1978. 37. Woods DC, Johnson AL. Regulation of follicle-stimulating hormone-receptor messenger RNA in hen granulosa cells relative to follicle selection. Biol Reprod 72: 643-650, 2005.
Scaricare