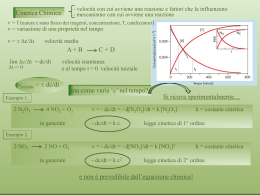
Cinetica Chimica la velocità delle reazioni I parametri termodinamici ∆G°, ∆H°, Keq ci consentono di prevedere in quale direzione (e fino a che punto) una reazione evolve. Non ci dicono nulla sui TEMPI DI REAZIONE impiegati N2 + 3H2 Æ 2 NH3 C + O2 Æ CO2 Keq. A 25°C = 5 108 Keq. A 25 °C = 2 1069 Entrambe queste reazioni procedono a velocità apprezzabili Cinetica chimica Data una generica reazione La velocità di reazione si esprime in termini differenziali v= Variazione della concentrazione tempo • k è la costante di velocità • m ed n sono coefficienti che possono essere pari a zero, numeri interi o frazionari, il cui valore può essere determinato solo sperimentalmente, non coincidono con i coefficienti stechiometrici • Ogni coefficiente determina l'ordine di reazione, rispetto al proprio componente • la somma m+n determina l'ordine globale della reazione Cinetica chimica m n ordine globale di reazione 0 0 0 1 0 1 0 1 1 2 0 2 1 1 2 legge cinetica Gli ordini di reazione NON coincidono, in generale, con i coefficienti stechiometrici. Da cosa dipende la velocità di reazione? 1.Dipendenza dalla concentrazione. L’equazione cinetica correla la velocità di una reazione chimica alle concentrazioni dei reagenti elevate ad opportuni coefficienti. La costante K detta costante di velocità o costante cinetica è una costante di proporzionalità tra le velocità di reazione e le concentrazioni. E’ funzione della natura dei reagenti e della temperatura. 2. Dipendenza dalla temperatura Aumentando la temperatura la velocità di reazione aumenta Teoria delle collisioni e dello stato stazionario. Teoria delle collisioni Affinché una reazione avvenga è necessario che le molecole dei reagenti collidano con una energia superiore ad un valore minimo, e con una opportuna orientazione. L’energia minima richiesta perché l’urto sia efficace è chiamata Energia di attivazione Ea. Energia potenziale A↔B Complesso attivato A Ea B Grado di avanzamento della reazione Le molecole nel recipiente in cui avviene la reazione sono in movimento, hanno una energia cinetica media ma anche una distribuzione dell’energia: esistono cioè molecole a maggiore energia che scontrandosi scaricano nell’urto la loro energia con la possibilità di superare la barriera di attivazione. La frazione di molecole gassose a energia maggiore di una certa energia minima di soglia è data dalla relazione e-E/kT Data una generica reazione La cui velocità di reazione è data dalla relazione La costante cinetica k segue la relazione K=Ae –E/RT Equazione di Arrhenius Questa equazione esprime la dipendenza della costante cinetica dalla temperatura Catalisi e catalizzatori Quando l’energia di attivazione è un ostacolo alla realizzazione de una reazione chimica in tempi ragionevoli è utile ricorrere alla catalisi. Per aumentare la velocità di reazione si può intervenire su due parametri: a) aumento della temperatura b) diminuzione della barriera di attivazione che si ottiene mediante l’impiego di un catalizzatore. Se il catalizzatore si trova nella stessa fase della miscela di reazione (reagenti e prodotti) si parla di cataliso omogenea, se invece non è in fase con la miscela si parla di catalisi eterogenea. 2N2O(g) Æ2N2(g) + O2(g) in presenza di Cl2(g) omogenea 3H2(g) + N2(g) Æ 2NH3(g) in presenza di Fe(s) eterogenea In generale il catalizzatore non influenza la posizione dell’equilibrio, modifica soltanto la velocità con la quale sta procedendo il sistema.
Scaricare