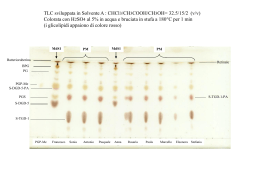
Estrazione ed analisi dei lipidi Lezione del 17- 5- 07 Estrazione dei lipidi (Bligh & Dyer) CELLULE o MEMBRANE in soluzione fisiologica + CH3OH Agitazione per 15’ + CHCl3 Agitazione per 15’ centrifuga SISTEMA MONOFASICO H2O/CH3OH/CHCl3 0,8 2 1 SN1 + pellet centrifuga SN2 CHCl3 + H2O + CH3OH / CHCl3 / H2O 1 1 0,9 CH3OH+H2O SN1+SN2 CHCl3 SISTEMA BIFASICO ESTRATTO LIPIDICO H2O /CH3OH/ CHCl3 0,8 2 1 Cos’e’ la Cromatografia ? La cromatografia e’ una tecnica che serve a separare i singoli componenti di una miscela omogenea. E’ basato sulla diversa ripartizione di molecole tra una fase mobile (liquida o gassosa) ed una fase stazionaria (solida o liquida) • Analisi qualitativa • Analisi quantitativa • Purificazione Miscela Componenti Differenti tipi di cromatografia • Cromatografia liquida ( cromatografia su colonna, su strato sottile o TLC, e HPLC) – Fase stazionaria: gel di silice, allumina, etc. – Fase mobile: solventi organici – importanti proprieta’: polarita’ • Gas cromatografia – Fase stazionaria: un polimero impaccato o capillare. – Fase mobile: gas inerte (Elio) – importanti proprieta’: punto di ebollizione (evaporazione soluti) Cromatografia su strato sottile (TLC) Il gel di silice o di allumina (fase stazionaria) e’ deposto in strato sottile su una lastra di vetro. La silice e’ molto polare. La superficie dei granuli di silice è caratterizzata dalla presenza di gruppi silanolici (SiOH) e di gruppi silossanici (Si-O-Si). Sui primi ha luogo l’interazione tra fase fissa e soluto Si OH Si O OH O Si Si O OH Si Si O O O O La silice è resa attiva dai gruppi silanolici ≡Si-OH. Questi, però, sono bloccati da molecole di acqua legate mediante legami idrogeno H Si O H HO Quindi, è necessario essiccare in stufa ( 180 °C) per eliminare le molecole di acqua, senza però superare i 300 °C, perché si avrebbe la condensazione interna con formazione nuovamente di gruppi silossanici + Si OH Si HO Si Si + H2O O La fase mobile dovrà avere caratteristiche tali da competere, con il soluto, per l’adsorbimento sulla fase stazionaria. L’effetto della fase mobile è quello di differenziare la capacità dei vari soluti di essere adsorbiti. Un soluto molto polare interagisce fortemente con la fase fissa e, per far si che la fase mobile competa con il soluto, dovra’ anch’essa essere abbastanza polare. Affinità di classi di composti con fasi stazionarie polari Composto fosfolipidi Gruppo funzionale O O Acidi O C H2C O C R2 OH Alcoli R1 OH Ammine O CH H2C NH2 Mercaptani C O O O X O SH glycerophospholipid H Aldeidi P C O Chetoni C Esteri C O O R O O Eteri R H Alcheni C C H Alcani R forza di assorbimento crescente R1, R2= catene acidi grassi non polari Glicerolo, gruppi fosfato e X = parte polare O O R C O CH2 R' C O CH O H2C O O P H O CH2 O- C NH3+ R C O CH2 R' C O CH H2C O O O P O CH2 CH2 NH3+ O- COO- Fosfatidiletanolammina Fosfatidilserina O O R C O CH2 R' C O CH O H2C O O P OH O CH2 CH2 N+(CH3)3 OH H O- O H OH H H H OH HO Fosfatidilcolina O P O CH2 O C R CH O C R' CH2 O OH Fosfatidilinositolo Cromatografia su strato sottile (TLC) • Applicazione del campione • Corsa cromatografica • Visualizzazione • Interpretazione dei risultati 1. Applicazione del campione A. Disegnare la linea di deposizione e il fronte del solvente con una matita “fronte del solvente” 1 cm. B. Risospendere i campioni in cloroformio C. Depositare il campione mediante capillari o siringhe tipo Hamilton “linea di deposizione” 1 cm. 2. Corsa cromatografica A. La lastra viene posta in una vaschetta chiusa saturata dai vapori del solvente di sviluppo Lastra cromatografica B. Il campione viene trasportato attraverso la fase stazionaria C. Rimuovere la lastra dalla cameretta quando il solvente ha raggiunto la linea superiore } Solvente di sviluppo (fase mobile) Camera di slivuppo 3. Visualizzazione dei risultati A. Attendere l’evaporazione del solvente dalla superficie della lastra B. Per rilevare la posizione dei componenti esistono metodi chimici e metodi fisici C. Un metodo fisico si basa sull’osservazione della lastra alla luce ultravioletta (254 nm 365 nm). I metodi chimici consistono nello spruzzare sulla lastra reagenti cromogeni come soluzioni di H2SO4, di iodio, blu di molibdeno ecc.. 4. Interpretazione dei risultati A. Determinare il fattore di ritenzione (Rf) per ciascuna macchia. Rf = distanza tra macchia e linea di deposizione distanza tra il fronte del solvente e linea di deposizione dA Rf componente A = d S Rf componente B = dB dS B. I componenti incogniti vengono identificati per confronto con gli Rf degli standard . ? - - - - - - - - - - - - - - - - - - 1- - - - - - - - - - - - - dc ? - - - - - - - - - - - - - - - - - - -2- - - - - - - - dB ? - - - - - - - - - - - - - - - - - - -3- - - - dA miscela incognita std std std dS Fronte del solvente component B - polare! component A + polare! Fronte del solvente componente B componente A Miscela incognita Linea di deposizione Linea di deposizione Corsa cromatografica I componenti meno polari presentano una minore interazione con la silice e migrano piu’ velocemente I componenti piu’ polari stabiliscono maggiori interazioni con la silice e migrano piu’ lentamente I componenti neutri migrano con il fronte del solvente TLC preparativa (purificazione dei singoli componenti) BPG Scraping della silice PG PGP-Me PGS GlyC S-TGD-1 Estrazione dei lipidi (Bligh & Dyer) Analisi quantitativa Retta di calibrazione 18 16 area macchia 14 12 10 8 6 4 2 0 0 2 4 6 microgrammi 8 10
Scaricare