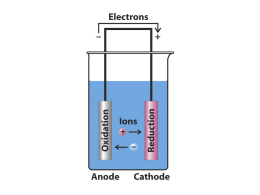
Esercizio 3 Marco Bonechi ESERCIZIO 3 Calcola la solubilità del fosfato di bario Ba3(PO4)2 espressa in g/L. (Kps Ba3(PO4)2 = 3,4x10-23) (MM Ba3(PO4)2 = 601,93 g/mol) (R: 0,0193 g/L) Reazione: 3 Ba2+ Ba3(PO4)2 + 2 PO43- Dati: Kps Ba3(PO4)2 = 3,4x10-23 MM Ba3(PO4)2 = 601,93 g/mol Risoluzione: Kps = [Ba2+]3 ∙ [PO43-]2 = S3 ∙ S2 = S5 S (mol/L) = = = 3,2x10-5 mol/L S (g/L) = S (mol/L) ∙ MM Ba3(PO4)2 = 3,2x10-5 mol/L ∙ 601,93 g/mol = 0,0193 g/L
Scaricare