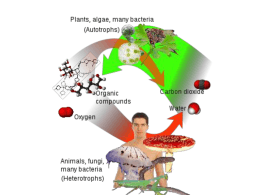
BIOENERGETICA branca della biochimica che si occupa di trasferimento e utilizzazione di E Si applicano le leggi della termodinamica I, II e III legge della termodinamica Negli organismi viventi l’ordine è conservato prelevando E dall’ambiente (nutrienti o luce solare) e restituendo E all’ambiente (calore ed entropia) DG’= DG°’+ RTln [prodotti]/[reagenti] Tendenza a spostarsi verso l’equilibrio forza trainante la reazione In tutti gli organismi viventi le sostanze vengono prodotte in una serie di reazioni biochimiche rigorosamente coordinate. Le energie libere di reazioni in successione sono additive L’E prodotta da processi esoergonici fornisce la forza termodinamica per alimentare quelli endoergonici. Le reazioni biochimiche accoppiate sono catalizzate da enzimi Gli organismi viventi richiedono un continuo apporto di energia per favorire tre processi biologici: 1) produzione di lavoro meccanico durante la contrazione muscolare e i movimenti cellulari • 2) il trasporto attivo di molecole e ioni • 3) la sintesi di macromolecole e di altre biomolecole a partire da precursori più semplici • L’energia libera utilizzata in questi processi viene ricavata dall’ambiente circostante • Gli organismi fotosintetici o fototrofi ottengono l’energia sfruttando l’intrappolamento della luce solare • I chemiotrofi, che comprendono gli animali, ottengono l’energia attraverso l’ossidazione di combustibili carboniosi Principi generali alla base del flusso di energia negli organismi viventi • Le sostanze nutrienti vengono degradate e le grandi macromolecole vengono costruite passo passo in una serie di reazioni dette vie metaboliche • Una molecola comune a tutte le forme di vita, l’ATP, mette in collegamento la via di rilascio di energia con la via di richiesta di energia • L’ossidazione dei combustibili carboniosi fornisce l’energia necessaria alla formazione dell’ATP • Le vie metaboliche sono numerose ma molte hanno in comune un limitato numero di tipi di reazioni e intermedi • Le vie metaboliche sono finemente regolate A pH 7 l’unità trifosforica contiene 4 cariche negative che si respingono. La repulsione diminuisce quando la molecola si idrolizza L’ADP e il Pi vanno incontro a stabilizzazione per risonanza D G°’ = -30.5 kJ/mole L’ADP e il Pi legano più molecole di acqua e vengono stabilizzati per idratazione I processi vitali che richiedono energia sono alimentati dall’idrolisi di molecole di ATP Il flusso di E coinvolge la molecola di ATP e la maggior parte di reazioni prevede il trasferimento di un gruppo Pi da ATP ad un’altra sostanza o da una molecola ad alto contenuto di E ad ADP per dare ATP, molecola che collega catabolismo ad anabolismo immagazzinando E da ossidazione dei nutrienti o luce solare e donandola per: • sintesi di metaboliti, •trasporto transmembrana •movimento meccanico. ATP molecola più versatile perché presente in tutte le cellule a concentrazioni elevate e con enzimi utili per i vari processi. Gli enzimi che catalizzano il trasferimento di Pi si chiamano chinasi. Il 90% di ATP, ADP e Pi forma complessi con lo ione Mg2+ Ciclo dell’ATP Nel ciclo ATP/ADP, un apporto di energia permette a una molecola di ADP (adenosindifosfato) di legarsi a un gruppo fosfato (uno ione fosfato inorganico PO43indicato con Pi) formando una molecola di ATP; a sua volta, poi, la molecola di ATP cede un gruppo fosfato e si trasforma nuovamente in una molecola di ADP. Il processo per cui un gruppo fosfato viene aggiunto a una molecola è detto fosforilazione. Quando una molecola viene fosforilata dall’ATP generalmente il suo contenuto di energia aumenta, sicché la molecola viene attivata e messa in grado di partecipare a una determinata reazione. Altre molecole ad alto contenuto energetico Molecole con potenziale di trasferimento di Pi maggiore di ATP trasferiscono Pi ad ADP, quelle con potenziale di trasferimento minore ricevono Pi da ATP. Trasferimento di e- di cruciale importanza nelle reazioni metaboliche Flusso di e- nelle reazioni redox responsabile di tutto il lavoro prodotto dagli organismi viventi Gli e- passano da intermedi metabolici a trasportatori specializzati in reazioni catalizzate da enzimi, che a loro volta li danno ad accettori ad alta affinità per gli elettroni con rilascio di E (conversione del flusso elettronico in lavoro utile). Potenziali standard di ossido-riduzioni di interesse biologico Il nicotinnamide adenina dinucleotide è il principale trasportatore di elettroni nell’ossidazione di molecole organiche combustibili Trasferiscono 2 e- e 2 H+ NADH prodotto nelle reazioni cataboliche NADPH usato nelle reazioni anaboliche, si spostano entrambi rapidamente da un enzima all’altro L’altro importante trasportatore di elettroni nel processo di ossidazione di molecole organiche è il FAD Nucleotidi flavinici sono spesso saldamente legati agli enzimi (flavoproteine) Acquista due protoni Chinoni solubili nei lipidi trasportano e- nelle membrane I trasportatori di elettroni sono disposti in ordine di potenziale dei riduzione crescente, poiché gli e- tendono a fluire da trasportatori con E°’< a E°’>
Scaricare