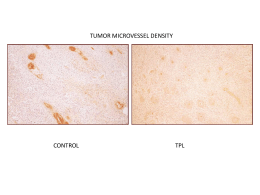
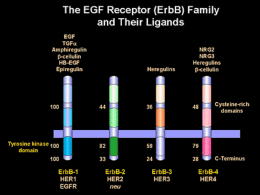
Perché usare farmaci bersaglio-specifici? FINESTRA TERAPEUTICA RISTRETTA SVILUPPO DI RESISTENZA EFFICACIA LIMITATA L’ANGIOGENESI È UN PROCESSO ESSENZIALE ALLO SVILUPPO TUMORALE Fattori di crescita Tumore Vasi sanguigni Angiogenesi patologica Figure 13.34b The Biology of Cancer (© Garland Science 2007) IL VEGF È IL PRINCIPALE FATTORE CHE REGOLA L’ANGIOGENESI Facilita la soparvvivenza dei vasi esistenti Contribuisce alle anomalie vascolari che possono impedire l’accesso dei chemioterapici al tumore Stimola la crescita di nuovi vasi, contribuendo alla progressione tumorale 1 Ligands VEGF-B VEGF-E VEGF-A 2 VEGF-A ANGIOGENESI 3 PlGF VEGF-C/D Recettori VEGFR-1 Chinasi VEGFR-3 VEGFR-2 Il sistema del VEGF STABILITÀ GENETICA DEI BERSAGLI ANTITUMORALI Fattori di crescita autocrini (p.e. PDGF) Tumore Vaso sanguigno PROLIFERAZIONE TUMORALE mediata principalmente attraverso vie autocrine di trasduzione del segnale I recettori presenti sulle cellule tumorali sono suscettibili a mutazioni L’instabilità delle cellule tumorali limita la possibilità di inbire in modo continuativo una via autocrina di trasduzione del segnale Fattori di crescita paracrini (p.e. VEGF) Tumore Vaso sanguigno ANGIOGENESI via di trasduzione del segnale paracrina diretta IL VEGF è una proteina geneticamente stabile La relativa stabilità di ligando e recettori fa sì che l’inibizione continuata del sistema del VEGF sia una strategia antitumorale praticabile VANTAGGI DELLE TERAPIE ANTI-ANGIOGENICHE facile accessibilità del bersaglio selettività minore probabilità di sviluppo di fenotipi resistenti Espressione di fattori angiogenici durante il ciclo vitale di un tumore VEGF VEGF bFGF VEGF TGF-1 bFGF TGF-1 PIGF VEGF bFGF TGF-1 PIGF PDECGF VEGF bFGF TGF-1 PIGF PD-ECGF Pleiotrofina L’ESPRESSIONE DEL VEGF È CONTINUA STRATEGIE PER L’INIBIZIONE DEL SISTEMA DEL VEGF 1 VEGF Anticorpi contro il ligando VEGFR-1 (flt-1) VEGFR-2 (KDE/flk-1) Cellula endoteliale VEGFR-3 (fls-4) 2 TKI a basso peso molecolare EFFETTI DELL’INIBIZIONE CONTINUATA DEL VEGF rete 1 Regressione della 1-4 microvascolare esistente 2 “Normalizzazione” dei vasi maturi sopravvissuti Inibizione della ricrescita 3 vascolare e della neovascolarizzazione 1 2 3 Jubb et al. Nature Reviews Cancer advance online publication; published online 13 July 2006 | doi:10.1038/nrc1946 LA SOSPENSIONE DEL TRATTAMENTO anti-VEGF È SEGUITA DA UNA RAPIDA RICRESCITA VASCOLARE 1 VEGF Tumore bFGF TGF-1 PIGF 2 Vaso sanguigno Progressione attraverso vie non-mutazionali LEUCEMIA MIELOIDE CRONICA (CML) Chronic phase Advanced phase FUNZIONI DI c-Abl • Riconoscimento di lesioni a carico del DNA • Progressione del ciclo cellulare • Effetti trascrizionali BCR SH3 Ras, Raf, MAPK SH2 KINASE PI3K, Akt/PKB DNA BD STAT5 AUMENTO DELLA PROLIFERAZIONE INIBIZIONE DELL’APOPTOSI ACTIN BD NFB (Glivec; Gleevec; Imatinib) Meccanismi di Attivazione dei recettori ErbB nei Tumori • Mutazione (p.e., EGFRvIII— forma mutante di ErbB1 costitutivamente attiva per delezione della maggior parte del dominio extracellulare) Attivazione della trasduzione del segnale • Alterazioni genetiche risultanti nella sovraespressione di recettori normali o costitutivamente attivi • Produzione di EGF o TGF-α da parte delle cellule tumorali: creazione di un circuito autocrino che causa l’ attivazione costitutiva di ErbB-1 Circuito autocrino Strategie per l’inibizione dei recettori ErbB • MAbs in grado di bloccare l’interazione con il ligando o la dimerizzazione dei recettori • Inibitori chinasici a basso peso molecolare • Antagonisti competitivi del recettore • Coniugati ligando-tossina o Ab-tossina • Oligonucleotidi antisenso • Vaccini MAb Inibitore chinasico Antagonista Ligandotossina + Time Death or failure to proliferate
Scaricare