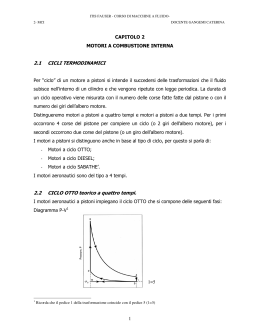
Termodinamica Gas perfetto e sue leggi 1 Un po’ di chimica… La materia è fatta di atomi distinti per Massa molecolare: somma delle masse atomiche di tutti gli atomi che compongono la molecola. Numero atomico Massa atomica espressa in u 1 C12H22O11 molecola di zucchero H 12 (12 u) +22 (u) + 11 (16u) = 342 u 1,0079 u è pari a 1/12 dell’isotopo C12 Ed è pari alla massa di un protone o neutrone. Mole (mol): Quantità di materia che contiene NA = 6,02 * 1023 mol-1 particelle (numero di Avogadro). Corrisponde alla quantità di materia tale che la misura in grammi della sua massa sia pari alla massa atomica o molecolare. 2 Applicazione n (mol) massa (g) massa molecolare (g/mol) Consideriamo ora 12g di Carbonio-12 calcoliamo la massa in kg del singolo atomo di C 12 g / mol 23 26 1 , 99 10 g 1 , 99 10 kg 23 1 6,02 10 mol Essendo u la dodicesima parte della massa atomica del carbonio 1,99 1023g 1u 1,66 10 24 g 1,66 1027 kg 12 quindi 1kg 6,02 1026 u 3 Principio di Avogadro Volumi uguali di gas perfetti Uno stesso numero di molecole di gas Alla stessa P Alla stessa T Alla stessa P Alla stessa T Contengono le stesse molecole Occupano lo stesso volume In particolare alla P = 1 atm e alla T = 0°C, 1 mole di gas occupa un volume di 22,4 litri ( volume molare) 4 Sistema termodinamico Un sistema termodinamico, S, è costituito da tutti gli elementi oggetto della nostra osservazione. L’ambiente esterno, A, è tutto ciò che non appartiene al sistema L’ambiente universo è S U A, l’unione del sistema e dell’ambiente esterno. 5 Descrizione di un sistema termodinamico Sistema termodinamico Può essere Aperto, Chiuso, Isolato Per essere descritto macroscopicamente Temperatura T, Pressione p Volume V, Densità d Per misurarle Eq. termico Eq. meccanico Equilibrio termodinamico Eq. chimico 6 Il gas perfetto:definizione e leggi Una sostanza allo stato aeriforme è detta GAS PERFETTO se soddisfa esattamente le leggi di Boyle Mariotte Gay – Lussac isobara Gay - Lussac isocora 7 Boyle Mariotte: isoterma (1660 circa) La legge: p V = costante isoterme sul piano di Clapeyron 40,0 35,0 Pressione 30,0 25,0 20,0 Come realizzarla: Immergendo il sistema (cilindro con pistone mobile) in una miscela di acqua e ghiaccio. Variando il volume o la pressione avremo una isoterma a 0°C (273 K) 15,0 10,0 5,0 0,0 Volume 8 Gay – Lussac: isobara (1800) Come realizzarla: La legge: V = V0 (1+a t) Dove V0 è il volume a temperatura 0°C. Lasciando il pistone libero di muoversi, la pressione del gas intero al cilindro sarà sempre uguale alla pressione atmosferica. La temperatura e il volume aumenteranno linearmente isobara sul piano di Clapeyron 1,2 1 pressione 0,8 0,6 0,4 0,2 0 0,0 0,2 0,4 0,6 0,8 1,0 1,2 1,4 1,6 1,8 2,0 volum e 9 Gay – Lussac: isocora (1800) La legge: P = P0 (1+a t) Dove P0 è il volume a temperatura 0°C. Isocora 2,0 1,8 1,6 1,4 Come realizzarla: Bloccare il pistone oppure zavorrare in modo progressivo il pistone in modo da mantenere il volume costante. Ponendo il sistema su una sorgente di calore la temperatura e il volume aumenteranno linearmente. pressione 1,2 1,0 0,8 0,6 0,4 0,2 0,0 0 0,5 volum e 1 1,5 10 Isocora in funzione della temperatura 0,40 0,35 0,30 pressione (atm) o Pa Poiché il valore a è indipendente dal tipo di gas, è possibile realizzare un termometro a gas utilizzando un cilindro con pistone bloccato e con un manometro registrare la variazione della pressione. 0,25 0,20 0,15 0,10 0,05 -273,15 °C 0,00 0 50 100 150 temperatura ( °C) 200 250 11 Isobara in funzione della temperatura 1,00 Se, mantenendo immutato l’intervallo di temperature corrispondente ad 1 °C, spostiamo lo zero a -273,15 °C, otteniamo la T (K) = t(°C) + 273,15 0,80 0,70 volume (cm^3) SCALA TERMOMETRICA ASSOLUTA o SCALA KELVIN K 0,90 0,60 0,50 0,40 0,30 0,20 -273,15 °C 0,10 0,00 0 50 100 150 200 250 temperatura (°C) 12 Leggi dell’isobara nella scala K La legge: V = V0 (1+a t) Dove V0 è il volume a temperatura 0°C. 1 V V0 1 t facendo il m.c.m. 273,15 273,15 t V V0 chiamando T 273,15 t e con T0 273,15 273,15 cioè passando alla scala termometr ica assoluta la legge si scrive : VT V 0 T0 similmente anche l' isocora verrà descritta dalla legge p 0T p T0 13 La legge dei gas perfetti Condizioni iniziali stato A Temperatura T0 = 273 K = 0°C Pressione = p0 e Volume = V0 Trasformazione isoterma A B V p Vo' p V0 p0 quindi Vo' 0 0 p Trasformazione isobara B C p0 V ' 0 V V p V p p V oT T 0 0 T pV 0 0 T T0 T0 pT0 T0 Ma per la legge di Avogadro fissati P0, T0 il volume V0 è proporzionale al numero n di moli del gas Equazione di stato pV nRT dove R 8,3 J mol K 14
Scaricare