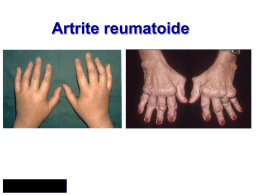
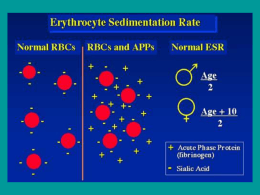
NEWS Suppl. al n. 5/2011 di www.pilloledifarmacoeconomia.it Atti del “Corso residenziale di farmacoeconomia in reumatologia” Segreteria Scientifica Dr. Maurizio Benucci Dr. Alessandro Mannoni www.pilloledifarmacoeconomia.it iii parte Firenze - 12-15 ottobre 2011 Indice iii parte Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini 63 Raccomandazioni Eular Cost-effectiveness analysis Fabiola Atzeni 76 Analisi di impatto economico dell’impiego dei farmaci biologici dopo fallimento dei farmaci tradizionali Irma Aruta Improta 82 Analisi di budget impact nei farmaci biologici non anti-TNF nell’artrite reumatoide Giovanni Giuliani 87 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini “2000-2010 Bone and Joint decade Analisi Cost‐effec/veness dei principali trials clinici Piercarlo Sarzi‐Pu8ni Director, Rheumatology Unit L Sacco University Hospital, Milan ‐Italy Il numero di soggetti artropatici invalidi soprattutto anziani raggiungerà entro i prossimi 20 anni un numero notevolmente sproporzionato alle disponibilità finanziarie dei singoli governi da devolvere alla loro assistenza. In questo contesto si inseriscono le iniziative della “Decade” della WHO e dell’ONU, cui il nostro paese ha aderito, con la sollecitazione di destinare fin dall’esordio maggiori risorse al trattamento di tali patologie, finalizzato alla prevenzione dell’evoluzione invalidante cui esse si correlano. Malattie muscolo scheletriche elevata incidenza notevole impatto sociale per i costi economici diretti ed indiretti ad esse legate ridotta qualità e durata di vita. L’Organizzazione Mondiale della Sanità e l’ONU hanno dedicato la decade 2000/2010 alla prevenzione e al trattamento delle malattie muscolo scheletriche sin dall’esordio In Italia le patologie Immuno-Reumatologiche occupano il secondo posto come causa di invalidità fra tutte le malattie. I costi dell’assistenza socio sanitaria rappresentano un grave problema per l’economia complessiva del nostro paese superando complessivamente i 4 miliardi di euro/anno solo per l’Artrite Reumatoide. 63 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Ward MM.Arthrisis Rheum 2001;44:1467-9 PC.Taylor Reumatismo 2007;59:9-14 I dati epidemiologici evidenziano che dopo 10 anni di malattia, oltre il 50% dei soggetti con Artrite Reumatoide hanno abbandonato l’attività lavorativa per incapacità allo svolgimento delle funzioni richieste Di questi oltre la metà è rappresentato dalla assenza per malattia con secondaria perdita di produttività lavorativa producendo Si stima che l80% dei pazienti affetti da AR presenterà una disabilità dopo 20 anni dalla comparsa della malattia e laspettativa di vita si riduce da 3 a 18 anni. 287.000 lavoratori malati Si determina frequentemente un progressivo isolamento del paziente con perdita di vita di relazione, grave compromissione del tono dell’umore e tendenza alla depressione. 23 milioni di giornate lavorative (perdita) Osservatorio Sanità e Salute-2010 EULAR recommendations for de management of Rheumatoid Arthritis with synthetic and biological disease-modifying antirheumatic drugsAnn Rheum.Dis 2010-vol 69;964-975 • È stato ormai dimostrato che un trattamento precoce e aggressivo con DMARD (farmaci anti-reumatici che modificano il decorso della malattia) sia in monoterapia che in terapia di associazione riduce notevolmente la comparsa di queste lesioni con notevoli benefici per i pazienti a medio e lungo termine. • Il ritardo nellinizio di una terapia può portare ad effetti devastanti in termini di progressione del danno radiologico e marcata disabilità funzionale peggiorando la prognosi. Lattesa di vita è ridotta, correlata in particolare con letà,la disabilità e la gravità di malattia. Bathon JM,et al N Engl J Med 2000; Visser H, et al Rheum 2002; Landewe RBM,et al Arthritis Rheum 2002; M. Padovan, M. Govoni, F. Trotta Reumatismo, 2003; 55(3):187-194 . Tale approccio terapeutico impone lidentificazione precoce delle forme che necessitano di un trattamento con DMARDs e la stratificazione prognostica al fine di riservare i trattamenti farmacologici più aggressivi alle forme maggiormente severe ed evolutive. Solo in tempi relativamente recenti si è sviluppato il tema della early arthritis pochi Prima degli anni 90 si ritrovavano in letteratura solo contributi dedicati a tale problematica. The economics of treatment in early rheumatoid arthri/s Early Arthritis Clinics Lattenzione posta alle fasi di esordio del processo infiammatorio articolare cronico, inizialmente limitata solo ad alcuni paesi (U.K, Olanda, Paesi Scandinavi), si è estesa sempre più fino alla istituzione nelle diverse realtà, di strutture dedicate allo studio di questa popolazione di pazienti creando degli ambulatori Dedicati definiti Early Arthritis Clinics (E.A.C.) Schema/c representa/on of disease progression in rheumatoid arthri/s (RA) This figure was updated in a later study which showed that pa/ent variability was much higher than in this figure. However, this remains a useful descrip/on of how disease progression might occur in a cohort of early RA pa/ents. From Kirwan (1999, Journal of Rheumatology 26: 720–725) with permission. Bansback N. et al. Best Prac0ce & Research Clinical Rheumatology 23 (2009) 83–92 64 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Schema/c representa/on of how costs could vary aYer suppression of radiographic change for the first 4 years of disease. Here the example shows that the cost of early interven/on might be recouped by preven/ng joint replacements or loss of employment in later years (e.g. the area depic/ng cost savings is larger than the area depic/ng addi/onal costs over a life/me). Bansback N et al. Best Prac0ce & Research Clinical Rheumatology 23 (2009) 83–92 The economics of treatment in early rheumatoid arthri/s Economic aspects of treatment op&ons in rheumatoid arthri&s: a systema&c literature review informing the EULAR recommenda&ons for the management of rheumatoid arthri&s PICO strategy for the search Propor&on of pa&ents in full‐&me work over 15 years in 148 pa/ents with early rheumatoid arthri/s (RA) with mean disease dura/on of 1 year at the start of the study. Adapted from Eberhart et al (2007, Journal of Rheumatology 34: 481–487) Bansback N et al. Best Prac0ce & Research Clinical Rheumatology 23 (2009) 83–92 Economic aspects of treatment op&ons in rheumatoid arthri&s: a systema&c literature review informing the EULAR recommenda&ons for the management of rheumatoid arthri&s Funding as declared in published cost‐effec&veness analyses: acknowledgements/grants/affilia&ons ABA, abatacept; ADA, adalimumab; DMARD, disease‐modifying an/rheuma/c drug; ETA, etanercept; HCQ, hydroxychloroquine; IFX, infl iximab; LEF, lefl unomide; MTX, methotrexate; RTX, rituximab; SSZ, sulfasalazine; TCZ, tocilizumab. Monika Schoels M. et al. Ann Rheum Dis 2010;69:996 Economic aspects of treatment op&ons in rheumatoid arthri&s: a systema&c literature review informing the EULAR ecommenda&ons for the management of rheumatoid arthri&s ICERs of biological agents published in cost‐effec&veness analyses AB, published in abstract form only; HTA, Health Technology Assessment Report; NICE, Na0onal Ins0tute for Health and Clinical Excellence; NS, not stated; PYR, year of publica/on . § DMARD naïve (ie, fi rst‐line treatment), # aYer DMARD failure (*aYer failure of one DMARD, **aYer failure of more than one DMARD), ◊In their analyses, the authors also differen/ated between early RA and fi rst‐line TNFi, as well as between late RA and TNFi used as last drug yet ICERs reported did not differ substan/ally). AB; published in abstract form only; ADA, adalimumab; c, combina/on therapy (with MTX, if not otherwise stated); DMARD, disease‐modifying an/rheuma/c drug; ETA, etanercept; ICER, incremental cost‐effec/veness ra/o; IFX, infl iximab; ITT, inten/on to treat analysis; m, monotherapy; MTX, methotrexate; NS, not specifi ed; NSAIDs, non‐steroidal an/inflammatory drugs; PYR, year of publica/on; QALY, quality‐adjusted life‐year; RA, rheumatoid arthri/s; s, sequen/al use; SSZ, sulfasalazine; TNFi, TNFα inhibitors; WR, weighted response. Monika Schoels M. et al. Ann Rheum Dis 2010;69:996 Monika Schoels M. et al. Ann Rheum Dis 2010;69:996 65 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Economic aspects of treatment op&ons in rheumatoid arthri&s: a systema&c literature review informing the EULAR ecommenda&ons for the management of rheumatoid arthri&s § DMARD naïve (ie, fi rst‐line treatment), # aYer DMARD failure (*aYer failure of one DMARD, **aYer failure of more than one DMARD), ◊In their analyses, the authors also differen/ated between early RA and fi rst‐line TNFi, as well as between late RA and TNFi used as last drug yet ICERs reported did not differ substan/ally). AB; published in abstract form only; ADA, adalimumab; c, combina/on therapy (with MTX, if not otherwise stated); DMARD, disease‐modifying an/rheuma/c drug; ETA, etanercept; ICER, incremental cost‐effec/veness ra/o; IFX, infl iximab; ITT, inten/on to treat analysis; m, monotherapy; MTX, methotrexate; NS, not specifi ed; NSAIDs, non‐steroidal an/inflammatory drugs; PYR, year of publica/on; QALY, quality‐adjusted life‐year; RA, rheumatoid arthri/s; s, sequen/al use; SSZ, sulfasalazine; TNFi, TNFα inhibitors; WR, weighted response. Economic aspects of treatment op&ons in rheumatoid arthri&s: a systema&c literature review informing the EULAR ecommenda&ons for the management of rheumatoid arthri&s § DMARD naïve (ie, fi rst‐line treatment), # aYer DMARD failure (*aYer failure of one DMARD, **aYer failure of more than one DMARD), ◊In their analyses, the authors also differen/ated between early RA and fi rst‐line TNFi, as well as between late RA and TNFi used as last drug yet ICERs reported did not differ substan/ally). AB; published in abstract form only; ADA, adalimumab; c, combina/on therapy (with MTX, if not otherwise stated); DMARD, disease‐modifying an/rheuma/c drug; ETA, etanercept; ICER, incremental cost‐effec/veness ra/o; IFX, infl iximab; ITT, inten/on to treat analysis; m, monotherapy; MTX, methotrexate; NS, not specifi ed; NSAIDs, non‐steroidal an/inflammatory drugs; PYR, year of publica/on; QALY, quality‐adjusted life‐year; RA, rheumatoid arthri/s; s, sequen/al use; SSZ, sulfasalazine; TNFi, TNFα inhibitors; WR, weighted response. Monika Schoels M. et al. Ann Rheum Dis 2010;69:996 Monika Schoels M. et al. Ann Rheum Dis 2010;69:996 Economic aspects of treatment op&ons in rheumatoid arthri&s: a systema&c literature review informing the EULAR ecommenda&ons for the management of rheumatoid arthri&s Economic aspects of treatment op&ons in rheumatoid arthri&s: a systema&c literature review informing the EULAR recommenda&ons for the management of rheumatoid arthri&s Search and selec/on process. (Ini/al comprehensive search strived for cost‐ effec/veness analyses and cost of illness studies.) Monika Schoels M. et al. Ann Rheum Dis 2010;69:996 Published incremental cost‐effec/veness ra/os. x‐Axis=incremental cost‐effec/veness ra/o in US$ per quality‐ adjusted life‐year gained (log scale); y‐axis=indica/on for the use of biological agents; dots represent reported ICERs of the drugs inves/gated. Values to the leY of the ver/cal lines at US$50 000 and US$100 000 are commonly considered to be cost effec/ve. Note, that comparing ICERs between trials is inappropriate. ABA, abatacept; ADA, adalimumab; DMARD, disease‐modifying an/rheuma/c drug, ETA, etanercept; ICER, incremental cost‐effec/veness ra/o; IFX, infl iximab; RTX, rituximab; TNFi ns., tumour necrosis factor α inhibitor, not specifi ed. Monika Schoels M. et al. Ann Rheum Dis 2010;69:996 Economic aspects of treatment op&ons in rheumatoid arthri&s: a systema&c literature review informing the EULAR recommenda&ons for the management of rheumatoid arthri&s Modelled treatment sequences in cost‐effec&venes analyses inves&ga&ng first‐line TNFi use Economic aspects of treatment op&ons in rheumatoid arthri&s: a systema&c literature review informing the EULAR ecommenda&ons for the management of rheumatoid arthri&s Final results Final results Quality assessment according to the Oxford EBM level of evidence classifi ca/on.13 *MTX or SSZ; †LEF. NB. ABA, abatacept; CEAs, cost‐effec/veness analyses; DMARD, disease‐modifying an/rheuma/c drug; LEF, lefl unomide; MTX, methotrexate; RTX, rituximab; SSZ, sulfasalazine; TNFi, TNFα‐inhibitors. ABA, abatacept; ADA, adalimumab; DMARD, disease‐modifying an/rheuma/c drug; ETA, etanercept; IFX, infl iximab; LEF, lefl unomide; MTX, methotrexate; NSAID, non‐steroidal an/‐infl ammatory drug; pall, pallia/ve treatment; PYR, year of publica/on; salv, salvage treatment; SSZ, sulfasalazine; TNFi, TNFα inhibitors Monika Schoels M. et al. Ann Rheum Dis 2010;69:996 66 Monika Schoels M. et al. Ann Rheum Dis 2010;69:996 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Cost‐Effec&veness of Biologic Response Modifiers Compared to Disease‐Modifying An&rheuma&c Drugs for Rheumatoid Arthri&s: A Systema&c Review Review of Economic Evalua2ons of Biologics Versus DMARDs for RA Flow chart of the study selec/on. NHS EED Na/onal Health Services Economic Evalua/on Database; CEA Cost‐Effec/veness Analysis van der Velde et al. Arthri/s Care & Research Vol. 63, No. 1, January 2011, pp 65–78 Cost‐Effec&veness of Biologic Response Modifiers Compared to Disease‐Modifying An&rheuma&c Drugs for Rheumatoid Arthri&s: A Systema&c Review van der Velde et al. Arthri/s Care & Research Vol. 63, No. 1, January 2011, pp 65–78 Cost‐Effec&veness of Biologic Response Modifiers Compared to Disease‐Modifying An&rheuma&c Drugs for Rheumatoid Arthri&s: A Systema&c Review van der Velde et al. Arthri/s Care & Research Vol. 63, No. 1, January 2011, pp 65–78 Cost‐Effec&veness of Biologic Response Modifiers Compared to Disease‐Modifying An&rheuma&c Drugs for Rheumatoid Arthri&s: A Systema&c Review van der Velde et al. Arthri/s Care & Research Vol. 63, No. 1, January 2011, pp 65–78 Cost‐Effec&veness of Biologic Response Modifiers Compared to Disease‐Modifying An&rheuma&c Drugs for Rheumatoid Arthri&s: A Systema&c Review van der Velde et al. Arthri/s Care & Research Vol. 63, No. 1, January 2011, pp 65–78 67 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Cost‐Effec&veness of Biologic Response Modifiers Compared to Disease‐Modifying An&rheuma&c Drugs for Rheumatoid Arthri&s: A Systema&c Review van der Velde et al. Arthri/s Care & Research Vol. 63, No. 1, January 2011, pp 65–78 Cost‐Effec&veness of Biologic Response Modifiers Compared to Disease‐Modifying An&rheuma&c Drugs for Rheumatoid Arthri&s: A Systema&c Review van der Velde et al. Arthri/s Care & Research Vol. 63, No. 1, January 2011, pp 65–78 Introduc&on to economic modeling for clinical rheumatologists: applica&on to biologic agents in rheumatoid arthri&s Marra ca et al. Clin Rheumatol (2011) 30 (Suppl 1):S9–S18 68 Cost‐Effec&veness of Biologic Response Modifiers Compared to Disease‐Modifying An&rheuma&c Drugs for Rheumatoid Arthri&s: A Systema&c Review van der Velde et al. Arthri/s Care & Research Vol. 63, No. 1, January 2011, pp 65–78 Introduc&on to economic modeling for clinical rheumatologists: applica&on to biologic agents in rheumatoid arthri&s Marra ca et al. Clin Rheumatol (2011) 30 (Suppl 1):S9–S18 Introduc&on to economic modeling for clinical rheumatologists: applica&on to biologic agents in rheumatoid arthri&s Marra ca et al. Clin Rheumatol (2011) 30 (Suppl 1):S9–S18 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Introduc&on to economic modeling for clinical rheumatologists: applica&on to biologic agents in rheumatoid arthri&s Marra ca et al. Clin Rheumatol (2011) 30 (Suppl 1):S9–S18 Treatment strategies aiming at remission in early rheumatoid arthri&s pa&ents: star&ng with methotrexate monotherapy is cost‐effec&ve Treatment strategies aiming at remission in early rheumatoid arthri&s pa&ents: star&ng with methotrexate monotherapy is cost‐effec&ve Schipper LG etl al. Rheumatology 2011;50:13201330 Treatment strategies aiming at remission in early rheumatoid arthri&s pa&ents: star&ng with methotrexate monotherapy is cost‐effec&ve Schipper LG etl al. Rheumatology 2011;50:13201330 Schipper LG etl al. Rheumatology 2011;50:13201330 Treatment strategies aiming at remission in early rheumatoid arthri&s pa&ents: star&ng with methotrexate monotherapy is cost‐effec&ve Treatment strategies aiming at remission in early rheumatoid arthri&s pa&ents: star&ng with methotrexate monotherapy is cost‐effec&ve Schipper LG etl al. Rheumatology 2011;50:13201330 Schipper LG etl al. Rheumatology 2011;50:13201330 69 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Assessing the cost‐effec&veness of biologic agents for the management of moderate‐to‐severe rheumatoid arthri&s in an&‐TNF inadequate responders in Italy: a modelling approach Cimmino MA et al. Clinical and Experimental Rheumatology 2011; 29: 633‐641 Assessing the cost‐effec&veness of biologic agents for the management of moderate‐to‐severe rheumatoid arthri&s in an&‐TNF inadequate responders in Italy: a modelling approach Cimmino MA et al. Clinical and Experimental Rheumatology 2011; 29: 633‐641 Assessing the cost‐effec&veness of biologic agents for the management of moderate‐to‐severe rheumatoid arthri&s in an&‐TNF inadequate responders in Italy: a modelling approach Cimmino MA et al. Clinical and Experimental Rheumatology 2011; 29: 633‐641 70 Assessing the cost‐effec&veness of biologic agents for the management of moderate‐to‐severe rheumatoid arthri&s in an&‐TNF inadequate responders in Italy: a modelling approach Cimmino MA et al. Clinical and Experimental Rheumatology 2011; 29: 633‐641 Assessing the cost‐effec&veness of biologic agents for the management of moderate‐to‐severe rheumatoid arthri&s in an&‐TNF inadequate responders in Italy: a modelling approach Cimmino MA et al. Clinical and Experimental Rheumatology 2011; 29: 633‐641 Assessing the cost‐effec&veness of biologic agents for the management of moderate‐to‐severe rheumatoid arthri&s in an&‐TNF inadequate responders in Italy: a modelling approach Cimmino MA et al. Clinical and Experimental Rheumatology 2011; 29: 633‐641 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Assessing the cost‐effec&veness of biologic agents for the management of moderate‐to‐severe rheumatoid arthri&s in an&‐TNF inadequate responders in Italy: a modelling approach Cimmino MA et al. Clinical and Experimental Rheumatology 2011; 29: 633‐641 Medicare and Cost‐Effec&veness Analysis Neumann PJ et al. N Engl J Med 353;14:1516‐1522 Biologic Drugs for Rheumatoid Arthri&s in the Medicare Program Assessing the cost‐effec&veness of biologic agents for the management of moderate‐to‐severe rheumatoid arthri&s in an&‐TNF inadequate responders in Italy: a modelling approach Cimmino MA et al. Clinical and Experimental Rheumatology 2011; 29: 633‐641 Biologic Drugs for Rheumatoid Arthri&s in the Medicare Program A Cost‐Effec&veness Analysis Wailoo AJ et al.ARTHRITIS & RHEUMATISM Vol. 58, No. 4, April 2008, pp 939–946 Biologic Drugs for Rheumatoid Arthri&s in the Medicare Program A Cost‐Effec&veness Analysis A Cost‐Effec&veness Analysis Wailoo AJ et al.ARTHRITIS & RHEUMATISM Vol. 58, No. 4, April 2008, pp 939–946 Wailoo AJ et al.ARTHRITIS & RHEUMATISM Vol. 58, No. 4, April 2008, pp 939–946 71 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Biologic Drugs for Rheumatoid Arthri&s in the Medicare Program Biologic Drugs for Rheumatoid Arthri&s in the Medicare Program A Cost‐Effec&veness Analysis A Cost‐Effec&veness Analysis Wailoo AJ et al.ARTHRITIS & RHEUMATISM Vol. 58, No. 4, April 2008, pp 939–946 Biologic Drugs for Rheumatoid Arthri&s in the Medicare Program Wailoo AJ et al.ARTHRITIS & RHEUMATISM Vol. 58, No. 4, April 2008, pp 939–946 Modelling Cost‐Effec&veness of Biologic Treatments Based on Disease Ac&vity Scores for theManagement of Rheumatoid Arthri&s in Spain A Cost‐Effec&veness Analysis Wailoo AJ et al.ARTHRITIS & RHEUMATISM Vol. 58, No. 4, April 2008, pp 939–946 Modelling Cost‐Effec&veness of Biologic Treatments Based on Disease Ac&vity Scores for theManagement of Rheumatoid Arthri&s in Spain Beresniak A et al.Interna/onal Journal of Inflamma/on Vol 2011:1‐9 72 Beresniak A et al.Interna/onal Journal of Inflamma/on Vol 2011:1‐9 Modelling Cost‐Effec&veness of Biologic Treatments Based on Disease Ac&vity Scores for theManagement of Rheumatoid Arthri&s in Spain Beresniak A et al.Interna/onal Journal of Inflamma/on Vol 2011:1‐9 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Modelling Cost‐Effec&veness of Biologic Treatments Based on Disease Ac&vity Scores for theManagement of Rheumatoid Arthri&s in Spain Beresniak A et al.Interna/onal Journal of Inflamma/on Vol 2011:1‐9 Modelling Cost‐Effec&veness of Biologic Treatments Based on Disease Ac&vity Scores for theManagement of Rheumatoid Arthri&s in Spain Modelling Cost‐Effec&veness of Biologic Treatments Based on Disease Ac&vity Scores for theManagement of Rheumatoid Arthri&s in Spain Beresniak A et al.Interna/onal Journal of Inflamma/on Vol 2011:1‐9 Modelling Cost‐Effec&veness of Biologic Treatments Based on Disease Ac&vity Scores for theManagement of Rheumatoid Arthri&s in Spain Beresniak A et al.Interna/onal Journal of Inflamma/on Vol 2011:1‐9 Beresniak A et al.Interna/onal Journal of Inflamma/on Vol 2011:1‐9 Review of Eight Pharmacoeconomic Studies of the Value of Biologic DMARDs (Adalimumab, Etanercept, and Infliximab) in the Management of Rheumatoid Arthri&s Doan QV et al. JMCP, 2006; 12 (7):555‐569 Review of Eight Pharmacoeconomic Studies of the Value of Biologic DMARDs (Adalimumab, Etanercept, and Infliximab) in the Management of Rheumatoid Arthri&s Doan QV et al. JMCP, 2006; 12 (7):555‐569 73 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Review of Eight Pharmacoeconomic Studies of the Value of Biologic DMARDs (Adalimumab, Etanercept, and Infliximab) in the Management of Rheumatoid Arthri&s Review of Eight Pharmacoeconomic Studies of the Value of Biologic DMARDs (Adalimumab, Etanercept, and Infliximab) in the Management of Rheumatoid Arthri&s Doan QV et al. JMCP, 2006; 12 (7):555‐569 Doan QV et al. JMCP, 2006; 12 (7):555‐569 Review of Eight Pharmacoeconomic Studies of the Value of Biologic DMARDs (Adalimumab, Etanercept, and Infliximab) in the Management of Rheumatoid Arthri&s Doan QV et al. JMCP, 2006; 12 (7):555‐569 Review of Eight Pharmacoeconomic Studies of the Value of Biologic DMARDs (Adalimumab, Etanercept, and Infliximab) in the Management of Rheumatoid Arthri&s Doan QV et al. JMCP, 2006; 12 (7):555‐569 74 Review of Eight Pharmacoeconomic Studies of the Value of Biologic DMARDs (Adalimumab, Etanercept, and Infliximab) in the Management of Rheumatoid Arthri&s Doan QV et al. JMCP, 2006; 12 (7):555‐569 Review of Eight Pharmacoeconomic Studies of the Value of Biologic DMARDs (Adalimumab, Etanercept, and Infliximab) in the Management of Rheumatoid Arthri&s Doan QV et al. JMCP, 2006; 12 (7):555‐569 Analisi Cost-effectiveness dei principali trials clinici Piercarlo Sarzi-Puttini Review of Eight Pharmacoeconomic Studies of the Value of Biologic DMARDs (Adalimumab, Etanercept, and Infliximab) in the Management of Rheumatoid Arthri&s Doan QV et al. JMCP, 2006; 12 (7):555‐569 Review of Eight Pharmacoeconomic Studies of the Value of Biologic DMARDs (Adalimumab, Etanercept, and Infliximab) in the Management of Rheumatoid Arthri&s Doan QV et al. JMCP, 2006; 12 (7):555‐569 While the conceptual argument for early, aggressive DMARD therapy appears to be strong, the large addi/onal costs will always make the value of early biologic therapy debatable. This may change if the cost of biologics is reduced through greater compe//on. Confirmatory economic studies are unlikely to be feasible to conduct given the ethical limita/ons in conduc/ng long studies, the /me burden required from pa/ents, and the cost of conduc/ng clinical trials. However, the uncertainty can be reduced by adding simple economic outcomes to clinical trials, and observa/onal cohorts. The BeSt study and the Na/onal Databank for Rheuma/c Diseases are examples of studies that have done this. Evidence on early RA is quickly emerging, and this will hopefully include all pa/ents with early RA, and not just those who have severe disease. 75 Raccomandazioni Eular Cost-effectiveness analysis Fabiola Atzeni Raccomandazioni Eular Cost-effectiveness analysis Dr Fabiola Atzeni Rheumatology Unit, L.Sacco University Hospital of Milan and Queen Mary University of London, UK Rheumatoid arthritis and disability Rheumatoid arthritis affects people at an age of high work productivity and has significant consequences on physical functioning and working capacity. The use of biological antirheumatic drugs has led to marked improvements in disease activity and joint damage, but has dramatically raised direct medical costs. Fautrel B, et al. Decis Making 2007;27:138–50.; Jacobsson LT, et al. Scand J Rheumatol 2007;36:179–83;.Pugner KM, Scott DI, Holmes JW, et al. Semin Arthritis Rheum 2000;29:305–20. 4.Fautrel B, Guillemin F. OpinRheumatol 2002;14:121–6. Michaud K, et al. ArthritisRheum 2003;48:2750–62. Definition Incremental cost-effectiveness ratio (ICER), the most frequently repor ted outcome in costeffectiveness analyses (CEAs) reflecting the additional cost per quality-adjusted life-year (QALY) gained by a particular treatment. Although the exact societal willingness-to-pay threshold remains controversial, based on ICERs of other commonly accepted medical interventions, we defined ICERs below US$50 000–100 000 per QALY, as being cost effective. 76 Raccomandazioni Eular Cost-effectiveness analysis Fabiola Atzeni P I Rheumatoid arthritis Analysis of costs in RA (treatment and societal costs) C - - O O1: Costs of RA O2: Cost-effectiveness of DMARDs: MTX, SSZ, LEF, HCQ, ciclosporin A O3: Cost-effectiveness of biological agents: ADA, ETA, IFX, RTX, ABA, TCZ O4: Cost-effectiveness of steroids O5: Cost-effectiveness of treatment strategies: switching, adding, initial combination, step-up, step-down; visit intervals, early start, ... O6: Economic methods used Different treatments No treatment Materials and methods Search and selection process Medline (1950-2008), EMBASE (1980-2008), Cochrane - Cost-effectiveness ratio (ICER), the most frequently reported outcome in costeffectiveness analyses (CEAs) reflecting the additional cost per quality-adjusted life-year (QALY) gained by a particular treatment. “ACR/EULAR abstracts (2007, 2009) Hand Search of articles retrieved Sub-division of studies by category Classification of the studies found Studies were classified according to their randomisation and to the blinding level used. For each treatment class identified, the highest quality study was used as a basis for the recommendations. The highest quality being a randomized controlled trial. Category of Definition evidence Ia Evidence for meta-analysis of randomized controlled trials Ib Evidence from at least one randomized controlled trial IIa Evidence from at least one controlled study without randomization * IIb Evidence from at least one other type of quasi-experimental study III Evidence from non-experimental descriptive studies, such as comparative studies, correlation studies, and case-control studies IV Evidence from expert committee reports or opinions or clinical experience of respected authorities, or both Only if there was no higher quality study within the category, were open or single blinded studies included. 77 Raccomandazioni Eular Cost-effectiveness analysis Fabiola Atzeni The strength of each study’s evidence was then classified according to the following criteria Strength Definition Recommendations DMARD naïve early RA In DMARD naïve patients, MTX*, LEF† and SSZ* have been shown to be cost effective A Directly based on category I evidence Level of Evidence 2 b B Directly based on category II evidence, or extrapolated recommendation from category I evidence Grade B C Directly based on category III evidence, or extrapolated recommendation from category I or II evidence Combination therapy including biological agents in Directly based on category IV evidence, or extrapolated recommendation from category II or III evidence Level of Evidence 1 b D First-line monotherapy with anti-TNF agents in DMARD naïve patients DMARD naïve patients may not be cost effective compared with MTX monotherapy Grade A Evidences associated to the previous reccomendations The use of first-line combination - MTX and anti- The Therefore, MTX monotherapy, and subsequent The starting with ETA monotherapy was calculated TNF agents as initial treatment in early RA resulted = in high ICERs in several studies. escalation with TNFi if necessary. Initial combination: therapy including biological agents has shown clinical superiority over monotherapy. Howerer, there is no evidence supporting this strategy with regards to cost effectiveness. MTX is cheap and efficient, in many patients. Choi HK, et al.J Rheumatol 2002;29:1156–65. 21.Finckh A, Bansback N, Marra CA, et al. Ann Intern Med 2009;151:612–21. 22.Schädlich PK, Zeidler H, Zink A, et al. Pharmacoeconomics 2005;23:395– 420.23.Emery P, Breedveld FC, Lemmel EM, et al. Rheumatology (Oxford) 2000;39:655–65. DMARDs after DMARD failure starting treatment with ADA monotherapy produced a high ICER (US$63 769) than with MTX monotherapy, to produce an even higher ICER of US$89 772. The lowest ICER was generated for ETA plus MTX, but this still amounted to £78 000 (year of pricing 2004). Similarly, ADA plus MTX in early RA had an ICER of US$23 377 per QALY based on effectiveness data A, Cifaldi MA, Segurado OG, et al. J Rheumatol from registration trials Davies 2009;36:16–26.van den Hout WB, et al. Arthritis Rheum 2009;61:291–9. Van Vollenhoven RF, Roy S, Ray S, et al.. Ann Rheum Dis 2008;67(Suppl II):P650. Recommendations Biological DMARDs after DMARD failure Given its higher price, only LEF has been investigated intensively among synthetic DMARDs. Use of LEF after DMARD failure, followed by a switch to ETA only if LEF proved insufficient after 3 months, was considered to be more cost effective than using ETA earlier, but still an ICER of £163 556 was reported. However, indirect costs were not incorporated. in the model LEF was arbitrarily assumed to be 25% less effective when following MTX failure than when used in MTX naïve patients. Welsing PM, Severens JL, Hartman M, et al. M. Arthritis Rheum 2004;51:964–73. Maetzel A, Strand V, Tugwell P, et al. Arthritis Rheum 2002;47:655–61. Cohen S, Cannon GW, Schiff M, et al. Arthritis Rheum 2001;44:1984–92. 78 anti- TNF therapy after DMARD failure appears to be cost effective Level of Evidence 1b Grade B Raccomandazioni Eular Cost-effectiveness analysis Fabiola Atzeni Biological agents after DMARD failure ICERs of biological agents published in cost-effectiveness analyses A combination of anti-TNF plus MTX as a group is cost effective after synthetic DMARD failure with thorough analyses of ADA, ETA and IFX. IFX is cost effective that the doses of IFX have to remain constant over time, There is no strong evidence that one anti-TNF is better than another. Brennan A, Bansback N, Nixon R, et Wailoo AJ, Bansback N, Brennan A, et al. Biologic drugs for rheumatoid arthritis in the Medicare program: a cost-effectiveness analysis. Arthritis Rheum 2008;58:939–46. Bansback NJ, Brennan A, Ghatnekar Ann Rheum Dis 2005;64:995–1002. Kobelt G, Lindgren P, Singh A, et al. Ann Rheum Dis 2005;64:1174–9. Dis 2004;63:4–10. Brennan A, Bansback N, Reynolds A, et al. Rheumatology (Oxford) 2004;43:62–72.–24. Barbieri M, Wong JB, Drummond M. Pharmacoeconomics 2005;23:607–18. Kobelt G, Jönsson L, Young A, et al. 2003;42:326–35. Wong JB, Singh G, Kavanaugh A. Am J Med 2002;113:400–8. ICERs of biological agents published in cost-effectiveness analyses Cost-effective of Anakinra and Abatacept after DMARDs’s Failure ICERs of biological agents published in cost-effectiveness analyses After failure of one or more anti-TNF agents RTX and ABA appear to be cost effective Anakinra has not been considered cost effective in two CEAs, essentially because of its low efficacy in RCTs. Abatacept after MTX failure has been showed to be cost effective based on efficacy data from the AIM trial after TNFi failure Level of Evidence 2b Grade B Cohen SB, Emery P, Greenwald MW, et al. Arthritis Rheum 2006;54:2793–806. Genovese MC, Becker JC, Schiff M, et al. N Engl J Med 2005;353:1114–23.68.NICE Technology Appraisal Guidance 141. Abatacept for the treatment of rheumatoid arthritis. NHS National Institute for Health and Clinical Excellence, 2008 79 Raccomandazioni Eular Cost-effectiveness analysis Fabiola Atzeni After failure of one or more anti-TNF agents Sequential anti-TNF agents use ABA was also reported as cost effective (models were based on ATTAIN trial data although it has initially been rejected by the National Institute for Health and Clinical Excellence report because it exceeds the £30 000 threshold. Rituximab has been shown to be cost effective based on modelling of REFLEX trial data. A systematic review showed that: ETA, unlike ADA and IFX, to be cost effective when used as the second, and even as the third anti-TNF agent A treatment sequence of ETA following ADA plus MTX had a calculated ICER of US$19 663,32. However, there are no randomised head-to-head comparisons of RTX and ABA available. Chen YF, Jobanputra P, Barton P, et al.. Health Technol Assess 2006;10:iii–iv, xi–xiii, 1–229.. Davies A, Cifaldi MA, Segurado OG, et al. J Rheumatol 2009;36:16–26. Cost effectiveness of treatment strategies Cost effectiveness of treatment strategies There is evidence of cost effectiveness for intensive TICORA study compared aggressive versus conservative treatment, but the available data are limited (no CEAs) Level of Evidence 2c Grade B treatment for analysing the cost effectiveness and showed: - at 18 months, higher costs had accrued in the group treated aggressively (due to a larger number of outpatient visits, and higher costs for travel, diagnostic tests and prescriptions), - considerably lower costs in this group owing to lower hospitalisation costs and fewer additional health professional visits. Grigor C, Capell H, Stirling A. Lancet 2004;364:263–9. Cost effectiveness of treatment strategies Glucorticoids In a subanalysis of the FinRA-Co, combination N o d a t a ab o u t t h e c o s t e f fe c t ive n e s s o f Two COBRA subanalyses found combined Level of Evidence 5 DMARD + glucocorticoids was shown to be a protective factor against productivity loss after 5 years of follow-up. treatment effective at equal or lower costs than monotherapy Puolakka K, Kautiainen H, Möttönen T, et al. Ann Rheum Dis 2005;64:130–3.73.Verhoeven AC, Bibo JC, Boers M, et al. Br J Rheumatol 1998;37:1102–9.74.Korthals-de Bos I, Van Tulder M, Boers M, et al.. J Rheumatol 2004;31:1709–16. 80 glucocorticoid treatment are available, but they are quite inexpensive (although long-ter m consequences may be potentially very expensive) Grade D Raccomandazioni Eular Cost-effectiveness analysis Fabiola Atzeni Summary of the previous reccomendations Published incremental cost-effectiveness ratios. x-Axis=incremental costeffectiveness ratio in US$ per quality-adjusted life-year gained (log scale); y-axis=indication for the use of biological agents; dots represent reported ICERs of the drugs investigated. Values to the left of the vertical lines at US$50 000 and US$100 000 are commonly considered to be cost effective 81 Analisi di impatto economico dell’impiego dei farmaci biologici dopo fallimento dei farmaci tradizionali Irma Aruta Improta In Italia si s)mano circa 230.000 pazien) adul) con artrite reumatoide (AR)1 • La prevalenza dell’artrite reumatoide nella popolazione adulta italiana è pari allo 0,46%1 (≈ 229.292 pazienti). • Le donne sono maggiormente colpite degli uomini (circa 2,5 volte di più)2 • La fascia d’età con la maggiore incidenza è quella tra i 30 e i 50 anni3 I farmaci biologici nell’Artrite Reumatoide 3.788 37.363 16.881 17.290 Analisi di impatto economico dell’impiego dei farmaci biologici dopo fallimento dei farmaci tradizionali Numero di pazienti adulti con AR 4.825 18.690 490 6.069 3.483 6.412 14.506 5.154 1.241 6.509 21.527 15.276 21.224 18.736 2.253 7.572 Stima del numero di pazienti adulti con AR ottenuta applicando il tasso di prevalenza nazionale alla popolazione adulta residente 2009 1 F. Salaffi, R. De Angelis, W. Grassi, Prevalence of musculoskeletal conditions in an Italian population sample: results of a regional community based study. The MAPPING study. Clinical and Experimental Rheumatology 2005; 23: 819 828. 2Lee DM. Lancet 2001; 358: 903-911 3ACR. Available at: http://www. rheumatology.org/public/factsheets/ra_new.asp?aud=pat#3, accessed June 2007 Impa<o dell’Artrite reumatoide Cos) dell’artrite reumatoide Italia ed in Toscana Prevalenza a livello mondiale 0,5% - 1% Paesi europa meridionale 0,45% Paesi europa centrale e settentrionale / USA 0,66% % DALYs persi sul totale % morti legate all’AR sul totale USA 0.69 0.12 Europa 0.84 0.09 Italia 0.91 0.10 Impatto su disabilità e mortalità DALY: “disability adjusted life year” è un indice predisposto dall’ Organizzazione mondiale della sanità che integra la mortalità e la disabilità e che può essere interpretato come un anno di vita in salute. Le conseguenze dell’artrite reumatoide hanno un forte impatto sulla morbilità (più che sulla mortalità) e di conseguenza sulla qualità di vita dei pazienti. Impatto sulla produttività % <60 anni 60% % lavoratori 50% In conseguenza della severità della patologia molti pazienti in età attiva (<60 anni) non hanno la possibilità di lavorare. 40% 30% 20% 10% 0% <0.5 0.5-1.0 1.0 - 1.5 1.5 - 2.0 2.0 - 2.5 > 2.5 Severità della patologia (score HAQ) 1. Lundkvist J, Kastäng F, Kobelt G. The burden of rheumatoid arthritis and access to treatment: health burden and costs; Eur J Health Econ. 2008 Jan;8 Suppl 2:S49-60 82 Scuola superiorie S.Anna di Pisa 2011 Analisi di impatto economico dell’impiego dei farmaci biologici dopo fallimento dei farmaci tradizionali Irma Aruta Improta Confronto dei cos) annui di terapia U)lizzo biologici in Italia (Dosaggi da RCP) (€) per paziente/anno Costi annuali, calcolati in base alle indicazioni posologiche presenti nel Riassunto delle Caratteristiche del Prodotto e ai prezzi ex-factory in € inclusi eventuali sconti obbligatori alle strutture pubbliche al netto delle riduzioni temporanee (Suppl. nr.161 alla GU nr.156 del 7 lug 2006 + GU nr. 227 del 29 set 2006) e aggiornati secondo quanto disposto dalla det. AIFA del 28 feb 2007 (payback), dal D.L. 248/2007 (proroga payback 2008), dal D.L. 207/2008 (proroga payback 2009) e dal D.L. 194/2009 (proroga payback 2010) Senato della Repubblica: DOCUMENTO APPROVATO DALLA 12ª COMMISSIONE PERMANENTE; 8 Marzo 2011 Costo dei farmaci Evidenze derivan) da studi condoI in altri Paesi Le componen) da valutare I Interruzione di trattamento COSTO DI ACQUISTO DEL FARMACO II III Paese Infliximab Adalimumab Etanercept Referenza COSTI DI PREPARAZIONE E SOMMINISTRAZIONE: UK 30% (11 mesi) 30% (11 mesi) 29% (13 mesi) Hyrich K et al. Arthritis & Rheumatism 2007;56:13-20 materiali (aghi, siringhe,soluzioni, ecc.), gestione magazzino, lavoro (farmacisti, medici, infermieri), ecc. Olanda 31% (12 mesi) 22% (12 mesi) 21% (12 mesi) Kievit W et al. Ann Rheum Dis 2008;67:1229-1234 Francia Anti TNF: 36% (12 mesi) 50% (24 mesi) 61% (36 mesi) Duclos M et al. J Rheumatol 2006;33:2433-2439 Anti TNF: da 21% a 55% (12 mesi) Kim MM et al. ISPOR 2008; Abstract AR4 COSTI DI MONITORAGGIO EFFICACIA/TOSSICITA’: tests di laboratorio microbiologico e chimico-clinico, monitoraggio farmacocinetico e consulenze irrinunciabili Medline (5 studi EU + 2 US) IV COSTI DELLE COMPLICAZIONI: reazioni avverse al farmaco (allergie, tossicità renale, ematica, gastrointestinale, ecc.) V COSTI DELL’ INSUCCESSO TERAPEUTICO: resistenze emergenti note o insospettate, superinfezioni, risposte terapeutiche lente Dose escalation (incremento di dose e/o aumento della frequenza) Paese Infliximab USA Anti TNF: 36% (12 mesi) Olanda 31,1% (12 mesi) Svizzera Anti TNF: 18% (12 mesi) N. pazienti N. centri coinvolti AO Sacco Milano AO Niguarda Milano Istituto ortop. Pini Milano 3 23 5 Infliximab (n=248) Trattamenti Etanercept (n=259) Adalimumab (n=196) Follow-up medio 39,71 mesi AOU Ferrara AOU Modena 2 1 1 Pol. Murri Jesi 70% 60% 60% 43,2% * Dip. Magrassi e Lanzara Napoli 54% 28,0% 25,8% 40% 22% 30% 20% 20% 10% 10% 0% Infliximab 107) 1 75% 50% 0% 1 Pol. Umberto I Roma Pol. Gemelli Roma Tasso di interruzioni del tra/amento con il 2° an4‐TNFa in Italia (24 mesi) 70% 40% Pol. S.Salvatore L’Aquila 2 Kievit W et al. Ann Rheum Dis 2008;67:1229-1234 Finck A et al. Ann Rheum Dis 2006;65:746-753; 80% 30% 4 4,8% (12 mesi) 80% 50% Osp. La colletta Arenzano AO Pisana (Osp. S. Chiara) AO Careggi Firenze II Ospedale Prato AOU Siena Referenza Stern R. J Rheumatol 2004;31:1538-1541 Tasso di interruzioni del tra/amento con il 1° an4‐TNFa in Italia (36 mesi) AOU Padova Osp. S. Giovanni e Paolo Venezia Pol. Rossi Verona Osp. Valeggio Osp. Ex Busonera Padova 703 7,1% (12 mesi) Etanercept Tassi di interruzione dei farmaci biologici maggiormente impiega) nel tra<amento dell’AR (Studio Episurvey) 1 Da) real world italiani rela)vi ai farmaci biologici maggiormente impiega) nel tra<amento dell’AR (Studio Episurvey)1 Studio retrospettivo di coorte Adalimumab (n. Adalimumab 67) (n. Etanercept (n. 55) Infliximab 12) (n. Adalimumab (n. Etanercept (n. 112) 25) p=0,0001 vs etanercept; † p=0,0002 vs adalimumab 1 AO S.Carlo Potenza AOU Messina AOU Palermo Dal 25,8% al 43,2% dei pazienti discontinuano il trattamento con il primo anti-TNF dopo 3 anni Dal 22% al 75% dei pazienti discontinuano il trattamento con il secondo anti-TNF dopo 2 anni 2 1. L. Punzi, M. Matucci Cerinic, F. Cantini, G. Bagnato, U. Fiocco, C. Ferri, S. Bombardieri; Treatment Patterns of Anti-TNF Agents in Italy: an observational study; Reumatismo, 2011; 63 (1): 18-28 1. L. Punzi, M. Matucci Cerinic, F. Cantini, G. Bagnato, U. Fiocco, C. Ferri, S. Bombardieri; Treatment Patterns of Anti-TNF Agents in Italy: an observational study; Reumatismo, 2011; 63 (1): 18-28 83 Analisi di impatto economico dell’impiego dei farmaci biologici dopo fallimento dei farmaci tradizionali Irma Aruta Improta Incremento di dose dei farmaci biologici maggiormente impiega) nel tra<amento dell’AR (Studio Episurvey)1 Dose escalation (36 mesi)* 40% 35% 34,30% 30% 25% 20% 15% 10% 4,22% 5% 6,26% 0% Infliximab Adalimumab Etanercept * Incremento della dose o aumento della frequenza di somministrazione Come definire il valore di una tecnologia farmaceu)ca Incremento del costo di terapia** 35% 30% 25% 20% 15% 10% 5% 0% -5% -10% ossia il... value for money ...? 29,6% 4,4% -2,1% Infliximab Adalimumab Etanercept ** vs costo terapia atteso da dosi approvate (RCP) Definire il rapporto qualità – prezzo, ossia il rapporto beneficio terapeu6co ‐ prezzo Per effetto della dose escalation il costo terapia realmente sostenuto può essere maggiore di quello atteso. efficienza tecnica in relazione alla sostenibilità finanziaria 1. L. Punzi, M. Matucci Cerinic, F. Cantini, G. Bagnato, U. Fiocco, C. Ferri, S. Bombardieri; Treatment Patterns of Anti-TNF Agents in Italy: an observational study; Reumatismo, 2011; 63 (1): 18-28 Ogni scelta compiuta da un decisore dovrebbe necessariamente tener conto del principio del “value for money” BIA vs ACE informazioni diverse ma complementari MISSIONE DEL VALUE FOR MONEY: massimizzare la salute che si può o<enere con il finanziamento a disposizione (valore clinico in cambio di denaro) Finanziamento gestito dal SSN Guadagno di salute (miglioramento della salute) determinato dall’intervento sanitario = en4tà della spesa per quell’intervento = “ritorno di salute” Budget Impact Analysis La priorità di intervento è stabilita dal vincolo della limitatezza delle risorse nel sistema sanitario pubblico La BIA ha lo scopo di stimare le conseguenze dell’adozione e della diffusione di una tecnologia sanitaria in termini finanziari in uno specifico contesto caratterizzato da limitata disponibilità di risorse 84 Impa<o economico di abatacept in prima linea biologica nei pazien) con AR Analisi di impatto economico dell’impiego dei farmaci biologici dopo fallimento dei farmaci tradizionali Irma Aruta Improta HAQ score e classificazione ACR Efficacia dei tra6amen7 L’efficacia dei trattamenti biologici è espressa in termini di riduzione percentuale media del punteggio HAQ dopo i primi 6 mesi di trattamento. Per tutti i farmaci biologici questi dati sono stati calcolati come variazione percentuale media rispetto al dato baseline sulla base dei risultati dei rispettivi trial clinici Confronto 1° linea Delta HAQ 6mo. (%) Fonte ABA 1° linea ‐40,00 AIM [Kremer, 2006] TCZ 1° linea ‐34,38 OPTION [Smolen, 2008] ETN 1° linea ‐46,67 [Weinbla/, 1999] ADA 1° linea ‐40,00 ARMADA [Weinbla/, 2003] GLM 1° linea ‐27,64 GO‐FORWARD [Keystone, 2009] CZP 1° linea ‐31,25 RAPID 2 [Smolen, 2009] IFX 2° linea ‐22,75 ReAct [Bombardieri, 2007] Riepilogo dei dati di efficacia dei trattamenti espressi come riduzione media del punteggio HAQ dopo 6 mesi HAQ score: misura la funzionalità fisica dei pazienti con AR in una serie di attività tipiche (vestirsi autonomamente, alzarsi in piedi, camminare, alimentarsi, ecc.). Il punteggio può variare con continuità da 0 (massima funzionalità) a 3 (massima disabilità) ACR (American College of Rheumatology) functional status index [Hochberg, 1992]: formato da 4 classi a seconda della capacità a svolgere autonomamente le attività quotidiane (ACR I = leggero, ACR IV = grave) Nel modello è stata assunta una correlazione tra il punteggio HAQ e la classificazione ACR sulla base dell’elaborazione dei dati presentati nello studio di Leardini e colleghi [Leardini, 2002] Nella simulazione si assume che la coorte di pazienti simulata abbia un punteggio HAQ medio iniziale pari a 0,71 (come nello studio di Leardini) Limi4 HAQ ACR I ACR II ACR III ACR IV 0‐1,13 1,14‐1,78 1,79‐2,38 2,39‐3 Limiti del punteggio HAQ per le quattro classi ACR derivati dall'analisi statistica della coorte nello studio di Leardini e colleghi [Leardini, 2002] Tasso di abbandono Gli switch di trattamento, all’interno delle sequenze prescelte, possono essere causati da intolleranza, insorgenza di eventi avversi o carenza di efficacia Per tutti i trattamenti biologici i dati di permanenza sono stati ricavati dal numero di pazienti ancora in trattamento al termine dei rispettivi studi open-lable estensione nel lungo termine dei trial clinici randomizzati. In presenza di più fonti sono stati selezionati gli studi di maggiore durata La permanenza in trattamento nel lungo termine è stata riparametrata in un tasso al ciclo (6 mesi) mediante una funzione di sopravvivenza di tipo esponenziale, corrispondente all’assunzione di rischi costanti nel tempo Confronto 1° linea Tasso abbandono/6mo. Fonte ABA (1° linea) 4,30% AIM‐4y [Kremer, 2008] TCZ (1° linea) 4,30% STREAM [Nishimoto, 2009] ETN (1° linea) 8,21% TEMPO 2y [van der Heijde, 2006] ADA (1° linea) 7,95% ARMADA 4y [Weinbla/, 2006] GLM (1° linea) 6,07% GO‐FORWARD 52w [Keystone, 2010] CZP (1° linea) 5,72% RAPID 2 3y [Smolen, 2010] IFX (2° linea) 23,51% ReAct [Bombardieri, 2007] Riepilogo dei dati di permanenza in trattamento, espressi come tassi di abbandono semestrali Vs etanercept 85 Analisi di impatto economico dell’impiego dei farmaci biologici dopo fallimento dei farmaci tradizionali Irma Aruta Improta Vs adalimumab Vs tocilizumab Vs golimumab Vs certolizumab Conclusioni • Gli a/uali farmaci biologici sono farmaci costo‐efficaci • Il “value for money” di ciascun farmaco deve essere correlato alla quan4tà di salute prodo/a (valore clinico) in funzione dell’inves4mento del SSN (valore economico) • La scelta di un farmaco deve quindi considerare le due componen4 di appropriatezza , ossia quella terapeu4ca e quella economica, nell’onca di garan4re un SSN orientato ai principi di qualità e sostenibilità finanziaria a lungo termine. 86 Grazie Analisi di budget impact nei farmaci biologici non anti-TNF nell’artrite reumatoide Giovanni Giuliani • 1. Il ruolo del budget impact nel contesto delle valutazioni economiche Analisi di budget impact nei farmaci biologici non anti-TNF nell’artrite reumatoide • 2. Aspetti tecnici dellanalisi di budget impact Giovanni Giuliani P&HE - Roche SpA – lesempio di tocilizumab nel trattamento dellartrite reumatoide dopo fallimento con tDMARDs • 3. Considerazioni finali Slide 1 Approccio tradizionale alla valutazione di un trattamento vs HTA Slide 2 4 Dimensioni dell’HTA Efficacia clinica L’intervento è efficace nella pratica clinica? È sicuro? Efficienza allocativa Tollerabilità Efficacia clinica Efficacia epidemiologica + Valutazione Economica (farmacoeconomia) La nuova terapia è sostenibile a livello economico? Comporta dei risparmi per il SSN? Impatto sui budget sanitari? Stiamo ottenendo il miglior risultato possibile, in termini di salute, con le risorse disponibili? HTA Aspetti Organizzativi La nuova tecnologia comporta delle modifiche a livello di percorso diagnostico-terapeutico? Questioni inerenti il paziente Preferenze del paziente / Qualità della vita Aspetti psicologici, sociali, etici Slide 3 Slide 4 87 Analisi di budget impact nei farmaci biologici non anti-TNF nell’artrite reumatoide Giovanni Giuliani BIA e CEA definizioni Cost Effectiveness Analysis (CEA) L’analisi di budget impact - finalità Scopo Budget Impact Analysis (BIA) Stima del potenziale impatto finanziario conseguente all’adozione e diffusione di una nuova tecnologia Valuta esiti e costi di tecnologie alternative in uno specifico orizzonte temporale Stima la costo-efficacia Analizza le conseguenze finanziarie, correlate all’adozione e diffusione delle tecnologie, per ogni anno in cui si manifestano Funzioni Verifica la sostenibilità economica Utilizzatori Previsioni di utilizzo delle tecnologie e conseguenti costi Pianificazione di Budget Redazione di linee guida per l`introduzione di nuove tecnologie sanitarie (o nuove indicazioni) Decisori sanitari responsabili della gestione dei budget a livello nazionale, regionale e locale Slide 5 Slide 6 Flusso di budget impact Dimensione del mercato Potenziali beneficiari Candidabili al trattamento • 1. Introduzione Trattati Composizione del mercato • 2. Aspetti tecnici dellanalisi di budget impact – lesempio di tocilizumab nel trattamento dellartrite reumatoide dopo fallimento con tDMARDs Composizione storica del mercato (alternative rilevanti) Proiezioni future quote di mercato Proiezioni future quote di mercato comprensive della nuova terapia Costi per paziente o per episodio/trattamento Costi per paziente o per episodio/trattamento Costi nello scenario di riferimento Costi nel nuovo scenario Costi • 3. Considerazioni finali Budget Impact Costi (o risparmi) incrementali rispetto allo scenario di riferimento Slide 7 Tocilizumab – budget impact model Slide 8 Tocilizumab – budget impact model La simulazione si basa su un modello analitico decisionale. La sua costruzione può essere sintetizzata come segue: • Stima del numero di pazienti affetti da AR, in base ai dati epidemiologici nazionali; • Individuazione della frazione di pazienti potenzialmente trattabili con tocilizumab, sulla base delle indicazioni approvate; • Definizione delle due strategie terapeutiche, intese come sequenze di trattamenti da porre in confronto; • Analisi dei costi diretti sanitari a carico del SSN collegati con le strategie; • Valutazione comparativa dell’impatto sul budget SSN delle strategie terapeutiche considerate. Italian Journal of Public Health (Year 8, Volume 7, Number 2, Summer 2010, Suppl. 2) Slide 9 88 Slide 10 Analisi di budget impact nei farmaci biologici non anti-TNF nell’artrite reumatoide Giovanni Giuliani Toscana – Impatto sul budget Toc 1^ linea vs an.‐TNF cycling Impa7o sul budget a 5 anni Popolazione del modello • 1. Introduzione • 2. Aspetti tecnici dellanalisi di budget impact – lesempio di tocilizumab nel trattamento dellartrite reumatoide dopo fallimento con tDMARDs Var.% • 3. Considerazioni finali Simulazione regionale utilizzando il modello di budget impact pubblicato su Italian Journal of Public Health (Year 8, Volume 7, Number 2, Summer 2010, Suppl. 2) Slide 11 Quando utilizzare i modelli di BI Slide 12 Considerazioni conclusive L’analisi di budget impact permette di effettuare previsioni sull’impatto finanziario delle nuove tecnologie e valutarne la sostenibilità Fase In prossimità del lancio Pre-lancio Dopo il lancio Lancio Un modello di BI flessibile costituisce uno strumento dinamico che può essere aggiornato e completato con nuove evidenze cliniche ed economiche, consentendo ai decisori di perfezionare progressivamente le valutazioni Fornire evidenze ai payer nazionali Definire Strategie P&R Utilizzo Fornire evidenze ai payer regionali / locali / utilizzatori finali Negoziazione prezzo La distanza temporale tra il momento dell’analisi di BI e la disponibilità di una nuova tecnologia condiziona il margine di incertezza delle stime ottenute Slide 13 Slide 14 Identificazione dei costi per singolo paziente e delle risorse utilizzate consente la quantificazione economica Costo per singolo paziente Numero di risorse Tipologia di risorse Costo unitario Numero di trattamenti Fonti Visite Medico Medicina Generale Studi clinici • Visite Medico Specialista • Studi non interventistici, analisi di database • Terapia •Somministrazione e consumabili • Eventuali esami di laboratorio • Letteratura scientifica • Panel di esperti (preferibilmente per trasferibilità alla pratica clinica) • DRG ospedalieri e tariffe ambulatoriali • Prontuario farmaceutico nazionale Slide 15 89
Scaricare