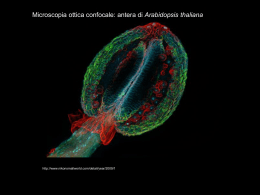
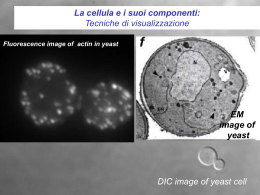
Metodi di Indagine Fisiologica La fisiologia è una scienza eminentemente sperimentale e, poichè ha l'ambizione di fondare la comprensione dei meccanismi biologici sui principi delle scienze fisiche chimiche e matematiche, condivide le modalità e le tecniche di indagine con queste discipline. La Fluorescenza SINGOLETTO SINGOLETTO Rilassato Il fatto di maggior importanza in questo processo è che l'energia del fotone emesso è inferiore a quella del fotone assorbito. La lunghezza d'onda del fotone assorbito è più bassa di quella del fotone emesso. Questo fenomeno si chiama spostamento di Stokes. Indicatori fluorescenti: Fluorofori •Molecole organiche poliaromatiche o eterocicliche •Assorbono emettono intorno alle lungh. d’onda del visibile •Coniugati a molecole che legano le proteine (sonde fluorescenti) Indicatori fluorescenti: Fluorofori Indicatori fluorescenti : Indicatori di concentrazione di ioni •Fluoroforo+molecola affine per uno ione •Il legame dello ione modifica le caratteristiche spettrali del fluoroforo •Esempi FLUO-3 e FURA-2 -> Fluoroforo + BAPTA (chelante) APPLICAZIONI: misura di variazioni di ioni untracellulari come il Calcio (secondo messaggero) Proteine Fluorescenti Aequorea Victoria La GFP: •Taglia molecolare 30 Kda •Assorbe a 360 nm •Le EGFP sono modificate per assorbire nel visibile Green Fluorescent Protein GFP Uso della GFP come gene reporter Puo’ essere inserito a monte o a valle del gene di interesse Microscopia in Fluorescenza (epifluorescenza) Sistemi di illuminazione: lampade a Mercurio o Xenon Filtri: Eccitazione, Dicroico, Emissione Obiettivo (condensatore): alta apertura numerica, bagno d’olio per ingrandimenti superiori a 40X Dispositivi di detezione del segnale: Oculari, Pellicola fotografica, Sensore fotografico (CCD), Fotomoltiplicatore Microscopia in Fluorescenza (Microscopia Confocale laser) La microscopia confocale si avvale di una particolare configurazione ottica messa a punto da M. Minsky nel 1957, che consiste essenzialmente nell'illuminare non tutto il campione, ma solo il piano focale che si sta osservando e nel raccogliere la luce solo dal medesimo. L'immagine risultante viene quindi depurata dalle componenti fuori fuoco e si ha un incremento della risoluzione massima. Microscopia in Fluorescenza (Epifluorescenza verso Confocale) Il sistema Immunitario Protegge l’organismo dalle infezioni ed agenti tossici Antigene (Ag) Immunogeno (capace di indurre una risposta immune) Anticorpo (Ab) Immunoglobulina Struttura delle Immunoglobuline (Ig) •4 catene polipeptidiche: 2 catene pesanti 2 catene leggere •Ponti disolfuro legano le 4 catene •5 classi diverse di Ig IgG, IgA, IgD, IgE, IgM Sito di legame per l’antigene Sito di legame per l’antigene Catena pesante Regione cerniera Catena leggera Frammento cristallizzabile Un esempio…… Localizzazione di proteine cellulari Anticorpo anti-anticorpo Coniugato ad un fluorocromo Anticorpo primario Microscopia in Fluorescenza (Microscopia Confocale a due fotoni) Alcuni fluorocromi possono essere eccitati assorbendo due fotoni di energia pari alla metà di quella corrispondente all'assorbimento di un fotone singolo (da cui l'utilizzo di un laser infrarosso a lunghezza d'onda di emissione variabile); questo passaggio di stato avviene solo se i due fotoni vengono forniti in rapida successione temporale, nell'ordine dei femtosecondi (s-15). Come risultato di queste particolari proprietà si ottiene un ridotto danneggiamento del preparato, perchè la luce infrarossa ha meno energia di quella visibile; inoltre, la luce fornita è pulsante e, quindi, il preparato è mediamente illuminato per un tempo inferiore e si ha una notevole riduzione del photobleaching, che si verifica solo nel piano focale; infine, l'infrarosso ha una capacità di penetrazione maggiore nei tessuti rispetto al visibile. L'unico inconveniente è costituito dal fatto che il tipo di laser necessario è molto costoso e raddoppia i costi rispetto a un sistema di microscopia confocale convenzionale. Microscopia in Fluorescenza (FRAP) La FRAP (Fluorescence Recovery After Photobleaching) e’ utile nello studio della mobilita’ delle molecole all’interno delle membrane biologiche Microscopia in Fluorescenza (TIRFM) Total Internal Refraction Fluorescence Microscopy APPLICAZIONI: Interazioni di proteine con la membrana plasmatica 1. Obiettivo 2. Fluorescenza emessa 3. Olio per immersione 4. Vetrino 5. Campione (cellule) 6. Campo di evanescenza 7. Raggio di eccitazione 8. Prisma di quarzo Microscopia in Fluorescenza (FRET) Fluorescence Resonance Energy Transfer Trasferimento di energia per risonanza (senza emissione di fotoni) Distanza tra le molecole < 100 Å e ben orientate Permette di studiare: interazione tra domini di una proteina (a), interazione tra proteine (b) SDS-PAGE (Sodio Dodecil Solfato Poliacrilammide Gel Elettroforesi) Immunoblotting NBT, BCIP (substrati) Prodotto Anti IgG-AP coniugato 1° anticorpo (IgG) Proteina (precipitato violetto) Membrana SDS-PAGE ed Immunoblotting Interazione proteina-proteina Co-immunoprecipitazione Co-precipitazione con Proteine di fusione Proteina A Proteina di interesse Ligandi non noti Proteina di fusione Immunoprecipitazione Aggiungere un Ab Diretto contro la Proteina nota Estratto cellulare I complessi sono sedimentati L’aggiunta di proteina L’Ab lega la proteina A o G rende il complesso ed isolati dal resto delle proteine cellulari di interesse insolubile Coprecipitazione
Scaricare