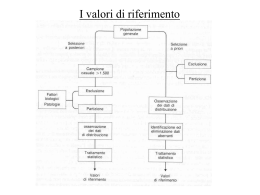
• Per la valutazione statistica del test è necessario conoscere alcune caratteristiche del risultato del test quali: • la sensibilità diagnostica o clinica, • la specificità diagnostica o clinica, • l’incidenza e la prevalenza della malattia nella popolazione osservata • Sensibilità • Il termine sensibilità (diagnostica o clinica) di un test indica l’incidenza percentuale di risposte positive che si ottengono applicando il test a pazienti affetti dalla malattia evidenziabile con il test. • Il concetto di sensibilità è quindi assimilabile a quello di positività del test nella malattia, o di potenza (diagnostica) del test e può essere espresso nel seguente modo percentualizzato: VP sensibilità (diagnostica) = x 100 VP + FN • Specificità • Il termine specificità (clinica o diagnostica) di un test è impiegato per caratterizzare, l’incidenza di risultati negativi che si ottengono applicando il testo a soggetti non portatori della malattia evidenziabile con il test. VN specificità = x100 VN+FP • Specificità e sensibilità sono due caratteristiche interdipendenti di un test e non è possibile aumentare la specificità se non abbassando la sensibilità e viceversa. SENSIBILITA’ E SPECIFICITA’ Malattia presente Malattia assente Test positivo Veri positivi Falsi positivi Test negativo Falsi negativi Veri negativi Sensibilità = Veri positivi/tutti i malati Specificità = Veri negativi/tutti i sani Sensibilità = Veri positivi/ Veri pos + falsi neg (tutti i malati ) Specificità = Veri negativi/Veri neg + falsi pos (tutti i sani) > Sens < Spec FP • La possibilità di disporre di test con diversi gradi di sensibilità e di specificità consente il loro impiego differenziato in relazione agli obiettivi epidemiologici prefissati Sensibilità = Veri positivi/ Veri pos + falsi neg (tutti i malati ) Specificità = Veri negativi/Veri neg + falsi pos (tutti i sani) > Spec < Sens FN • Test di riconoscimento Nelle campagne di screening occorre disporre di un test estremamente sensibile, accettando per contro una bassa specificità. Un test di conferma si rende necessario per identificare successivamente i falsi positivi. • Test di conferma Questi test devono possedere un’elevata specificità allo scopo di identificare i soggetti sani che hanno dimostrato una positività al test (falsi positivi); in questo caso la bassa sensibilità del test non è rilevante, in quanto la selezione effettuata dal precedente test di screening ha consentito di eliminare i pazienti affetti da malattia ma con test negativo (falsi negativi). Valore predittivo • Il valore predittivo rappresenta dal punto di vista clinico il parametro più importante al fine di una corretta strategia diagnostica o terapeutica. Esso si basa sull’integrazione di diversi dati noti al clinico: • la prevalenza della malattia nella popolazione, • la sensibilità e la specificità del test. • Attraverso una equazione si ricava il valore predittivo, ossia la probabilità a posteriori, che indica la probabilità che il soggetto sottoposto al test abbia la malattia in caso di esito positivo del test medesimo. • Si possono calcolare due diversi tipi di valore predittivo: • • valore predittivo positivo, che rappresenta la probabilità che un paziente con un test positivo abbia realmente la malattia; • • valore predittivo negativo, che rappresenta la probabilità che un soggetto sano con un test negativo effettivamente non abbia la malattia. • Teorema di Bayes valore predittivo positivo = (prevalenza) (sensibilità) (prevalenza) (sensibilità) + (1- prevalenza) (1-specificità) • valore predittivo negativo = (1-prevalenza) (specificità) (1-prevalenza) (specificità) + (prevalenza) (1-sensibilità) Valore predittivo • I valori predittivi variano secondo la prevalenza della malattia • Lo stesso test avrà valore predittivo positivo più alto nella popolazione con più alta prevalenza • Questo spiega perché un buon test diagnostico fallisce come test di screening quando viene applicato ad una popolazione in cui la prevalenza della malattia è molto bassa • Es: test per diagnosi di IMA con 95% sens. e spec. • Prevalenza IMA in pronto soccorso 0.05 in unità coronarica: 0.5 VPP in pronto soccorso = 0.5 (50% di falsi positivi) VPP in unità coronarica = 0.95 (5% di falsi positivi) Nel caso di indagini di screening la prevalenza della malattia non supera lo 0.05 Valore predittivo Cut off point o soglia discriminante (o limite di riferimento) e Curva ROC Può risultare problematica la scelta più opportuna del valore discriminante o di separazione (cui off point) fra le due popolazioni considerate. Per risolvere questo specifico problema può risultare utile l’impiego della cosiddetta curva ROC che rappresenta graficamente l’andamento dei falsi positivi in funzione dei veri positivi Sensibilità • 1-Specificità Curva ROC • Le curve ROC, non tengono conto della prevalenza della malattia in studio. Il modo più comune per quantificare l’accuratezza diagnostica consiste nel misurare l’area che giace sotto la curva ROC. Per convenzione essa è sempre compresa tra >=0.5 e <=1 • Efficienza diagnostica del test: VP + VN VP+FP+FN+VN Curva ROC VARIABILITÀ BIOLOGICA E VALORI DI RIFERIMENTO Differenti tipi di variabilità biologica Variab. Biologiche “controllabili” • Genetiche (età, sesso, razza, ecc.) • Fisiopatologiche (gravidanza, fumatori, bevitori, ecc.) • Ritmiche (circadiane, sonno/veglia, alimentazione, esercizio fisico, ecc.) Variab. Biologiche non “controllabili” • Variabilità Biologica intra-individuale • Variabilità Biologica inter-individuale VARIABILITA’ BIOLOGICA RITMICA Concentrations of serum cortisol and growth hormone over a typical day with a usual sleep/wake pattern Concentrations of four hormones during a classical 28-day menstrual cycle Concentrations of three serum analytes in males aged 20-70 years (analyte specific patterns of age related changes) Ai fini della interpretazione del valore osservato in un paziente, come vengono “controllate” le variabilità biologiche controllabili ? • Usando per il confronto valori (normali • Genetiche e o di riferimento) da fisiopatologiche (età, individui comparabili sesso, gravidanza, per il maggiore numeecc.) ro di caratteristiche • Ritmiche (circadiane, • Ottenendo il campione biologico (es. sonno/veglia, alimenprelievo di sangue) da tazione, esercizio paziente in condizioni fisico, ecc.) “basali” definite. Il Concetto di Variabilità Biologica (1) • In ogni momento la concentrazione dei componenti del sangue è il risultato di un equilibrio dinamico • Tale equilibrio è controllato da forze che tendono a mantenerlo regolato ad un valore fisso, vantaggioso per l’organismo, detto punto omeostatico Il Concetto di Variabilità Biologica (2) • La inevitabile oscillazione intorno al punto omeostatico, per ciascun componente e individuo, rappresenta la variabilità biologica intraindividuale (Vbe) • Il punto omeostatico di ogni componente varia da individuo a individuo: variabilità biologica interindividuale (Vbt) Il Concetto di Variabilità Biologica (3) E’ importante rammentare che: • Vbt e Vbe variano da componente a componente • Vbe varia da individuo ad individuo: si considera in genere un valore medio • Vbt e Vbe sono misurate con opportuni protocolli sperimentali includenti adeguati metodi statistici VARIABILITÀ BIOLOGICA Perchè le variabilità biologiche ci interessano ? Perchè hanno rilevanza analitica ed interpretativa ! Rilevanza Analitica, per es.: Definizione dei traguardi analitici di: • imprecisione • inaccuratezza • errore totale Rilevanza Interpretativa, per es.: • Differenza critica • Valori di riferimento • Termini di confronto per i valori osservati VARIABILITA’ ANALITICA • La variabilità analitica è responsabile delle differenze che si osservano tra i valori analitici ripetuti e dipende dal metodo analitico utilizzato. • • imprecisione che dipende dall’errore casuale inaccuratezza che dipende dall’effetto dell’errore sistematico • La variabilità analitica dipendente dall’imprecisione viene espressa come coefficiente di variazione (ds/media x 100) Le variabilità analitica e biologica si sommano Distribuzione di frequenza teorica per Vb=10% e per 3 differenti valori di Va Frequenza relativa, arb 60 Va = 0 50 Va = 7,5% 40 Va = 15% 30 20 10 0 45 60 75 90 105 120 135 150 Valore, U arb Se la variabilità totale aumenta, aumenta la probabilità di sovrapposizione di due valori differenti Frequenza relativa, arb 60 50 1° misura 2° misura (100 U arb) (175 U arb) 40 30 20 10 0 45 75 105 135 165 Valore, U arb 195 225 Le variabilità biologiche e le loro implicazioni “interpretative” Variazione di riferimento (Reference Change Value, RCV, Differenza critica): il concetto • La differenza tra due misure consecutive in un paziente [medesimo metodo] può essere dovuta alla combinazione di Va e Vbe delle due misure • La differenza massima ancora dovuta all’effetto di tali variabilità è la variazione di riferimento (RCV) Valori della variazione di riferimento (reference change value, RCV) Differenza critica: calcolo e significato 3 Conoscendo Va e Vbe la RCV viene calcolata come: RCV = 2,77 x (Va2 + Vbe2 ) 1/2 3 La differenza tra due misure consecutive può essere considerata significativa per una variazione delle condizioni del paziente se superiore alla differenza critica (RCV) RCV: un esempio Colesterolo: Va=3%; Vbe=6%; Dcr=19% • Due pazienti: entrambi con colesterolo 350 mg/dL iniziano un trattamento • Dopo un mese: uno ha colesterolo=290 mg/dL, l’altro colesterolo= 410 mg/dL • In entrambi i casi: la differenza è pari al 17% del primo valore, non si può concludere nè per miglioramento nè per peggioramento VALORI DI RIFERIMENTO • possono essere definiti come l’insieme dei valori di una grandezza appartenente a un gruppo di individui che possiedono alcune caratteristiche prefissate quali l’età, il sesso, la razza, ecc. • Gli intervalli di riferimento sono una carattersitica biologica della popolazione, l’ampiezza della loro distribuzione dipende dalla variabilità biologica interindividuale. VALORI DI RIFERIMENTO • Per convenzione, l’intervallo di riferimento comprende abitualmente il 95% centrale dei risultati ottenuti dal gruppo-campione • Nel caso la distribuzione sia di tipo gaussiano si applica per il calcolo dell’intervallo una statistica parametrica: due deviazioni standard sopra e sotto la media identificano l’intervallo di riferimento • Nel caso di una distribuzione non gaussiana si applica la statistica non parametrica individuando l’intervallo di riferimento tra i valori che rappresentano il 2.5 e il 97.5 percentile • L’intervallo può essere esageratamente ampio: ciò si verifica quando la variabilità interindividuale è molto più ampia di quella intraindividuale. VALORI DI RIFERIMENTO Nel caso di una distribuzione asimmetrica L’ambito dei valori di riferimento è compreso fra il valore del percentile 2.5% e quello del precentile 97.5% VARIABILITA’ BIOLOGICA • Se la variabilità intra-individuale è molto minore della inter-individuale i valori di riferimento hanno poco significato. • Se la variabilità intra-individuale è molto maggiore della inter-individuale i valori di riferimento sono utilizzabili. Valori (O Livelli) Decisionali • questi rappresentano dei valori soglia sopra o sotto i quali è raccomandabile seguire un determinato comportamento clinico • I valori decisionali non sono una caratteristica biologica e sono stabiliti in base all’esperienza clinica e spesso per accordi internazionali. Valori decisionali e valori di riferimento biochimica clinica, 2009;33(4):229-233 Differenze fra intervalli di riferimento e valori decisionali Intervalli di riferimento Dipendono da sesso, età, etc Sono validi per determinata popolazione Valori decisionali Dipendono dalla situazione clinica una Sono validi universalmente Vengono stabiliti mediante Vengono stabiliti mediante studio di una popolazione esperienza clinica o per definita accordi collaborativi Non indicano necessariamente Indicano l’intervento clinico un intervento clinico
Scaricare