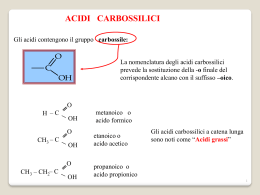
• Il gruppo COOH è molto polare e può formare legami a idrogeno • Gli acidi carbossilici hanno temperature di ebollizione e fusione superiori a tutti i composti organici con la medesima lunghezza della catena idrocarburica • Fino a 4C gli acidi carbossilici sono solubili in acqua, poi sempre meno solubili Nomenclatura degli acidi carbossilici H COOH acido metanoico CH3 COOH acido etanoico CH3CH2 COOH acido propanoico Gli acidi carbossilici sono acidi più forti degli alcoli corrispondenti Ka = 1.8 x 10-5 CH3 COOH + H2O CH3COO- + H3O+ Ka = 1 x 10-16 CH3 CH2OH + H2O CH3CH2O- + H3O+ risonanza • Gli acidi insolubili e componenti di di grassi e oli animali e vegetali sono chiamati acidi grassi • Il Nome IUPAC è acido R–oico ma sono molto diffusi i nomi tradizionali • Esistono anche acidi bicarbossilici e tricarbossilici O C R OH Acido carbossilico • Il gruppo carbossilico è frequentemente associato ad altri gruppi funzionali come accade per l’acido lattico (acido 2idrossipropanoico) e l’acido citrico (acido 3-idrossi-1,3,5pentatrioico) CH3 O O CH3CH2COH CH3CHCH2CH2COH 3 5 2 1 Acido propanoico 4 3 2 1 Acido-4-metilpentanoico Nomi Comuni e Sistematici di alcuni Acidi Carbossilici Formula Nome Comune Origine Nome IUPAC Punto di Eboll. HCO2H Acido Formico Formiche (L. formica) Acido Metanoico 101° C CH3CO2H Acido Acetico Aceto (L. acetum) Acido Etanoico 118° C CH3CH2CO2H Acido Propionico Latte (Gk. protus prion) Acido Propanoico 141° C CH3(CH2)2CO2H Acido Butirrico Burro (L. butyrum) Acido Butanoico 164° C CH3(CH2)3CO2H Acido Valerianico Radice della valeriana Acido Pentanoico 186° C CH3(CH2)4CO2H Acido Capronico Capra (L. caper) Acido Esanoico 205° C CH3(CH2)5CO2H Acido Enantico Vite (Gk. oenanthe) Acido Eptanoico 223° C Proprietà chimiche • A causa dell’attrazione tra il gruppo carbonilico e quello ossidrilico, il gruppo carbossilico presenta proprietà acide più spiccate degli alcoli. • Tutti gli acidi carbossilici possono perdere uno ione H+ trasformandosi in ioni carbossilato COO-. La reazione è reversibile e lo ione carbossilato si comporta da base coniugata forte e stabile Neutralizzazione • Con basi forti gli acidi carbossilici danno luogo a Sali e acqua • R-COOH + NaOH R-COO-Na+ • I Sali degli acidi carbossilici sono solubili in acqua • Il nome del sale si ottiene mettendo la desinenza –ato • I Sali degli acidi grassi prendono il nome di saponi. Gli acidi carbossilici reagiscono con gli idrossidi degli elementi metallici dando luogo alla formazione di sali CH3COO Na+ etanoato di sodio (CH3CH2COO- )2 Ca2+ propanoato di calcio ossidazione e riduzione R CH2OH alcool riduzione ossidazione O R aldeide C H riduzione ossidazione O R C acido OH Riduzione e trasformazione ad alcoli • In presenza di un riducente forte, si riducono, trasformandosi in alcoli: • R-COOH R-CH2OH (con LiAlH4 e H2O) Condensazione con alcoli • In presenza di un catalizzatore acido e a T elevate, producono un estere. La reazione è nota come esterificazione e la reazione inversa è un’idrolisi • R-COOH + HO-R’ ROO-R’ + H2O H O H3C C OH O H O CH3 H3C C H O OCH3 estere Esteri • Gli esteri sono derivati dagli acidi carbossilici in cui è presente il gruppo acilico (COO) unito a un radicale R, alifatico o aromatico. • Il nome si ottiene aggiungendo la desinenza ato al nome del radicale dell’acido seguito dalla desinenza di e dal nome del radicale dell’alcol. H etanoato di 2-butile O acetato di 2-butile H C C H O CH2 etanoato di etile acetato di etile CH3 H O H C C O H CH3 CH2 C H CH3 • Gli esteri vengono considerati Sali organici dove al posto del metallo c’è un gruppo derivato da un composto organico. • Sono solitamente insolubili in acqua • In generale sono dotati di un aroma caratteristico e gradevole • Importanti gli esteri che deviano dal glicerolo (1,2,3-propantriolo) che può unirsi a tre acidi grassi formando i trigliceridi, principali componenti dei grassi e degli oli • Addizionando una molecola d’acqua gli esteri vanno incontro a reazioni di idrolisi riformando l’alcol e l’acido di provenienza (reazione inversa dell’esterificazione) • Quando un estere reagisce con idrossido di sodio o di potassio si produce il sale dell’acido e l’alcol in una reazione di idrolisi • Benzoato di metile+Idrossido di sodio Benzoato di sodio + alcol metilico • I trigliceridi reagiscono con idrossido di sodio o di potassio producendo tre molecole di sapone e glicerolo • I poliesteri hanno struttura filamentosa e vengono dall’unione di alcoli e acidi carbossilici
Scaricare