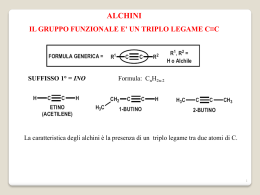
FARMACI NICOTINICI ACETILCOLINA E RECETTORI COLINERGICI L'acetilcolina è il neurotrasmettitore più diffuso. Si trova nel S.N.C. (principalmente nella corteccia cerebrale e nel nucleo caudato), nel sistema nervoso autonomo e nel sistema volontario. L'acetilcolina è il neuromediatore di: - tutti i gangli - della giunzione neuromuscolare - delle sinapsi postgangliari del sistema parasimpatico BIOSINTESI, RILASCIO E BIODEGRADAZIONE - Sintesi della colina nel fegato HO NH2 - CO2 HO NH2 N-metiltrasferasi decarbossilasi COOH + N HO - Nel citoplasma delle cellule delle terminazioni nervose O Colina + SCoA O Colina acetiltrasferasi CH3 (CAT) O assorbita dal fluido extracellulare sintetizzato nei mitocondri acetilcolinesterasi Colina CH3 CH3 CH3 Acetilcolina (ACh) - Nella fessura sinaptica AcetilColina + N H3C AcetilCoA CH3 CH3 Colina Serina CH3 O + NMe3 H3C O ACETILCOLINA Sir H.Dale, 1914 H HO 3 4 5 1 O 2 MUSCARINA Amanita muscaria 2S,4R,5S S + NMe3 N CH3 N NICOTINA Nicotiana tabacum (S)-(-) PROPRIETA' CONFORMAZIONALI La molecola dell'acetilcolina è molto flessibile. Le varie conformazioni possono essere descritte dai valori dei quattro angoli di torsione: 0 1 2 3 CH3 O H N C + CH3 O 0 H 2 1 H 3 CH3 La conformazione biologicamente attiva è probabilmente: trans-trans ( 1 = 2 = 180°) Deduzione ottenuta dalla diversa attività di analoghi rigidi: - selettivo muscarinico - lieve attività nicotinica OCOCH3 H + NMe3 OCOCH3 S 2 1 H 3 2 NMe3 + TRANS: attiva 1S,2S - (+) >100 + di 1R,2R - (-) 1 H H 3 CIS: inattiva I recettori nicotinici sono selettivamente stimolati (agonisti) oltre che dalla S(-)-nicotina anche da: Me + N Me Me +N N Me Me DMPP 1,1-Dimetil-4-fenil-piperazinio (Agonista dei gangli) PTMA Feniltrimetilammonio (Agonista della Placca motrice) e bloccati (antagonisti) da: + + Me3N (CH2)6 NMe3 + + Me3N (CH2)10 NMe3 ESAMETONIO (Antagonista gangliare) DECAMETONIO (Antagonista muscolatura scheletrica) - I recettori muscarinici sono attivati (agonista) selettivamente dalla muscarina e bloccati (antagonista) selettivamente da: N CH3 CH2OH OCO CH C6H5 ATROPINA Atropa Belladonna I recettori nicotinici e muscarinici differiscono oltre che per l’affinità verso differenti agonisti e antagonisti anche per molti altri aspetti: localizzazione funzione architettura molecolare meccanismi biochimici connessi con la loro attivazione RECETTORI NICOTINICI I recettori nicotinici sono recettori a canale ionico (quattro domini transmembranali e cinque subunità) e la loro attivazione provoca il flusso degli ioni Na+, K+, Ca++ attraverso la membrana cellulare secondo il gradiente di concentrazione. NEURONALI N1 o NN 1 - Gangli del sistema simpatico e parasimpatico 2 - CNS MUSCOLARI N2 o NM Giunzione neuromuscolare Azione diretta (Agonisti) Nicotino-mimetici Azione indiretta (Anticolinesterasici) Farmaci Nicotinici Antinicotinici Involvement of neuronal nicotinic receptors Physiology various complex cognitive functions arousal alertness food intake pain perception control of locomotor activity control of autonomous nervous system body temperature regulation nAChRs are particularly important in two periods of brain life: • early pre- and perinatal circuit formation • age-related cell degeneration neuronal survival nicotine exposure in cultures protects neurones from drug-induced neurotoxicity Potential Therapeutic Targets Alzheimer’s disease Parkinson’s disease Dyskinesias nAChRs ADHD Anxiety and pain Schizophrenia Tourette’s syndrome Preterminal nAChRs Ca2+ Presynaptic nAChRs Na+ ACh or Nicoti ne Postsynaptic nAChRs K+ Ligand-gated ion channels Ligand Gated Channels Family 1 – GABAA 5HT3, nAChR Drug site Conformations of nAChRs Antagonists (APO-state) Partial Agonists Full Agonists Y. Bourne et al., The Embo J. 2005, 24, 3635. Nicotinic Receptors Subty pes Homom eric neuron al Heterom eric muscle pCa/pN a BgTx block ++ 20 ++ ~ 0.2 1 - 2 Heterome ric neuronal 11.5 2 2 Ad oggi sono state clonate 17 subunitàche sono state divise in tipo muscolare [α1, β1, δ, γe ε(nel feto)] e in tipo neuronale(α2-α10 e β2-β4) Heteropentameric receptors C P C P Homopentameric receptors C P Competitivi AGONISTI NICOTINICI Non Competitivi Alcuni composti come TMA, DMPP e -Lobelina sono stati utilizzati come tools farmacologici senza alcun impiego terapeutico. C6H5 CH3 H3C + N N H CH3 N Cl + O OH CH3 CH3 H3C TMA N + CH3 -Lobelina DMPP Recentemente è stata studiata la possibilità di utilizzare agonisti nicotinici nel trattamento del morbo di Alzheimer. I composti sotto riportati sono stati utilizzati come tools farmacologici o come modelli per successive elaborazioni strutturali O H3C H N O C2H5 S N CH3 N (S)-ABT-418 selettivo per ( 4)2( CH3 ARECOLONE H N HN N Cl N EPIBATIDINA Epipedobates tricolor O CITISINA (-)-Epibatidine (1R,2R,4S) Cl H N N Ki: ( )- Epibatidine: 0.058 nM (+)-Epibatidine: 0.045 nM Ki: endo-Epibatidine: 7.6 nM Ki: ( )-Nicotine: 1 nM (+)-Nicotine: 38 nM Epipedobates tricolor > Potent analgesic (Daly: 1974; structure: early 1990’s) > Antagonized by mecamylamine, but not by naloxone > Minimal tolerance to the analgesic effect > Limited therapeutic index > Side effects: respiratory paralysis, seizures and death CONOTOXINS G-E-- -L-Q- -N-Q--L-I-R--K-S-N* Conantokins: NMDA Antagonists G-CC-S-N-P-V-C-H-L-E-H-S-N-L-C* -Conopeptides: nAChRs Antagonists C-K-G-K-G-A-K-C-S-R-L-M-Y-D-CC-T-G-S-C-R-S-G-K-C* Conus -Conopeptides: Calcium Channel Blockers Marketed drug: ZICONOTIDE (Prialt) R-D-CC-T-O-O-K-K-C-K-D-R-Q-C-K-O-Q-R-CC-A* -Conopeptides: Sodium Channel Blockers The primary structures of more than 100 conotoxins have been determined and classified into gene superfamilies. -Conotoxin subfamilies 4/7-conotoxins G-CC-S-N-P-V-C-H-L-E-H-S-N-L-C* block neuronal nAChRs MII E-CC-N-P-A-C-G-R-H-Y-S-C* 3/5-conotoxins block muscular nAChRs -GI The primary structures of more than 100 conotoxins have been determined and classified into gene superfamilies. The -conotoxins are competitive antagonists of nAChRs. Targeting the 4 2 nAChR subtype H H N Cl H N O N N N N N EPIBATIDINE CYTISINE (Tabex) VARENICLINE (Chantix, Champix) Targeting the 4 2 nAChR subtype H N O N ON ON N CH3 Epiboxidine Ki 4 2: 0.3 nM CH3 N ABT 418 Ki 4 2: 20 nM Ki (Z)-(S) 4 2: 330 nM Cl H Cl H N N N Ki UB-165 4 2: 0.27 nM H N H N Anatoxin-a Ki 4 2: 1.1 nM H3C N N Epibatidine Ki 4 2: 0.026 nM O Cl N Ki 4 2: 1.6 nM O Ferruginine Ki 4 2: 120 nM H N N N H = o > attività della Nicotina per recettori centrali N 3' 4 1' 5' N 2 H N H N N N N H 3' 4 1' N 5' N N H 2 N = o > attività della Nicotina per recettori centrali H H3C H O N Ferruginina affinità per recettori nicotinici centrali R N O Anatossina-a Anabaena flos-agnae più potente di Ach e Nicotina sia per recettori centrali che periferici H3C H3C H3C N N O O R Isoarecolone Arecolone attività comparabile alla Nicotina per recettori centrali H H 2' N N 5' N 2 Cl N 1 4 MODIFICHE STRUTTURALI EFFETTUATE SULL'ANELLO PIRROLIDINICO DELLA NICOTINA (CH2)n + N N N CH3 n = 1-4 n = 1 10> n = 3,4 10-30< (R = H, C2H5, n-C3H7) diminuzione 3' CH3 H3C R = perif. 4' CH3 5' 2' N R CH3 R = H , CH3 5' N N CH3 CH3 N trans > cis attività nicotinica R = C3H7 ottimo 3' R CH3 N N N H CH3 CH3 R R = H , CH3 attività nicotinica (CH2)n O O CH3 N N H N (CH2)n H n=1,2 -2 n = 1 5x10 nM n = 2 15x10-2 nM L'anello piridinico, che si ripete inalterato in tutti i derivati, non è indicato. nAchR modulators neuronal nAChR ligands, Abbott Preclinical dev. RJR-2429R, J Reynolds Tobacco Co (S)-nicotine, Endovasc Stanford University ABT-089, Abbott Laboratories Phase 2 Clinical SIB-1553A, SIBIA Neurosciences Inc DERIVATI SOTTOPOSTI A SPERIMENTAZIONE CLINICA O NH N O N CH3 N Cl ABT-418 TEBANICLINA Sviluppato come analgesico per il dolore neuropatico. Lo sviluppo clinico è stato arrestato da effetti collaterali a livello della muscolatura gastrointestinale E' stato sottoposto a saggi clinici per migliorare la sintomatologia di AD. Recentemente la sperimentazione clinica è stata sospesa. O N R N N Me2N O N R = H, Me alta selettività per il sottotipo affinità nel range nM N HN H N Ar N VARENICLINA (CHANTIX) O selettivi per N Approvato dal FDA nel 2006 per disassuefazione da nicotina Agonista parziale e agonista pieno FARMACOFORO NICOTINICO c N + a O CH3 Distanza a-b: 7.3-8.0 Å Distanza a-c: 6.5-7.4 Å bâc: 30.4-35.8° N b • Interazione tra un sito anionico del recettore (a) ed un atomo di azoto protonato del ligando. • Un legame a idrogeno fra un donatore di legame a idrogeno localizzato sul recettore (b) e un accettore di legame a idrogeno sul ligando. • Un’interazione fra un sistema (anello eteroaromatico o gruppo carbonilico) del ligando (c) e un sistema di elettroni o un residuo carico positivamente localizzati nel ‘binding site’ del recettore. • Un’interazione -catione fra un residuo aromatico (Trp-149) del ‘binding site’ del recettore e l’atomo di azoto protonato del ligando. • Interazioni steriche positive e negative localizzate sulla parte alifatica ed eteroaromatica del ligando. MODIFICHE STRUTTURALI APPORTATE ALLA STRUTTURA DELL'ACh modifica del ponte etilenico modifica della funzione acetossilica modifica della testa cationica O + N H3C O CH3 CH3 CH3 5.9 A° O CH3 + H N C CH3 O CH3 H H CH3 CH3 N+ CH3 P+ CH3 CH3 CH3 CH3 CH3 + S As+ CH3 CH3 CH3 Attività nicotinica decrescente CH3 N CH3 CH3 CH3 N H CH3 NH2 NH3 CH3 C2H5 CH3 CH3 N CH3 CH3 CH3 N CH3 C2H5 N C2 H 5 C2H5 N C2H5 C2H5 O CH3 R1 H N C CH3 O CH3 H R2 H Ach + R2 R1 EPMR (retto di rana) H H 1 H CH3 CH3 H 180 2 O CH3 H N C + CH3 O CH3 H H Eliminando o sostituendo il ponte etereo non si hanno importanti variazioni di attività Aumentando la lunghezza della catena si ha diminuzione di attività CH3 N R + CH3 O CH3 I composti con R = C2H5 , nC3H7 , nC4H9 , CH2=CH hanno la stessa attività dell'acetilcolina (CH2)n + NMe3 Acetilcolina n=1 n=2 n=3 n=4 EPMR (retto di rana) 1 9.3 1.1 0.38 Antagonista ANTAGONISTI DEI RECETTORI NICOTINICI neuronali GANGLIOPLEGICI placca motrice CURAROSIMILI PACHICURARI LEPTOCURARI ANTAGONISTI DEI RECETTORI NICOTINICI NEURONALI GANGLIOPLEGICI Bloccano la trasmissione dell'impulso nervoso sia della via simpatica che della via parasimpatica. Gli effetti sul sistema simpatico sono più marcati. Per tale ragione i gangloplegici venivano usati come antiipertensivi. Effetti collaterali: - riduzione generalizzata del tono simpatico e parasimpatico - secchezza delle fauci - inibizione motilità intestinale - ritenzione urinaria Composti con attività ganglioplegica - I sali bis-ammonici quaternari danno inibizione competitiva C2H5 C2H5 + N CH3 H3C C2H5 N+ +N (CH2)5 C2H5 TEA Tetraetilammonio Pentolinio + + Me3N (CH2)6 NMe3 Esametonio - Le ammine terziarie danno inibizione non competitiva NHCH3 H3C H3C CH3 N CH3 CH3 CH3 Pempidina CH3 CH3 Mecamilammina RELAZIONE STRUTTURA-ATTIVITA' E MECCANISMO D'AZIONE + + Me3N (CH2)n NMe3 - Variando n si può modulare la selettività verso i recettori nicotinici gangliari o muscolari. - L'attività nicotinica a livello della placca neuromuscolare raggiunge il valore massimo per n = 5 o 6. - La distanza fra i due gruppi ammonici quaternari è di 5-6 A°. - Solo uno dei due gruppi ammonici occupa il sito anionico dell'ACh.. - L'altro gruppo ammonico va ad occupare un sito accessorio. RECETTORE DEI GANGLI 5.3 A° + Me3N - O CH3 O sito anionico Me3N + sito anionico secondario NMe3 + PENTAMETONIO RECETTORE DEI GANGLI 5.3 A° + Me3N - CH3 O sito anionico secondario O - sito anionico Me3N + NMe3 + PENTAMETONIO RECETTORE PLACCA MOTRICE 10.6 A° + Me3N sito anionico - O CH3 sito anionico secondario O NMe3 + Me3N + DECAMETONIO O O Me3N + O O SUCCINILCOLINA = SUXAMETONIO NMe3 + PACHICURARI (non depolarizzanti) competitivi BLOCCANTI NEUROMUSCOLARI CURAROSIMILI LEPTOCURARI (depolarizzanti) non competitivi PACHICURARI H3CO +N CH3 CH3 HO Cl- O OH O Cl- H N+ OCH3 H3C d-tubocurarina cloruro 20-40 volte più potente dell'enantiomero l Chondodendron tormentosum CH3 +N R OCOCH3 N+ CH3 H3C + OCH2CH2NEt3 3I- + OCH2CH2NEt 3 + OCH2CH2NEt3 H3COCO R = CH3 Pancuronio R=H Vecuronio Gallamina O CH3 O CH3 N CH3 O N+ H H Br- H CH2 H O CH3 Rapacuronium Br 1999 - Bloccante neuromuscolare non depolarizzante - Utilizzato come coadiuvante di anestetici generali LEPTOCURARI Sono molecole a catena lunga e lineare. Si ha un massimo di attività quando i due gruppi onio sono separati da una catena metilenica compresa nell'intervallo fra C-10 e C-16. La distanza fra le due teste cationiche varia nell'intervallo 10.8 A° - 18.2 A°. Se si aumenta l'ingombro sterico dei gruppi legati agli atomi di azoto quaternari si pass progressivamente da leptocurari a pachicurari. + Me3N (CH2)10 + NMe3 + Et3N (CH2)10 + NEt3 Me + N (CH2)10 Me + Me3N DEPOLARIZZANTE (non competitivo) più potente, competitivo Me + N NON DEPOLARIZZANTE Me (CH2)10 + NMe3 2I- CH2 COO CH2CH2 CH2 COO CH2CH2 + NMe3 + NMe3 Decametonio Suxametonio Più potente della tubocurarina. Ha interesse storico, non è più in commercio Ha azione brevissima. Viene idrolizzato rapidamente da colinesterasi ematiche. Viene somministrato per infusione continua. Dose 10-30 mg. LEPTOCURARI + + Me3N NMe3 - - sito anionico sito anionico secondario PACHICURARI + NEt3 CH2CH2 O ACh O CH2CH2 + NEt3 O CH2 X - sito anionico CH2 + NEt3 - sito anionico secondario Tubocurarina : si ottiene per estrazione dalla corteccia di Chondrodendron tomentosum. Breve durata d'azione. Non è assorbita per via orale; si somministra per e.V. o i.m. Gallamina: azione trascurabile sui gangli; meno potente della tubocurarina. Si somministra per e.v. alla dose di 1mg/Kg. Pancuronio: 4 volte più potente della tubocurarina con azione più rapida. Unico effetto collaterale importante è la tachicardia. Dose: 0.04-0.08 mg/Kg. Proprietà farmacologiche, insorgenza, durata d’azione e metabolismo degli antagonisti nicotinici muscolari riportati nell’Informatore Farmaceutico Italiano (1996) Farmaco (Specialità medicinale®) Meccanismo d’azione Insorgenza dell’azione (minuti) Durata d’azione (minuti) Metabolismo Sussametonio cloruro (Midarine, Myotenlis) depolarizzante 1-1,5 6-8 idrolisi da colinesterasi plasmatiche Atracurio besilato (Tracrium ) competitivo 2-4 30-40 degradazione di Hofmann; idrolisi da colinesterasi plasmatiche Mivacurio cloruro (Mivacron) competitivo 2-4 12-18 idrolisi da colinesterasi plasmatiche Pancuronio bromuro (Pavulon) competitivo 4-6 120-180 metabolismo nel fegato e clearance; eliminazione renale Vecuronio bromuro (Norcuron) competitivo 2-4 30-40 metabolismo nel fegato e clearance; eliminazione renale Pipecuronio bromuro (Arduan) competitivo 2-4 80-100 metabolismo nel fegato e clearance; eliminazione renale SINTESI PANCURONIO O OCOCH3 CH3 CH3COO C CH2 + HgSO4 O H3C CH3 CO3H Cl OCOCH3 O O N N O HN HO NaBH4 COCH3 OH O N N N N Ac2O/Py HO CH3OCO COCH3 O N + 2 CH3Br CH3OCO N CH3 + CH3 2 Br-
Scarica