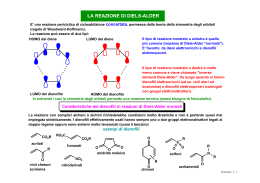
Chimica Organica II Formazione di legami C-C: reazione di Diels-Alder Z Diene Z Dienofilo Etilene e altre olefine semplici sono dienofili poveri. La reazione procede bene con dienofili sostuiti con gruppi Z elettronattrattori o coniugati (-X, -NO2, -COR, COOR, -CN, -CH2X, -C=C). Possono essere utilizzati come dienofili alchini, benzini (in situ). Composti con legami doppi e tripli con eteroatomi (-CN, -N=N-, -C=O, O2). Tutti i dieni coniugati vanno bene, possono essere utilizzati anche l’antracene (ma non benzene, naftalene e fenantrene), il furano e composti carbonilici α,β insaturi. Sostituenti elettrondonatori accelerano la reazione. L’effetto della polarità del solvente sulla velocità della reazione è trascurabile (con l’eccezione dell’acqua) 1 Chimica Organica II Reazione di Diels-Alder Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Aldrin Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl NC Cl Cl Cl Cl CN NON REAGISCE NC CN Domanda elettronica inversa 2 Chimica Organica II Reazione di Diels-Alder Z Z Reazione lenta Z Z Reazione veloce Z nessun prodotto Per poter subire la reazione di Diels-Alder, il diene deve poter raggiungere la conformazione cisoide (S-cis). Ea = 28 KJ/mol S-trans S-cis 3 Chimica Organica II Reazione di Diels-Alder: orientazione Z Z Z' Z' H H Z Z H Z' H Z' La configurazione del dienofilo (e anche del diene) viene mantenuta nei prodotti: entrambi i nuovi legami vengono formati nello stato di transizione della reazione 4 Chimica Organica II Reazione di Diels-Alder: orientazione R R R Z Z Z Z Z R R R Z La reazione tra un diene e un dienofilo asimmetrici porta preferenzialemente alla formazione dei prodotti “orto” e “para”. La selettività è molto alta se Z = NO2. H COOH endo COOH COOH eso H La reazione tra un diene ciclico e un dienofilo asimmetrico porta preferenzialemente alla formazione dei prodotto “endo”. 5 Chimica Organica II Reazione di Diels-Alder: meccanismi Z Z Intermedio diionico · · Intermedio diradicalico Meccanismo concertato 6 Chimica Organica II Reazione di Diels-Alder: orbitali di frontiera La reazioni avvengono per sovrapposizione tra l’orbitale molecolare occupato a più alta energia (HOMO) di un reagente e l’orbitale vuoto a più bassa energia (LUMO) dell’altro solo se i lobi positivi e negativi di ciasun orbitale si sovrappongono. LUMO HOMO Non c’è corretta sovrapposizione 7 Chimica Organica II Reazione di Diels-Alder: orbitali di frontiera Diene Antilegame Dienofilo E LUMO HOMO Legame 8 Chimica Organica II Reazione di Diels-Alder: effetto dei sostituenti Domanda elettronica inversa Diene Dienofilo Diene Dienofilo Diene Dienofilo SED SEA SED SEA E 9 Chimica Organica II Reazione di Diels-Alder: orientazione I sostituenti non alterano solamente l’energia degli orbitali molecolari, ma anche la loro distribuzione. Effetto dei sostituenti sugli MO del dienofilo X: C Z C: sost. debolmente ED Z: sost. EA X: Sost. fortemente ED X: C Z 10 Chimica Organica II Reazione di Diels-Alder: Effetto dei sostituenti sugli MO del diene X: C Z C :X Z X: C Z C :X Z 11 Chimica Organica II Reazione di Diels-Alder C Z Z Domanda elettronica “normale” C Z X: Domanda elettronica inversa X: Z 12 Chimica Organica II Reazione di Diels-Alder: selettività endo-eso O O O O O O O O O O O O 13
Scaricare