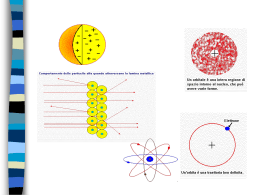
MPT – Capitolo 7 Orbitali ed elettroni Orbitali ed elettroni Elettroni : Carica elettrica negativa; sono attratti dal nucleo Forza elettrostatica: Quindi: • L'attrazione aumenta con l'aumentare di Z (carica del nucleo). • L'attrazione diminuisce con l'aumentare della distanza dal nucleo. C'è quindi un parallelismo tra la forza di attrazione che gli elettroni percepiscono nei confronti del nucleo e l'energia che si deve impiegare per togliere all'atomo in questione i suoi elettroni (uno alla volta). Maggiore è la forza di attrazione e maggiore sarà l'energia impiegata per separare l'elettrone dal suo atomo. Un atomo a cui è stato tolto uno o più elettroni non è più un elemento neutro, ed è chiamato quindi ione. Per questo motivo l'energia necessaria per rimuovere un elettrone da un atomo è chiamata energia di ionizzazione. Energia di ionizzazione E1: L'energia di prima ionizzazione è la quantità di energia che è necessaria per togliere il primo elettrone da un atomo (quello legato in modo più debole. Esempio: Per rimuovere un elettrone da un atomo di cloro occorrono 1251 KJ/mol di energia. Cl(g) + E1 --------> Cl+ + eL'importante è paragonare le energie di ionizzazione dei vari elementi (Vedi tab. 13.1 e pag. 205 libro). Sarebbe logico un aumento costante di E1, aumentando Z. Non è così. L'unica spiegazione è che il valore basso che segue il picco significa che questo elettrone si trova ad una distanza maggiore rispetto agli altri elettroni precedenti. E consegue un modello di organizzazione degli elettroni a livelli. Gli elettroni si muovono attorno al nucleo, disponendosi su determinati livelli che si trovano a distanze diverse dal nucleo e ai quali corrispondono precisi valori di energia. Guardiamo le ionizzazioni del Litio 1 MPT – Capitolo 7 Orbitali ed elettroni Ione o atomo Energia in KJ/mol Fattore rispetto al precedente Li 520 - Li+ 7297 14 volte maggiore Li2+ 11816 Meno di 2 volte maggiore Osservando lo schema a pagina 207 si osservano 6 (7) livelli (l'ultimo non ècompleto). Livello Atomi Elettroni Primo 2 elementi 2 Secondo 8 elementi 8 Terzo 8 elementi 8 Quarto 18 elementi 18 Quinto 18 elementi 18 Sesto 32 elementi 32 Settimo (32 elementi) (32) Regole per l'ordine degli elettroni • • • • Gli elettroni si dispongono su livelli energetici ben distinti. Ci sono 7 livelli. Ciascun livello ha un numero massimo di elettroni che può contenere. Gli elettroni si dispongono a partire dal primo livello, in ordine. Solo quando un livello è pieno si passa al successivo, che si trova ad una distanza maggiore. 2 MPT – Capitolo 7 Orbitali ed elettroni Primo approccio alla tavola periodica • Osservate la lunghezza delle righe, chiamate anche periodi. • I periodi terminano con un elemento che ha tanti elettroni quanti ne servono per riempire tutto il livello indicato dal periodo (nonché quelli sottostanti). • Si osservano 7 periodi. • C'è anche un ordine verticale; le colonne si chiamano gruppi e il significato dei gruppi verrà discusso più avanti. Energia di ionizzazione Dall'altoal basso aumenta la distanza che gli elettroni hanno dal nucleo e quindi diminuisce l'energiadi ionizzazione. Da sinistra a destra aumenta la carica del nucleo senza che aumenti la distanza degli elettroni, per cui si ha un aumento dell'energia di ionizzazione. Ei diminuisce Ei aumenta Affinità elettronica È il contrario della energia di ionizzazione, corrisponde cioè all'energiache si guadagna regalando un elettrone ad un atomo neutro. Si osservi come da sinistra a destra aumenta l'affinitàelettronica (aumentando la carica Z del nucleo). In verticale si osserva una variazione minima. C'èquindi un analogia per gruppi. 3 MPT – Capitolo 7 Orbitali ed elettroni Dimensione dell'atomo Da sinistra a destra aumenta Z: gli elettroni sono più attratti dal nucleo e quindi più compatti. In verticale la dimensione aumenta perché aumenta la distanza dei livelli dal nucleo. Raggio aumenta Raggio diminuisce Metalli, non metalli e semimetalli I metalli hanno come caratteristica: Ei bassa, Ae bassa. Gli elettroni più esterni sono poco attratti dal nucleo e non c'è una grande tendenza ad acquistare elettroni; tendenzialmente perdono elettroni. I non metalli: Ei alta, Ae alta. Gli elettroni esterni sono molto attratti dal nucleo e c'èuna forte tendenza all'acquisto di ulteriori elettroni; tendenzialmente acquistano elettroni. I semimetalli sono gli elementi sulla linea di confine. Hanno un comportamento ambiguo. I gas nobili, avendo l'ultimoorbitale pieno non interagiscono mai con gli altri elementi. Per questo motivo hanno una “classificazione” a sé. 4 MPT – Capitolo 7 Orbitali ed elettroni 5 I gruppi Osserviamo la collocazione degli elementi nella tavola periodica e la struttura elettronica suddivisa in livelli. Esempio 1: I metalli alcalini Elemento Z 1° 2° 3° 4° 5° 6° Li 3 2 1 Na 11 2 8 1 K 19 2 8 8 1 Rb 37 2 8 8 18 1 Cs 55 2 8 8 18 18 1 Fr 87 2 8 8 18 18 32 7° 1 Il livello più esterno contiene sempre solamente un elettrone. Questo è l'elettroneche viene scambiato nelle reazioni chimiche. Tutti gli altri non hanno influsso sulla reattività. Composti tipici: Con l'acqua : MetOH Con l' ossigeno : Met 2O Con il cloro : MetCl Facciamo lo stesso ragionamento per i metalli del secondo gruppo II Elemento Z 1° 2° 3° 4° 5° 6° Be 4 2 2 Mg 12 2 8 2 Ca 20 2 8 8 2 Sr 38 2 8 8 18 2 Ba 56 2 8 8 18 18 2 Ra 88 2 8 8 18 18 32 7° 2 Composti tipici Con l'acqua : Met(OH) 2 Con l' ossigeno : MetO Con il cloro : Met2Cl Con gli elementi alogeni del VII gruppo Elemento Z 1° 2° 3° 4° F 9 2 7 Cl 17 2 8 7 Br 35 2 8 8 17 I 53 2 8 8 18 5° 17 Problemino! Qui abbiamo a volte 7 a volte 17 elettroni sull'ultimolivello. Tuttavia per motivi che vediamo poco più avanti i 17 elettroni sono divisi in un primo gruppo di 10 e un secondo di 7. Il MPT – Capitolo 7 Orbitali ed elettroni 6 primo gruppo di 10 è irrilevante dal punto di vista chimico, quindi abbiamo di nuovo 7 elettroni per tutti i livelli più esterni. Composti tipici Con il sodio: NaAlog Con l'idrogeno: HAlog Nota Il comportamento chimico di un elemento non dipende da tutti gli elettroni, e neppure sempre da quelli dell'ultimolivello ma solamente da quelli più esterni; questi elettroni sono chiamati elettroni di valenza. Il numero di elettroni di valenza corrisponde al numero romano che si trova indicato sopra il gruppo. Orbitali e sottolivelli I livelli introdotti prima, in realtà non sono altro che una osservazione empirica. Gli elettroni hanno una organizzazione più complessa che si suddivide in orbitali (una specie di livello, ma più sofisticato) e dei sottolivelli (chiamati s,p,d,f) cioè delle suddivisioni interne degli orbitali. Le passiamo ora in rassegna. I livelli 6 e 7 sono analoghi al livello 5. Orbitale Sottolivello Occupazione Totale di elettroni 1 s 2 2 2 s p 2 6 8 3 s p d 2 6 10 18 4 s p d f 2 6 10 14 32 5 s p d f g 2 6 10 14 - Osservazioni • Ogni orbitale ha uno o più sottolivelli. • Ciascun sottolivello ha un numero massimo di elettroni che più accogliere. • I livelli visti prima e gli orbitali non coincidono, quindi non coincidono nemmeno con i periodi. • Gli elettroni nei sottolivelli vanno a 2 a 2, quindi in un orbitale ci sono: – 1 sottolivello s con 2 elettroni. – 3 sottolivelli p con 2 elettroni ciascuno e un totale di 6 elettroni. – 5 sottolivelli d con 2 elettroni ciascuno e un totale di 10 elettroni. – 7 sottolivelli f con 2 elettroni ciascuno e un totale di 14 elettroni . MPT – Capitolo 7 Orbitali ed elettroni – 9 sottolivelli g con 2 elettroni ciascuno e un totale di 18 elettroni, ma i sottolivelli oltre f non sono in pratica mai osservati e così via... Simbologia tecnica degli orbitali Il numero indica l'orbitale,la lettera il sottolivello, il numero all'esponenteindica il numero di elettroni presenti nello specifico sottolivello Esempio: Mg : Z=12 1s22s22p63s2 La suddivisione in livelli è la seguente 1s2 2s22p6 3s2 1 livello 2 livello 3 livello Si può anche abbreviare indicando la configurazione elettronica del gas nobile inferiore cioè 1s22s22p63s2 è equivalente a [Ne]3s2 Il riempimento dei sottolivelli segue un ordine che non coincide con quello degli orbitali (cioè incerti casi il sottolivello influisce più che il livello stesso). Per esempio il 3° orbitale ha posto per 18 elettroni , mentre il 3 livello solo per 8. Questo perché il sottolivello 3d ha una distanza dal nucleo maggiore del sottolivello 4s e si riempie dopo 4s; tutti i livelli di si comportano in maniera analoga! L'ordinedel riempimento dei sottolivelli è a zig-zag, come indicato a pag. 219 nella figura 13.18. Osserva anche la figura 13.21 a pag. 221, vedrai come sono gli elettroni di valenza per gli elementi. Esempi Calcio Ca: 1s22s22p63s23p64s2 qui tutto regolare Bromo Br: 1s22s22p63s23p64s23d104p5 qui si vede l'effetto d Nel caso del bromo gli elettroni più esterni sono 4s24p5, 3d anche se viene riempito dopo 4s in realtà si trova più vicino al nucleo e nel caso del bromo questi elettroni non hanno un influsso sul comportamento chimico dell'elemento.Per questo, come già precedentemente visto, sono 7 gli elettroni di valenza. Nota: Gli elettroni s e p si trovano sempre sul proprio periodo, mentre i sottolivelli d e f saltano. Gli elettroni s e p sono sempre di valenza, se ci sono, mentre gli elettroni d e f sono di valenza (cioè vengono in qualche modo scambiati con altri atomi) solamente se nella descrizione della configurazione elettronica sono gli ultimi elettroni indicati nella stringa Esempio Br: 1s22s22p63s23p64s23d104p5 gli elettroni d non sono di valenza Fe: 1s22s22p63s23p64s23d6 gli elettroni d sono di valenza La proiezione di Lewis Per l'effettovisto prima spesso per indicare la configurazione elettronica di un elemento si indicano 7 MPT – Capitolo 7 Orbitali ed elettroni solamente gli elettroni di valenza. Nella proiezione di Lewis si indicano solamente gli elettroni s e p dell'ultimoorbitale, nella maniera indicata dal libro a pagina 217. La proiezione di Lewis, naturalmente, può essere unicamente indicata per gli elementi del gruppo principale; se infatti la descrizione della configurazione elettronica termina con d o f, anche questi elettroni sono di valenza e devono essere descritti. Con questa drastica limitazione, in realtà possiamo ben convivere perché la maggior parte degli elementi e dei composti che vedremo sono costituiti da elementi del gruppo principale. 8
Scaricare