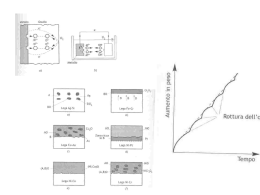
Fondamenti di corrosione Termodinamica Celle galvaniche con elettroliti senza ioni metallici E =E + a 0, Fe 0.059 ⎛ log⎜⎜ a 2 ⎝ Fe + + ⎞ ⎟⎟ ⎠ ⎛ ⎜ ⎜a + E =E + 0.059 log⎜ H c 0, H ⎜ 12 2 ⎜⎜ p H ⎝ 2 non dipende da pH; ⎞ ⎟ ⎟ ⎟ ⎟ ⎟⎟ ⎠ dipendono da pH. ⎛ ⎜ 1 E =E + 0.059 log⎜ c 0, O ⎜a 2 ⎝ OH − ⎞ ⎟ ⎟ ⎟ ⎠ Diagrammi di Pourbaix Contengono linee di equilibrio che suddividono campi di stabilità di metallo ed ossidi: Significato del diagramma: indicare le regioni di immunità e passività dalla corrosione e di corrosione. Microcelle su elettodo singolo +O2 +H2O anodi e catodi localizzati: - celle di concentrazione di ossigeno - celle al bordo di grano - celle tra fasi multiple - celle da impurezze. Cinetica La quantità di metallo corroso si ottiene dalla eq. di Faraday: iAt nF con i la densità di corrente, A l’area dell’elettrodo, da cui si ottiene la velocità di corrosione: n °moli = d (n °moli) iA = ∝ i. dt nF All’equilibrio la velocità di reazione diretta ed inversa sono uguali ⎛ − ∆G ⎞ ⎛ − ∆G ⎞ C⎟ A ⎜ ⎟ i = L exp = L exp⎜ ⎜ RT ⎟ ⎜ RT ⎟ 0 A C ⎝ ⎠ ⎝ ⎠ i0 è la corrente di scambio. Se si applica un potenziale al metallo, ηA, lo schema di energia diventa x x Le barriere si modificano di + xη A nF (anodo) e − (1 − x)η AnF (catodo).La corrente risultante è ⎛ − ∆GC − (1 − x)η A nF ⎞ ⎛ − ∆G A + xη A nF ⎞ ⎟ ⎜ ⎟ i = L exp − L exp⎜ A A C ⎜ ⎟ ⎜ ⎟ RT RT ⎝ ⎠ ⎝ ⎠ ⎧⎪ ⎛ xη nF ⎞ ⎛ − (1 − x)η A nF ⎞⎫⎪ A ⎜ ⎟ ⎟⎬ i = i ⎨exp − exp⎜ A 0 ⎪ ⎜ RT ⎟ ⎜ ⎟⎪ ; RT ⎠ ⎝ ⎠⎭ ⎩ ⎝ se ηA è alto, il secondo temine è trascurabile e quindi ⎧⎪ ⎛ xη nF ⎞⎫⎪ i = i ⎨exp⎜ A ⎟⎬ da cui A 0 ⎪ ⎜ RT ⎟⎪ ⎩ ( )+ a A ( ). η = b log i A ⎝ A A a = −b log i A A 0 ⎠⎭ eq. di Tafel Es. corrosione di Zn in HCl parametri importanti: icorr, Ecorr, bA. Polarizzazione Passivazione Formazione di uno stato superficiale protettivo Æ inibizione delle reazioni di corrosione. Per ogni ambiente di reazione occorre conoscere la specifica serie galvanica (es. acqua di mare) che differisce dalla serie elettrochimica degli elementi. Si notano inversioni di nobiltà dovute a fenomeni di passivazione o de-passivazione nello specifico ambiente. Forme di corrosione Corrosione generalizzata: reazione elettrochimica uniforme sulla superficie metallica. Non c’è caduta ohmica. Corrosione per contatto galvanico: reazione che avviene quando due metalli diversi siano in contatto. La velocità di corrosione dipende dal potenziale misto Ecorr, M+N. La corrente di corrosione sarà quasi del tutto a carico del metallo N. Corrosione selettiva (lega multifasica) e de-alligazione (soluzione solida). Corrosione per vaiolatura (pitting): attacco corrosivo localizzato. Avviene soprattutto per attacco da cloruri. Corrosione in fessura (crevice): attacco localizzato in fessure dove vi siano soluzioni stagnanti. Corrosione intergranulare: attacco localizzato ai bordi grano. Corrosione sotto sforzo (stress corrosion): formazione di cricche per effetto combinato di corrosione e sollecitazione meccanica. Ampia casistica: da innesco in punti “deboli” a infragilimento da idrogeno Corrosione erosione: aumento della velocità di reazione per moto relativo di soluzione e metallo. Corrosione per cavitazione, sfregamento (fretting). Protezione dalla corrosione Inibitori: modificano la cinetica elettrodica. - anodici: aumentano la sovratensione del processo anodico. Es. per il Fe cromati, nitriti, alcalini (Na3PO4) in presenza di ossigeno. - catodici: aumentano la sovratensione del processo catodico. Es. sali mercurici per Zn, bicarbonato di Ca che precipita come carbonato. - di adsorbimento: bloccano le aree elettrodiche adsorbendosi. Es. ammine, grosse molecole organiche contenenti S, OH,... Strati metallici: placcature ricoprenti (anche elettrodeposte). Strati di conversione: film superficiali formati in situ. Anodizzazione di Al, cromatizzazione (attenzione! Cr6+), fosfatizzazione. Strati organici: vernici, plastiche. Protezione catodica: correnti impresse, anodi sacrificali (lega di Mg).
Scaricare