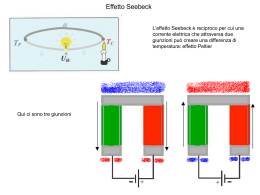
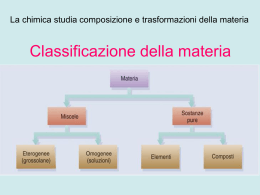
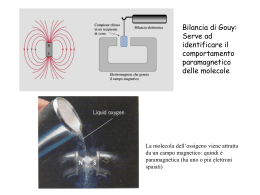
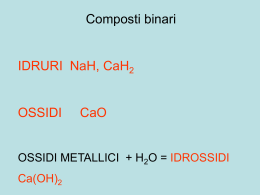
UNIVERSITA' DEGLI STUDI DI SASSARI Dipartimento di Chimica Mauro Rustici Dipartimento di chimica, Via Vienna 2, 07100 Sassari email [email protected] Elementi di Chimica Anno Accademico 2011/2012 2 Indice 1 Materia ed Energia 1.1 Materia ed Energia . . . . . . . . . . . . . . . . . 1.1.1 Elementi e composti . . . . . . . . . . . . 1.1.2 Teoria atomica di Dalton . . . . . . . . . . 1.1.3 Particelle fondamentali dell’atomo . . . . . 1.1.4 Modelli atomici di Thomson e Rutherford 1.1.5 Numero atomico, numero di massa. Isotopi 1.1.6 Pesi atomici e unità di massa atomica . . . 1.1.7 Mole. Numero di Avogadro . . . . . . . . . . . . . . . . . 7 7 7 10 13 14 15 17 20 . . . . . 23 23 28 32 34 37 . . . . 41 41 42 43 46 . . . . . 47 47 47 48 49 52 5 Legame covalente 5.1 Teoria del legame covalente . . . . . . . . . . . . . . . . . . . . . 5.1.1 Teoria del legame di valenza . . . . . . . . . . . . . . . . . 5.1.2 Legami singoli e doppi . . . . . . . . . . . . . . . . . . . . 55 55 55 57 . . . . . . . . . . . . . . . . 2 Teorie Atomiche 2.1 Modello atomico di Bohr . . . . . . . . . . . . . . . . 2.1.1 Dualismo onda particella . . . . . . . . . . . . 2.1.2 Modello quantomeccanico dell’atomo . . . . . 2.1.3 Atomi polielettronici . . . . . . . . . . . . . . 2.2 Struttura elettronica e tavola periodica degli elementi 3 Legame Chimico 3.1 Legame Chimico . . . . . . . . . . 3.1.1 Legame Ionico . . . . . . . . 3.1.2 Teoria del legame di valenza 3.1.3 Legami covalenti polari . . . . . . . . . . . . . . . . . . . 4 Geometria molecolare 4.1 Geometria molecolare . . . . . . . . . . . . 4.1.1 Strutture di Lewis a legame singolo 4.1.2 Eccezioni alla regola dell’ottetto . . 4.1.3 Teoria VESPR e forma molecolare . 4.1.4 Forma molecolare e polarità . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 4 INDICE 5.1.3 5.1.4 Teoria dell’Orbitale molecolare MO . . . . . . . . . . . . . Legame metallico . . . . . . . . . . . . . . . . . . . . . . . 6 Numeri di ossidazioni, nomenclatura e reazioni 6.1 Numero di ossidazione . . . . . . . . . . . . . . 6.2 Nomenclatura tradizionale . . . . . . . . . . . . 6.3 Nomenclatura IUPAC . . . . . . . . . . . . . . 6.4 Reazioni di ossido riduzione . . . . . . . . . . . 7 Stati di aggregazione della materia 7.1 Stati di aggregazione della materia 7.1.1 Regola delle fasi . . . . . . . 7.1.2 Forze intermolecolari . . . . 7.2 Stato gassoso . . . . . . . . . . . . 7.2.1 Legge di Dalton . . . . . . . 7.3 Stato solido . . . . . . . . . . . . . 7.4 Stato liquido . . . . . . . . . . . . . 7.4.1 Viscosità . . . . . . . . . . . 7.4.2 Tensione superficiale . . . . 7.5 La diffusione . . . . . . . . . . . . . . . . . . . . . . . 8 Termodinamica 8.1 termodinamica cenni . . . . . . . . . 8.1.1 Principio zero . . . . . . . . . 8.1.2 lavoro e calore . . . . . . . . . 8.1.3 Entalpia . . . . . . . . . . . . 8.2 La seconda legge della termodinamica 8.3 Riflessioni sul significato dell’entropia . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . chimiche . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9 Soluzioni 9.1 Soluzioni . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9.2 Proprietà colligative . . . . . . . . . . . . . . . . . . . . . . . . 9.2.1 Abbassamento della tensione di vapore . . . . . . . . . . 9.2.2 Innalzamento ebullioscopico e abbassamento crioscopico . 9.2.3 Pressione osmotica . . . . . . . . . . . . . . . . . . . . . 9.3 Distillazione . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 9.3.1 Diagramma temperatura-composizione . . . . . . . . . . 9.3.2 Gli azeotropi . . . . . . . . . . . . . . . . . . . . . . . . 58 60 . . . . 63 63 65 72 74 . . . . . . . . . . 77 77 78 78 81 82 85 87 88 88 90 . . . . . . 91 91 91 91 94 95 100 . . . . . . . . 103 103 104 104 107 107 110 113 114 10 Equilibrio chimico 117 10.1 Equilibrio chimico . . . . . . . . . . . . . . . . . . . . . . . . . . . 117 10.2 Equilibri eterogenei implicanti fasi gassose . . . . . . . . . . . . . 126 10.3 Equilibri di solubilità . . . . . . . . . . . . . . . . . . . . . . . . . 127 5 INDICE 10.4 Equilibri acido base . . . . . . . . 10.4.1 Prodotto ionico dell’acqua 10.4.2 Acidi e basi deboli . . . . 10.4.3 Acidi poliprotici . . . . . . 10.4.4 Equilibri idrolitici . . . . . 10.4.5 Soluzioni tampone . . . . 10.4.6 Capacità tamponante . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 129 132 134 136 139 145 147 11 Processi elettrochimici e reazioni redox 151 11.1 Processi elettrochimici e reazioni redox . . . . . . . . . . . . . . . 151 11.1.1 Serie dei potenziali normali . . . . . . . . . . . . . . . . . 154 12 Cinetica chimica 12.1 Velocità di reazione . . . . . . . . . . . . . . . . . . 12.1.1 Le leggi base della cinetica . . . . . . . . . . 12.1.2 Cinetica del primo ordine . . . . . . . . . . 12.2 Effetto della temperatura sulla velocità di reazione . 12.3 Reazioni catalizzate da enzimi . . . . . . . . . . . . 13 Stechiometria 13.1 Mole . . . 13.2 Soluzioni . 13.3 Gas . . . . 13.4 pH . . . . 13.5 Solubilità esercizi . . . . . . . . . . . . . . . . . . . . . . . . . tipici . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 157 157 158 161 162 164 . . . . . 167 167 172 174 176 177 14 libri consigliati 181 14.1 Libri di testo consigliati . . . . . . . . . . . . . . . . . . . . . . . 181 6 INDICE Capitolo 1 Materia ed Energia 1.1 Materia ed Energia La materia costituisce la sostanza che ci circonda e che presenta una massa e un volume. In particolare la chimica è interessata alla composizione della materia e ai tipi e alle quantità di sostanze semplici che la costituiscono. Una sostanza è un tipo di materia con composizione definita e costante. Per conoscere la materia è necessario conoscere le sue proprietà che possiamo distinguere in proprietà fisiche e proprietà chimiche, le prime sono quelle proprietà che una sostanza ha di per sé come il colore, il punto di fusione, la densità la polarizzabilità e cosı̀ via. Le proprietà che invece sono relative alla capacità che ha la materia di cambiare la propria composizione appartengono alla seconda categoria. La materia come è noto si trova in tre forme fisiche definite come stato gassoso, stato liquido e stato solido. Vedremo che questi tre stati della materia sono in relazione tra loro attraverso la temperatura e attraverso le forze di coesione che sussistono tra i vari elementi che la costituiscono. Cercheremo di capire le proprietà macroscopiche di una sostanza (osservabili) mediante le proprietà microscopiche che non sono direttamente osservabili. Le trasformazioni chimiche e fisiche sono accompagnate generalmente da variazione di energia cercheremo pertanto di capire in che modo l’energia permette il verificarsi di questi processi fisici o chimici. 1.1.1 Elementi e composti La materia si presenta in stati di aggregazione diversi a seconda della temperatura e della pressione, è costituita da particelle elementari piccolissime, dette atomi che si differenziano per le loro proprietà. Gli atomi con le stesse proprietà costituiscono gli elementi. Attualmente si conoscono 118 elementi di cui solo 90 presenti in natura mentre tutti gli altri sono ottenuti artificialmente. I 90 elementi naurali si trovano in natura in percentuali diverse. Mentre gli elementi sono costituiti da atomi della stessa specie, i composti sono costituiti da due o più atomi di specie M. Rustici, Chimica di base 8 Materia ed Energia diverse presenti in proporzioni definite e costanti. Un aggregato di pochi atomi costituisce una molecola. La concezione atomistica della materia è molto antica e risale alla scuola filosofica di Leucippo e del suo allievo Democrito (460 a. C.). Questi filosofi postulavano che l’universo, nella sua totalità, fosse costituito da atomi (particelle indivisibili), con diverse dimensioni e forma, che si muovevano continuamente e che impartivano alla materia le proprietà caratteristiche. Il moto degli atomi non dipendeva da forze esterne, ma era una qualità intrinseca della materia. L’atomismo di Leucippo e Democrito era puramente meccanico: il movimento, gli atomi e il vuoto erano i tre ingredienti necessari per spiegare l’esistenza del cosmo, in una visione puramente materialistica. La concezione atomistica fu completamente oscurata dal pensiero di Aristotele il quale negando l’esistenza del vuoto assumeva che la materia fosse continua (horror vacui). Secondo la fisica Aristotelica la velocità di un corpo varia con il peso e la resistenza del mezzo in cui si muove; nel vuoto, pertanto, il corpo raggiungerebbe una velocità infinita indipendemente dal suo peso in contrasto con l’esperienza. L’esistenza degli atomi avrebbe portato come conseguenza alla presenza del vuoto e pertanto la materia non avrebbe potuto avere una struttura atomica ma solo una struttura continua. La materia era quindi divisibile all’infinito e proprio perché era impossibile arrivare a porzioni di materia indivisibili la divisione avrebbe portato le particelle di materia ad essere sempre più piccole, fino a quando, se ulteriormente divise, le proprietà della sostanza iniziale sarebbero state perdute. Da quel momento in poi la sostanza iniziale sarebbe diventata una sostanza nuova. La tesi aristotelica della divisibilità all’infinito della materia portò ad accantonare completamente le teorie di Leucippo e Democrito che rimasero nell’ombra per molti secoli. Il concetto di atomo come costituente fondamentale della materia fu ignorato per tutto il Medioevo e solo nel XVI secolo cominciò a ripresentarsi nella discussione filosofica. Due forme di atomismo, l’una di tipo meccanico, ereditata dalla filosofia degli empiristi greci l’altra derivata dall’idea della divisibilità infinita nella teoria del continuo aristotelico si contrastarono per circa due secoli, convergendo alla fine nella teoria atomica moderna. La combinazione dei principi atomistici con i principi aristotelici condusse al concetto dei minima naturalia come le più piccole parti di materia che continuavano ad avere le proprietà della sostanza iniziale, ogni tipo di sostanza ha la sua specifica minima naturalia. Intorno al 1600 gli alchimisti dell’epoca avevano imparato a diventare esperti nella metallurgia, a produrre metalli e nello stesso tempo avevano imparato ad usare la bilancia, come strumento di misura, nei loro esperimenti. Uno dei principali padri della moderna chimica è sicuramente Lavoiser, il quale effettuando accurate misure quantitative rivoluzionò i principali concetti relativi alla materia e alle sue trasformazioni. Nel 1768 Lavoiser dimostrò la falsità dell’antica credenza che la terra potesse generarsi dall’acqua. Lavoisier studiò la M. Rustici, Chimica di base 9 Materia ed energia combustione osservando che l’aria fosse essenziale a tale processo . Dimostrò che il diamante poteva essere bruciato all’aria liberando la stesso tipo di gas (anidride carbonica) che si produce bruciando carbone; cosı̀ facendo mise in evidenza che anche il diamante è costituito da carbone. Attente misure sulla combustione dei metalli distrussero la teoria del flogisto. Fino ad allora si pensava che i metalli scaldati all’aria perdessero il cosiddetto flogisto trasformandosi in calce. Fu Lavoiser che controllando, il peso della massa prima della reazione e dopo, si accorse che il peso aumentava dopo il riscaldamento e quindi il metallo reagiva con uno dei gas costituenti l’aria (ossigeno). Si deve sempre a Lavoisier la scoperta che l’aria privata di ossigeno conteneva un altro gas che non permetteva la combustione e al quale Lavoisier dette il nome di Azoto. Tutti questi esperimenti portarono alla conclusione che il peso totale delle sostanze che prendono parte alla reazione rimane invariato anche dopo la reazione. In una trasformazione chimica la massa dei reagenti è uguale a quella dei prodotti, in altre parole nulla si crea e nulla si distrugge ma tutto si trasforma. Questa legge rappresenta la legge empirica della conservazione della massa. Una diramazione degli studi sulla combustione portarono Lavoisier ad esplorare il processo della respirazione e assieme al fisico Laplace dimostrò che l’energia degli animali dipenedeva dalla quantità di ossigeno inalata e che il processo della respirazione è un processo analogo alla combustione che porta a produrre anidride carbonica come prodotto della respirazione. Sfortunatamente il padre della chimica moderna, che ai fantasmi del flogisto aveva sostituito la legge della conservazione della massa e che aveva battezzato l’ossigeno, l’idrogeno, l’azoto verrà ghigliottinato nella repubblica di Robespierre accusato da Jean-Paul Marat al quale Lavoisier aveva impedito di far parte dell’Accademia delle Scienze. Marat era un medico e sosteneva la teoria del flogisto assieme ad altre astruse teorie e per tale motivo non fu accetato all’Accademia. Marat divenuto uno dei protagonisti della rivoluzione francese e trovò il modo di vendicarsi accusando Lavoiser di aver diluito il tabacco e di aver bloccato l’erogazione dell’ aria facendo costruire un muro difensivo intorno alla città. Il processo davanti al tribunale rivoluzionario durò meno di ventiquattor ore. Il pomeriggio dell’8 maggio 1794 Lavoisier salı̀ i gradini del patibolo, offrendo la sua bella testa di cinquantenne alla lama della ghigliottina. Si racconta infatti, che nella Parigi del terrore, la replica di un giudice del tribunale rivoluzionario alla domanda dell’imputato Antoine Lavoisier: il chimico più illustre del suo tempo, che aveva pregato i magistrati di rinviare la sua condanna a morte come ex ministro di Luigi XVI per dargli modo di perfezionare, dal carcere, le misure del nuovo sistema metrico decimale fu: “La repubblica non ha bisogno di scienziati”. Quando la testa di Lavoisier rotolò per terra tra le urla della plebaglia, il matematico Joseph Lagrange, che aveva assistito all’esecuzione, guardò l’orologio e disse: È “bastato un secondo per staccargli la testa, ma non basterà un secolo M. Rustici, Chimica di base 10 Materia ed Energia perche’ nasca un altro come lui”. Non era retorica. Lo scopritore dell’ossigeno e dell’azoto, “l’uomo che rivoluzionò la chimica con la bilancia”, fu davvero una personalità irripetibile. 1.1.2 Teoria atomica di Dalton La legge di Lavoiser e le altre che seguirono condussero John Dalton ad esprimere la prima teoria atomica basata sulla legge di conservazione della massa ( Lavoisier); dalla legge di Proust o legge delle proporzioni definite e dalla legge stessa individuata da Dalton legge delle proporzioni multiple. La legge di Proust asserisce che “quando due o più elementi reagiscono, per formare un determinato composto, si combinano sempre secondo proporzioni in massa definite e costanti”. La legge delle proporzioni multiple asserisce invece che “quando due o più elementi formano un composto tra loro, allora il rapporto delle masse dei secondi elementi che si combinano con una massa fissa del primo elemento stanno tra loro in rapporti definiti da numeri interi piccoli.”. Ad esempio il carbonio forma due composti diversi con l’ossigeno, monossido di carbonio e biossido di carbonio. 100 grammi di carbonio reagiscono con 133 grammi di ossigeno per dare il monossido di carbonio e con 266 grammi di ossigeno per dare il biossido di carbonio. Il rapporto tra le masse di ossigeno che reagiscono con 100 grammi di carbonio è 266 2 ' 133 1 Queste leggi portarono Dalton a formulare la sua teoria atomistica che può essere cosı̀ riassunta a La materia è costituita da particelle indivisibili dette atomi. b Gli atomi sono caratterizzati da una loro massa. Gli atomi di uno stesso elemento hanno la stessa massa e le stesse proprietà; elementi diversi hanno proprietà e masse diverse. c I composti sono formati dalla combinazione chimica di atomi di differenti elementi in un rapporto espresso da numeri piccoli e interi. d Nel corso di una reazione chimica gli atomi non si creano né si distruggono e mantengono la loro individualità. La teoria atomistica formulata da Dalton oltre ad interpretare in modo soddisfacente molte osservazioni sperimentali ha costituito un approccio euristico utile per condurre a nuove speculazioni come la la determinazione delle masse atomiche. M. Rustici, Chimica di base 11 Materia ed energia Dalton assunse che ogni atomo possedesse una sua specifica massa (peso atomico) la cui determinazione assoluta risultava ovviamente impossibile da determinare. Dalton provò a superare il problema determinando le masse atomiche relative ad un elemento convenientemente scelto. Per convenzione assunse che l’atomo di idrogeno avesse peso atomico pari ad 1 e costruı̀ nel 1803, sulla base di tale assunzione, la prima tabella dei pesi atomici. Il chimico e fisico francese Joseph Louis Gay-Lussac sula base di una serie di reazioni in fase gassosa enunciò la legge di combinazione dei volumi. Quando due sostanze gassose reagiscono tra loro per formare nuove sostanze, anche esse gassose, a temperatura e pressione costante i volumi dei gas reagenti e quelli dei prodotti stanno tra loro in rapporti espressi da numeri interi e semplici. Sulla base di queste osservazioni il chimico Avogadro nel 1811 sperimentali ipotizzò che le particelle ultime che costituiscono gli elementi allo stato gassoso siano costituiti da raggruppamenti atomici dette molecole. In particolare enunciò il seguente postulato volumi uguali di gas diversi nelle stesse condizioni di temperatura e pressione contengono lo stesso numero di molecole In questo modo si poteva comprendere dai dati sperimentali perchè 1 volume di cloro mescolato con un volume di idrogeno potesse dare 2 volumi di acido cloridrico e non solo 1 volume di acido cloridrico. infatti se la reazione fosse stata H + Cl = HCl i rapporti stechiometrici sarebbero stati 1:1:1 dato che sperimentalmente si ottenevano rapporti stechiometrici di 1:1:2 si doveva assumere che la reazione avesse luogo tra molecole H2 + Cl2 = 2HCl analogamente per la reazione di produzione dell’ammoniaca a partire dai suoi elementi ci si sarebbe attesi 3H + N = NH3 un rapporto stechiometrico del tipo 3:1:1. Viceversa sperimentalmente si ottenevano rapporti stechiometrici 3:1:2 Che potevano essere perfettamente spiegati attraverso l’ipotesi di Avogadro, ipotizzando cioè l’esistenza delle molecole quindi 3H2 + N2 = 2NH3 M. Rustici, Chimica di base 12 Materia ed Energia Un’immediata applicazione pratica dell’ipotesi di Avogadro è data dalla determinazione delle masse molecolari ed atomiche relative delle varie sostanze allo stato gassoso. Supponiamo che wA e wB siano le masse di volumi uguali di gas contenenti un ugual numero di molecole. Il rapporto wA /wB costituisce il rapporto delle masse delle molecole dei due gas. Sia inoltre ρr la densità relativa (cioè il rapporto tra la densità di una sostanza rispetto ad una sostanza di riferimento entrambe nelle stesse condizioni di temperatura e pressione), ρA e ρB le densità dei gas A e B e infine wA e wB i pesi dei due gas occupanti un uguale volume V nelle stesse condizioni di pressione e temperatura allora ρA = wA V ρB = wB V (1.1) la densità relativa del gas A rispetto al gas B sarà ρr = ρA wA = ρB wB (1.2) poiché wA e wB contengono lo stesso numero di molecole il loro rapporto deve essere uguale al rapporto tra i rispettivi pesi molecolari MA e MB intesi come sommatoria dei rispettivi pesi atomici degli atomi costituenti le molecole. Quindi: ρr = MA ρA = ρB MB (1.3) In questo modo, il chimico italiano, calcolò con buona approssimazione il peso atomico dell’ossigeno valutandolo circa 15 volte quello dell’idrogeno anziché 8 volte, come allora si riteneva. Se infatti si esegue il rapporto tra le masse di un litro di ossigeno e un litro di idrogeno, nelle stesse condizioni di temperatura e di pressione, si hanno i seguenti risultati: massa di un litro di ossigeno 1.429 = = 16 massa di un litro di idrogeno 0.089 Considerando valido il principio di Avogadro, il valore 16 rappresenta quante volte la massa di una molecola di ossigeno supera quella di una molecola di idrogeno. Ripetendo la stessa esperienza per altri gas, si possono pertanto determinare le masse molecolari relative di tutti gli elementi allo stato gassoso (per l’azoto 14, per l’elio 2 ecc). Ponendo, per convenzione, la massa molecolare dell’idrogeno pari a 2 (perché la molecola di idrogeno è biatomica) e conoscendo il rapporto tra le masse di ossigeno ed idrogeno, si attribuisce alla molecola di ossigeno una massa pari a 32, a quella dell’azoto 28, a quella dell’elio 4 ecc). M. Rustici, Chimica di base 13 Materia ed energia L’ ipotesi di Avogadro, però, non venne accettata dai chimici più autorevoli del tempo. Il grande chimico Berzelius, ad esempio, non riusciva ad immaginare come due atomi simili potessero legarsi tra loro. Berzelius, infatti, immaginava che fossero le forze elettrostatiche a tenere uniti gli atomi e due atomi uguali avrebbero dovuto possedere le stesse caratterische elettriche e pertanto non c’erano ragioni affinché i due atomi possano unirsi tra loro. Passerà quasi mezzo secolo prima che i chimici rivalutino l’ipotesi di Avogadro. Fu grazie all’opera di un altro chimico italiano, che l’ipotesi di Avogadro venne rilanciata; Stanislao Cannizzaro comprese che proprio quelle idee costituivano la base per spiegare buona parte dei risultati di laboratorio conseguiti negli ultimi anni. Se B è rappresenta l’atomo di idrogeno per il quale assumiamo, secondo Cannizzaro, peso atomico 1 e peso molecolare 2 per la molecola biatomica, allora la densità relativa della specie A ricavabile dalla 2.3 diventa ρr = MA 2 ∴ MA = 2ρr (1.4) Il calcolo della densità relativa rispetto all’idrogeno permette quindi di valutare il peso atomico. I pesi molecolari ottenuti da misure di densità permisero a Cannizzaro di determinare, attraverso l’analisi chimica, la quantità con cui un elemento era contenuto in una quantità di composto numericamente uguale al suo peso molecolare. Cannizzaro ritenne che il peso atomico di un elemento è dato dalla più piccola quantità in peso con cui l’elemento si ritrova nei pesi molecolari dei suoi vari composti I pesi molecolari cosi determinati sono dei pesi relativi e pertanto adimensionali. 1.1.3 Particelle fondamentali dell’atomo Gli atomi contrariamente a quanto indicato dall’etimologia della parola non sono particelle indivisibili, ma sono costituiti a loro volte da particelle elementari; elettroni, protoni e neutroni. Le principali conoscenze sulla natura degli elettroni derivano dagli studi sulla carica dei gas. Tali studi venivano effettuati su tubi di vetro riempiti di gas rarefatti all’interno dei quali veniva fatta avvenire una scarica elettrrica tra due elettrodi metallici. Si generavano cosı̀ dei raggi che furono denominati raggi catodici poiché venivano emessi dal catodo (polo negativo) e si dirigevano verso l’anodo (polo positivo). Questi fasci avevano la caratteristica di essere deviati in presenza di campi elettrici e magnetici e la loro deflessione poteva essere visualizzata su uno schermo fluorescente. In particolare applicando un campo elettrico i fasci venivano deviati verso il polo positivo ed erano indipendenti dalla natura del gas. Il fisico Thomson riuscı̀ a determinare, attraverso M. Rustici, Chimica di base 14 Materia ed Energia questi esperimenti, il rapporto carica/massa (e/m) di queste particelle, denominate elettroni, sottoponendole all’azione contemporanea di un campo elettrico e di un campo magnetico. Se con H indichiamo il campo magnetico uniforme ed imponiamo ad esso di essere perpendicolare alla direzione dei raggi allora gli elettroni subiranno una forza pari a Hev dove v è la velocità dell’elettrone. In particolare l’elettrone percorrerà in tale situazione una traiettoria circolare con raggio di curvatura r che può essere misurato sperimentalmente, dalla deviazione del punto luminoso sullo schermo. Applicando la legge di Newton F = ma e sapendo che in questo caso l’accelerazione è l’accelerazione centrifuga v 2 /r possiamo scrivere che v2 e v ∴ = r m Hr Se, a sua volta, applichiamo un campo elettrico, esso eserciterà sull’elettrone una forza pari a Ee con E intensità del campo elettrico. In particolare se operiamo in modo tale che la forza che agisce sull’elettrone operata dal campo elettrico sia uguale a quella operata dal campo magnetico possiamo scrivere Hev = m Hev = Ee ∴ v= E H e quindi e E = 2 m H r tale valore risulta essere −1.76 · 1011 coulomb/Kg. Millikan a sua volta misurò la carica dell’elettrone che risultò essere pari a 1.602 · 10−19 coulomb e pertanto la massa di un singolo elettrone poteva essere valutata pari a 9·10−31 Kg. Essendo gli atomi elettricamente neutri l’atomo doveva contenere a sua volta particelle cariche positivamente. Esperimenti ottenuti sulla ionizzazione dell’idrogeno hanno mostrato che tali particelle positive denominate protoni sono effettivamente contenute negli atomi e hanno la stessa carica in valore assoluto dell’eletrone ma con una massa molto più grande precisamente 1836 volte maggiore di quella dell’elettrone ( 1.67 · 10−27 ). La massa dell’atomo di idrogeno risultò praticamente identica a quella del protone, tuttavia per gli altri atomi si trovarono masse molto più grandi a quelle calcolate con il contributo dei soli protoni. Questa differenza fu attribuita alla presenza nell’atomo di una nuova particella detta neutrone. 1.1.4 Modelli atomici di Thomson e Rutherford Il primo modello atomico prevedeva che i protoni costituissero una sfera di cariche positive all’interno della quale circolassero gli elettroni, modello che presto M. Rustici, Chimica di base 15 Materia ed energia Figura 1.1. Schema dell’esperienza di Thomson fu superato da quello di Rutherford. Rutherford era figlio di contadini scozzesi emigrati in Nuova Zelanda. Aveva lavorato in Canada sulla radioattività e la sua scoperta dei raggi alfa (fasci di nucleo di elio), beta (fasci di elettroni) e della loro origine atomica, gli aveva valso il premio Nobel. Spostandosi a Manchester in Inghilterra, Rutherford studia gli atomi lanciando i suoi raggi alfa contro un sottilissimo foglio d’oro (oro perchè, per la sua grande malleabilità, può essere reso molto sottile). La sorpresa fu che alcune delle particelle che formano i raggi alfa rimbalzano all’indietro. “È come se sparaste una fucilata contro un sottile foglio di carta, e ogni tanto una pallottola rimbalzasse” è il commento di Rutherford. La sua interpretazione corretta, è che gli atomi d’oro sono quasi completamente vuoti (per cui quasi tutte le particelle) passano senza problema) eccetto per un piccolissimo nucleo centrale denso e pesante, su cui qualche particella rimbalza o viene deviata. L’immagine di Rutherford dell’atomo come un piccolo sistema solare è intuitiva e convincente, ma presto le cose cominceranno a non tornare. L’idea di un’orbita classica, quasi quella di un pianeta intorno al sole, qui non può reggere, poiché l’elettrone carico, irraggiando e perdendo energia, dovrebbe terminare il suo moto precipitando sul nucleo in un miliardesimo di secondo. Quello dell’instabilità degli atomi fu uno dei misteri del mondo microscopico, risolto solo dalla rivoluzionaria teoria della meccanica quantistica. 1.1.5 Numero atomico, numero di massa. Isotopi Il numero dei protoni presenti in un nucleo atomico viene chiamato numero atomico e rappresentato con la lettera Z ed essendo l’atomo elettricamente neutro il M. Rustici, Chimica di base 16 Materia ed Energia Figura 1.2. Schema dell’esperienza di Rutheford numero dei protoni è uguale al numero degli elettroni. La discrepanza osservata tra il numero atomico di un atomo e la sua massa atomica indusse Rutherford nel 1920 a postulare l’esistenza di particelle neutre all’interno del nucleo atomico alle quali fu dato il nome di neutroni. In seguito da parte di altri fisici fu dimostrato sperimentalmente l’esistenza di tali particelle neutro. Il numero totale di nucleoni, vale a dire la somma di protoni e neutroni costituisce il numero di massa ed è rappresentato con il simbolo A. In altre parole A=Z +N N =A−Z Dove N rappresenta il numero di neutroni. Il numero atomico e il numero di massa caratterizzano in maniera univoca non solo i nuclei degli elementi, ma qualsiasi particella atomica o subatomica, mediante la notazione A ZX X= simbolo della particella (1.5) 1 1 ad esempio 12 6 C; 1 p; 0 n; dove abbiamo indicato il carbonio, il protone e il neutrone. Gli elementi sono sostanze costituite da atomi chimicamente identici e quindi con lo stesso numero atomico Z. Gli atomi di uno stesso elemento possono avere un diverso numero di neutroni, in altre parole un diverso numero di massa A e sono chiamati isotopi. Una ventina degli elementi stabili non presenta isotopi (come il sodio o il fluoro). La maggior parte degli elementi sono presenti sotto forma di una miscela M. Rustici, Chimica di base 17 Materia ed energia isotopica. Esistono inoltre numerosissimi isotopi instabili come quelli radioattivi che in un tempo più o meno breve si trasformano in altri nuclei. Le quantità in cui gli isotopi sono presenti nella miscela isotopica vengono espresse con abbondanza percentuale o come abbondanza relativa (frazione con la quale l’isotopo si trova nella miscela). 1.1.6 Pesi atomici e unità di massa atomica Come abbiamo visto il valore dei pesi atomici relativi dipendono dal valore arbitrario attribuito all’elemento di riferimento. La prima scala dei pesi atomici è stata ottenuta scegliendo l’idrogeno come atomo di riferimento, considerando la sua massa pari ad 1. Successivamente, fu scelto l’ossigeno e tenendo presente che la sua massa è circa 16 volte quella dell’idrogeno si convenne di assegnare a tale atomo il peso di 16, conseguentemente il peso atomico dell’idrogeno risultò 1.008. Nel 1961 si è scelto come unico riferimento la dodicesima parte dell’atomo di carbonio 12 6 C. Cosı̀ il peso atomico del carbonio-12 viene, per definizione, viene ad essere pari a 12 unità di massa atomica. Perciò l’unità di massa atomica simbolo u è 1/12 della massa dell’atomo di carbonio-12. In base a questo campione la massa dell’atomo di 1 H è 1.008 u, in altre parole la massa di 12 C ha una massa circa 12 volte quella di 1 H. L’unità di massa atomica è chiamata anche dalton (simbolo Da. L’unità di massa atomica, che è un unità di massa relativa, equivale ad una massa assoluta di 1.66054 ·10−24 g. Se ad esempio sperimentalmente si ottiene che il rapporto tra le masse del 28 Si e del 12 C (massa28 Si/massa12 C )è 2.331411 allora il peso atomico sarà massa28 Si = 2.331411 · massa12 C = 2.331411 · 12 = 27.97693 La quantità indicata come massa atomica o peso atomi è rappresenta un nome improprio dato che in realtà rappresenta un numero puro. Potremmo a questo punto chiederci perché il peso atomico del 28 Si 27.97693 e non 28 come sarebbe intuitivo aspettarci? Analizzando le masse dei singoli isotopi si ricava che non sono numeri interi. Ad esempio se andiamo a misurare il peso atomico del 63 Cu non si trova il valore di 63 ma di 62.9296011. Misure accurate hanno mostrato che nemmeno il protone e il neutrone hanno un peso atomico di 1, ma hanno rispettivamente il valore di 1.0073 e 1.0087. Osserviamo che la massa complessiva del nucleo è sempre minore alla somma delle masse dei singoli nucleoni. Ad esempio consideriamo gli isotopi 11 H e il deuterio 12 H che si forma per addizione di un neutrone all’isotopo più abbondante dell’idrogeno secondo lo schema di reazione 1 1H +10 n →21 H M. Rustici, Chimica di base (1.6) 18 Materia ed Energia si misura l’esistenza di una variazione di massa ∆m (cioè la differenza tra la massa dei nucleoni legati rispetto a quella della somma dei nucleoni liberi ) pari a −3.926 · 10−30 Kg. Tale quantità è nota come difetto di massa. Che fine ha fatto il resto della massa? Applicando la relazione di Einstein E = mc2 si calcola che a questa perdita di massa corrisponde un’energia di −3.533 · 10−13 J. Ricordando che 1 eV è l’energia acquistata da un elettrone in quiete sottoposto ad una differenza di potenziale di 1 V è pari a 1.602 · 10−19 J e che quindi un megaelettronvolt MeV corrisponde a 1.602 · 10−13 J questo implica che l’energia espressa in MeV nella formazione del deuterio da un protone e da un neutrone è: ∆E = −3.533 · 10−13 /1.602 · 10−13 = −2.206 MeV L’energia sviluppata è di un milione di volte superiore all’energia che si sviluppa nella formazione della molecola di idrogeno. Se si divide l’energia di legame per il numero di nucleoni in esso contenuti si ottiene l’energia di legame per nucleone. che nel caso del deuterio è pari a -1.103 MeV. L’energia di legame per nucleone corrisponde alla perdita media di massa di ogni nucleone che entra a far parte di un nucleo e misura la forza con cui il nucleone è legato al nucleo e rappresenta una misura quantitativa della stabilità del nucleo stesso. I nuclei atomici sono più o meno stabili, questa stabilità viene rappresentata dall’energia di stabilità nucleare e tanto maggiore è l’energia di legame nucleare e tanto maggiore risulta la stabilità del nucleo. Dalla Figura 1 si evince che l’energia di legame per nucleone dapprima aumenta rapidamente con l’aumentare del numero di massa per poi raggiungere un massimo di circa 8.8 MeV in prossimità del ferro per poi diminuire. Questo implica che tutti gli elementi sono più instabili rispetto al ferro. I nuclei più leggeri tendono a formare elementi più pesanti attraverso un processo di fusione mentre quelli più pesanti del ferro tenderanno a formare elementi più leggeri attraverso un procedimento di fissione. Sia i processi di fusione che quelli di fissione avvengono con sviluppo di energia. Quando parliamo del peso atomico di un elemento in generale non ci riferiamo al peso atomico di un particolare isotopo ma al peso atomico medio della miscela isotopica che si trova in natura. Possiamo pesare il singolo contributo isotopico in base alla sua percentuale e attraverso una media pesata si determina il peso atomico medio che risulterà essere nel caso del silicio pari a 28.09 . Cerchiamo di vedere meglio il procedimento corretto per la costruzione dei pesi atomici medi che si osservano nella tavola periodica. Il Silicio si trova in natura 30 29 sotto forma di 3 isotopi stabili 28 14 Si, 14 Si e 14 Si rispettivamente nelle percentuali del 92.23% 4.67 % e 3.1%. Possiamo allora calcolare il contributo degli isotopi al peso atomico medio partendo ovviamente dai pesi atomici dei rispettivi isotopi M. Rustici, Chimica di base 19 Materia ed energia Figura 1.3. che sono nell’ordine di 27.97693 u, 28.976495 u e 29.973770 u. allora il contributo relativo al 28 14 Si sarà 27.97693 · 0.9223 = 25.8031u quello relativo al 29 14 Si sarà di 28.976495 · 0.0467 = 1.3532u quello relativo al 30 14 Si sarà di 29.973770 · 0.031 = 1.9292u conseguentemente il peso atomico del silicio sarà 25.8031 + 1.3532 + 1.9292 = 28.09u Questo significa che nessun atomo di silicio avrà questo particolare valore del peso atomico, questo si tratta solo del peso atomico medio che tuttavia per la maggior parte dei problemi di laboratorio consideriamo che un campione di Silicio abbia questo valore di massa media. M. Rustici, Chimica di base 20 1.1.7 Materia ed Energia Mole. Numero di Avogadro Un concetto fondamentale relativo all’utilizzo pratico della chimica e in particolare necessario per quantificare i processi chimici, come ad esempio la resa di una reazione chimica, è il concetto di mole. La mole è definita come la quantità di sostanza di un sistema che contiene tante entità elementari quanti sono gli atomi contenuti in 0.012 Kg di carbonio-12. Questo numero è detto Numero di Avogadro. Esattamente una mole contiene un numero di entità pari a 6.022 · 1023 . La mole è una grandezza fondamentale del sistema internazionale (SI) il cui simbolo è n e la sua unità di misura è indicata con mol, analogamente alla grandezza fondamentale della lunghezza il cui simbolo è l e la cui unità di misura è m. La massa atomica di un elemento, espressa in unità di masse atomica (u) è numericamente uguale alla massa di una mole di atomi dell’elemento espresso in grammi. In altre parole possiamo dire che se prendiamo una quantità in grammi di Ferro numericamente pari al suo peso atomico (55.85) e una quantità in grammi di zolfo nmericamente pari al suo peso atomico (32.07) possiamo affermare che queste due quantità contengono lo stesso numero di atomi cioè 6.022·1023 atomi Applichiamo i concetti qui esposti al seguente esercizio Supponiamo di voler calcolare quanti grammi di ossigeno sono necessari per ossidare completamente 10 grammi di polvere di ferro assumendo che la reazione di ossidazione sia la seguente 4Fe + 3O2 → 2Fe2 O3 (1.7) La reazione chimica ci dice che 4 atomi di ferro reagiscono con 3 molecole di ossigeno per dare due “molecole” di ossido ferrico. Nello stesso modo possiamo dire che 4 moli di ferro reagiranno con 3 moli di ossigeno per dare 2 moli di ossido ferrico. Possiamo pertanto sulla base della definizione di mole andare a calcolare quante moli sono contenute in 10 grammi Fe. In base alla definizione di mole e al fatto che il peso atomico del Fe è 55.845 possiamo scrivere che n= grammi 10 = = 0.179 peso atomico 55.845 Tenendo allora presente che 4 moli di ferro vengono ossidate da 3 moli di ossigeno il numero di moli di ossigeno necessarie per un’ossidazione completa sarà pari a 3/4 delle moli di ferro. In altre parole 3 · 0.179 = 0.134 4 da cui i grammi di ossigeno necessario per la completa ossidazione saranno ottenibili moltiplicando il risultato ottenuto per il peso molecolare della ossigeno (32). nO2 = M. Rustici, Chimica di base 21 Materia ed energia gO2 = 0.134 · 32 = 4.288 M. Rustici, Chimica di base Capitolo 2 Teorie Atomiche 2.1 Modello atomico di Bohr Gli studi sull’interazione tra la radiazione elettromagnetica della luce e la materia mostrano la completa inadeguatezza della teoria dell’elettromagnetismo e della meccanica classica per la corretta interpretazione del mondo microsopico. L’inizio del 900 si presenta ricco di problematiche che verranno brillantemente risolte dai grandi scenziati che hanno vissuto nel secolo precedente a questo. La prima grande rivoluzione del ’900 si deve a Max Plank il quale riuscı̀ a risolvere il problema della radiazione del corpo nero. Qualunque oggetto caldo emette radiazioni elettromagnetiche ed ognuno di noi ha sperimentato come, ad esempio, un metallo cambia la sua luminosità aumentando il riscaldamento del metallo stesso. Il ferro ad esempio emette una luce rossa quando viene riscaldato ma se aumentiamo la temperatura di riscaldamento la luce diventa bianca. La figura 2.1 mostra come varia la lunghezza d’onda al variare della temperatura. Queste curve sono calclate sul modello di un emettitore ideale detto corpo nero che è un oggetto capace di emettere e assorbire radiazioni in modo uniforme. La figura 2.1 mostra come, innalzando la temperatura, il picco dell’energia si sposti verso lunghezze d’onda minori e la densità di energia totale aumenta con l’aumentare della temperatura. L’analisi dei dati condusse Wilhelm Wien a riassumere il risultato nella seguente legge sperimentale T λmax = 0.288 e in seguito fu mostrato da Stefan nella famosa relazione di Stefan-Boltzmann M = σT 4 dove M è la potenza per unità di tempo, σ la costante di Stefan-Boltzmann e T la temperatura. Il fisico Lord Rayleigh cerco di interpretare la radiazione del M. Rustici, Chimica di base 24 Teorie Atomiche Figura 2.1. corpo nero in modo classico interpretando l’energia emessa come dovuta all’emissione denergetica di un oscillatore elettromagnetico eccitato, il modello proposto portò ad un cmpleto insuccesso. Il fisico tedesco Max Plank risolse il problema introducendo un ipotesi nuova assumendo che l’energia di ciascun oscillatore elettromagnetico fosse associata a valori discreti e non potesse variare in modo continio Nasce cosı̀ con Plank la quantizzazione dell’energia. Max Plank riuscı̀ cosı̀ ad interpretare perfettamente i dati introducendo una teoria completamente nuova e ipotizzando che un corpo riscaldato è in grado di emettere o di assorbire solo quantità discrete di energia definita dalla relazione E = nhν (2.1) dove h è una costante di proporzionalità detta costante di Plank, ν è la frequenza della radiazione emessa, E è l’energia associata ed n un numero intero. In altre parole la quantità di energia emessa o assorbita poteva essere solo un multiplo della quantità minima di energia detta hν. Questo implicava che l’energia associata alla radiazione emessa non poteva assumere qualunque valore. In M. Rustici, Chimica di base 25 Teorie atomiche Figura 2.2. altre parole l’energia risultava quantizzata e il numero n vaniva chiamato numero quantico. Si poteva pertanto affermare che se un atomo poteva emettere solo quantità discrete di energia l’energia stessa dell’atomo doveva risultare quantizzata. Ogni pacchetto di energia è detto quanto e la sua energia è espressa da hν. In altri termini un atomo passa da uno stato energetico all’altro assorbendo o emettendo uno o più quanti di energia. L’energia della radiazione emessa o assorbita dall’atomo sarà esprimibile come ∆E = ∆nhν (2.2) Nello stesso periodo l’effetto fotoelettrico costituiva un altro problema da risolvere. In particolare tale effetto era associato alla capacità da parte di un metallo, sottoposto ad una differenza di potenziale, di emettere elettroni quando questo fosse soggetto ad una radiazione elettromagnetica. Secondo la teoria ondulatoria qualunque radiazione luminosa purchè sufficientemente intensa avrebbe dovuto essere capace di emettere un flusso di elettroni. Infatti l’onda luminosa avrebbe dovuto far oscillare l’elettrone fino a farlo strappare dall’atomo stesso. Tuttavia l’esperienza mostrava che solo oltre una frequenza di soglia era possibile l’emissione di elettroni. Oltre questa frequenza il flusso di corrente emesso dal metallo era regolabile con l’intensità luminosa. Nel 1905 Einstein prende il premio Nobel per aver interpretato l’effetto fotoelettrico sulla base di una teoria corpuscolare della luce. In particolare Einstein propose che la luce fosse costituita da quanti luminosi (fotoni) privi di massa e solo quei fotoni che possedevano un energia superiore alla forza con la quale l’elettrone risultava legato al nucleo potevano essere espulsi dal metallo e generare la corrente fotoelettrica. Un altro problema da risolvere concerneva l’interpretazione degli spettri atomici, in altre parole l’interpretazione dell’energia elettromagnetica emessa da atomi vaporizzati ed eccitati. L’osservazione sperimentale mostrava che la luce emessa, una volta analizzata, nelle sue componenti non formava uno spettro continuo ma uno spettro discreto, in particolare uno spettro a righe; M. Rustici, Chimica di base 26 Teorie Atomiche dove le frequenze che si generano sono caratteristiche dell’elemento chimico che si studia. Per motivi incomprensibili la luce riemessa dagli atomi ha sempre e solo particolari frequenze e non altre (è il motico per cui ogni materiale ha un suo caratteristico colore). É come se l’elettrone potesse ruotare solo su particolari orbite e non altre. Le varie righe spettrali cosı̀ generate potevano essere messe in relazione attraverso l’equazione di Rydberg 1 =R λ µ 1 1 − 2 2 n1 n2 ¶ (2.3) dove R è la costante di Rydberg (1.096776 · 107 m−1 , n1 e n2 sono numeri interi piccoli. Quest’equazione era di tipo sperimentale e nessuno era in grado di derivarla dalla teoria corrente. Tutto questo era in contrasto stringente con la fisica newtoniana, che insegna che la che le orbite possano stare a qualunque altezza, e la luce emessa dovrebbe essere un misto di tutte le frequenze. Dobbiamo attendere Niels Bohr con la sua formulazione di un nuovo modello atomico per poter interpretare gli spettri atomici e per risolvere il problema della stabilità atomica. L’atomo di idrogeno risulterà stabile perchè le sue “orbite” sono bloccate su livelli precisi di energia. Più precisamente Bohr introdusse al sua teoria mediante i seguenti postulati. 1. L’atomo di idrogeno possiede solo livelli energetici permessi detti stazionari dove l’elettrone ruota attorno al nucleo atomico seguendo orbite circolari. Ad ogni livello stazionario è associato un numero detto quantico che può assumere solo valori interi. 2. L’elettrone durante il suo moto sull’orbita stazionaria non emette né irradia energia. 3. Il momento angolare dell’elettrone mvr è quantizzato e può assumere solo un numero definito di valori. 4. L’atomo assorbe o irradia energia quando un elettrone passa da un orbita all’altra assorbendo o cedendo un fotone la cui energia è uguale alla differenza di energia tra i due stati ∆E = EA − EB = hν. Le orbite permesse all’elettrone di massa m e di velocità v in ogni stato stazionario sono quelle in cui il raggio r è tale che il prodotto mvr è un multiplo di h/2π. possiamo cosı̀ scrivere che mvr = n h 2π n = 1, 2, 3 · · · ∞ M. Rustici, Chimica di base (2.4) 27 Teorie atomiche e ponendo ~ = h/2π possiamo scrivere mvr = n~ n = 1, 2, 3 · · · ∞ (2.5) il numero n è detto numero quantico principale. In meccanica classica l’energia può essere espressa come la somma tra l’energia cinetica e l’energia potenziale. Pertanto possiamo scrivere che l’energia di un elettrone che si muove in un orbita circolare è 1 kZe2 E = mv 2 − 2 r (2.6) dove k è la costante di Coulumb, Ze la carica dell’elettrone. Ricordando inoltre la seconda legge di Newton F = ma possiamo sostituire in questa equazione l’accelerazione centripeta a = v 2 /r e la forza di attrazione coulumbiana. Otteniamo allora kZe2 v2 − 2 =m r r (2.7) Il primo termine è relativo alla forza di attrazione coulombiana dove abbiamo un segno negativo a causa del prodotto tra una carica negativa (elettrone) e una carica positiva (protone). Il secondo termine invece è quello relativo alla massa per l’accelerazione centripeta. da cui si ricava che 1 2 1 kZe2 mv = − 2 2 r (2.8) cioè che l’energia cinetica è esattamente la metà dell’energia potenziale. Se inoltre ricaviamo dalla 3.7 l’espressione della velocità otteniamo che r v= kZe2 mr (2.9) sostituendo questa espressione nella 3.5 otteniamo √ mkZe2 r = n~ (2.10) elevando tutto al quadrato e risolvendo in r otteniamo r= n2 ~2 = a0 n2 Ze2 m M. Rustici, Chimica di base (2.11) 28 Teorie Atomiche dove a0 è il cosiddetto raggio di Bohr e vale 0.529 ·10−10 m. L’energia del livello n-esimo è regolata dal raggio di Bohr e sostituendo l’espressione 3.8 nella 3.7 possiamo scrivere (Zke2 )2 m 1 Zke2 −13.6eV =− E=− = 2r 2~2 n2 n2 (2.12) dove abbiamo inoltre sostituito al posto del raggio r la sua espressione (3.11). Cosı̀ la formula di Rydberg, conosciuta empiricamente prima di quella di Bohr è ora contenuta nella teoria di Bohr capace di descrivere le energie di transizione o i cosiddetti salti quantici tra un livello energetico ed un altro. La formula di Bohr conduce al valore numerico empirico della costante di Rydberg in termini di costanti fondamentali includenti la carica dell’elettrone e la costante di Plank. Quando un fotone si muove da un livello energetico all’altro viene emesso un fotone e usando la formala di Bohr per i livelli dell’atomo di idrogeno si può calcolare la lunghezza d’onda. L’energia del fotone emessa dall’atomo di idrogeno è esprimibile come la differenza di energie tra i due livelli energetici à E = Ei − Ef = RE 1 1 − 2 2 nf ni ! (2.13) Si noti come le energie dei livelli energetici siano sempre più vicine tra loro con il crescere del numero quantico n. Nonostante il grande successo nello spiegare le righe spettrali dell’atomo di idrogeno, il modello di Bohr non era in grado di prevedere lo spettro di nessun altro atomo, neppure quello dell’elio, l’elemento successivo più semplice. 2.1.1 Dualismo onda particella Il passo successivo capace di superare i problemi associati all’atomo di Bohr si deve al fisico francese De Broglie il quale nella sua tesi di dottorato propone che la materia possa avere una natura ondulatoria. Sulla base del postulato di Bohr, per il quale l’elettrone può occupare solo orbite discrete di energia, De Broglie pensò quali siano gli altri sistemi noti che posseggono solo un certo tipo di moti permessi. Se noi ad esempio pensiamo alle onde che si trasmettono su una corda (vedi chitarra) fissata a due estremità osserviamo che sono possibili solo un certo tipo di frequenze di vibrazione. La figura 3.2 mostra un esempio di onde stazionarie che si possono stabilire quando la corda risulta fissata alle due estremità. In questo caso non tutte le frequenze sono possibili ma solo alcune saranno permesse e ciò dipenderà dalla lunghezza della corda. Le lunghezze d’onda permesse sono dei multipli interi della lunghezza della corda secondo la relazione: M. Rustici, Chimica di base 29 Teorie atomiche Figura 2.3. nλ = 2L n = 1, 2, 3 · · · (2.14) la figura 3.2 mostra inoltre i nodi che sono definiti come quei punti in cui la funzione d’onda cambia di segno. La frequenza più bassa è detta fondamentale o prima armonica e non possiede nodi. la frequenza successiva è la seconda armonica e possiede un nodo ed è doppia della frequenza fondamentale. Sulla base di quanto detto De Broglie ipotizzò che gli elettroni, benché aventi massa, si muovessero di moto ondulatorio e fossero limitati ad orbite di raggi fissi. Quest’ipotesi spiegherebbe allora perché gli elettroni possono avere solo certe frequenze e certe energie. Nasce cosı̀ l’idea che una particella sufficientemente piccola possa avere una natura sia corpuscolare che ondulatoria. Ricordando che la quantizzazione dell’energia veniva descritta dall’equazione E = hν e tenendo presente che la frequenza è esprimibile come il rapporto tra la velocità della luce rispetto alla lunghezza d’onda possiamo allora scrivere che E = hν → E = hc λ (2.15) Applicando l’equazione di Einstein E = mc2 otteniamo che λ= h mc (2.16) allora per una particella generica che si muove con velocità v possiamo scrivere che M. Rustici, Chimica di base 30 Teorie Atomiche Figura 2.4. h (2.17) mv Analogamente alla 3.14 possiamo scrivere, nel caso il vincolo sia espresso da una circonferenza, che λ= 2πr = nλ n = 1, 2, 3 · · · (2.18) Quest’equazione significa che la circonferenza dell’orbita circolare dell’elettrone deve essere un multiplo intero della lunghezza d’onda di de Broglie in altre parole le onde dell’elettrone dovranno essere continue. Se la circonferenza dell’orbita circolare non fosse un multiplo intero della lunghezza d’onde, le onde non potrebbero essere continue. La figura 3.3 mostra il caso in cui l’onda non si sovrappone con se stessa a causa del fatto che non è un multiplo intero della lunghezza d’onda. Questa onda non rappresenta pertanto una corretta onda di de Broglie. Le onde di de Broglie giocano cosı̀ un ruolo essenziale per la comprensione della teoria quantistica di Bohr. In particolare il postulato di Bohr relativo al momento angolare diventa deducibile dalla ipotesi primaria di considerare una particella subatomica, quale l’elettrone, come un onda. Sostituendo allora a λ il valore espresso dalla 3.17 otterremmo il vecchio postulato di Bohr dell’equazione 3.4. L’interpretazione ondulatoria dell’elettrone costituisce la base della cosı̀ detta meccanica ondulatoria di Schrödinger o meccanica quantistica. Se le particelle si muovessero di moto ondulatorio, gli elettroni dovrebbero presentare diffrazione e interferenza e gli esperimenti sugli elettroni mostrano proprio le figure classiche di interferenza associate a i fenomeni ondulatori. Possiamo allora affermare che materia ed energia presentano sia il comportamento ondulatorio che particellare. In alcuni esperimenti osserviamo una faccia della medaglia e in altri l’altra faccia. Questa caratteristica duale della materia e dell’energia è noto come dualismo onda-particella. M. Rustici, Chimica di base 31 Teorie atomiche Nel mondo macroscopico una particella è ben localizzata nello spazio dalle sue coordinate, viceversa un’onda non è localizzata ma sparpagliata nello spazio. Se l’elettrone è un’onda come possiamo localizzarlo all’interno dell’atomo? Nel 1927 il fisico tedesco Werner Heisemberg formulò il principio di indeterminazione, secondo cui è impossibile conoscere simultaneamente la posizione esatta di una particella. Nel caso di una particella con quantità di moto p, il principio di indeterminazione è espresso matematicamente dalla relazione ∆x∆p ≥ h 2π (2.19) dove ∆x è l’incertezza nella posizione e ∆p l’incertezza nella quantità di moto. Non abbiamo pertanto la possibilità di assegnare, alle particelle in movimento, una traiettoria ben definita ma come vedremo possiamo solo conoscere la sua probabilità. L’equazione 3.19 è solo una forma del principio di indeterminazione la cui formulazione assume una forma più generale, è utile comunque riportare che una analoga indeterminazione può essere associata all’energia e al tempo, nel senso che una misurazione precisa dell’una rende imprecisa quella dell’altra e viceversa. Il principio di indeterminazione pone, pertanto, la necessità di dover descrivere lo stato di un sistema attraverso una nuova definizione dello stesso. In meccanica classica la conoscenza dello stato del sistema implica la specificazione della posizione e della velocità delle singole particelle costituenti il sistema in ogni istante di tempo. In accordo alla seconda legge di Newton, dato lo stato di un sistema in ogni tempo è possibile determinare esattamente lo stato futuro. Proprio questa concezione espressa dalla meccanica classica aveva condotto il filosofo e matematico Laplace ad ipotizzare il suo famoso demone. Laplace infatti sosteneva che se esistesse un demone capace di conoscere esattamente le velocità delle singole partecelle e le rispettive posizioni di tutte le particelle dell’universo, sarebbe stato in grado di prevedere il futuro e retrodire il passato. Questa costituisce la metafora di un mondo regolato in modo assolutamente deterministico. Il principio di indeterminazione, se accettato nella sua interezza, fa cadere definitivamente questa metafora. In quantomeccanica viene postulata l’esistenza di una funzione detta funzione d’onda o funzione di stato Ψ che descrive lo stato di un sistema. Poiché lo stato varia nel tempo questa funzione dipenderà sia dalle coordinate spaziali che temporali. La funzione d’onda contiene cosı̀ tutte le possibili informazioni circa il sistema. Il concetto della funzione d’onda e dell’equazione che governa il cambiamento nel tempo fu introdotto dal fisico austriaco Erwin Schrödinger. La funzione d’onda contiene tutte le informazioni che noi possiamo conoscere circa il sistema da essa descritto. Quali sono allora le informazioni che Ψ ci fornisce, ad esempio, circa il risultato di una misura sulla coordinata di una particella? Ovviamente noi non possiamo aspettarci che la funzione d’onda Ψ implichi una specificazione definita della posizione. La risposta completa a questa domanda M. Rustici, Chimica di base 32 Teorie Atomiche Figura 2.5. si deve a Max Born il qual postulò che |Ψ|2 dà la probabilità di trovare la particella in una certa regione dello spazio. La funzione |Ψ|2 rappresenta quindi la probabilità di trovare la particella in diverse zone dallo spazio. Conoscendo lo stato, allora, non possiamo predirre con certezza un risultato di una misura della posizione della particella possiamo solo fare una predizione di probabilità dei vari possibili risultati. La teoria di Bohr dell’atomo di idrogeno specifica esattamente la traiettoria dell’elettrone e quindi non rappresenta una esatta rappresentazione quantomeccanica. La quantomeccanica non ci dice che un elettrone è distribuito in una certa regione dello spazio come un’onda piuttosto che la distribuzione della probabilità di comporta come un’onda e soddisfa l’equazione di’onda. L’equazione di Schrödinger è un postulato di una teoria i cui risultati vengono confrontati con i risultati sperimentali. 2.1.2 Modello quantomeccanico dell’atomo Possiamo allora utilizzare l’equazione di Schrödinger per descrivere l’atomo di idrogeno in cui l’unica assunzione sarà quella di immaginare l’elettrone sottoposto ad un campo di forze centrali indotte dal nucleo atomico. Sulla base di ciò è possibile dedurre le caratteristiche dell’atomo di idrogeno risolvendo l’equazione differenziale. Qui cercheremo di fornire solo i risultati ottenuti dalla risoluzione dell’equazione di Schrödinger a causa della complessità matematica del problema. Per l’atomo di idrogeno la funzione Ψ prende anche il nome di orbitale atomico e nel suo stato fondamentale è rappresentato dalla figura 3.4. che prende il nome di orbitale 1s. Come possiamo vedere dalla figura si tratta di un orbitale a simmetria sferica. Nello stato fondamentale l’elettrone è descritto dall’orbitale detto 1 s e la densità elettronica è massima in corrispondenza del nucleo. Un orbitale atomico è specificato da tre numeri quantici, uno è in relazione alla distribuzione di probabilità radiale dell’orbitale, un altro alla sua forma e il terzo al suo orientamento nello spazio. 1. Il numero quantico principale (n) è un intero positivo (1,2, 3 . . . ). Tale nu- M. Rustici, Chimica di base 33 Teorie atomiche Figura 2.6. mero quantico specifica il livello energetico dell’atomo di idrogeno e maggiore è il suo numero, maggiore è l’energia posseduta dall’elettrone. Quando n=1 l’elettrone si trova nel suo stato fondamentale (orbitale 1s). Se n=2 l’elettrone si troverà nel primo stato eccitato. 2. Il numero quantico angolare (l) è un numero intero compreso tra 0 e n-1. Esso è in relazione alla forma dell’orbitale. Quando n=1 l può avere solo il valore 0, per n=2 l può avere i valori 0 e 1. 3. Il numero quantico magnetico (m) è un numero intero compreso tra −l e + l passando per 0. esso impone l’orientamento dell’orbitale. Pertento per l=1 possiamo avere tre possibili orbitali. Abbiamo visto che l’orbitale dell’atomo di idrogeno nel caso più semplice ha una simmetria sferica e prende il nome di orbitale 1s. Nel momento in cui passiamo al livello eccitato n = 2 abbiamo che l può assumere i valori 0 e 1. Nel caso in cui n = 2 e l = 0 abbiamo ancora un orbitale a simmetria sferica più grande del precedente che prende il nome di orbitale 2s e che mostra una superfice nodale al suo interno, in altre parole una zona con densità di probabilità nulla. Il caso invece rappresentato da n = 2, l = 1 e m = −1, 0 + 1 è rappresentato dalla figura 3.5 che mostra 3 orbitali noti come orbitali 2px , 2py e 2pz . Come si osserva dalla figura 3.5 l’orbitali p sono caratterizzati da due lobi di alta probabilità situati in parti opposte rispetto al nucleo. Il nucleo giace sul piano nodale. A differenza dell’orbitale s gli orbitali p hanno un orientamento specifico nello spazio. I tre orbitali hanno la stessa energia (sono degeneri) e sono identici in dimensione ma sono diversamente orientati. In particolare sono tra loro ortogonali e orientati nello spazio secondo gli assi ortogonali. Un orbitale con l = 2 è detto orbitale d per il quale sono possibili 5 valori di m (-2,-1,0,+1,+2) Per tale motivo ogni orbitale d può avere 5 diverse orientazioni. come mostrato in figura 3.6. Tre di questi giacciono nei piani mutualmente ortogonali xy, xz, yz con i lobi tra gli assi e sono denotati con i simboli dxy , dxz e dyz . Un quarto orbitale denotato dx2 −y2 giace nel piano xy ma con i lobi orientati lungo gli assi. Il quinto orbitale è il dz2 formato da due lobi orientati lungo l’asse z e una regione a forma di ciambella circonda il centro. Gli orbitali con l = 3 sono gli orbitali f . M. Rustici, Chimica di base 34 Teorie Atomiche Figura 2.7. 2.1.3 Atomi polielettronici L’equazione di Shrödinger per gli atomi polielettronici non è risolubile esattamente a causa delle repulsioni elettroniche. In prima approssimazione, ignoriamo le repulsioni interelettroniche e la funzione d’onda può essere immaginata come una funzione definita dal prodotto di funzioni monoelettroniche. Gli orbitali atomici sono utilizzati per descrivere approssimativamente gli orbitali polielettronici. Gli stessi orbitlai verranno a loro volta utilizzati per costruire le funzioni d’onda molecolari. per gli atomi polielettronici l’energia non dipende solo più dal numero quantico principale n ma anche dal numero quantico l a causa della repulsione elettronica. La disposizione degli elettroni nei singoli orbitali per quanto concerne lo stato fondamentale si basa su semplici principi ottenuti in modo rigoroso da considerazioni teoriche ed energetiche. Il meccanismo attraverso il quale si costruisce tale configurazione elettronica dello stato fondamentale è detto aufbau (dal tedesco costruire) e si basa sulle seguenti regole • principio di minima energia per il quale l’elettrone occuperà sempre solo stato disponibile ad energia più bassa • principio di esclusione di Pauli per il quale in un atomo non possono esistere due elettroni con gli stessi numeri quantici. Tenendo presente che oltre ai numeri quantici introdotti precedentemente, dobbiamo anche tener conto del numero quantico di spin ms che può assumere i valori di +1/2 e 1/2. Questo principo implica a sua volta che ogni orbitale può al massimo “contenere” due elettroni e questi devono essere tra loro antiparalleli • regola di Hund: se due elettroni occupano orbitali degeneri si deve raggiungere al massima molteplicità di spin in altre parole gli spin devono essere paralleli. Per prima cosa prima di poter applicare le regole dell’aufbau dobbiamo avere un’idea della disposizione energetica degli orbitali. La figura 3.7 ci fornisce un’idea M. Rustici, Chimica di base 35 Teorie atomiche Figura 2.8. della sequenza dei livelli energetici. Sulla base di quanto detto non è difficile iniziare a costruire le configurazioni elettroniche degli elementi dalla conoscenza del numero atomico. Per H (che ha Z=1), n=1, l=0, non c’è molta scelta: dobbiamo usare l’orbitale a più bassa energia, 1s; la configurazione elettronica potrà venire indicata con 1s oppure, sinteticamente, con 1s1 . Per He (Z=2), n = 1, l = 0, occorre applicare il principio di Pauli: poiché due numeri quantici sono eguali, occorre che almeno uno degli altri due sia diverso perchè il secondo elettrone possa stare col primo; poiché l = 0, anche m = 0; resta solo la possibilità di avere diverso ms : è necessario che se un elettrone ha ms = +1/2, l’altro abbia ms = -1/2. Devono perciò essere antiparalleli: la configurazione verrà indicata con 1s2 . Continuiamo ora da Z=3 a Z=11, lo schema rappresentato in figura 3.8 mostra le configurazioni elettroniche associate ai primi elementi della tavola periodica a partire dall’atomo di Li fino ad arrivare al gas nobile Ne. Nella prima colonna sono indicati i numeri atomici Z. Nella seconda, la configurazione elettronica secondo Lewis: sui quattro lati del simbolo sono evidenziati i doppietti e gli elettroni spaiati (del guscio esterno). Nella terza, una rappresentazione che dà il guscio (shell) già completato, come (He) o (Ne), seguito dal nome degli orbitali disponibili ed occupati; quando il guscio è completato (solo per s e p), cambia il simbolo del gas nobile corrispondente; sono evidenziati anche gli spin accoppiati nel caso di doppietti o, nel caso di elettroni spaiati, gli spin paralleli degli elettroni che occupano orbitali degeneri diversi, secondo la regola di Hund. In una analoga rappresentazione (He) è sostituito dal nome del guscio, K; (Ne) da KL (sono completi ambedue i gusci) etc. Nella quarta una rappresentazione completa della configurazione, che non evidenzia però se gli elettroni si trovano nello stesso orbitale o in orbitali degeneri diversi; ricordando però la regola di Hund, è ovvio, per esempio, che N ha tre elettroni 2p a spin paralleli e in tre orbitali degeneri diversi; l’esponente dei vari tipi di orbitali degeneri indica il numero di elettroni che li occupa. M. Rustici, Chimica di base 36 Teorie Atomiche Figura 2.9. Finora, nell’aufbau, abbiamo esaminato solo gli orbitali fino al 3p. Infatti, nella tabella dell’E degli orbitali, la sequenza è:1s, 2s, 3p, 3s, 3p. A questo punto, proseguendo il riempimento, poiché i 3d sono a energia leggermente superiore ai 4s, riempiremo prima i 4s e poi i 3d, anche se fanno parte del guscio inferiore. La figura 3.9 mostra le configurazioni elettroniche relative al riempimento degli orbitali d Si possono osservare delle piccole anomalie come nel caso del cromo per il quale invece della configurazione 3d4 4s2 si ha la configurazione 3d5 4s1 . Questo avviene perchè la configurazione elettronica che comporta una serie completa di orbitali degeneri completamente piena o piena a metà (cioè con un elettrone in ogni orbitale) è energeticamente favorita, tanto da utilizzare uno degli elettroni 4s per completare il quintetto. La stessa cosa avviene con Cu, che si trova con tutti i 3d completi, utilizzando 1 elettrone 4s (configurazione 3d10 4s1 ). Avremo perciò due atomi con 5 elettroni 3d, Cr e Mn, e due atomi con 10 elettroni 3d, Cu e Zn. Cr e Cu, avendo un solo elettrone s, avranno perciò comportamento chimico diverso (diverse valenze) rispetto ad altri atomi con Z vicino al loro. M. Rustici, Chimica di base 37 Teorie atomiche Figura 2.10. 2.2 Struttura elettronica e tavola periodica degli elementi Eseguendo le operazioni dell’ aufbau si possono notare alcune caratteristiche comuni ad alcuni atomi ed evidenziare una periodicità nelle configurazioni elettroniche degli atomi. Per esempio, alcuni atomi hanno il guscio corrispondente completo e, dal punto di vista chimico-fisico, sono tutti gas monoatomici a temperatura e pressione ambiente; sono molto stabili chimicamente (questa mancanza di reattività ha reso molto difficile la loro scoperta), hanno energia di ionizzazione alta e affinità elettronica quasi nulla. (Il termine chimicamente, per la stabilità, è stato usato poiché, in effetti, Rn lo è dal punto di vista della reattività chimica, ma non lo è dal punto di vista nucleare: infatti è radioattivo). Sono stati perciò chiamati gas nobili. Gli atomi che seguono direttamente i gas nobili costituiscono il gruppo dei metalli alcalini (litio Li con 2s1 , sodio Na con 3s1 , potassio K con 4s1 , rubidio Rb con 5s1 , cesio Cs con 6s1 , francio Fr con 7s1 ) hanno ognuno 1 elettrone nell’orbitale s del guscio superiore, ed hanno anch’essi caratteristiche molto simili tra loro: M. Rustici, Chimica di base 38 Teorie Atomiche Figura 2.11. analogo comportamento chimico, hanno energia di ionizzazione molto bassa e affinità elettroniche paragonabili tra loro. Gli elementi chimici, molto prima dell’avvento della meccanica quantistica, furono raggruppati sotto forma di una tabella nota come tavola periodica degli elementi sulla base delle affinità chimiche riscontrate da il chimico russo Mendeleev. É interessante notare che la tavola periodica degli elementi organizzata alla fine dell’800 sulla base delle proprietà chimiche risulta a sua volta coincidente con quella che possiamo organizzare sulla base della configurazione elettronica. Possiamo allora individuare le famiglie o gruppi di atomi con proprietà chimiche simili hanno la stessa configurazione elettronica esterna. I metalli alcalino terrosi (berillio Be, magnesio Mg, calcio Ca, bario Ba, stronzio Sr, radio Ra) ad esempio hanno configurazione esterna ns2 . Il gruppo degli alogeni (fluoro F, cloro Cl, bromo Br, iodio I, astato At), ha configurazione esterna ns2 np5 . Gli elementi che invece si trovano lungo un periodo sono gli elementi che chimicamente si differenziano gradatamente mano a mano che si allontanano lungo il periodo. La figura 3.10 mostra ad esempio come varia l’energia di prima ionizzazione per i rispettivi atomi. Si può notare come i gas nobile che posseggono l’ottetto completo mostrano la più forte stabilità nel senso che è più difficile rimuovere un elettrone da un gas nobile rispetto ad un altro elemento. I metalli alcalini invece hanno l’energia di ionizzazione più bassa. Avendo questi elementi una configurazione elettronica ns1 si trovano in una condizione di bassa stabilità e se consideriamo l’esistenza di un ottetto completo come caratteristica della stabilità si capisce perché sia più semplice rimuovere un elettrone ad un metallo alcalino. In questo modo infatti raggiungiamo la configurazione elettronica del gas nobile che lo precede. La figura 3.11 mostra invece le proprietà periodiche associate al raggio atomico degli atomi in funzione del numero atomico. Si osserva che generalmente il raggio M. Rustici, Chimica di base 39 Teorie atomiche Figura 2.12. Figura 2.13. diminuisce lungo il periodo fino al gas nobile e poi aumenta bruscamante fino al metallo alcalino successivo. Un’altra interessante proprietà periodica osservabile tra gli elementi è l’affinità elettronica definita come l’energia sviluppata da una mole di un atomo quando acquisisce una mole di elttroni per diventare un anione. La figura 3.12 mostra le proprietà di periodicità di questa grandezza. Possiamo vedere che l’affinità elettronica diminuisce nell’ambito dei gruppi mentre cresce lungo il periodo per raggiungere il suo massimo con gli alogeni. Nella tavola periodica inoltre si distinguono gli elementi tra metalli e non metalli. Resta ancora in uso una tradizionale classificazione degli elementi in metalli e non-metalli. In breve, sono chiamati: metalli gli elementi con un numero di elettroni esterni basso, minore o, talvolta, eguale a quello degli orbitali esterni s e p, e con energia di ionizzazione bassa. Perciò gli elementi di transizione, M. Rustici, Chimica di base 40 Teorie Atomiche i lantanoidi e gli attinoidi, avendo 1 o 2 elettroni s, sono considerati metalli. Il carattere metallico aumenta scendendo lungo ogni gruppo (infatti diminuisce l’energia di ionizzazione); non-metalli: gli elementi con numero di elettroni esterni maggiore del numero di orbitali esterni s e p e con energia di ionizzazione alta. semimetalli: elementi che possono comportarsi da metalli o da non-metalli in situazioni particolari; sono quelli di confine tra i due tipi. M. Rustici, Chimica di base Capitolo 3 Legame Chimico 3.1 Legame Chimico Il capitolo sul legame chimico è probabilmente l’argomento centrale di tutto il corso di Chimica. Comprendere il legame e la sua natura è di fondamentale importanza per comprendere la differenza sostanziale fra composti ionici e covalenti. Da tale comprensione dipende anche la capacità di prevedere le proprietà chimico-fisiche dei composti e il loro comportamento chimico (reattività). È importante tener presente fin dall’inizio che alla base della formazione del legame chimico vi è il tentativo di raggiungere una condizione di stabilità: un composto o una molecola sono sempre più stabili degli atomi isolati che li costituiscono. Il concetto di stabilità, in chimica come in fisica, è sempre associato ad un minor contenuto di energia potenziale. Sappiamo già che fra gli elementi vi è un gruppo (lo zero) i cui componenti, i gas nobili, sono caratterizzati da una configurazione elettronica eccezionalmente stabile: questa configurazione elettronica, in cui il guscio esterno contiene otto elettroni, può essere considerata la forma necessaria per raggiungere la stabilità. È proprio la ricerca del raggiungimento di tale configurazione elettronica che spinge gli atomi a formare il legame chimico. Quando due atomi sono a grandissima distanza tra loro le forze di interazione fra le nuvole elettroniche sono nulle e l’energia potenziale del sistema E è pari a 0. Se i due atomi si avvicinano si possono avere due possibilità come evidenziato dalla figura 4.1. Se all’avvicinarsi dei due atomi prevalgono le forze repulsive tra le nuvole elettroniche l’energia del sistema aumenta. Le condizioni di energia minima si hanno quando gli atomi sono lontani tra loro, praticamente quando gli atomi sono isolati. Questo è il caso dei gas nobili che non manifestano nessuna tendenza a legarsi e rimangono nello stato monoatomico. Se all’avvicinarsi dei due atomi si ha un’interazione attrattiva fra le nuvole elettroniche e i nuclei, l’energia E diminuisce finché la distanza non diventa cosı̀ piccola che prevalgono le forze repulsive sulle attrattive con conseguente aumento dell’energia potenziale. La distanza associata al minimo di energia è detta distanza di legame. In tal caso tra gli atomi si è formato un legame chimico. Nei vari tipi di legami sono coinvolti M. Rustici, Chimica di base 42 Legame Chimico Figura 3.1. gli elettroni periferici, detti anche elettroni di valenza. Le interazioni attrattive responsabili del legame hanno origine diversa a seconda della natura degli atomi interessati al legame. 3.1.1 Legame Ionico Il legame ionico è un legame di natura elettrostatica ed è il tipico legame che si stabilisce tra elementi con basso potenziale di ionizzazione ed elementi con alta affinità elettronica. Ricordando l’andamento di queste due proprietà periodiche, possiamo aspettarci che i più semplici composti ionici binari siano costituiti quasi esclusivamente dagli elementi dei primi tre gruppi e dei metalli di transizione (che posseggono basso potenziale di ionizzazione) e da elementi del VI e VII gruppo (caratterizzati da alta affinità elettronica). L’elemento con bassa energia di ionizzazione trasferisce elettroni al guscio di valenza dell’altro caricandosi positivamente e diventando un catione l’elemento che invece acquista gli elettroni diventa un anione. Tra i due ioni aventi carica opposta si instaura un legame di natura elettrostatica. Ad esempio il comune sale da cucina con formula NaCl è costituito da cationi Na+ e anioni Cl− . Come vedremo meglio in seguito il sistema ione positivo e ione negativo non raggiunge la massima stabilità con la formazione di una singola coppia di ioni, ma nella formazione di un solido cristallino in cui ogni ione attrae il maggior numero possibile di ioni di segno opposto in modo da minimizzare la repulsione elettrostatica. Nel caso del cloruro di sodio la formula indica semplicemente che il rapporto tra gli ioni sodio e gli ioni cloruro è di 1:1 mentre ad esempio per il BaBr2 il rapporto tra gli ioni bario e gli ioni bromuro è di 1:2. M. Rustici, Chimica di base 43 Legame chimico Figura 3.2. Nella formazione dei legami ionici, la maggior parte degli elementi dei blocchi s e p raggiunge, nel caso di ioni positivi, la configurazione del gas nobile che li precede e, nel caso degli ioni negativi, quella del gas nobile che li segue. Come evidenziato nel caso della formazione del cloruro di sodio dalla figura 4.2. 3.1.2 Teoria del legame di valenza Quando si incontrano due atomi uguali o con potenziale di ionizzazione e affinità elettronica simili, non vi può essere ovviamente un trasferimento completo di elettroni dall’uno all’altro, come avviene nella formazione del legame ionico. In questo caso i due atomi possono tuttavia raggiungere la configurazione elettronica stabile del gas nobile, mettendo in compartecipazione i propri elettroni spaiati. Questo è quanto avviene nella formazione del legame covalente. Il legame covalente è formato da una coppia di elettroni condivisa fra due atomi. È attraverso questo tipo di legame che si formano le molecole, aggregati atomici stabili, capaci di esistere come unità indipendenti in tutti gli stati di aggregazione della materia. L’ipotesi del legame covalente come doppietto elettronico condiviso fra due atomi fu suggerita dal chimico americano Gilbert Newton Lewis (1874-1946) nel 1916 che sviluppò, la teoria dell’ottetto. Lewis propose anche di rappresentare le configurazioni elettroniche esterne degli elementi, ponendo dei punti attorno al simbolo elementare stesso, che di per sé aveva lo scopo di indicare il nocciolo, ovvero i gusci elettronici completi più interni. Similmente, il legame nelle formule si sarebbe rappresentato con i due punti ( : ). Attualmente, anziché i due punti, si preferisce usare un trattino; il trattino che si usa nelle formule di struttura non è quindi un semplice formalismo, ma ha il preciso significato di doppietto elettronico, sia esso di legame o solitario. In altre parole ogni trattino che compare in una formula di struttura rappresenta una coppia di elettroni: questa può essere una coppia di legame, quando è in compartecipazione tra due atomi, o un doppietto solitario. Il simbolismo di Lewis per indicare gli elettroni di valenza, unitamente alle sue due ipotesi centrali: M. Rustici, Chimica di base 44 Legame Chimico Figura 3.3. Figura 3.4. • legame covalente (doppietto condiviso) • teoria dell’ottetto Ad esempio nel caso dell’idrogeno, in cui abbiamo due atomi con un elettrone spaiato, quando questi si avvicinano formeranno un legame covalente per compartecipazione elettronica. In altre parole la descrizione energetica offerta mediante la figura 4.1 si adatta perfettamente alla descrizione della formazione del legame covalente, che rappresentato mediante le formule di Lewis sarà H-H e simboleggato come H2 . Quello che avviene nella formazione della molecola di idrogeno può essere esteso, con le opportune precisazioni, a molte altre molecole biatomiche. Gli alogeni ad esempio, che hanno configurazione elettronica esterna ns2 np5 , possono mettere in compartecipazione l’elettrone spaiato di uno degli orbitali p e raggiungere la configurazione elettronica stabile del gas nobile successivo come mostrato in figura 4.3. Il legame covalente non è esclusivo di molecole formate da atomi uguali (omonucleari). Idrogeno e fluoro, ad esempio, possono mettere in compartecipazione una coppia di elettroni (1s dell’H e 2p del F), raggiungendo entrambi la configurazione elettronica stabile dell’He e del Ne, rispettivamente (Fig.4.4). In questo caso parleremo di legami eteronucleari. Il legame covalente nelle molecole di H2 , F2 o HCl è un legame singolo, costituito cioè da una singola coppia di elettroni di legame. Si dice che un legame singolo ha ordine di legame 1 dove l’ordine di legame indica il numero di coppie condivise tra due atomi legati. Molte molecole presentano doppi o tripli legami cioè legami multipli. un legame doppio è costituito da due coppie di legame, quattro elettroni condivisi tra due atomi e l’ordine di legame è 2, un legame triplo è invece costituito da tre legami (Fig 4.5). La forza di legame dipende dalla mutua attrazione tra i nuclei legati e gli elettroni condivisi e definiamo l’energia di legame l’energia necessaria per vincere M. Rustici, Chimica di base 45 Legame chimico Figura 3.5. questa attrazione. Tale energia risulta a sua volta correlata con la lunghezza di un legame e dipende prima di tutto dalle dimensioni atomiche; tuttavia, a parità di dimensioni atomiche, la lunghezza di un legame è funzione dell’ordine di legame: in particolare, come si può facilmente intuire, la lunghezza di legame diminuisce all’aumentare dell’ordine di legame. Quindi è ovvio che un legame triplo sia più forte del doppio che a sua volta è più forte del singolo. Un importante concetto nel legame chimico è quello di elettronegatività cioè la capacità di un singolo atomo legato di attrarre gli elettroni condivisi. Il chimico statunitense Linus Pauling propose una scala arbitraria, basata su calcoli di energia di legame, nella quale il fluoro è il primo, cioè l’elemento più elettronegativo, seguito dall’ossigeno. I metalli alcalini sono gli elementi meno elettronegativi. Sono state proposte anche scale di tipo diverso, basate su altre proprietà atomiche, ma, in ogni caso, l’ordine relativo degli elementi rimane lo stesso. La differenza in elettronegatività fra due elementi determina il carattere ionico o covalente del legame che si può instaurare fra di loro. Come vedremo l’elettronegatività trova un impiego importante per la determinazione del numero di ossidazione di una atomo che viene definito come la differenza tra il numero degli elettroni di valenza meno la somma tra il numero degli elettroni condivisi e non condivisi. Ad esempio nell’HCl il cloro ha 7 elettroni di valenza al cloro, essendo l’elemento più elettronegativo si assegnano 8 elettroni (2 condivisi e 6 non condivisi) quindi il suo numero di ossidazione è 7-8=-1 ovviamente all’atomo di idrogeno non esssendo assegnato nessun elettrone ed avendo 1 elettrone di valenza risulta che il suoi numero di ossidazione sarà pari a +1. Abbiamo osservato come sia naturale concepire il legame chimico attraverso una coppia elettronica, cerchiamo comunque di capire il motivo per cui come il legame cosı̀ concepito possa condurre ad un abbassamento locale dell’energia della molecola rispetto agli atomi singoli. Consideriamo per prima cosa la descrizione di due atomi di H separati da una distanza infinita. La funzione d’onda totale dei due elettroni è cosı̀ rappresentata dal prodotto a(1)b(2) dove abbiamo idnicato con a l’orbitale 1s dell’atomo a e con b l’orbitale 1s associato all’atomo b. ovviamente l’energia totale risulterà essere pari 2E1 s dove con E1 s indichiamo l’energia associata allo stato fondamentale dell’atomo di idrogeno. Quando gli atomi si trovano invece alla distanza di legame si potrebbe pensare che la funzione a(2)b(1) possa descrivere, altrettanto bene, il nostro stato legante data l’indistinguibilità degli elettroni ne consegue che una buona funzione di partenza per la descrizione M. Rustici, Chimica di base 46 Legame Chimico Figura 3.6. dello stato legante possa essere descritta da una funzione del tipo Ψ = a(1)b(2) ± a(2)b(1) Utilizzando una funzione di questo tipo è possibile valutare, con qualche sforzo, l’energia associata allo stato fondamentale della molecola H2 è esprimibile come 2E1 s + ∆E. Essendo queste quantità negative, l’energia della molecola risulta più stabile di quella dei due atomi separati. Il successo della teroia sta inoltre nel fatto che il termine ∆E corrisponde all’energia di dissociazione che risulta confrontabile con il valore ottenuto sperimentalemnte. La teoria del legame di valenza costituisce pertanto un’ottima descrizione del legame covalente. 3.1.3 Legami covalenti polari Quando atomi con diversa elettronegatività formano un legame, la coppia di legame viene condivisa in modo disuguale, pertanto il legame ha un polo parzialmente negativo e uno parzialmente positivo. Questo legame si ottiene a causa del fatto che il baricentro delle cariche negative non coincide con quello delle cariche positive e ciò implica la formazione di una polarità di legame(fig 4.6). Se ci chiediamo se il legame tra una molecola XY sia ionico o covalente la risposta è quasi sempre parzialmente ionico e parzialmente covalente. Per dipolo si intende un sistema costituito da due cariche elettriche dello stesso valore assoluto e di segno contrario, poste a distanza r fra di loro. Ogni dipolo è caratterizzato da un momento dipolare, definito da µ = qr, dove q indica l’intensità della carica. Il momento dipolare è una grandezza vettoriale, il cui verso è per convenzione dalla carica negativa a quella positiva. Nel caso delle molecole poliatomiche, per valutarne la polarità occorre considerare la geometria molecolare. M. Rustici, Chimica di base Capitolo 4 Geometria molecolare 4.1 Geometria molecolare Prima di comprendere meglio le basi teoriche del legame chimico attraverso la teoria del legame di valenza e dell’orbitale molecolare conviene affrontare il problema della geometria molecolare a tale scopo vedremo che possiamo sfruttare la teoria della repulsione elettronica che fornisce un’utile metodo per la costruzione della geometria molecolare. La teoria VSEPR (Valence Shell Electron Pair Repulsion) proposta da Gillespie permette di spiegare in modo semplice la forma delle molecole. Tuttavia prima di passare alla vera e propria geometria molecolare è utile rappresentare la molecolare nella formula di Lewis corrispondente. 4.1.1 Strutture di Lewis a legame singolo Esaminiamo allora le varie tappe per il raggiungimento delle strutture di Lewis che possiamo schematizzare come segue. • Collocare gli atomi uno rispetto all’altro. Per molecole aventi formula ABn si colloca al centro l’atomo avente il numero di gruppo più basso • determinare il numero totale di elettroni di valenza disponibili • disegnare un legame singolo da ciascun atomo circostante all’atomo centrale e sottrarre due elettroni di valenza per ciascun legame • distribuire gli elettroni restanti in coppie in modo che ogni atomo ottenga otto elettroni o due nel caso dell’idrogeno. Le figura 5.1 mostra come si possono realizzare tali strutture per le molecole del metano CH4 , dell’ammoniaca NH3 e dell’idruro di boro BH3 . Siamo spesso in grado di scrivere più di una formula di struttura di Lewis, ciascuna con la stessa posizione relativa degli atomi per molecole o ioni con legami doppi adiacenti ai legami singoli. La figura 5.2 mostra le due possibili strutture di Lwies associate alla M. Rustici, Chimica di base 48 Geometria molecolare Figura 4.1. Figura 4.2. molecola dell’ipoazotide NO2 . In realtà nessuna delle due strutture rappresenta accuratamente la molecola in questione. Le misure mostrano ad esempio che le lunghezze di legame sono identiche con proprietà intermedie ad un doppio legame e ad un singolo legame. La molecola è rappresentata più correttamente da quello che si chiama ibrido di risonanza e le due strutture si dicono in risonanza tra loro. Le strutture di risonanza non sono reali rappresentazioni del legame diciamo che il doppio legame è in questo caso delocalizzato su tutta la molecola. Un altro tipo esempio è rappresentato dallo ione carbonato. La figura 5.3 mostra le strutture di risonanza e l’ibrido di risonanza ad esso associato. 4.1.2 Eccezioni alla regola dell’ottetto La regola dell’ottetto è un utile guida per la maggior parte di molecole con atomi centrali del periodo 2 ma non è sempre valida. A partire dai non metalli del III periodo (Si, P, S, Cl), la regola dell’ottetto M. Rustici, Chimica di base 49 Geometria molecolare Figura 4.3. può essere superata. L’espansione dell’ottetto si giustifica supponendo che questi elementi, disponendo di orbitali d nello strato di valenza, possano sfruttare questi orbitali per disaccoppiare i loro elettroni, in modo da utilizzare ciascuno di essi per formare un legame covalente. Dobbiamo comunque sottolineare che la possibilità di espandere l’ottetto si manifesta generalmente solo quando si formano legami con elementi molto elettronegativi, come gli alogeni o l’ossigeno. In pratica, non incontreremo mai composti tipo PH5 o analoghi. Per effetto della promozione degli elettroni negli orbitali d, gli elementi del III periodo potranno presentare covalenze diverse (vedi figura 5.4): Si deve fare attenzione a non confondere il concetto di covalenza (numero di coppie elettroniche, o numero di legami, che un atomo può condividere con altri atomi) con il numero di atomi che un elemento può legare. Ad esempio, in H3 PO4 (acido fosforico) il fosforo è pentacovalente, ma lega solo quattro atomi; in CO2 il carbonio è tetracovalente, ma lega solo due atomi. Un atomo espande il suo guscio di covalenza per formare più legami e l’unico modo in cui ciò è possibile è quello di usare orbitali d esterni 4.1.3 Teoria VESPR e forma molecolare Tramite la teoria VSEPR (dall’inglese Valence Shell Electron-Pair Repulsion cioè repulsione delle coppie di legame dello strato di valenza) è possibile spiegare la forma di un certo numero di molecole applicando il concetto che: gli elettroni di valenza di ogni singolo atomo, sia quelli utilizzati nei legami sia quelli non utilizzati, tendono a respingersi in quanto di carica uguale e a occupare le posizioni più distanti nello spazio. M. Rustici, Chimica di base 50 Geometria molecolare Figura 4.4. Figura 4.5. Gli elettroni di valenza vengono considerati a coppie e siccome ogni atomo tende, di norma, a circondarsi di otto elettroni nel livello più esterno, saranno quattro le coppie di elettroni in gioco. Esaminiamo come primo esempio la molecola dell’anidride carbonica CO2 In questa molecola esistono due legami doppi (ogni legame doppio è costituito da quattro elettroni in comune) tra il carbonio e gli atomi di ossigeno; tutte quattro le coppie di elettroni di legame sono dunque impegnate in legami chimici. La posizione in cui questi due gruppi di elettroni sono il più distante possibile è quella mostrata in figura, con un angolo di legame tra gli atomi di 1800 ; in questo caso la repulsione è minima e la molecola acquista una disposizione lineare (vedi figura 5.5). Nella molecola BH3 invece le tre coppie di elettroni di valenza del boro per M. Rustici, Chimica di base 51 Geometria molecolare Figura 4.6. Figura 4.7. stare alla maggior distanza reciproca possibile si collocano ai vertici di un triangolo equilatero. La molecola assume quindi una disposizione planare triangolare con angoli di legame di 1200 . Osservate che in questa molecola gli elettroni di valenza sono soltanto sei e dunque la regole dell’ottetto non è rispettata (vedi figura 5.7). Osserviamo invece come si dispongono gli atomi nella molecola del metano CH4 (vedi figura 5.6). In questo caso la massima distanza possibile tra le coppie di elettroni è raggiunta con la disposizione di queste ai vertici di un tetraedro. Gli angoli di legame sono di 109.50 e la molecola assume una disposizione tetraedrica. Anche nella molecola dell’acqua H2 O la situazione è analoga (vedi figura 5.8), ma mentre nel metano le coppie di elettroni sono tutte di legame, nell’ acqua due coppie sono libere e sono più vicine all’atomo di ossigeno di quanto non lo siano le altre due impegnate nei legami con l’idrogeno. Tutto questo fa sı̀ che le coppie di legame siano spinte un po’ più vicine l’una all’altra e giustifica il minor angolo di legame (1050 ) presente nell’acqua rispetto al metano. La molecola dell’acqua è dunque caratterizzata da una disposizione angolata degli atomi che ne determina M. Rustici, Chimica di base 52 Geometria molecolare Figura 4.8. l’elevata polarità. Quando abbiamo 5 gruppi di elettroni la disposizione geometrica è di tipo bipiramide trigonale. Un esempio di tale struttura è quella del pentacloruro di fosforo PCl5 . Se ci sono coppie solitarie a causa del fatto che le coppie solitarie danno luogo ad una maggiore repulsione si trova in generale che tali coppie si posizionano nella bipiramide trigonale nelle posizioni equatoriali come nel caso del tetrafloruro di zolfo SF4 nel caso che le coppie solitarie siano due la tendenza a posizionarsi nelle posizioni equatoriali genera una forma a T come nel caso trifloruro di bromo BrF3 . Le molecole con tre coppie solitarie genarano invece una struttura lineare è il caso dello ione I− 3. Le forme molecolari con sei gruppi di elettroni generano una disposizione ottaedrica questo è il caso dell’esafloruro di fluoro SF6 . Quando compare una coppia solitaria come nel caso del pentafloruro di iodio (IF5 ), dato che ogni posizione è equivalente, non esiste una posizione privilegiata per la coppia solitaria e si raggiunge cosı̀ una struttura a forma di piramide a base quadrata. Nel caso in cui le coppie solitarie siano 2 esse giacciono sempre in vertici opposti per evitare le più forti repulsioni e questo genera struttura planare quadrata. Questo è il caso del tetrafloruro di xeno (XeF4 ). In generale possiamo sfruttare lo schema rappresentato dalla Figura 5.9 per la determinazione delle geometrie molecolari. 4.1.4 Forma molecolare e polarità La conoscenza della struttura molecolare è essenziale per comprendere il suo comportamento chimico-fisico. Uno degli effetti più importanti è quello della polarità molecolare. Nelle molecole biatomiche, come l’HF in cui c’è soltanto un legame, la polarità di legame implica a sua volta una polarità molecolare. Nelle moleco- M. Rustici, Chimica di base 53 Geometria molecolare Figura 4.9. le con più atomi sia la forma che la polarità di legame determinano la polarità molecolare. Se prendiamo ad esempio la molecola del biossido di carbonio CO2 , il cui legame C-O è fortemente polare, essa risulta apolare a causa del fatto che la molecola è lineare e le identiche polarità si controbilanciano perfettamente e conferiscono alla molecola un momento dipolare nullo (µ = 0 D). Anche nella molecola dell’acqua vi sono atomi identici legati all’atomo centrale ma essa ha un rilevante momento dipolare (µ = 1.85 D). In questo caso infatti le polarità di legame non si controbilanciano perchè la molecola d’acqua è angolata. M. Rustici, Chimica di base Capitolo 5 Legame covalente 5.1 Teoria del legame covalente La teoria moderna del legame chimico viene spiegata attraverso due teorie quantomeccaniche entrambi capaci di spiegare le proprietà delle molecole a partire dale proprietà atomiche. Si tratta della teoria del legame di valenza e quella dell’orbitale molecolare. 5.1.1 Teoria del legame di valenza Il principio fondamentale che sottende alla teoria del legame di valenza (VB) è relativo al fatto che un legame chimico si definisce tale quando gli orbitali dei due atomi si sovrappongono e sono occupati da una coppia di elettroni che hanno la massima probabilità di trovarsi tra i due nuclei. Da questo principio possiamo derivare tre temi centrali 1. la coppia di elettroni che formano il legame covalente deve essere costituita da elettroni antiparalleli per soddisfare il principio di esclusione di Pauli 2. Maggiore è la sovrapposizione degli orbitali e maggiore è la forza di legame. Ques’ultima è infatti regolata dall’attrazione esercitata dai nuclei sugli elettroni condivisi. 3. Gli orbitali atomici nella molecola sono diversi da quelli atomici a causa del fatto che gli orbitali atomici possono mescolarsi (ibridazione) generando nuovi orbitali diversamente orientati nello spazio. La teoria dell’ibridazione spiega molto bene la geometria molecolare. Abbiamo visto nel capitolo precedente come sia possibile derivare la struttura di una semplice molecola attraverso la teoria delle repulsioni elettroniche. Vogliamo analizzare ora come la teoria dell’ibridazione permette di fornire una semplice teoria quantomeccanica per la spiegazione della geometria molecolare. Una volta nota la geometria molecolare possiamo ipotizzare i tipi di orbitali ibridi. Ad ogni ibridazione corrisponde infatti una particolare geometria. M. Rustici, Chimica di base 56 Legame covalente sp La teoria VB mostra che quando si ha un mescolamento tra un orbitale p e un orbitale s si ottengono due nuovi orbitali ibridi equivalenti separati da 1800 (Figura 6.1). Questa struttura corrisponde a quella quando l’atomo centrale è circondato da due gruppi di elettroni, in tal caso si osserva una struttura lineare. Inoltre, la forma e l’orientamento dei nuovi orbitali massimizzano la sovrapposizione degli orbitali. Questo implica a sua volta una minimizzazione dell’energia della molecola. Come esempio molecolare possiamo pensare all’HCl o al BeCl2 gassoso. sp2 Per spiegare la disposizione trigonale planare di coppie di elettroni si ricorre all’ibridazione sp2 in cui l’atomo centrale mescola due orbitali p con un orbitale s generando a sua volta tre orbitali orientati a 1200 uno rispetto all’altro (Figura 6.1). Ad esempio secondo tale teoria l’atomo centrale del B nella molecola BF3 è ibridato sp2 . Un altro caso è rappresentato dall’ozono O3 in cui l’atomo centrale di O è ibridato sp2 e una coppia solitaria riempie uno dei sui tre orbitali e quindi l’ozono ha una forma molecolare piegata. sp3 Il caso tipico di questa ibridazione è quello della molecola del metano CH4 in cui gli atomi di idrogeno si trovano ai vertici di un ideale tetraedro. Quando infatti l’atomo centrale mescola tre orbitali p con un orbitale s si ottengono 4 orbitali ibridi con geometria tetraedrica. Altri esempi tipici sono quelli della molecola dell’ammoniaca NH3 con struttura di tipo piramidale dove una orbitale ibrido è occupato da una coppia solitaria o analogamente nella molecola dell’acqua H2 O dove due orbitali ibridi sono occupati da due coppie solitarie generando una struttura piegata. sp3 d Le forme molecolari con disposizione bipiramidali trigonali od ottaedriche si ottengono mediante ragionamenti simili. Ad esempio per spiegare la forma trigonale bipiramidale del PCl5 si ipotizza che l’orbitale 3s si mescoli con tre orbitali 3p e 1 orbitale 3d dell’atomo di fosforo. Cosı̀ si ottengono 5 orbitali equivalenti sp3 d orientati secondo i vertici di una piramide trigonale. sp3 d2 Per spiegare la forma della molecola SF6 il modello VB ipotizza che l’orbitale 3s si mescoli con 3 orbitali 3p e con 2 orbitali 3d in questo modo si genererà un insieme di 6 orbitali ibridi con geometria corrispondente a quella di un ottaedro. Non sempre la teoria risulta necessaria per spiegare la geometria. Se prendiamo ad esempio la molecola dell’acido solfidrico H2 S si osserva che l’angolo di legame tra gli atomi di idrogeno è dell’ordine di 920 in questo caso l’angolo di legame risulta più vicino a quello degli atomi non ibridati che rispetto a quelli ibridati. M. Rustici, Chimica di base 57 Legame covalente Figura 5.1. 5.1.2 Legami singoli e doppi Come abbiamo visto precedentemente le molecole possono formare legami semplici, doppi e tripli. Nel caso in cui la sovrapposizione tra orbitali ibridi generi una densità elettronica concentrata lungo l’asse di legame parliamo di legami σ (Figura 6.2). Viceversa quando abbiamo una sovrapposizione di fianco si parla di legame π (figura 6.3). Per comprendere meglio questo legame possiamo riferirci alla molecola del dell’etilene. I due atomi centrali di carbonio sono ibridati sp2 e pertanto l’angolo tipico di legame è di 1200 . I due atomi di carbonio sono legati tra loro tramite un legame σ e ogni atomo di carbonio lega a sua volta sempre mediante legami σ 2 atomi di H. Tuttavia cosı̀ facendo rimangono ancora su ogni atomo di carbonio due orbitali p puri contenenti un elettrone ciascuno. Il legame σ permette tuttavia una forte vicinanza tra i due atomi di carbonio che a sua volta permette una sovrapposizione dei due orbitali p. Cosı̀ facendo si generano due regioni di densità elettronica una al di sopra l’altra al di sotto dell’asse formato dal legame σ. Un legame π contiene due elettroni che si muovono attraverso entrambe le regioni di legame. Un legame doppio è sempre costituito da un legame σ e un legame π. Un legame triplo quale quello che si forma nella molecola dell’acetilene è costituito da un legame σ e da due legami π. Questo tipo di sovrapposizione genera una simmetria cilindrica della molecola. M. Rustici, Chimica di base 58 Legame covalente Figura 5.2. L’entità della sovrapposizione influenza la forza di legame. La sovrapposizione generata dal legame π è meno pronunciata di quella del legame σ per tale motivo il legame π è più debole del legame σ. 5.1.3 Teoria dell’Orbitale molecolare MO La teoria del legame di valenza descrive in modo semplice i legami chimici e le strutture molecolari ma è del tutto insoddisfacente quando si tratta di giustificare l’esistenza di molecole a numero dispari di elettroni, come ad esempio lo ione H+ 2, e specialmente gli stati energetici delle molecole. la teoria assegna gli elettroni di una molecola ad una serie di orbitali, detti orbitali molecolari, che appartengono all’intera molecola. Come gli orbitali atomici sono funzioni matematiche che descrivono il comportamento di un elettrone in un atomo analogamente gli orbitali molecolari sono funzioni matematiche che descrivono il comportamento di un elettrone in una molecola. Il quadrato di queste funzioni corrisponde alla probabilità di trovare un elettrone in una determinata regione della molecola. Nell’approssimazione più semplice queste funzioni sono combinazioni lineari di orbitali atomici. Si ottiene in tal modo una serie di orbitali molecolari, che si estendono su tutti gli atomi della molecola, che vengono ordinati secondo energie crescenti; gli elettroni, in numero uguale al totale di elettroni vengono assegnati a questi orbitali seguendo il principio di Pauli e le regole di Hund. M. Rustici, Chimica di base 59 Legame covalente Figura 5.3. Nella molecola di H+ 2 i due orbitali atomici 1s dei due atomi di idrogeno interagiscono all’avvicinarsi dei due nuclei e generano due orbitali molecolari indicati ∗ con σ1s orbitale di legame e σ1s orbitale di antilegame. All’orbitale di legame corrisponde l’energia più bassa e l’elettrone in tal caso andrà ad occupare l’orbitale di legame ad energia più bassa. I due orbitali sono di tipo σ perché la nuvola elettronica si concentra lungo l’asse. internucleare. La formazione degli orbitali molecolari, il cui numero è uguale a quello degli orbitali atomici combinati, richiede che gli orbitali atomici soddisfino i seguenti requisiti: 1. gli orbitali atomici che si combinano devono avere energie simili; 2. le superfici limite devono sovrapporsi il più possibile: maggiore è la sovrapposizione minore è l’energia dell’orbitale molecolare risultante; 3. gli orbitali atomici che si combinano devono possedere un’opportuna simmetria; La figura 6.4 mostra uno schema generico relativo alla combinazione di orbitali atomici per la generazione di orbitali molecolari per il numero quantico principale n=2. Gli orbitali atomici di tipo 2s si combinano nel modo analogo a quelle degli orbitali 1s come abbiamo precedentemente descritto. In questo caso genereranno ∗ di legame e antilegame. gli orbitali 2σ2s e 2σ2s La combinazione lineare degli orbitali p può essere ottenuta solo per le coppie ∗ di px − px , py − py e pz − pz . Nel primo caso si otterranno orbitali 2σ2px e 2σ2p x legame e antilegame. Nel secondo ( combinazione py − py ) e terzo caso (combinazione pz − pz ) gli orbitali molecolari che si formano si dicono π, in particolare ∗ e π2pz ∗ sono di gli orbitali π2py e π2pz sono di legame mentre gli orbitali π2p y antilegame. Gli orbitali p erano degeneri mentre gli orbitali ottenuti per combinazione lineare non sono più tutti degeneri. Abbiamo due orbitali π degeneri. M. Rustici, Chimica di base 60 Legame covalente Figura 5.4. 5.1.4 Legame metallico I metalli che costituiscono circa due terzi della tavola periodica hanno basse energie di ionizzazione e bassa elettronegatività come abbiamo già visto in precedenza. Ricordiamo inoltre che i metalli sono caratterizzati da un’elevata conducibilità elettrica e termica da una buona malleabilità e duttilità da una struttura compatta opacità e lucentezza caratteristiche. Il legame metallico viene interpretato da un’estensione della teoria dell’orbitale molecolare che prende il nome di teoria delle bande. Quando la teoria dell’orbitale molecolare viene impiegata per un numero elevato di orbitali atomici a seguito dell’interazione degli orbitali di valenza si ottiene un numero di orbitali molecolari ad energia ravvicinata con infittimento dei livelli energetici tanto maggiore quanto aumenta il numero di orbitali atomci interagenti. Questa interazione genera tanti orbitali molecolari di energia cosı̀ simile tra loro da dar luogo ad una banda praticamente continua di energia. 1. la distribuzione di elettroni in una banda avviene dapprima nei livelli infe- M. Rustici, Chimica di base 61 Legame covalente riori e via via in quelli superiori. Poiché in un livello della banda possono stare due elettroni una banda formata da N livelli può ospitare 2N elettroni. 2. quando sono interessati gli orbitali atomici di valenza si parla di banda di valenza. 3. se le energie degli orbitali atomici di partenza sono molto diverse le bande di energia rimangono distinte, altrimenti si sovrappongono. Per avere conduzione elettrica occorre che la banda di valenza oppure la banda che si sovrappone a quella di valenza satura sia vuota o parzialmente occupata in modo da costituire una banda di conduzione. M. Rustici, Chimica di base Capitolo 6 Numeri di ossidazioni, nomenclatura e reazioni chimiche Per meglio conoscere la chimica è necessario saper utilizzare anche il suo linguaggio formale allo scopo di saper scrivere correttamente i composti chimici e rappresentare i processi di reazione che coinvolgono i singoli elementi, molecole o composti in genere. A tale scopo è necessario introdurre alcuni concetti elementari, quali il numero di ossidazione, la nomenclatura e le generalità delle reazioni chimiche. 6.1 Numero di ossidazione Per prima cosa definiamo il concetto di numero di ossidazione inteso come il numero di cariche reali o virtuali possedute da un elemento in composto. Questo concetto che, nella sua prima lettura, può apparire astratto risulta, invece molto utile per la descrizione delle formule chimiche ed in particolare per quelle reazioni che coinvolgono una variazione dei numeri di ossidazione nel corso della reazione. Dalla definizione che abbiamo fornito, è evidente che la carica posseduta dagli ioni metallici del tipo Na+ , Fe2+ , Cr3+ o anioni come Cl− , coincide esattamente con la definizione di numero di ossidazione. Il numero di ossidazione non è fisso per gli atomi, essitono infatti elementi come il ferro che può trovarsi sia come Fe2+ che come Fe3+ ; i suoi numeri di ossidazione principali saranno allora +2 o +3. Che cosa intendiamo invece per cariche virtuali possedute da un elemento in un composto? Quando ci troviamo con composti covalenti il numero di ossidazione viene assegnato sulla base della diversa elettronegatività degli elementi che costituiscono la molecola. Per convenzione assegnamo il doppietto di un legame covalente all’atomo più elettronegativo, cosı̀ facendo l’atomo che acquista un elettrone acquisisce una carica formale di -1 mentre quello che lo perde acquisisce una carica formale di +1. Supponiamo di prendere in considerazione la molecola dell’acido cloridrico (HCl), l’elettronegatività del cloro è superiore a quella dell’idrogeno formalmente M. Rustici, Elementi di Chimica 64 Numeri di ossidazioni, nomenclatura e reazioni chimiche possiamo scomporre la molecola HCl in due ioni H+ e Cl− . Ovviamente in fase gassosa, esiste la molecola HCl, con un legame covalente di tipo σ, e non esistono gli ioni H+ e Cl− , tuttavia possiamo assegnare ai due atomi rispettivamente numero di ossidazione +1 e -1. Lo stesso ragionamento possiamo farlo per la molecola H2 O in cui ogni atomo di H è legato mediante due legami σ all’atomo di ossigeno. Possiamo, pertanto, assegnare i due doppietti di legame all’atomo di ossigeno, in questo modo l’ossigeno si troverà a possedere due elettroni in più acquistando una carica virtuale pari a -2 (O2− ) viceversa ogni atomo di idrogeno acquisterà una carica virtuale pari a +1 (H+ ). In altre parole l’ossigeno, nella molecola dell’acqua avrà, numero di ossidazione -2 e l’idrogeno numero di ossidazione +1. Sulla base di quanto detto possiamo cercare di individuare delle regole generali che possiamo cosı̀ schematizzare: • Gli elementi allo stato elementare sia che si trovino in forma atomica o pluriatomica avranno necessariamente numero di ossidazione 0. Nel caso in cui siano in forma pluriatomica non esiste nessun modo per assegnare il doppietto di legame ad un atomo rispetto all’altro e pertanto il numero di ossidazione sarà sempre 0 (es O2 , O3 , P4 , N2 , H2 etc) • Essendo il fluoro l’elemento con la massima elettronegatività esso avrà sempre un numero di ossidazione pari a -1 salvo quando si trova allo stato elementare F2 e in quel caso avrà numero di ossidazione 0. • l’ossigeno O essendo l’atomo con la maggiore elettronegatività, dopo quella del fluoro F, avrà sempre numero di ossidazione pari a -2 a parte alcune eccezioni. La prima eccezione riguarda il composto OF2 , in questo caso l’ossigeno avrà ovviamente numero di ossidazione +2. La seconda eccezione riguarda i composti, noti come perossidi, nei quali due atomi di ossigeno sono tra loro legati. Il capostipite di questi composti è l’acqua ossigenata o perossido di idrogeno H2 O2 in cui il doppietto di legame O-O non contribiusce al numero di ossidazione perché, al solito, non è possibile assegnare il doppietto a nessuno dei due atomi di ossigeno, mentre per i doppietti di legame idrogeno ossigeno vengono assegnati rispettivamente ai due atomi di ossigeno. In altre parole sulla base di questa assegnazione si ottengono gli ioni virtuali H+ e O2− 2 , quest’ultimo è noto come ione perossido. Ogni atomo di ossigeno avrà pertanto numero di ossidazione -1. • L’idrogeno H ha sempre numero ossidazione +1 eccetto il caso in cui non sia legato ad atomi più elettronegativi come negli idruri (es NaH, CaH2 , NaBH4 ) in cui il numero diossidazione è sempre -1. • il numero di ossidazione degli elementi del primo gruppo (Li, Na, K, Rb, Cs, Fr) è sempre +1 salvo quando si trovano allo stato elementare. M. Rustici, Elementi di Chimica Numeri di ossidazioni, nomenclatura e reazioni chimiche 65 • il numero di ossidazione degli elementi alcalino terrosi (Be, Mg, Ca, Sr, Ba, Ra) è sempre +2 salvo quando si trovano allo stato elementare. Sulla base delle regole spraesposte risulta particolarmente semplice calcolare i numeri di ossidazione degli elementi in un composto tenendo, tuttavia, ben presente che dovrà a sua volta valere la regola che la somma dei numeri di ossidazione in un composto sarà uguale a 0 se il composto è neutro e sarà uguale alla carica dello ione se il composto è uno ione. Supponiamo si voglia calcolare il numero di ossidazione dell’azoto nella molecola dell’acido nitrico HNO3 . Ricordando che l’idrogeno ha sempre numero di ossidazione +1 (eccetto che quando si trova allo stato naturale e negli idruri) e l’ossigeno ha sempre -2 (eccetto il caso in cui non sia allo stato elementare o sotto forma di perossido) allora se indichiamo con x il numero di ossidazione dell’azoto e applicando la regola sopraesposta possiamo scrivere 1 + x + 3 · (−2) = 0 ∴ x = +5 il numero di ossidazione dell’azoto nell’acido nitrico sarà allora +5. Supponaimo invece che si voglia calcolare il numero di ossidazione dello S nello ione solfato (SO2− 4 ) allora x + 4 · (−2) = −2 ∴ x = +6 il numero di ossidazione dello S nello ione solfato sarà allora +6. 6.2 Nomenclatura tradizionale Ossidi e anidridi Gli ossidi sono composti binari che l’ossigeno forma con quasi tutti gli elementi chimici. Le proprietà degli ossidi sono ovviamente molto diverse a secondo del gruppo di elementi con i quali l’ossigeno forma il composto binario. Tradizionalmente questa differenza veniva, in passato, messa in evidenza, quando l’ossigeno formava composti binari con i non metalli (es C, N, P, As, S, Cl, Br, I) chiamando questi composti anidridi. Oggi si tende a non usare molto questa dizione, tuttavia nel linguaggio usuale si continua ad utilizzare tale distinzione. Tutti gli altri composti binari, costituiti invece da metallo ed ossigeno si chiamano ossidi sia nella nomenclatura IUPAC che in quella tradizionale. Una delle caratteristica principale degli ossidi è quella di avere proprietà, come meglio vedremo in seguito, basiche o alcaline mentre quella delle anidridi di avere proprietà acide. Inoltre nelle anidridi il legame è covalente e negli ossdi ionico. M. Rustici, Elementi di Chimica 66 Numeri di ossidazioni, nomenclatura e reazioni chimiche Quando non sussiste ambiguità nei numeri di ossidazione, nel senso che il metallo possiede, oltre al numero di ossidazione 0, un solo numero di ossidazione, il composto binario si chiama semplicemente ossido. Ad esempio se vogliamo costruire il composto binario sodio-ossigeno, avendo il primo numero di ossidazione +1 e l’ossigeno numero di ossidazione +2, la formula, affinché sia elettricamente neutra (in altre parole la somma dei numeri di ossidazione sia pari a zero) dovrà essere scritta come Na2 O e prenderà semplicemente il nome di ossido di sodio. Analogamente il composto binario calcio-ossigeno potrà solo essere scritto come CaO e prenderà il nome di ossido di calcio. La situazione si complica leggermente, quando il numero di ossidazione del metallo può assumere, ad esempio, oltre allo 0, due numeri di ossidazione. Il ferro ad esempio possiede i numeri di ossidazione 0, +2 e + 3, di conseguenza per rispettare la regola per la quale la somma dei numeri di ossidazione dei rispettivi elementi nel composto sia nulla possiamo scrivere i due seguenti ossidi FeO e Fe2 O3 . rispettivamente per il numero di ossidazione +2 e +3. In questo caso l’ossido associato al numero di ossidazione più basso prende il suffisso oso mentre quello associato al suffisso più alto prende il suffisso ico. I due composti si chiameranno pertanto ossido ferroso e ossido ferrico. I due principali stati di ossidazione del rame sono +1 e +2 di conseguenza avremo l’ossido rameoso Cu2 O e l’ossido rameico CuO. In modo del tutto analogo possiamo seguiremo le stesse regole, appena descritte, per rappresentare i composti binari non metallo-ossigeno che nella nomenclatura d’uso prendono il nome di anidridi. Nei composti binari zolfo-ossigeno, lo zolfo presenta i numeri di ossidazione +4 e +6. Rispettivamente le formule SO2 e SO3 soddisfano il criterio per cui la somma dei numeri di ossidazione degli elementi costituenti la molecola è nulla, nomineremo,allora, le molecole anidride solforosa e anidride solforica. Nei composti binari cloro-ossigeno il cloro può assumere i numeri di ossidazione +1, +3, +5, + 7. In questo caso i composti associati allo stato +3 e +5 prenderanno rispettivamente il suffisso oso e ico, quelli associati ai numeri di ossidazione +1 e +7 prenderanno rispettivamente il prefisso ipo e per. Allora i rispettivi composti Cl2 O, Cl2 O3 , Cl2 O5 , Cl2 O7 prenderanno rispettivamente il nome anidride ipoclorosa, anidride clorosa, anidride clorica, anidride perclorica. Il carbonio con l’ossigeno mostra in genere i numeri di ossidazione +2 e +4. In questo caso la molecola CO2 che corrisponde al carbonio con numero di ossidazione +4, si chiama semplicemente anidride carbonica o biossido di carbonio, mentre quello con +2 prende il nome di ossido di carbonio o monossido di carbonio. Idrossidi Gli idrossidi o basi, tradizionalmente, si fanno derivare dalla reazione di un ossido con acqua M. Rustici, Elementi di Chimica Numeri di ossidazioni, nomenclatura e reazioni chimiche 67 Ossido + H2 O → Idrossido e sono caratterizzate dalla generica formula M(OH)m dove M è il metallo e m è il numero di ossidazione del metallo. Il gruppo OH è noto come gruppo idrossile o idrossido. In generale se l’idrossido è solubile in acqua esso si trova dissociato, come vedremo meglio in seguito, in ione OH− e ione Mm+ . Formalmente le reazioni per la formazione degli idrossidi possono essere descritte nel seguente modo Na2 O + H2 O → 2NaOH CaO + H2 O → Ca(OH)2 FeO + H2 O → Fe(OH)2 Fe2 O3 + 3H2 O → 2Fe(OH)3 formazione idrossido di sodio formazione idrossido di calcio formazione idrossido ferroso formazione idrossido ferrico Le reazioni indicate vengono utilizzate per la costruzione formale dell’idrossido. La reazione di idrolisi può essere veloce, lentissima o non avvenire affatto. L’idrossido può originarsi anche per una via diversa da quella indicata tuttavia noi possiamo derivarlo formalmente dallo schema sopra riportato. Le reazioni sono state bilanciate in modo da rispettare che le masse a destra siano identiche a quelle a sinistra. Per non commettere errori nel bilanciamento conviene bilanciare prima il metallo, poi l’idrogeno o l’ossigeno. Il nome dell’idrossido deriva, come si evince dalla tavola direttamente dal nome dell’anidride, dal quale formalmente deriva. Ossiacidi Un ossiacido può essere formalmente derivato dalla reazione di idrolisi di un anidride con acqua. Anche in questo caso, analogamente al caso degli idrossidi scriviamo una generica reazione dalla quale possiamo immaginare di derivare l’acido indipendentemente dal fatto che la reazione possa o meno avvenire. Lo schema generale è riassumibile nella reazione Anidride + H2 O → Ossiacido La formula generale dell’ossiacido è schematizzabile con la formula Hn MOm , dove M è il non metallo n è il numero di atomi di idrogeno e m il numero di atomi di ossigeno presenti nella molecola. Anche in questo caso, come in quello relativo agli idrossidi, l’idrogeno è sempre direttamente legato all’atomo di ossigeno. La separazione degli atomi di idrogeno rispetto agli atomi di ossigeno indica che tali sostanze in acqua tendono, come vedremo più dettagliatamente in seguito, a dissociarsi generando ioni H+ e, nel caso in M. Rustici, Elementi di Chimica 68 Numeri di ossidazioni, nomenclatura e reazioni chimiche (n−1)− (n−2)− cui n fosse uguale a 3, ioni MOn− , H2 MOm come ad esemm , HMOm pio negli acidi triprotrici in cui l’acido ortofosforico ne è un rappresentante H3 PO4 . prendiamo allora come primo esempio la reazione di produzione dell’acido a partire dall’anidride solforica per trattamento con acqua SO3 + H2 O → H2 SO4 tale acido proveniendo dall’anidride solforica prende di conseguenza il nome di acido solforico, nel caso fossimo partiti dall’anidride solforosa SO2 + H2 O → H2 SO3 l’acido derivato sarà l’acido solforoso. In generale dato una generica anidride schematizzata come Mx Oy possiamo arrivare alla formula dell’acido mediante uno schema del tipo Mx Oy + H2 O → Hx+2 My Oy+1 e nel comune caso in cui tutto x+2, e y+1 fossero divisibili per y scriviamo direttamente Mx Oy + H2 O → 2H(x+2)/y MO(y+1)/y ovviamente questo è solo uno schema che può essere utilizzabile per memorizzare le formule comuni degli acidi. Ad esempio consideriamo l’idrolisi dell’anidride nitrosa e dell’anidride nitrica. Avremo in questo caso N2 O3 + H2 O → [H2 N2 O4 ] ≡ 2HNO2 N2 O5 + H2 O → [H2 N2 O6 ] ≡ 2HNO3 le specie tra parentesi quadra non esistono e pertanto si devono omettere e scrivere correttamente N2 O3 + H2 O → 2HNO2 N2 O5 + H2 O → 2HNO3 M. Rustici, Elementi di Chimica Numeri di ossidazioni, nomenclatura e reazioni chimiche 69 i composti ottenuti si chiameranno ovviamente acido nitroso e acido nitrico. In modo del tutto analogo possiamo ad esempio derivare gli ossiacidi che si originano dalle anidridi del gruppo degli alogeni. Nel caso del cloro, ad esempio, possiamo ottenere l’acido ipocloroso HClO, l’acido cloroso HClO2 , l’acido clorico HClO3 e infine l’acido perclorico HClO4 . Non tutte le formule degli acidi sono derivabili da questo semplice schema mnemonico ad esempio le anidride fosforica (P2 O5 ) attraverso il meccanismo appena descritto genera l’acido meta fosforico P2 O5 + H2 O → [H2 P2 O6 ] ≡ 2HPO3 Tuttavia l’acido più comune è l’acido ortofosforico che può essere derivato per idratazione dell’anidride fosforica con 3 molecole di acqua P2 O5 + 3H2 O → [H6 P2 O8 ] ≡ 2H3 PO4 mentre per idratazione se la stessa anidride si idrata con due molecole di acqua si ottiene l’acido pirofosforico P2 O5 + 2H2 O → H4 P2 O7 L’anidride fosforica genera pertanto tre tipi diversi di acido in cui il fosforo mantiene lo stesso numero di ossidazione (+5). Questi composti prendono il nome rispettivamente di acido meta fosforico, acido pirofosforico e acido ortofosforico. Il prefisso orto viene utilizzato per i composti contenenti il maggior numero di gruppi OH per non metallo e il suffisso meta per i composti contenenti il minor numero di gruppi OH per non metallo. Ovviamente tutti e tre mantengono il suffisso ico in quanto sono associati allo stato di ossidazione maggiore (+5). Partendo dall’anidride fosforosa (P2 O3 ), possiamo derivare in modo analogo l’acido metafosforoso HPO2 e l’acido ortofosforoso H3 PO3 . Lo stesso discorso vale per i derivati dell’arsenico. É necessario precisare che le regole che indicate non indicano se la reazione realmente avviene o se il composto indicato esista nella realtà ma ci forniscono solo le regole per la costruzione di ipotetiche formule. Spesso può capitare, ad esempio, che l’acido non esista ma possono invece esistere i suoi derivati. Ad esempio possiamo immaginare di applicare la stessa regola per quanto concerne l’anidride carbonica CO2 + H2 O → H2 CO3 M. Rustici, Elementi di Chimica 70 Numeri di ossidazioni, nomenclatura e reazioni chimiche l’acido in questione prende il nome di acido carbonico, tuttavia quest’acido non esiste ma esistono i suoi sali quali quelli derivati dagli ioni HCO− 3 o 2− CO3 . Idracidi Gli idracidi sono composti binari generati da un non metallo e dall’idrogeno e come gli ossiacidini hanno la caratteristica principale di dissociarsi in acqua sotto forma di ione H+ e anione corrispondente. Gli idracidi più comuni sono quelli derivati del VII gruppo HF, HCl, HBr e HI che prendono il nome, rispettivamente di acido fluoridrico, acido cloridrico, acido bromidrico e acido iodidrico. Gli idracidi derivanti dal VI gruppo H2 S, H2 Se e H2 Te che prendono il nome di acido solfidrico, selenidrico e tellurico. Sali I sali sono composti cristallini derivati da un anione di un ossiacido o di un idracido con un catione. La formula deve essere scritta in modo da rispettare sempre la sua elettroneutralità e conseguentemente la somma dei numeri di ossidazione dei rispettivi atomi deve essere uguale a 0. Formalmente possono essere derivati dalla reazione di un acido con una base. Acido + Idrossido → Sale + H2 O I sali che derivano da un idracido prendono il suffisso uro. Consideriamo la reazione HCl + NaOH → NaCl + H2 O Il sale derivato costituito dagli ioni Na+ e Cl− prenderà il nome cloruro di sodio e lo ione Cl− si chiamerà direttamente ione cloruro. Supponiamo ora di derivare il sale partendo sempre dall’acido cloridrico e trattandolo rispettivamente con idrossido ferroso e successivamente con idrossido ferrico. Le reazioni saranno 2HCl + Fe(OH)2 → FeCl2 + 2H2 O 3HCl + Fe(OH)3 → FeCl3 + 3H2 O Chiameremo il composto FeCl2 cloruro ferroso, mentre il composto FeCl3 cloruro ferrico. Il primo sale è costituito dagli ioni cloruro Cl− e dagli ioni ferroso Fe2+ , e il secondo sale è costituito dagli ioni cloruro Cl− e dagli ioni ferrico Fe3+ . Nel caso in cui volessimo derivare i sali provenienti, ad esempio, da un acido diprotico come l’acido solfidrico, dobbiamo tener presente che è possibile M. Rustici, Elementi di Chimica Numeri di ossidazioni, nomenclatura e reazioni chimiche 71 generare due diversi tipi di sali uno derivante dallo ione S2− e l’altro derivante dallo ione HS− . Il primo ione prende il nome di ione solfuro, mentre il secondo prende il nome di idrogeno solfuro o (ione bisolfuro). Nel caso volessimo derivare i due rispettivi sali sodici le reazioni saranno H2 S + 2NaOH → Na2 S + 2H2 O H2 S + NaOH → NaHS + H2 O avremo cosı̀ il sale solfuro di sodio (Na2 S) e l’idrogeno solfuro (o bisolfuro) di sodio (NaHS). I sali derivanti dagli ossiacidi seguono ovviamente gli stessi schemi. Dobbiamo comunque tener presente che in questo caso il nome del sale prende il suffisso ito quando deriva da acidi con il suffisso oso, mentre il suffisso ato quando deriva dagli acidi con suffisso ico. Partendo ad esempio dagli acidi nitroso e nitrico per l’ottenimento del sale sodico possiamo scrivere HNO2 + NaOH → NaNO2 + H2 O HNO3 + NaOH → NaNO3 + H2 O I due sali si chiameranno rispettivamente nitrito di sodio (NaNO2 ) e nitrato di sodio (NaNO3 ). Nel caso volessimo formare, ad esempio sali dell’acido nitrico con lo ione rameoso Cu+ o con lo ione rameico Cu2+ le reazioni possibili potrebbero essere HNO3 + Cu(OH) → CuNO3 + H2 O 2HNO3 + Cu(OH)2 → Cu (NO3 )2 + 2H2 O i rispettivi sali si chiameranno nitrato rameoso (CuNO3 ) e nitrato rameico (Cu (NO3 )2 ) Per un acido biprotico come l’acido carbonico i possibili sali che possiamo 2− derivare sono quelli associati agli ioni HCO− 3 e CO3 che prendono rispettivamente il nome di ione idrogeno carbonato (o bicarbonato), carbonato. Per un acido triprotico come l’acido ortofosforico sarà possibile costruire i 2− − sali con i seguenti anioni PO3− 4 , HPO4 , H2 PO3 i cuoi nomi saranno riM. Rustici, Elementi di Chimica 72 Numeri di ossidazioni, nomenclatura e reazioni chimiche spettivamente ione ortofosfato, ione idrogeno ortofosfato, e ione diidrogeno ortofosfato. La seguente tabella mostra qualche esempio di sale Na3 PO4 Na2 HPO4 Fe2 (HPO4 )3 NaH2 PO4 Co (HCO3 )3 K2 Cr2 O7 K2 CrO4 KMnO4 ortofosfato di sodio ortofosfato acido di sodio ortofosfato acido ferrico ortofosfato biacido di sodio Carbonato acido cobaltico bicromato di potassio cromato di potassio permanganato di potassio Idruri Gli Idruri sono composti binari formati da quasi tutti gli elementi con l’idrogeno. Questi composti presentano caratteristiche molto differenti a seconda che l’idrogeno sia legato ai metalli o non metalli. Quando l’idrogeno è legato ai non metalli ci troviamo in realtà con i composti che abbiamo già analizzato e che abbiamo indicato come idracidi. Quando viceversa l’idrogeno è legato con i metalli del I e II gruppo l’idruro è un composto ionico in cui l’idrogeno ha numero di ossidazione -1. Gli idruri propriamente detti anche secondo la nomenclatura IUPAC sono solo quelli in cui l’idrogeno ha numero di ossidazione (-1). Il composto KH prende il nome di idruro di potassio invece il composto HCl, come abbiamo visto prende il nome di acido cloridrico o cloruro di idrogeno nella nomenclatura IUPAC. Gli idruri metallici in acqua sviluppano idrogeno ad esempio per l’idruro di potassio abbiamo KH + H2 O → H2 + KOH 6.3 Nomenclatura IUPAC Per razionalizzare la nomenclatura ed eliminare i tanti casi particolari associati alla nomenclatura tradizionale l’ International Union of Pure and Applied Chemistry (IUPAC) suggerisce di utilizzare delle regole per le quali sia possibile che una certa formula e un certo nome siano comprensibili in tutto il mondo. Tuttavia come abbiamo osservato i nomi tradizionali vengo tuttora utilizzati non solo nella pratica comune ma anche nei prodotti commerciali. Composti Binari Il composto binario formato da un non metallo e un metallo si scrive in modo che l’elemento con minore elettronegatività sia scritto per primo (con qualche eccezione come i composti del carbonio e idrogeno e i composti dell’azoto e idrogeno. La IUPAC analogamente alla nomenclatura M. Rustici, Elementi di Chimica 73 Numeri di ossidazioni, nomenclatura e reazioni chimiche tradizionale suggerisce di mettere il suffisso uro alla radice del nome seguito dal nome del metallo inalterato. Ad esempio il composto KF si chiamerà floururo di Litio. Anche in questo caso analogamente alla nomenclatura tradizionale i composti binari tra metallo ed ossigeno quando quest’ultimo ha numero di ossidazione -2 si chiamano ossidi e perossidi quelli in cui l’ossigeno ha numero di ossidazione -1. Quando ci troviamo di fronte a metalli che possono avere più di un numero di ossidazione come ad esempio il Fe che può trovarsi negli stati di ossidazione +2 e +3 per evitare ambiguità la IUPAC suggerisce di adoperare i prefisssi mono, bi, tri, tetra ecc., a secondo del numero di atomi legati all’elemento. Supponiamo, ad esempio, che si voglia definire il nome dei seguenti composti FeCl3 , Fe2 O3 , P4 O10 allora sulla base della definizione data chiameremo questi composti rispettivamente tricloruro di ferro, triossido di diferro, decaossido di tetrafosforo. In alternativa si può usare la notazione di Stock che consiste nell’indicare il numero di ossidazione tra parentesi in numeri romani. Secondo questa notazione i composti prima citati si chiameranno rispettivamente cloruro di ferro (III), ossido di Ferro (III) e ossido di fosforo (V). Formule NaCl NH3 PH3 HI CO2 N2 O SO3 N2 O3 Cl2 O3 Cu2 O IUPAC cloruro di sodio triidruro di azoto, idruro di azoto (III) triidruro di fosforo, idruro di fosforo (III) bromuro di idrogeno, biossido di carbonio, ossido di diazoto triossido di zolfo triossido di diazoto triossido di dicloro, ossido di cloro (III) ossido di rame, ossido di cloro (I) tradizionale ammoniaca fosfina acido iodidrico anidride carbonica protossido di azoto anidride solforica anidride nitrosa anidride clorosa ossido rameoso sali e ioni La IUPAC suggerisce di chiamare i cationi monoatomici come ad esempio Na+ o ione Li+ semplicemente come ione sodio o ione litio. Per ionio che posseggono più di uno stato di ossidazione viene consigliata la notazione Stock. Pertanto gli ioni Mn2+ , Cu+ , Cr+ si chiameranno ione manganese (II), ione rame (I) e ione Cromo (III). Per quanto riguarda i cationi poliatomici le regole IUPAC suggeriscono di utilizzare il suffisso onio. La seguente tabella indica i composti cationici poliatomici più comuni. M. Rustici, Elementi di Chimica 74 Numeri di ossidazioni, nomenclatura e reazioni chimiche Formule NH+ 4 PH+ 4 SH+ 3 H3 O+ H3 Se+ IUPAC ammonio fosfonio solfonio ossonio o idroossonio selenonio per gli anioni monoatomici la nomenclatura è identica a quella tradizionale. Lo ione prende semplicemente il suffisso uro. Ad esempio ione cloruro, ione floururo, l’unica eccezione riguarda lo ione O2− che prende il nome di ione − 2− 2− ossido. Per gli anioni poliatomici come NO− 3 , NO2 , SO3 , SO4 . La IUPAC raccomanda di mettere il suffisso ato alla radice del nome preceduto dal nome ione, indicando inoltre il numero di ossidazione secondo la nomenclatura Stock. Gli anioni descritti si chiameranno rispettivamente ione nitrato (III) o ione diossinitrato, ione solfato (III) o ione triossisolfato, ione solfato (VI) o ione tetrossisolfato. Le stesse regole appena espste riguardano anche i sali. La tabella rappresenta alcuni nomi nella nomenclatura IUPAC. Formule Na3 PO4 Na2 HPO4 Fe2 (HPO4 )3 NaH2 PO4 Co (HCO3 )3 K2 Cr2 O7 K2 CrO4 KMnO4 IUPAC tetroossifosfato di sodio tetrossifosfato acido di sodio tetrossofosfato acido di ferro (III) tetrossifosfato biacido di sodio triossicarbonato acido di cobalto (III) eptaossidicromato di potassio tetraossicromato di potassio tetraossimanganato di potassio Acidi Gi acidi assumono lo stesso nome che assumono i sali a parte il fatto che al posto del catione metallico c’è l’idroveno. Ad esempio il comune acido solforico H2 SO4 si chiamerà tetraossisolfato di diidrogeno o analogamente solfato (IV) di diidrogeno.L’acido solforoso H2 SO3 si chiamerà triossisolfato di diidrogeno o solfato (IV) di diidrogeno. 6.4 Reazioni di ossido riduzione Le reazioni di ossido riduzione sono quelle reazioni in cui alcuni degli elementi, nei rispettivi composti, che reagiscono cambiano il proprio numero o stato di ossidazione In particolare si dice che un elemento si riduce quando il suo numero di ossidazione diminuisce mentre un elemento si ossida quando il numero di ossidazione aumenta. In altre parole un elemento si riduce quando acquista elettroni M. Rustici, Elementi di Chimica Numeri di ossidazioni, nomenclatura e reazioni chimiche 75 e si ossida se perde elettroni. Supponiamo si voglia prendere in considerazione la seguente reazione in cui lo ione permanganato (MnO− 4 ) ossida lo ione ferroso 2+ 3+ (Fe ) a ione ferrico (Fe ) riducendosi a ione manganoso (Mn2+ ). Possiamo scrivere la reazione, da bilanciare, nella forma seguente 2+ MnO− → Mn2+ + Fe3+ 4 + Fe (6.1) dove il manganese nello ione permanganato avrà numero di ossidazione -7, per gli altri ioni la carica formale coincide con quella reale e pertanto con il numero di ossidazione. Il bilanciamento della reazione le seguenti regole • bilanciamento elettronico • bilanciamento di carica • bilanciamento di massa Si osserva che nella reazione 10.13 il manganese passa da +7 a +2 in altre parole si riduce acquistando 5 elettroni. Il ferro viceversa si ossida cedendo un elettrone. Possiamo allora bilanciare gli elettroni moltiplecando ogni atomo di ferro per 5. Otteniamo cosı̀ 2+ MnO− → Mn2+ + 5Fe3+ 4 + 5Fe (6.2) Tenendo presente che la reazione avviene in ambiente acido possiamo usare i protoni (H+ ) per bilanciare le cariche. Osserviamo che a sinistra ci sono 9 cariche positive mentre a destra ci sono 17 cariche positive allora sarà necessario aggiungere a sinistra 8 protoni. in altre parole avremo che 2+ MnO− + 8H+ → Mn2+ + 5Fe3+ 4 + 5Fe (6.3) Possiamo a questo punto completare il bilanciamento delle masse, ciò può essere fatto aggiungendo a destra un numero di molecole di acqua sufficienti a bilanciare gli atomi di idrogeno e di ossigeno in eccesso alla sinistra della reazione. Aggiungendo cosı̀ a destra 4 molecole di acqua otterremo la 10.12 2+ MnO− + 8H+ → Mn2+ + 5Fe3+ + 4H2 O 4 + 5Fe Supponiamo ora di considerare l’ossidazione in ambiente acido dell’acqua ossigenata ad ossigeno da parte del bicromato di potassio come è deducibile dalla tabella 10.3. M. Rustici, Elementi di Chimica 76 Numeri di ossidazioni, nomenclatura e reazioni chimiche 3+ Cr2 O2− + O2 7 + H2 O2 → Cr Nell’acqua ossigenata ogni atomo di ossigeno (essendo tra loro legati) ha numero di ossidazione -1, Il Cr invece nello ione bicromato ha numero di ossidazione + 6 siamo infatti in presenza di due atomi di cromo. Ogni atomo di cromo passa pertanto da + 6 a + 3 acquistando (cioè riducendosi) in totale 6 elettroni. Dovremmo pertanto moltiplicare l’acqua ossigenata e l’ossigeno molecolare per 6. Ogni atomi di ossigeno, nell’acqua ossigenata, perde un elettrone ossidandosi si dovrebbe allora moltiplicare gli ioni contenenti il Cr per 2. Essendo però 6 divisibile per 2 è sufficiente moltiplicare gli ioni contenenti Cr per 1 e quelli contenenti O per 3 fermo restando che lo ione Cr3+ deve essere il doppio dello ione bicromato. Allora avremo 3+ Cr2 O2− + 3O2 7 + 3H2 O2 → 2Cr dato che siamo in ambiente acido possiamo usare i protoni per il bilanciamento di carica. Essendo le cariche a sinistra della reazione -2 e quelle a destra +6 dobbiamo aggiungere a sinistra della reazione 8 protoni, cioè Cr2 O72− + 3H2 O2 + 8H+ → 2Cr3+ + 3O2 basterà allora aggiungere a destra della reazione 7 molecole di acqua per bilanciare le masse 3+ + Cr2 O2− + 3O2 + 7H2 O 7 + 3H2 O2 + 8H → 2Cr Nel caso che le reazioni dovessero avvenire in ambiente alcalino il bilancio di carica viene effettuato mediante l’aggiunta di ioni ossidrili a destra o a sinistra della reazione. M. Rustici, Elementi di Chimica Capitolo 7 Stati di aggregazione della materia 7.1 Stati di aggregazione della materia Gli stati di aggregazione della materia sono lo stato gassoso, liquido e solido. Uno stato di aggregazione è caratterizzato da un’unica fase cioè da una regione omogenea in cui le proprietà chimico fisiche del sistema sono costanti. Lo stato di aggregazione o la fase della materia è definito dalla somma di due forze che agiscono in modo opposto. Queste due forze hanno origine nelle forze intermolecolari e nell’energia cinetica delle molecole o atomi. Come è noto è possibile passare da uno stato della materia all’altro fornendo calore al sistema. Essendo il calore un flusso di energia che esiste in virtù di un gradiente termico tale flusso provoca la variazione della temperatura del sistema e pertanto aumenta (quando la temperatura aumenta) l’energia cinetica delle molecole. È ovvio che se l’energia cinetica prevale sull’attrazione molecolare avremo lo stato solido se vale il viceversa avremo lo stato gassoso. La situazione intermedia possiamo classificarla come stato liquido. Ovviamente si tratta di una rozza spiegazione ma nonostante tutto dà una prima indicazione dell’esistenza degli stati della materia. Un fenomeno importante che possiamo osservare è che durante una transizione di fase la temperatura del sistema rimane costante. Durante tale periodo siamo in presenza di due fasi in equilibrio tra loro e l’energia fornita al sistema serve, non per aumentare l’energia cinetica delle molecole, ma per assorbire il calore latente associato alla transizione di fase. La temperatura inizierà nuovamente a salire quando sarà scomparsa una delle due fasi. Consideriamo ad esempio il diagramma di stato dell’acqua (figura 7.1). Possiamo vedere che lo stato di aggregazione dell’acqua dipende dalla pressione e della temperatura e al variare di questi due parametri si può passare da uno stato all’altro. Le linee di separazione tra le fasi indicano gli stati in cui due fasi sono in equilibrio tra di loro. Ogni punto lungo la curva rappresenta la temperatura e la M. Rustici, Chimica di base 78 Stati di aggregazione della materia Figura 7.1. pressione in cui le due fasi coesistono in equilibrio. Il punto di intersezione delle tre curve si chiama punto critico e indica quella particolare situazione in cui le tre fasi sono in equilibrio tra di loro. 7.1.1 Regola delle fasi Un importante regola che aiuta a comprendere meglio gli equilibri di fase è la regola delle fasi f =c−p+2 dove c è il numero dei componenti indipendenti p è il numero della fasi presenti nel sistema e f rappresenta il numero dei gradi di libertà del sistema. f esprime il numero delle variabili (volume, pressione e concentrazione) che possono essere variate indipendentemente senza variare il numero delle fasi in equilibrio. 7.1.2 Forze intermolecolari Come abbiamo detto la natura delle fasi della materia è principalmente dovuta alle forze che si esercitano tra le molecole (forze intermolecolari). Queste forze sono molto più deboli delle forze intermolecolari ma a sua volta sono abbastanza M. Rustici, Chimica di base Stati di aggregazione della materia 79 Figura 7.2. forti da spiegare le fasi di aggregazione della materia. Queste forze possono essere suddivise in base alla loro forza ione-dipolo Quando uno ione e una molecola polare vicina si attraggono mutuamente, si origina una forza ione-dipolo. Un importante esempio si manifesta ad esempio quando un sale si scioglie in acqua. Gli ioni si separano perché le attrazioni tra gli ioni e i poli opposti delle molecole vincono le attrazioni tra gli ioni stessi. dipolo-dipolo Quando le molecole polari sono vicine l’una all’altra, come nei liquidi e nei solidi le loro cariche parziali agisono da minuscoli campi elettrici e danno origine a forze dipolo-dipolo. legame ad idrogeno Le forze dipolo-dipolo non sono sufficienti a spiegare il comportamento di certo liquidi. Ad esempio se confrontiamo i punti di ebollizione di sostanze analoghe si possono trovare delle anomalie. In generale si osserva che il punto di ebollizione aumenta con l’aumentare del peso molecolare, tuttavia se noi proviamo a confrontare i punti di ebollizioni di sostanze come H2 O, H2 S, H2 Se, H2 Te dovremmo aspettarci, dato che i pesi atomici degli elementi del VI gruppo sono in ordine crescente Te>Se>S>O, che il punto di ebollizione cresca scendendo nella tavola periodica (figura 7.2). Questo non accade, anzi, il punto di ebollizione dell’acqua come è noto è M. Rustici, Chimica di base 80 Stati di aggregazione della materia Figura 7.3. di 1000 C e quello dell’acido solfidrico è intorno a -700 C. In questo caso e in tutti gli altri casi si parla allora del legame ad idrogeno. Questo particolare tipo di legame si origina tra molecole che hanno un atomo di H legato ad un atomo di piccole dimensioni, fortemente elettronegativo, con coppie di elettroni solitarie. La figura 7.3 mette in evidenza il legame a idrogeno nel caso di due molecole di acqua. carica-dipolo indotto Le nuvole elettroniche di legame o di non legame non sono fisse ma sono sempre in continuo movimento. Questo implica che si possano originare dei dipoli istantanei che a sua volta possono indurre la formazione di dipoli. La facilità con cui una nuvola elettronica può essere distorta è detta polarizzabilità. Questa proprietà aumenta con le dimensioni atomiche o molecolari. forze di London Nel caso di molecole apolari possiamo chiederci in che modo queste sostanze possono liquefarsi o solidificare. Nel caso di sostanze apolari la principale forza che è responsabile dei fenomeni di condensazione è nota come forza di dispersione o forza di London. Le forze di dispersione sono causate da oscillazioni momentanea della carica elettronica. In ogni istante la carica può non essere distribuita uniformemente e cosı̀ si vengono a generare dei dipoli istantanei, capace a sua volta di influenzare gli atomi vicini inducendo negli atomi vicini un dipolo indotto. Le forze di dispersione sono allora forze istantanee dipolo-dipolo indotto. Queste forze sono deboli ma si esercitano in qualsiasi tipo di particella. M. Rustici, Chimica di base Stati di aggregazione della materia 7.2 81 Stato gassoso Il concetto di gas ideale acquisterà un significato sempre più chiaro a mano a mano che si procederà nel corso del libro. Vogliamo comunque introdurre inizialmente il concetto del gas ideale per mezzo di una definizione microscopica. 1. Un gas è costituito da un numero enorme di molecole o atomi che saranno dell’ordine del numero di Avogadro. 2. Le molecole di un gas ideale vengono considerate come particelle puntiformi rigide, impenetrabili, indeformabili, e che si muovono seguendo traiettorie casuali. 3. Le molecole di un gas ideale non esercitano né forze attrattive né forze repulsive sulle altre molecole. 4. Gli urti che tali particelle effettuano contro le pareti del recipiente sono perfettamente elastici. 5. In assenza di forze esterne le molecole sono uniformemente distribuite e la densità molecolare è costante. 6. La velocità di una molecola non ha direzioni privilegiate e il suo modulo sarà distribuito su un intervallo di velocità. Da un punto di vista macroscopico è necessario invece, per poter definire lo stato e le sue proprietà di un gas, definire due concetti fondamentali che stanno alla base di tutta la termodinamica: temperatura e pressione. La temperatura può essere definita macroscopicamente facendo uso del concetto di equilibrio termico. Consideriamo un sistema descritto dalle coordinate macroscopiche X e Y . Si chiama equilibrio quello stato in cui X e Y assumono determinati valori e non cambiano nel tempo. Supponiamo di avere un sistema A ed un sistema B in equilibrio caratterizzati rispettivamente dalle coordinate X, Y e X 0 , Y 0 , separati da una parete adiabatica. Sostituiamo la parete adiabatica con una parete conduttrice; osserveremo allora che i valori X, Y, X 0 , Y 0 , cambieranno spontaneamente fino a che non si raggiungerà uno stato di equilibrio del sistema. Si dice allora che i due corpi sono in equilibrio termico. In particolare se due sistemi sono entrambi in equilibrio termico con un terzo allora sono in equilibrio termico tra loro. Questo costituisce il principio zero della termodinamica. Chiameremo temperatura la proprietà che determina se un sistema sia o non sia in equilibrio termico con altri sistemi. Come è noto la pressione viene definita come la forza normale alla superficie sulla quale si esercita divisa per l’area della superficie medesima. Per un fluido vale il principio dell’isotropia delle pressioni, per il quale la pressione che si esercita su un punto di un fluido non varia al variare della superficie sulla quale si esercita. M. Rustici, Chimica di base 82 Stati di aggregazione della materia Gli esperimenti di Boyle, Gay-Lussac e quelli dei loro successori effettuati sui gas hanno permesso di inferire una legge, nota oggi come legge dei gas ideali, che assume la forma P V = nRT (7.1) dove R è una costante universale indipendente dal tipo di gas considerato e P, V, n e T sono rispettivamente la pressione, il volume, il numero di moli, e la temperatura. Questa equazione è una legge limite per i gas reali. 7.2.1 Legge di Dalton Per un sistema conentenente 2 o più gas la pressione totale è esprimibile come somma delle pressioni parziali X P = p1 + p2 + · · · + pc = Pi (7.2) i dove Pi sono le pressioni parziali dei singoli componenti della miscela gassosa. L’equazione 7.2 è nota come legge di Dalton dal chimico e matematico inglese John Dalton. Consideriamo un sitema a due componenti (1 e 2) a T e V costanti la pressioni dei duie gas rispettivamente potranno essere scrittre come P1 V = n1 RT ∴ P2 V = n2 RT ∴ n1 RT V n2 RT P2 = V P1 = applicando la legge di Dalton possiamo scrivere P = P1 + P2 = n1 RT n2 RT RT + = (n1 + n2 ) V V V dividendo le pressioni parzili per la pressione totale cosı̀ ottenuta avremo n1 P = x1 P n1 + n2 n2 P = x2 P P2 = n1 + n2 P1 = dove x1 e x2 sono le frazioni molari dei gas 1 e 2. La frazione molare definita come il rapporto tra le moli di un gas e le moli complessive di tutti i gas presenti, è una grandezza adimensionale. Inoltre, per definizione, la somma di tutte le frazioni molari è uguale all’unità X xi = 1 M. Rustici, Chimica di base Stati di aggregazione della materia 83 Figura 7.4. 1.2 Gas reali Il comportamento dei gas reali può facilmente essere evidenziato per mezzo del fattore di compressibilità Z definito come il rapporto tra la pressione esercitata da un gas reale e quella esercitata dallo stesso gas nelle medesime condizioni di temperatura e pressione. Per un gas ideale evidentemente Z è costante ed è uguale ad 1, mentre per un gas reale si ha uno scostamento più o meno pronunciato da tale valore. A basse pressioni i gas hanno un fattore di compressibilità vicino ad 1 e sono cosı̀ più vicini ad un gas perfetto. Ad alte pressioni tutti i gas hanno Z > 1, questo significa che i gas reali sono meno comprimibili degli ideali. A basse pressioni e a temperature non elevate Z può essere negativo. Le proprietà dei gas reali, alla luce di questi dati sperimentali, possono essere spiegate per mezzo dell’effetto contrastante di due fattori: il covolume e le forze di interazione. Il covolume rappresenta il volume proprio delle molecole - pertanto un gas occupa in realtà un volume inferiore rispetto a quello del gas ideale. Quando il fattore predominante è quest’ultimo Z risulterà maggiore di 1, viceversa quando dominano le forze di interazione Z risulterà minore dell’unità. Un’ utile equazione per la descrizione dei gas reali è l’equazione di van der Waals. L’esistenza di un volume proprio delle molecole fa sı̀ che le particelle si muovano effettivamente in un volume inferiore V − nb rispetto al volume V del recipiente, dove nb è approssimativamente il volume totale occupato dalle molecole. Questo suggerisce che la legge dei gas perfetti dovrebbe essere modificata M. Rustici, Chimica di base 84 Stati di aggregazione della materia Figura 7.5. nella seguente P (v − nb) = nRT (7.3) Le interazioni attrattive, viceversa, dovrebbero ridurre la pressione da loro esercitata e, introducendo un termine di riduzione per la pressione a(n/V )2 , l’equazione assumerà la forma ³ n ´2 nRT P = −a (7.4) V − nb V dove a/V 2 è chiamata pressione interna. Le isoterme di Andrews rappresentate in Fig. 7.5 mettono bene in evidenza le deviazioni dal comportamento ideale. Ad alte pressioni il gas segue l’isoterma di Boyle mentre a temperature più basse si osserva l’esistenza di una regione in cui al diminuire del volume non si registra nessuna variazione della pressione. In questa regione il gas in realtà non è più definibile come tale e per questo motivo viene chiamato vapore. Esiste, infatti, una temperatura detta critica, TC , sotto la quale un gas per compressione si trasforma nella fase liquida: definiamo tale gas vapore. Un aeriforme che si trova ad una temperatura inferiore alla temperatura critica, e perciò liquefa per solo compressione, viene chiamato vapore. La pressione corrispondente viene detta pressione di vapor saturo. M. Rustici, Chimica di base Stati di aggregazione della materia 85 Figura 7.6. 7.3 Stato solido Possiamo suddividere i solidi in due categorie generali sulla base del grado di ordine delle loro forme, che a sua volta si basa sul grado di ordine delle particelle che lo costituiscono. I solidi cristallini hanno generalmente una forma ben definita in quanto le particella esistono in una disposizione ordinata. I solidi amorfi hanno forme mal definite perché sono privi di un vasto ordine delle loro particelle a livello molecolare. Comunque in genere la parola solido si riferisce allo stato cristallino. Lo stato cristallino è caratterizzato dalla distribuzione ordinata e periodica della materia costituente. Tale ordine, come abbiamo detto, è riconducibile ad un ordine a lungo raggio delle molecole o atomi che lo costituiscono. In particolare gli atomi o molecole si distribuiscono, almeno in una configurazione ideale, in un reticolo cristallino. Ovviamente questo reticolo non è identico per tutti i cristalli ma dipende dalla dimensioni atomiche e molecolari. In natura si osservano 7 sistemi cristallini e 14 tipi di cella elementare, quest’ultima rappresenta la più piccola parte del cristallo che se ripetuta genera tutto il cristallo. La struttura cristallina dei metalli è la più semplice, perché gli atomi di un dato metallo hanno tutti le stesse dimensioni e sono privi di carica. Il legame metallico non è direzionale; perciò in molti cristalli, gli atomi sono disposti in modo da raggiungere l’impacchettamento più efficiente secondo tre tipi di celle elementari. In alcuni cristalli, il numero di coordinazione è 8 e la struttura è cubica a corpo centrato (Li, Na, K); più frequentemente il numero di coordinazione è 12 e si possono avere due tipi di impacchettamento: cubico compatto (a facce centrate) ed esagonale compatto (figura 7.6). Per meglio comprendere questi due tipi di organizzazione, immaginiamo di disporre delle sfere su un piano nella maniera più compatta possibile. Si ottiene uno strato in cui ogni sfera è circondata da 6 sfere. A questo si può sovrapporre un secondo strato, in modo da disporre le sfere nelle cavità del primo strato. Un terzo strato può, a questo punto, essere sovrapposto solo in due modi diversi: o in modo da ricalcare il primo strato si ottiene l’impacchettamento esagonale compatto o M. Rustici, Chimica di base 86 Stati di aggregazione della materia Figura 7.7. Figura 7.8. in modo da non ricalcare il primo strato si ottiene l’impacchettamento cubico compatto (figura 7.7). Nei solidi ionici le particelle sono costituite da ioni di carica opposta che si attraggono per azione elettrostatica. L’impacchettamento dei cristalli ionici dipende dalle dimensioni del catione e dell’anione. Nel caso del cloruro di cesio CsCl (figura 7.8) la cui cella elementare contiene gli ioni clorurio ai vertici e lo ione cesio al centro abbiamo una cella elementare con un impacchettamento cubico semplice. Nel caso invece del cloruro di sodio in cui lo ione sodio è molto più piccolo dello ione cesio il cristallo assumerà una struttura diversa. In particolare possiamo immaginare la struttura cristallina che si origina quando due disposizioni di ioni si compenetrano in modo tale che gli ioni Na+ più piccoli finiscano nei buchi tra gli ioni Cl− più grandi. Ogni ione Na+ è circondato da 6 ioni Cl− e viceversa, dove gli ioni cloruro e gli ioni sodio sono organizzati in una disposizione cubica a facce centrate (figura 7.9). I solidi covalenti invece sono organizzati secondo una struttura reticolare di tipo covalente. Le due forme comuni del carbonio elementare sono esempi di solidi covalenti reticolari, diamante e grafite. Come è noto le proprietà chimico fisiche dei due solidi sono completamente diverse e questo è direttamente legato proprio a causa della diversa struttura elementare. La grafite si presenta sotto forma di strati piani impilati da anelli esagonali di atomi di carbonio con legami σ e π. Gli strati piani interagiscono tra loro mediante forze di dispersione. La presenza di elettroni π delocalizzati su tutto il cristallo fanno sı̀ che il cristallo sia un buon conduttore di elettricità. Nel diamante invece ogni atomo di carbonio è ibridato sp3 e ogni atomo di carbonio è legato ad un altro mediante legami σ secondo una struttura tetraedrica. Il diamante cristallizza in un sistema cubico a facce M. Rustici, Chimica di base Stati di aggregazione della materia 87 Figura 7.9. centrate , in cui ciascun atomo è circondato tetraedricamente da altri quattro atomi ci carbonio in una disposizione pressoché illimitata. Legami singoli forti in tutto il cristallo fanno del diamante la sostanza più dura che si conosca. Quando elementi esistono in forme differenti a causa del modo in cui gli atomi si legano tra loro si parla di allotropia. Quando invece una stessa specie chimica, o allo stato elementare o allo stato composto, si presenta in più forme cristalline che differiscano per il tipo di impacchettamento, si parla di polimorfismo. Ad esempio il carbonato di calcio cristallizza come aragonite(sistema rombico) o calcite (sistema romboedrico). Intendiamo invece per isomorfismo il fenomeno per cui sostanze chimicamente diverse danno luogo a cristalli simili. 7.4 Stato liquido Lo stato liquido è uno stato con caratteristiche intermedie tra lo stato solido e lo stato gassoso. Questa caratteristica rende difficile la spiegazione accurata delle interazioni intermolecolari. Le principali proprietà sono enunciate qui di seguito. • hanno un volume proprio grazie alle forze coesive ma non hanno forma propria • presentano ordine a corto raggio. Le molecole si raccolgono in grappoli, l’impacchettametno non è regolare. • Hanno densità minore rispetto a quella dei solidi l’acqua è un eccezione. • non sono comprimibili • si espandono all’aumentare della temperatura a causa dell’aumento del disordine molecolare causato dall’aumento dell’energia cinetica. • diffondono in genere l’uno nell’altro • sono isotropi M. Rustici, Chimica di base 88 Stati di aggregazione della materia • la loro viscosità è legata alla dimensione molecolare e dalla forma delle molecole costituenti. • Tendono ad avere la minore area superficiale possibile. Questo fenomeno è dovuto al fatto che le molecole al centro del liquido sono esposte a forze simmetriche quelle alla superficie a forze asimmetriche. Questo genera sulla superficie del liquido la cosiddetta tensione superficiale. • bagnano la superficie in cui sono messi a contatto. 7.4.1 Viscosità la viscosità di un fluido, come un gas, un liquido o una soluzione è un indice della sua resistenza allo scorrimento. La viscosità viene determinata, in genere, facendo scorrere un fluido all’interno di un capillare allo scopo di misurare la resistenza allo scorrimento. La viscosità di una soluzione è, in genere, più elevata di quella del solvente puro. La presenza del soluto altera il normale andamento del flusso, provocando un aumento della viscosità. Questo aumento è notevole specie quando il soluto è costituito da macromolecole. La viscosità solitamente diminuisce all’aumentare della temperatura. 7.4.2 Tensione superficiale L’asimmetria che si genera tra le molecole presenti nella fase massiva rispetto a quelle superficiali, a contatto con la fase gassosa dell’aria o del recipiente che lo contiene, rende le proprietà superficiali del liquido diverse da quella massive. Questa interazione non bilanciata subita dalle molecole nello strato superficiale ha come conseguenza che il liquido tende a minimizzare la sua area superficiale (fig. 7.10). Per questo motivo una goccia di liquido adotta la forma sferica. Questa forza prende il nome di tensione superficiale del liquido che può essere definita come l’energia superficiale per unità di superficie. L’innalzamento capillare è un modo per misurare la tensione superficiale dei liquidi. Sebbene si osservi abitualmente l’innalzamento dei liquidi in un tubo capillare, questo fenomeno non ha carattere universale. Per esempio quando si immerge un tubo capillare nel mercurio liquido, il livello superiore del liquido nel tubo è in realtà più basso della superficie del liquido libero (fig.7.11). Questi due diversi comportamenti sono comprensibili considerando l’attrazione intermolecolare tra molecole simili nel liquido, detta coesione e l’attrazione tra il liquido e la parete di vetro, detta em adesione. Se l’adesione è più forte della coesione le pareti diventano bagnabili e il liquido sale lungo le pareti. Poiché l’interfaccia vapore liquido resiste allo stiramento, anche il liquido al centro della colonna si innalza. Al contrario, se la coesione è più forte dell’adesione, il liquido del capillare forma una depressione. M. Rustici, Chimica di base Stati di aggregazione della materia 89 Figura 7.10. Forze intermolecolari che agiscono su una molecola dello strato superficiale e su una molecola nella fase massiva del liquido La tensione superficiale delle soluzioni saline è in genere vicina a quella dell’acqua pura, la tensione superficiale invece può diminuire nettamente quando la sostanza disciolta è ad esempio un acido grasso. In questo caso le molecole si accumulano sulla superficie disponendosi in modo da lasciare la testa idrofilica a contatto con l’acqua e la coda idrofobica a contatto con l’aria. Come conseguenza la tensione superficiale dell’acqua diminuisce notevolmente. Tutte le sostanze che provocano una diminuzione della tensione superficiale sono tensioattivi. Tra i tensioattivi più efficiaci ci sono i saponi e le proteine denaturate. L’azione dei tensioattivi gioca un ruolo importante anche nel processo della respirazione. La superficie dei polmoni è la superficie più estesa del corpo umano in contatto con l’ambiente. Durante la normale ispirazione , la pressione negli alveoli è inferiore a quella della pressione atmosferica di circa 3 mmHg cosa che permette all’aria di fluire attraverso i vasi bronchiali. Gli alveoli sono tappezzati da un fluido che ha una tensione superficale di 0.05 N/m. Durante l’ispirazione gli alveoli si espandono, ma affinché si verifichi l’espansione la pressione deve essere almeno di circa 15 mmHg, tuttavia la pressione effettiva è solo 1/15 della pressione necessaria per l’espansione dell’alveolo. Per superare questo problema le cellule secernono la dipalmitil leucina che è un particolare tensioattivo che riducendo fortemente la tensione superficiale permette all’alveolo di espandersi senza difficoltà. Quando il tensioattivo non è presente si ha il disturbo noto come sindrome da insufficienza respiratoria del neonato, che colpisce frequentemente i neonati immaturi in cui le cellule che secernono il tensioattivo non funzionano ancora in modo adeguato. Anche nei neonati in buona salute gli alveoli sono talmente collassati alla nascita che è necessria una differenza di pressione di circa 25-30 mmHg per espanderli la prima volta. M. Rustici, Chimica di base 90 Stati di aggregazione della materia Figura 7.11. Fenomeno dell’azione capillare dell’acqua rispetto a quella del mercurio 7.5 La diffusione La diffusione è un flusso di materia che si verifica in presenza di un gradiente di concentrazione. Attraverso questo processo i gradienti di concentrazione vengono eliminati fino a che il sistema non diventa omogeneo. Ogni qual volta si manifesta una disomogeneità nella concetrazione in un liquido il sistema cerca di raggiungere l’equilibrio annullando i gradienti di concentrazione presenti nella soluzione. Il flusso di materia si arresta non appena il sistema diventa omogeneo. Il flusso risulta direttamente proporzioale al gradiente come è stato osservato per la prima volta dal fisiologo tedesco Adolf Eugen Fick. Il coefficiente di porporzionalità è noto come coefficiente di diffusione D e varia da sostanza a sostanza. Possiamo riassumere la proporzianalità attraverso la relazione J = −D ∆C ∆x (7.5) il segno meno indica che il flusso si muove dalla concentrazione più alta verso quella più bassa e la quantità ∆C/∆x è l gradiente di concentrazione. L’equazione 7.5 è nota come prima legge di Fick. M. Rustici, Chimica di base Capitolo 8 Termodinamica 8.1 termodinamica cenni La termodinamica è una disciplina che nasce dallo studio delle macchine termiche e benché possa, in apparenza, sembrare lontana dalle scienze della vita, la termodinamica permette di individuare leggi generali valide per tutti i processi che avvengono nel nostro universo, sia in quello vivente che in quello non vivente. Nessun processo può sfuggire alle leggi regolate dalla termodinamica. 8.1.1 Principio zero Il primo problema che è necessario affrontare è il concetto di equilibrio termico che si stabilisce quando due o più corpi, tra loro in contatto mediante una superficie conduttrice, mantengono costanti le loro proprietà fisiche (come ad esempio pressione, volume , densità o altro ancora). Ad esempio se immaginassimo di mettere in contatto due recipienti a volume costante mediante una parete conduttrice, contenenti n1 e n2 moli di una sostanza gassosa, noi osserveremmo che i due recipienti varierebbero la loro pressione fino a che i due recipienti non raggiungono l’equilibrio termico. Da quel punto in puoi la pressione dei due sistemi rimarrà costante. La proprietà che determina se due o più corpi sono tra loro in equilibrio termico è la temperatura (T ). Questo principio costituisce il cosiddetto principio 0 della termodinamica. 8.1.2 lavoro e calore • lavoro In meccanica classica il lavoro si definisce come il prodotto scalare di una forza F per uno spostamento r, dove la forza e lo spostamento sono quantità vettoriali. Matematicamente il prodotto possiamo indicarlo come w = F · r = F r cos θ M. Rustici, Chimica di base 92 Termodinamica dove w (il lavoro) è una quantità scalare, F e r rappresentano i rispettivi moduli delle quantità vettoriali, ed infine θ rappresenta l’angolo compreso tra il vettore forza F e il vettore spostamento r. In termodinamica spesso ci riferiamo, come sistema modello, al lavoro compiuto su un gas o compiuto da un gas. Per meglio capire possiamo immaginare semplicemente un cilindro munito di pistone contenente un gas ad una certa pressione P che si espande verso la pressione atmosferica supposta costante. Senza entrare nel dettaglio del calcolo otteniamo che in questo caso specifico il lavoro di espansione del gas è esprimibile come w = −Pest ∆V Una delle caratteristiche peculiari del lavoro è che il suo valore non dipende semplicemente dallo stato iniziale e dallo stato finale ma dipende dal modo in cui il lavoro viene ottenuto, in altre parole dal procedimento che viene impiegato per produrre lavoro. • calore Il calore è una forma di energia che esiste solo in virtù di un gradiente termico. Anche il calore, prodotto o assorbito, in un processo, analogamente al lavoro, dipende dal modo in cui avviene la trasformazione, in altre parole non dipende solo dallo stato iniziale e finale del processo. Calore e lavoro sono in stretta connessione attraverso il primo principio della termodinamica. Il quale sancisce il principio della conservazione dell’energia e mette a sua volta in evidenza l’equivalenza tra calore e lavoro. Che il lavoro meccanico producesse calore era stato assunto, sulla base di rigorose misurazioni, già nel 1798 da conte Rumford, Benjamin Thomson osservando la grande quantità di calore prodotta durante la perforazione delle canne di pezzi di artiglieria di Monaco. É interessante osservare che le prime evidenze ed osservazioni sull’equivalenza tra calore e lavoro si devono ad un medico Julius Robert Mayer il quale nel 1840 era un giovane medico di bordo che effettuava il suo servizio su una nave mercantile olandese in spedizione a Giava. Il giovane medico si trovava nella necessità di praticare salassi ad alcuni marinai per una affezione polmonare epidemica che colpı̀ l’equipaggio e nel corso dell’operazione rimase impressionato dal colore rosso vivo del sangue estratto dal primo paziente tanto da indurlo a pensare di avere erroneamente inciso un’arteria. Il colore vivo del sangue si ripresentò anche negli altri marinai, escludendo cosı̀ l’errore chirurgico. Anche un malato, indigeno, che si sottopose a sottrazioni sanguigne presentava lo stesso tipo di colorazione. Il medico intervistò gli altri medici residenti sull’isola e si sentı̀ rispondere che M. Rustici, Chimica di base 93 Termodinamica quello era il colore tipico del sangue degli abitanti ai tropici. Dopo lunghe riflessioni il Mayer intravede la spiegazione ricorrendo alla teoria enunciata da Antoine Lavoisier nel 1777, secondo cui il calore animale è il risultato di un processo di combustione. Se il calore animale è prodotto dalla ossidazione dei cibi, cosa accade quando il corpo produce nello stesso tempo anche lavoro? dalla combustione di una stessa quantità di alimenti l’organismo animale può produrre calore e lavoro in proporzioni diverse, ma la loro somma deve rimanere costante, quindi il calore e il lavoro sono grandezze della stessa natura sostituibili tra loro. Se allora il calore animale è il risultato di un processo di combustione, il diverso colore del sangue nelle arterie e nelle vene è il segno visibile delle ossidazioni che avvengono nelle arterie. Per mantenere costante la temperatura del corpo, la produzione e l’eliminazione di calore devono essere ben regolate, in relazione alla temperatura dell’ambiente. Conseguentemente, se l’ipotesi è corretta, anche la produzione di calore e i processi ossidativi dovrebbero diminuire nei paesi più caldi e il sangue venoso dovrebbe differire meno da quello arterioso. In altre parole, nei paesi con clima tropicale, il colore del sangue è più rosso perché è necessario un minor consumo di ossigeno per mantenere la temperatura corporea rispetto alle fredde terre dell’europa del nord. Le conoscenze del Mayer relative alla fisica sono tuttavia non esatte e quando invia il suo manoscritto alla famosa rivista Annalen der Physik und Chemie a causa di alcuni errori il manoscritto non viene pubblicato e solo nel 1842 riuscirà a pubblicare i dati nella rivista Annalen der Chemie und Pharmacie. Purtroppo a causa della mancanza di rigorose conferme sperimentali le idee del Mayer non destarono lo scalpore che avrebbero dovuto suscitare. Leggendo il lavoro del Mayer si osserva per la prima volta l’equivalenza tra lavoro w e calore q con la relazione w = Jq dove J rappresenta l’equivalente meccanico del calore e venne calcolato dal Mayer in 3.56 joule/caloria. Sarà il fisico inglese James Prescott Joule nel suo lavoro sull’equivalente meccanico del calore presentato alla Royal Society nel 1949 a proporre per J il valore di 4.184 joule/caloria. La formulazione teorica del primo principio nella forma UA − UB = Q − W si deve Hermann Helmholtz nel 1847 il quale dette la forma definitiva al primo principio della termodinamica. Il primo principio sancisce cosı̀ che l’energia è conservata in ogni processo che coinvolga un sistema termodinamico e il suo intorno. UA e UB rappresentano rispettivamente l’energia dello stato iniziale e finale e la variazione è nota come la variazione dell’energia interna del sistema. Tale variazione è una combinazione del calore Q aggiunto al sistema e del lavoro W fatto dal sistema. Il segno meno di fronte al lavoro indica che un ammontare positivo di lavoro fatto dal sistema conduce ad una perdita di energia del sistema stesso. In forma differenziale il primo principio si esprime nella relazione M. Rustici, Chimica di base 94 Termodinamica dU = δQ − δW Questa equazione costituisce una legge generale applicabile ad ogni sistema fisico, chimico o biologico. Ad esempio si potrebbe sfruttare per studiare l’energia prodotta o assorbita durante una reazione chimica. Supponiamo ad esempio di fare avvenire la reazione all’interno della cosiddetta bomba calorimetrica che opera a volume costante. Applicando il primo principio e introducendo nella sua equazione il lavoro idrostatico possiamo scrivere ∆U = Qv − P ∆V Essendo il volume costante ∆V = 0 e conseguentemente ∆U siidentifica con Qv , dove il Qv sta ad indicare che la trasformazione è avvenuta a volume costante. Una misura calorimetrica, del calore sviluppato ci fornisce cosı̀ la variazione di energia associata ad una reazione chimica. Consideriamo la generica reazione aA + bB = cC + dD e supponiamo di far avvenire questa reazione in una bomba calorimetrica allora la misura del calore sviluppato o assorbito non è altro che la differenza di energia tra lo stato finale costituito da cC + dD e lo stato iniziale aA + bB. 8.1.3 Entalpia In laboratorio la maggior parte dei processi fisici e chimici avvengono a pressione costante e non a volume costante. In questi casi il primo principio potrebbe essere scritto come ∆U = Qp − P ∆V e quindi U2 − U1 = Qp − P (V2 − V1 ) dove il pedice indica che il processo avviene a pressione costante. Possiamo riscrivere l’equazione nella forma Qp = (U2 + P V2 ) − (U1 − P V1 ) M. Rustici, Chimica di base 95 Termodinamica La funzione (U + P V ) dipende solo dallo stato iniziale e finale chiameremo, allora, questa nuova funzione entalpia H. In altre parole possiamo scrivere che Qp = H2 − H1 Il calore scambiato a pressione costante dipende solo dallo stato iniziale e finale e può essere utilizzato per studiare l’energia che viene assorbita o sviluppata nella maggior parte dei processi chimici o fisici che avvengono a pressione costante. Le reazioni chimiche che avvengono con sviluppo di calore (∆H < 0) si dicono esotermiche mentre quelle che avvengono mediante assorbimento si dicono esotermiche (∆H > 0). 8.2 La seconda legge della termodinamica La prima legge della termodinamica asserisce che l’energia non può essere creata né distrutta, ma fluisce da una parte dell’universo all’altra o si trasforma da una forma all’altra. La quantità totale di energia dell’universo rimane costante. Tale principio, pur avendo un enorme valore nello studio dell’energetica delle reazioni chimiche non ci permette di capire il senso della generica reazione aA + bB → cC + dD In genere quando scriviamo la reazione nella forma soprascritta intendiamo dire che A e B si trasformano per dare C e D. Tuttavia non siamo in grado, utilizzando il primo principio di capire il perché della direzione indicata. Per avere una risposta a questa domanda dobbiamo riferirci alla seconda legge della termodinamica, attraverso la quale introdurremo la funzione S entropia. Vedremo che la variazione dell’entropia ∆S ci permetterà di capire la sponateneità di un processo. Ogni giorno della nostra vita ci capità di osservare centinaia di processi spontanei. Il fenomeno dell’evaporazione che si verifica lasciando un liquido a contatto con l’aria, la dissoluzione del sale da cucina in acqua, il calore che fluisce da un corpo caldo verso uno freddo non sono altro che alcuni esempi delle infinite possibilità che si presentano ogni giorno. Ogni volta che proviamo a vedere un filmato a ritroso spontaneamente ci ci viene da sorridere perché osserviamo un processo che non si può verificare nella realtà. Non ci capiterà mai di osservare la ricomposizione spontanea di un vaso una volta che questo si sia rotto mediante, ad esempio, una caduta accidentale. Eppure secondo la prima legge entrambi i processi possono avvenire in entrambe le direzioni, la realtà, tuttavia, ci insegna che solo una delle due possibilità avviene spontaneamente. In alcuni casi, è l’energia stessa ad indicarci la direzione di un processo, come quando osserviamo la caduta di un oggetto a causa della diminuzione della sua energia potenziale. M. Rustici, Chimica di base 96 Termodinamica Durante tale evento l’energia potenziale si trasforma in energia cinetica fino a che l’oggetto non cade a terra. Tuttavia se ipotizzassimo un urto completamente elastico l’oggetto in questione tornerebbe al punto di partenza e ci troveremmo di fronte ad un moto perpetuo. Per quanto l’urto si avvicini alla condizione di idealità, rappresentata da una completa elasticità, non lo sarà mai perfettamente e al massimo potremmo osservare un’oscillazione smorzata fino all’arresto dell’oggetto in questione. Tuttavia se andassimo a registrare la temperatura locale nel punto in cui è avvenuto l’urto osserveremo un aumento della stessa. In altre parole per il principio di conservazione dell’energia, l’energia potenziale si è trasformata in energia cinetica che a sua volta si è trasformata in calore. La domanda che ci sovviene è perché il calore non è in grado di ritrasformarsi in energia cinetica e successivamente in energia potenziale generando cosı̀ a sua volta un moto perpetuo? Nessuno ha mai osservato una completa trasformazione del calore in lavoro come nessuno ha mai osservato il passaggio di calore da un corpo freddo ad uno caldo. Queste due osservazioni sono state assunte da Kelvin e Clausis come postulati della seconda legge della termodinamica. La sola energia, non ci permette cosı̀ di stabilire il senso di un processo. Cerchiamo allora di individuare una motivazione statistica che ci permetta di spiegare la spontaneità dei processi macroscopici. A tale scopo consideriamo un esempio particolarmente semplice, ma utile, per il chiarimento del concetto di spontaneità. Consideriamo un recipiente di volume V che supponiamo di aver diviso attraverso un setto mobile in due volumi V1 e V2 con V = V1 + V2 . Supponiamo inoltre che nello scompartimento 1 di volume V1 si trovi un gas e lo scompartimento 2 di volume V2 sia vuoto. Nel momento in cui rimuoviamo il setto il gas spontaneamente fluisce anche nella zona indicata dal volume V2 fino ad occupare tutto il volume del recipiente. Questo processo è un processo spontaneo e si verifica senza nessuna variazione energetica, dato che né il gas compie lavoro né il gas subisce una variazione di temperatura. Per questo processo non possiamo coinvolgere l’energia per spiegarne la spontaneità. Immaginiamo ora che il nostro recipiente contenga una sola particella, da un punto di vista puramente statistico si potrebbe dire che la probabilità di trovare una particella del gas nel volume V è necessariamente uguale a 1, d’altra parte la probabilità di trovare un atomo del gas nello scompartimento 1 con volume V1 sarà necessariamente pari a 1/2. Quando le particelle sono 2, la probabilià di trovare entrambe le particelle in tutto il recipiente sarà ancora 1, ma quella di trovarli tutti e due nello scompartimento a volume V1 sarà questa volta ( 12 )( 12 ), ossia ( 14 ). All’aumentare del numero di particelle la probabilità di trovare tutte le particelle nello scompartimento 1 con volume V1 diventa sempre più piccola. µ ¶µ ¶µ ¶ µ ¶N 1 1 1 1 W = ··· = 2 2 2 2 É ovvio che quando parliamo di un numero di particelle pari a quelle di una mole (cioè pari a 6.022 · 1023 ) la probabilità diventa trascurabile e da un punto di M. Rustici, Chimica di base 97 Termodinamica vista pratico da considerarsi nulla. In altre parole possiamo dire che il gas tende ad occupare tutto il volume semplicemente perché questo rappresenta lo stato più probabile. Se con W indichiamo la probabilità degli stati iniziale e finale potrebbe essere conveniente definire una nuova funzione S proporzionale a tale probabilità. Questa funzione fu definita da Boltzmann come S = KB ln W Questa costituisce una formulazione statistica della funzione entropia e ci permette di interpretare il secondo principio in termini molecolari. Per sistemi complessi e macroscopici è possibile dimostrare che l’entropia può essere definita come ∆S = Qrev T In altre parole questa espressione afferma che la variazione di entropia per un processo reversibile è data dal calore assorbito diviso per la temperatura alla quale avviene il processo. Questa relazione è vera solo quando la trasformnazione viene fatta avvenire reversibilmente per tutti gli altri processi (cioè i processi reali e quindi irreversibili) vale la seguente disuguaglianza ∆S = Qrev Qirrev > T T (8.1) Per una adeguata comprensione dell’entropia dobbiamo comprendere anche quello che avviene nell’ambiente circostante al sistema. L’ambiente per le sue dimensioni e per la quantità di materia che contiene si può considerare con un serbatoio infinitamente grande. In altre parole lo scambio del lavoro o del calore che si verifica nel sistema altera quelle dell’ambiente solo in modo infinitesimo. Poiché un processo reversibile è caratterizzato solo da variazioni infinitesime, qualunque processo reversibile sull’ambiente produce lo stesso effetto. Allora, indipendentemente dal fatto che la trasformaione sia reversibile o irreversibile possiamo scrivere (δQamb )rev = (δQamb )irrev = δQamb per l’ambiente non è pertanto necessario specificare se la variazione è reversibile o irreversibile ∆Samb = Qamb Tamb M. Rustici, Chimica di base 98 Termodinamica allora la variazione totale dell’entropia dell’universo definita come la variazione entropica del sistema più quello dell’ambiente sarà esprimibile come ∆Suniv = ∆Ssist + ∆Samb = Qsist Qamb + T T (8.2) nel caso che la trasformazione del sistema sia reversibile, essa avrà ovviamente segno opposto a quella dell’ambiente e in altre parole avremo che per una trasformazione reversibile la variazione dell’entropia è nulla ∆Suniv = 0 (8.3) nel caso in ncui la trasformazione sia irreversibile vale la relazione 8.1 e la relazione 8.2 diventa ∆Suniv ≥ 0 (8.4) dove il segno di uguaglianza vale solo per le trasformazioni reversibili, mentre quello di disuguaglianza per i processi irreversibili, in altre parole per i processi spontanei. Possiamo allora formulare il secondo principio nella forma l’entropia di un sistema isolato aumenta in un processo spontaneo (irreversibile) mentre rimane costante per un processo reversibile. Abbiamo allora individuato una funzione termodinamica che regola la spontaneità dei processi e possiamo affermare che un processo è spontaneo quando la variazione dell’entropia del sistema più quella dell’ambiente risulta maggiore di 0. La legge dell’aumento di entropia benché sia fondamentale per la comprensione della spontaneità dei processi non è però di semplice applicazione per la difficoltà che esiste nel calcolo della variazione di entropia per un sistema isolato. Sarebbe particolarmente utile individuare una funzione termodinamica che indichi il senso di spontaneità di un processo ma che nello stesso tempo dipenda solo dal sistema e non dall’ambiente. Si deve a J. Willard Gibbs l’ndividuazione di tale funzione, a tale proposito riscriviamo la relazione 8.2 nella forma ∆Suniv = ∆Ssist + Qamb ≥0 T essendo inoltre Qamb Qsist =− T T posso scrivere M. Rustici, Chimica di base (8.5) 99 Termodinamica Qsis ≥0 (8.6) T nel caso in cui il processo avvenga a pressione costante Qsis = H scriveremo ∆Suniv = ∆Ssist − ∆H ≥0 T moltiplicando l’equazione per −T otteniamo ∆Ssist − ∆H − T ∆S ≤ 0 (8.7) (8.8) dove abbiamo tolto il suffisso del riferimento al sistema perché tutti gli elementi dell’equazione 8.8 si riferiscono al sistema. Definiamo pertanto la funzione G = H − TS (8.9) come energia libera di Gibbs. L’equazione 8.8 ci fornisce un criterio di spontaneità dei processi e sulla base della 8.9 possiamo riscrivere che il criterio di spontaneità è regolato dalla semplice relazione ∆G ≤ 0 (8.10) Possiamo allora affermare che un processo è spontaneo quando è associato ad una diminuzione di energia libera. Diremo inoltre che un sistema è in equilibrio ogni qual volta si verifica la condizione ∆G = 0. Il sistema evolverà spontaneamente fino a quando l’energia libera dello stato iniziale non uguaglia l’energia libera dello stato finale. L’osservazione della relazione 8.8 mette in evidenza come la spontaneità di un processo sia regolata dal termine entalpico e dal termine entropico che in alcuni casi possono operare in senso opposto. Dato che le reazioni chimiche possono essere sia esotermiche ∆H ≤ 0 o endotermiche ∆H ≥ 0 e nello stesso tempo possono avvenire con diminuzione ∆S ≤ 0 o aumento di entropia ∆S ≥ 0 ne consegue che il segno di ∆G dipende dai valori dei segni di ∆H e di ∆S come è intuibuile dall’osservazione dell’equazione 8.9. Possiamo allora individuare le seguenti possibilità ∆H < 0 ∆S > 0 ∆G < 0 reazione esotermica aumento di entropia reazione spontanea ad ogni temperatura ∆H > 0 ∆S < 0 ∆G > 0 reazione endotermica diminuzione di entropia reazione non spontanea ad ogni temperatura ∆H > 0 ∆S > 0 ∆G < 0 reazione endotermica aumento di entropia reazione non spontanea se T ∆S > ∆H ∆H < 0 ∆S < 0 ∆G > 0 reazione esotermica diminuzione di entropia reazione spontanea se |T ∆S| < |∆H| M. Rustici, Chimica di base 100 Termodinamica La spontaneità di un processo, sia di natura chimica, fisica o biologica è possibile descriverlo attraverso la variazione della funzione energia libera il processo evolverà fino a che non si verifica la condizione ∆G = 0 cioè la condizione di equilibrio. I sistemi pertanto cercheranno di raggiungere questa condizione diminuendo l’energia libera del sistema. 8.3 Riflessioni sul significato dell’entropia Il secondo principio della termodinamica mette in evidenza la necessità di introdurre a livello fenomenologico una distinzione essenziale tra processi reversibili e irreversibili. Un esempio di irreversibilità può essere la conduzione del calore che conduce ad una distribuzione uniforme della temperatura, un esempio di reversibilità può essere la propagazione delle onde se si trascurano attriti e perdite di energia. Il secondo principio tratta questa distinzione tra processi reversibili e irreversibili introducendo una funzione, entropia, che aumenta in seguito ai processi irreversibili. clausius dette a questa legge una formulazione drammatica quando affermò che l’entropia dell’universo è crescente. Secondo questa affermazione l’universo (inteso come sistema isolato) si muove verso la morte termica. Questo però non è esattamente quello che noi comunemente osserviamo attorno a noi, né ciò che possiamo dedurre dal passato dell’universo, per quanto ci è noto. Osserviamo viceversa una evoluzione verso la complessità. Ci potremmo infatti chiedere in che modo sia possibile che Clausis e Darwin abbiano ragione entrambi quando, l’uno afferma che l’universo evolve verso la morte termica e quindi verso il massimo disordine, mentre l’altro afferma che il nostro pianeta è in continua evoluzione verso sistemi più complessi. Queste due affermazioni, benché possono apparire in contraddizione, in realtà ad un più attento esame, osserviamo che esse si riferiscono a problemi diversi. Il principio di Clausis nella forma descritta è esclusivamente vero per sistemi isolati, mentre la teoria di Darwin si riferisce a sistemi aperti (cioè a quei sistemi che scambiano energia e materia con l’ambiente esterno). Per i sistemi aperti possiamo suddividere il contributio entropico in due termini ∆S = ∆e S + ∆i S (8.11) dove il termine ∆e S si riferisce a scambi entropici con l’ambiente esterno mentre il termine ∆i S si riferisce alle variazioni di entropia associate ai processi irreversibili che avvengono all’interno del sistema. Nel momento in cui il sistema diventa isolato il termine ∆e S diventa 0 e in altre parole la relazione 8.11 si trasforma ∆S = ∆i S ≤ 0 M. Rustici, Chimica di base (8.12) 101 Termodinamica Il secondo principio della termodinamica pertanto afferma che solo il termine ∆i S è necessariamente sempre positivo e non pone nessuna limitazione per quanto concerne il termine ∆e S che può in linea di principio essere positivo o negativo. Questo implica che, in linea di principio, nulla vieti che in un sistema aperto, possano verificarsi situazioni tali che |∆e S| > ∆i S con ∆e S < 0. Il verificarsi di queste condizioni implicherebbe necessariamente una diminuzione locale dell’entropia del sistema e quindi la formazione di ordine invece del disordine. Queste considerazioni termodinamiche, stanno alla base, della comprensione della nascita dell’ordine dal disordine e che portarono Ilya Prigogine a prendere il premio Nobel per la chimica nel 1977 per gli studi sulla termodinamica della vita. M. Rustici, Chimica di base Capitolo 9 Soluzioni 9.1 Soluzioni Una soluzione è una miscela fisicamente omogenea, cioè un insieme di due o più componenti che costituiscono un’unica fase. Se un componente della soluzione è in eccesso si dice solvente, mentre gli altri componenti sono detti soluti. Le soluzioni possono essere gassose, liquide o solide anche se le soluzioni liquide sono le più comuni. Affinché un soluto possa sciogliersi in un solvente è necessario che le forze di interazione tra le molecole e il solvente siano dello stesso tipo. Quando si parla di soluzioni è necessario definire quale sia la concentrazioni della soluzione stessa. Un modo per rappresentare una concentrazione è quello di definirla attraverso la percentuale in massa di un componente. Se con wi indichiaP mo la massa del componente iesimo e con wi la massa totale della soluzione la concentrazione espressa come percentuale in masse è definita come wi Percentuale in massa = P · 100 wi un altro modo per rappresentare la concentrazione è la percentuale in volume. P Se con Vi indichiamo il volume del componente iesimo e con Vi il volume totale della soluzione la concentrazione espressa come percentuale in volume è definita come Vi Percentuale in volume = P · 100 Vi Questo modo di esprimere la concentrazione è usato raramente in quanto volumi di liquidi diversi spesso non sono additivi e il volume totale non corrisponde alla somma dei volumi. Quando parliamo di concentrazioni molto piccole spesso si usa la concentrazione espressa come parti per milione ppm o parti per miliardo ppb di parti di soluzione espresse in massa o volume. M. Rustici, Chimica di base 104 Soluzioni ppm = parti di soluto di soluzione 106 parti La frazione molare xi rappresenta il numero di moli di un componente ni P rispetto al numero totale dei componenti ni ni xi = P ni P dalla quale si ricava facilmente che i xi = 1 La molarità Mi rappresenta invece il numero di moli di soluti (ni ) per unità di soluzione (in genere litro o dm3 ). Mi = ni mol/l V Un’altra misura di concentrazione è la molalità mi e rappresenta il numero di moli di soluto ni presenti in un 1Kg di solvente. Un’altra utile unità di concentrazione è la Normalità (N) che analizzeremo più avanti quando tratteremo gli acidi, le basi e le reazioni di ossidoriduzione. 9.2 Proprietà colligative Si parla di proprietà colligative quando le proprietà della soluzione non dipendono dal tipo di particelle ma solo dal numero di particelle contenute nella soluzione. Tali proprietà sono l’abbassamento della tensione di vapore, l’innalzamento ebullioscopico e l’abbassamento crioscopico e la pressione osmotica. Queste proprietà valgono comunque per soluzioni diluite. 9.2.1 Abbassamento della tensione di vapore La tensione di vapore rappresenta la pressione esercitata dal vapore in equilibrio con la fase liquida ad una data temperatura e pressione. Ogni solvente puro manifesta una sua tensione di vapore specifica, nelle condizioni di temperatura e pressione costante, che subisce delle variazioni quando un soluto è disciolto nel solvente. In termini quantitativi la diminuzione della tensione di vapore causata del soluto viene espressa dalla legge di Roult. Si tratta di una legge lineare in cui la tensione di vapore del solvente è proprorzionale alla tensione di vapore del solvente puro Ps0 mediante la frazione molare del solvente stesso. Ps = xs Ps0 M. Rustici, Chimica di base (9.1) 105 Soluzioni Figura 9.1. andamento della legge di Raoult per due solventi A e B Essendo la frazione molare un numero compreso tra 0 e 1 questo indica che necessariamente si abbia una diminuzione della tensione di vapore in presenza di un soluto. La relazione 9.1 può essere scritta anche in funzione della frazione molare del solvente. Ricordando infatti la proprietà della frazione molare è facile scrivere che ∆P = xs Ps0 (9.2) dove in questo caso dobbiamo ricordarci che xs rappresenta la frazione molare del soluto. Ovviamente le relazioni 9.1 e 9.2 funzionano altrettanto bene quando consideriamo una miscela di liquidi miscibili A e B. La relazione 9.1 in questi casi potranno essere espresse come PA = xA PA0 PB = xB PB0 La figura 9.1 mostra l’andamento della legge di Roult per due solventi A e B come espresso dalle espressioni matematiche, tuttavia la realtà sperimentale è in genere più complessa ed è possibile osservare deviazioni negative o positive della legge di Roult. La deviazione positiva (figura 9.2) corrisponde al caso in cui le forze intermolecoari dissimili sono più deboli di quelle tra le forze intermolecolari tra molecole M. Rustici, Chimica di base 106 Soluzioni (a) deviazione negativa (b) deviazione positiva Figura 9.2. Deviazioni positive e negative dalla legge di Raoult simili, le molecole manifestano, pertanto, una tendenza maggiore a sfuggire dalla suluzione rispetto a quanto accade per una soluzione ideale. Conseguentemente la tensione di vapore della soluzione è maggiore della somma delle pressioni di vapore di soluzioni ideali. L’opposto, ovviamente, vale per quelle soluzioni che manifestano una deviazione negativa dalla legge di Raoult (Figura 9.2). In questo caso le molecole diverse si attraggono più fortemente rispetto a quanto facciano le molecole uguali e la tensione di vapore è minore rispetto a quella della soluzione ideale. Quando un componente della soluzione è in forte eccesso rispetto all’altro (questo componente è chiamato solvente) e la sua pressione di vapore è descritta accuratamente dall’equazione 9.1. Al contrario la tensione di vapore del componente presente in piccole quantità (soluto) non varia con la composizione della soluzione secondo al relazione 9.1. La tensione di vapore del soluto varia ancora linearmente con la concentrazione secondo la relazione Psoluto = Kxsoluto (9.3) L’equazione 9.3 è nota come legge di Henry dal chimico inglese William Henry, dove K, la costante della legge di Henry, è espressa in atm o in torr. Tale legge è di solito associata alle soluzioni di gas nei liquiti, benché sia ugualmente applicabile a soluzioni che contengono soluti volatili non gassosi. L’effervescenza che si osserva quando si stappa una bottiglia di spumante mette bene in evidenza come si ababssa la solubilità del gas al diminuire della pressione parziale. un altro esempio di applicabilità della leggedi Henry è ben evidenziata nella formazione di emboli che si formano nei sommozzatori quando risalgono in superficie troppo velocemente. A 40 m sotto la superficie del mare la pressione è intorno a 6 atm, la solubilità dell’azoto nel plasma sanguigno è intorno a 3·10−3 mol/Kg(H2 O) cioè 6 volte la solubilità a livello del mare. Se il sommozzatore nuota troppo velocemente verso la superficie, l’azoto disciolto comincia a sfuggire dal plasma e questo conduce ad un embolia. Nelle immersioni subacquee si preferisce diluire l’ossigeno con l’elio dato che questo risulta meno solubile rispetto all’azoto facendo diminuire il rischio della formazione di emboli. M. Rustici, Chimica di base 107 Soluzioni 9.2.2 Innalzamento ebullioscopico e abbassamento crioscopico La temperatura di ebollizione di una soluzione è più alta di quella del solvente puro. La temperatura di ebollizione rappresenta la temperatura alla quale la tensione di vapore uguaglia la pressione esterna. La tensione di vapore di una soluzione è inferiore a quella del solvente puro a qualsiasi temperatura. Perciò, alla temperatura di ebollizione del solvente puro, la soluzione non bolle ancora. Questo può essere ben visto nella figura 7.1 in cui si osserva la sovrapposizione di due diagrammi di fase, uno relativo all’acqua pura e l’altro relativo alla soluzione. La curva gas liquido per la soluzione giace sotto quella per il solvente puro a qualsiasi temperatura e a destra di essa a qualsiasi pressione. Il valore dell’innalzamento ebullioscopico è direttamente proporzionale alla concentrazione delle particelle del soluto secondo la relazione. ∆T = Keb m (9.4) dove m è la molalità della soluzione e Keb è la costante ebullioscopica. In modo del tutto analogo all’innalzamento ebullioscopico parliamo di abbassamento crioscopico. Nella figura 7.1 possiamo osservare tale abbassamento. La relazione quantitativa è ∆T = Kcr m (9.5) dove m è la molalità della soluzione e Kcr è la costante ebullioscopica. La figura 9.3 mostra l’abbassamento crioscopico e l’innalzamento ebullioscopico. Il fenomeno dell’abbassamento crioscopico ha molteplici esempi nella vita quotidiana e nei sistemi biologici. Ad esempio il glicol etilenico è il comune anticongenalente per le automobili ed è usato per togliere il ghiaccio dagli aerei. Dal punto di vista biologico osserviamo, ad esempio, che nelle acque dell’antartide particolari pesci noti come ’ice-fish’ hanno sviluppato una spettacolare capacità di adattamento che consente loro di vivere e nuotare in acque che sfiorano i meno due gradi. In alcuni di essi si trovano liquidi anti-gelo mentre in altri non è presente l’ emoglobina né i globuli rossi, cosa che riduce la densità del sangue e rende questi pesci meno soggetti al congelamento. 9.2.3 Pressione osmotica Un’altra importante proprietà, che si applica solo alle soluzioni acquose, è nota come pressione osmotica e si si origina ogni qual volta si mettono in contatto, attraverso una membrana semipermeabile, (permeabile al solvente, impermeabile al soluto) una soluzione acquosa con il rispettivo solvente (acqua). In tale circostanza si osserva un netto passaggio di solvente dalla soluzione meno concentrata verso quella più concentrata (Figura 8.1). M. Rustici, Chimica di base 108 Soluzioni Figura 9.3. Diagramma di stato dell’acqua pura e di una soluzione La pressione che occorre applicare alla soluzione affinché il passaggio del solvente non avvenga è detta appunto pressione osmotica (π). Il meccanismo attraverso il quale la pressione osmotica si origina può essere interpretato considerando che le particelle di un soluto che si disperderdono uniformemente nel solvente esercitano una pressione analoga alla pressione gassosa. Se poi si considera un sistema costituito da una soluzione e dal relativo solvente puro separati da una membrana semipermeabile, il numero delle molecole di solvente che nell’unità di tempo attraversano la membrana verso la soluzione è superiore al numero di molecole di solvente che la attraversano in senso opposto, perché nel primo caso le molecole che vengono a contatto con la membrana sono tutte di solvente, nel secondo caso invece si ha una certa percentuale di particelle di soluto, che non passano ma che esercitano comunque con i loro urti sulla membrana una pressione, appunto la pressione osmotica. Questa non è direttamente misurabile, mentre è misurabile la pressione idrostatica che si determina nella soluzione a causa del maggior numero di molecole di solvente che vi penetrano rispetto a quelle che ne escono. La pressione osmotica è direttamente proporzionale al numero delle particelle di soluto in un dato volume di soluzione cioè alla molarità (M ). La costante di proporzionalità risulta essere RT e quindi possiamo scrivere una relazione analoga a quella della legge dei gas ideali. M. Rustici, Chimica di base 109 Soluzioni Figura 9.4. π = M RT (9.6) Indipendentemente dalla natura del soluto, soluzioni aventi la stessa concentrazione hanno medesima pressione osmotica e si dicono isotoniche; tra soluzioni a diversa concentrazione si dicono ipertoniche le più concentrate, ipotoniche quelle a più bassa concentrazione. Nei sistemi chimici e biologici si trovano molti esempi che descrivono il fenomeno osmotico. I globoli rossi, ad esempio, che sono protetti dall’ambiente esterno mediante una membrana semipermeabile, se si trovano in presenza di una soluzione ipotonica inglobano acqua nella loro cellula e scoppiani provocando il fenomeno dell’emolisi. In questo modo le cellule muoiono e rilasciano nell’ambiente emoglobina e molecole proteiche. Quando invece la cellula è esposta ad un ambiente ipertonico l’acqua intracellulare fuoriesce dalla cellula verso la soluzione esterna più concentrata. Questo effetto noto come crenatura, provoca una contrazione della cellula che alla fine smette di funzionare. Il rene dei mammiferi è un dispositivo osmotico particolarlmente efficacie la cui funzione principale è quella di rimuovere i prodotti metabolici di scarto e altre impurezze dal flusso sanguigno, verso la soluzione esterna di urina più concentrata, mediante una membrana semipermeabile. La pressione osmotica, inoltre, rappresenta un importante meccanismo anche M. Rustici, Chimica di base 110 Soluzioni per la vita delle piante. Le foglie dagli alberi perdono continuamente acqua verso l’ambiente, un processo chiamato traspirazione e le concentrazioni dei soluti fogliari aumentano. L’acqua è spinta, quindi, attraverso il tronco e i rami per pressione osmotica, che per raggiungere le cime più alte può arrivare anche a 10-15 atm. Un altro fenomeno colelgato all’osmosi è la cosiddetta osmosi inversa che viene utilizzata come processo di deionizzazione dell’acqua. Se si applica una pressione maggiore della pressione osmotica di equilibrio allora del solvente puro passerà dalla soluzione a quella del solvente. 9.3 Distillazione I concetti che abbiamo fino a qui mostrato possono aiutarci da un punto di vista pratico ad individuare quali sono le tecniche per la separazione di di due componenti che formano una fase liquida. Scegliamo come esempio una miscela cme benzene-toluene che si avvicina al comportamento delle soluzioni ideali che seguono la legge di Raoult. Se con 1 indichiamo il benzene e con 2 il toluene possiamo scrivere la legge di Raoult per questi due componenti nella forma P1 = x1 P10 P2 = x2 P20 la pressione totale sarà espressa dalla relazione P = P1 + P1 = x1 P10 + x2 P20 = (1 − x2 )P10 + x1 P20 = P10 + (P20 − P10 )x2 (9.7) La linea retta della figura 9.5 rappresenta la pressione del vapore in funzione della frazione molare x2 indicata dall’equazione 9.7. Nel caso specifico, il benzene (1) ha una tensione di vapore superiore a quella del toluene (2) in altre parole P10 > P20 la pendenza sarà pertanto negativa come indicato nella figura 9.5. Calcoliamo ora la frazione molare del componente 2 nella fase vapore xv2 che definiamo xv2 = P2 x2 P20 = 0 P P1 + (P20 − P10 )x2 ricavando x2 da questa relazione otteniamo M. Rustici, Chimica di base 111 Soluzioni Figura 9.5. La linea retta rappresenta la pressione di vapore totale in equilibrio con una soluzione ideale la cui composizione è descritta dalla frazione molare del componente 2. La linea inferiore rappresenta la tensione di vapore in funzione della frazione molare del componente 2 nella fase vapore. x2 = xv2 P10 (P20 − P10 )xv2 − P20 (9.8) ricordando le leggi di Dalton e di Raoult P2 = xv2 P P2 = x2 P20 possiamo scrivere xv2 P = x2 P20 ∴ P = P20 x2 xv2 utilizzando l’equazione 9.8 otteniamo P = P10 P20 (P20 − P10 )xv2 − P20 (9.9) La curva individuata nell’equazione 9.9 è riportata nello stesso grafico della figura 9.5. Complessivamente possiamo notare che sopra la linea retta il sistema è M. Rustici, Chimica di base 112 Soluzioni nella fase liquida (questo risultato è in accordo con il fatto che ad alte pressioni la fase liquida è la fase più stabile). Al di sotto della curva, cioè a basse pressioni, il sistema esiste come vapore. In un punto tra le due linee, cioè in un punto dell’area chiusa, il sistema è in equilibrio con le due fasi liquida e vapore. Supponiamo ora di trovarci in un punto della fase liquida ed applichiamo la regola delle fasi, tenendo presente che il nostro sistema è a due componenti (c = 2), il numero delle fasi (p = 1) avremo f =c−p+2 f =2−1+2=3 in altre parole i gradi di libertà del sistema sono 3. Questo implica che se scegliamo come variabili del sistema la temperatura T , la frazione molare x2 e la pressione P noi possiamo variare indifferentemente, per un ampio intervallo, queste tre grandezze senza che il sistema generi una nuova fase. Supponiamo ora di fissare una temperatura e una frazione molare (supponiamo x2 =0.6) se diminuiamo la pressione il sistema rimarrà monofasico per un ampio intervallo di pressione fino a che un ulteriore abbassamento provocherà il raggiungimento della linea retta, in altre parole il liquido inizierà ad evaporare e la fase liquida sarà in equilibrio con la fase vapore. Se abbassiamo ancora la pressione fino a raggiungere un generico punto situato nella zona tra la curva del liquido e quella del vapore la miscela alla composizione iniziale (x2 = 0.6) si scinderà in due fasi aventi diversa composizione nella fase vapore e nella fase liquida. La composizione potrà essere ottenuta tracciando dal punto scelto una ratta parallela all’asse delle ascisse che interseca la linea del liquido e quella del vapore. I punti di intersezione ci daranno la composizione della fase vapore e di quella liquida. Le quantità relative del liquido e del vapore possono essere ottenute mediante la regola della leva nL lL = nV lV dove nV e nL sono rispettivamente le moli del liquido e del vapore mentre lL elV sono le distanza dal centro alle intersezioni con le curve del liquido e del vapore. Applicando in questa zona la regola delle fase avremo f =2−2+2=2 2 gradi di libertà, e se scegliamo come nel caso specifico un valore determinato di pressione e temperatura avremo soltanto un valore di composizione che sarà definito come precedentemente indicato. M. Rustici, Chimica di base 113 Soluzioni Figura 9.6. Diagramma temperatura composizione La figura 9.5 illustra a sua volta come sia possibile separare i due componenti. Osserviamo che se la frazione molare della miscela di partenza è 0.6 la fase vapore risulta più ricca nel componente più volatile xv2 = 0.312. Se si condensa la fase vapore e di nuovo si fa evaporare il liquido, il vapore si arricchirà ancora di più nella fase più volatile. Ripetendo il processo più volte a temperatura costante arriveremo ad una separazione quantitativa del benzene dal toluene. 9.3.1 Diagramma temperatura-composizione nella pratica è più conveniente eseguire la distillazione a pressione costante piuttosto che a temperatura costante, pertanto, si ha bisogno di esaminare il diagramma temperatura composizione. Il grafico della figura 9.6 mostra, per prima cosa, che le regioni del liquido e del vapore sono invertite e che né liquido né vapore si trovano su una linea retta. Il componente più volatile si trova ad una pressione di vapore più elevata e dunque un punto di ebollizione più basso. La figura 9.6 ci dice, inoltre, che la fase stabile a basse temperature è quella liquida. Durante la distillazione frazionata schematizzata mediante le frecce indica che il processo alla fine porterà alla completa separazione dei due componenti. Ogni stadio di evaporazione e condensazione è detto piatto teorico. La figura 9.6 mostra un semplice schema di apparecchio di distillazione da M. Rustici, Chimica di base 114 Soluzioni Figura 9.7. Apparecchiatura da laboratorio per la distillazione laboratorio il quale può essere reso più efficiente inserendo una colonna tra il pallone e la refrigerazione in modo da aumentare il numero di piatti teorici. La raffinazione del petrolio utilizza un procedimento simile. Riscaldando il petrolio greggio su una colonna di distillazione che può essere alta fino ad 80 metri e che contiene centinaia di piatti teorici, si possono separare diverse frazioni in base agli intervalli dei punti di ebollizione. 9.3.2 Gli azeotropi La maggior parte delle soluzioni non sono ideali e di conseguenza i loro diagrammi temperatura-composizione sono più complicati di quelli riportati in figura 9.6. Se il sistema presenta una deviazione positiva dalla legge di Raoult, la curva mostrerà un minimo nelle temperature di ebollizione. Viceversa, una deviazione negativa dalla legge di Raoult risulterà in un massimo nelle temperature di ebollizione (Fig. 9.8). Esempi classici con azeotropi di massimo sono acido cloridrico-acqua, acetonecloroformio mentre quelli di minimo etanolo-acqua, acetone-disolfuro di carbonio. La distillaziione frazionata in questi casi non può condurre alla completa separazione dei rispettivi componenti, si potrà raggiungere un arricamento ma non la separazione completa per distillazione frazionata. Ripetendo più volte il processo si arriverà alla fina a quella miscela che è nota come azeotropo, in altre parole l’azeotropo si comporta come un composto puro. Tuttavia, a ben guardare, le sue proprietà sono diverse dai composti puri a causa del fatto che i grafici individuati dalla figura 9.8 possono cambiare al variare della pressione. Precisamente aumentando o diminuendao la pressione di esercizio il massimo o il minimo che M. Rustici, Chimica di base 115 Soluzioni Figura 9.8. Azeotropi: (a) altobollente o di massimo, (b) bassobollente o di minimo caratterizzano l’azeotropo si può sopstare a destra o a sinistra. In questo modo si può riuscire variando la pressione a migliorare la separazione della miscela attraverso una distillazione frazionata. Ad esempio nel caso della miscela etanoloacqua alla pressione di 760 mmHg la composione dell’azeotropo è del 91.6 % di etanolo e 8.4 % di acqua mentre a 200 mmHg la composizione passa al 94.2 % di etanolo e al 5.8 % di acqua. M. Rustici, Chimica di base Capitolo 10 Equilibrio chimico 10.1 Equilibrio chimico Nel capitolo 8 abbiamo formulato, nelle sue linee essenziali, le leggi fisiche che ci permettono di comprendere l’equilibrio. In particolare possiamo riassumere, in poche parole, che la condizione di equilibrio per un generico processo sia esprimibile dalla relazione ∆G = 0. Nel caso di una reazione chimica possiamo esprimere l’equilibrio attraverso un relazione nota come costante di equilibrio K. A tale proposito consideriamo un sistema omogeneo e per semplicità una reazione in fase gassosa. Immaginiamo che tra i componenti della miscela gassosa sia in atto la seguente reazione chimica aA + bB À cC + dD (10.1) Lo stato di equilibrio viene raggiunto quando la velocità della reazione diretta uguaglia la velocità inversa. Si tratta di un equilibrio dinamico, come si può facilmente intuire. A rigore tutte le reazioni chimiche andrebbero considerate di equilibrio, ma nella pratica comune quelle in cui le concentrazioni di reagenti sono irrisorie vengono tranquillamente considerate non di equilibrio (sono dette reazioni a completamento). Se supponiamo che i componenti dell’equilibrio indicato dallo schema di reazione 9.1 siano specie gassose possiamo immaginare di definire la costante di equilibrio come il rapporto tra il prodotto delle pressioni parziali dei prodotti elevate ai rispettivi coefficienti stechiometrici e il prodotto delle pressioni parziali dei reagenti sempre elevati ai rispettivi coefficienti stechiometrici. KP = (PC )c (PD )d (PA )a (PB )b (10.2) Attraverso considerazioni termodinamiche si può dimostrare che tale costante dipende solo dalla temperatura e pertanto risulta costante a temperatura costante e quindi indipendente dalla pressione e dal volume. Dobbiamo altresı̀ tener M. Rustici, Chimica di base 118 Equilibrio chimico presente che tale costante è adimensionale contrariamente da quello che si potrebbe evincere osservando la relazione 9.2. A tale risultato si arriva direttamente attraverso considerazioni termodinamiche, tuttavia basta ricordare che ogni pressione o concentrazione parziale è divisa per una pressione o concentrazione di riferimento e ciò rende la relazione adimensionale. Applicando la legge di stato dei gas alle rispettive pressioni parziali possiamo esprimere la KP in funzione delle concentrazioni. Otteniamo cosı̀: KP = (PC )c (PD )d (CC )c (CD )d = (RT )∆ν = KC (RT )∆ν (PA )a (PB )b (CA )a (CB )b (10.3) dove ∆ν = d + c − a − b. Possiamo allora osservare che solo nel caso in cui ∆ν = 0 la KC = KP . La KC analogamente alla KP risulta costante a temperatura costante. Risulta altresı̀ interessante definire la costante di equilibrio in funzione della frazione molare. Per far ciò sostituiamo nella costante di equilibrio KC al posto delle concentrazioni delle singole specie il rapporto ni /V KC = (CC )c (CD )d (nC /V )c (nD /V )d (nC )c (nD )d −∆ν = = V (CA )a (CB )b (nA /V )a (nB /V )b (nA )a (nB )b (10.4) (nC )c (nD )d (nA )a (nB )b (10.5) definendo Kn = Otteniamo KC = Kn V −∆ν (10.6) Applicando la legge di stato dei gas possiamo sostituire al posto di V la sua espressione nRT /P pertanto la relazione 9.6 diventa µ KC = Kn nRT P µ ¶−∆ν = Kx RT P µ ¶−∆ν = Kx P RT ¶∆ν (10.7) dove Kx è la costante di equilibrio in funzione delle frazioni molari xi = P ni / i ni cosı̀ definita: Kx = (xC )c (xD )d (xA )a (xB )b combinando la relazione 9.3 con la 9.7 otteniamo: M. Rustici, Chimica di base (10.8) 119 Equilibrio chimico Kp = Kx (P )∆ν (10.9) Quest’ultima relazione è importante in quanto ci permette di comprendere come si sposti l’equilibrio in funzione della pressione. Riscriviamo la 9.9 come: Kx = KP (P )−∆ν (10.10) e proviamo ad applicare questa relazione alla reazione di produzione dell’ammoniaca. 3H2 + N2 À 2NH3 (10.11) La reazione di produzione dell’ammoniaca che costituisce un importante processo industriale avviene con una diminuzione del numero di moli δν = 2 − (3 + 1) = −2 Possiamo allora scrivere che nel caso specifico Kx = x2NH3 x3H2 xN2 KP = p2NH3 p3H2 pN2 (10.12) e inoltre Kx = KP (P )2 (10.13) Dato che la costante di equilibrio KP dipende solo dalla temperatura e quindi è costante a temperatura costante possiamo dedurre che un aumento di pressione provochi un aumento della Kx . Questo implica che affinché la Kx aumenti è necessario che il denominatore della costante espressa in funzione delle frazioni molari diminuisca o che il numeratore aumenti. In altre parole la reazione si sposta a destra verso un aumento della produzione dell’ammoniaca. A parità di temperatura l’equilibrio è spostato, con l’aumento di pressione, verso la produzione dell’ammoniaca. Per questo motivo industrialmente la reazione viene fatta avvenire ad elevate pressioni. Generalizzando possiamo dire che le reazioni che si svolgono con una diminuzione del numero di moli si spostano verso destra mediante un aumento di pressione. Ovviamente la situazione opposta si verificherà se la reazione avviene con un aumento del numero di moli. Quando invece ci troviamo nel caso in cui ∆ν = 0 non si avrà nessuno spostamento dell’equilibrio al variare della pressione. La costante di equilibrio risulta a sua volta correlata alla variazione di energia libera, si può, infatti, dimostrare che M. Rustici, Chimica di base 120 Equilibrio chimico ∆G = ∆G0 + RT ln K Da qui risulta evidente che la costante di equilibrio dipenda solo dalla temperatura, e che inoltre sia rappresentata da un numero puro. Esercizio 10.88 g di anidride solforica vengono posti in un recipiente del volume V = 18 l e la temperatura viene portata a 8960 K. Si stabilisce l’equilibrio 2SO3 ¿ 2SO2 + O2 ad equilibrio raggiunto si misura una pressione totale di P = 0.76 atm. Si determini il valore della costante di equilibrio KP per la reazione di equilibrio in questione. Le moli iniziali dell’anidride solforosa sono n(SO3 )i = 10.88 = 0.136mol 80 attraverso la legge dei gas possiamo valutare le moli totali all’equilibrio nt = moli iniziali moli equilibrio PV 0.76 · 18 = = 0.19 RT 0.082 · 896 2SO3 ni ni − 2ne ¿ 2SO2 0 2ne + O2 0 ne le moli totali saranno nt = ni − 2ne + 2ne + ne = n1 + ne ∴ ne = nt − ni ne = 0.19 − 0.136 = 0.05 nSO3 = ni − 2ne = 0.036 nSO2 = 2ne = 0.01 nO2 = ne = 0.05 xSO3 = xSO2 = xO2 = nSO3 = 0.19 nt nSO2 = 0.54 nt nO2 = 0.27 nt M. Rustici, Chimica di base 121 Equilibrio chimico Ricordando che Kp = Kx P ∆ν e nel nostro caso δν = 3 − 2 = 1, avremo allora Kp = P xO2 x2SO2 = 1.62 x2SO3 Esercizio 4.91 g di acqua vengono posti in un recipiente del volume V = 30 l e la temperatura viene portata a 25730 K. Una volta stabilito l’equilibrio 2H2 O ¿ 2H2 + O2 la pressione totale misura P = 2.4 atm. Si determini il valore della costante di equilibrio Kp e Kc per la reazione di equilibrio in questione. Le moli iniziali dell’acqua sono nH2 O (i) = 4.91 = 0.27mol 18 attraverso la legge dei gas possiamo valutare le moli totali all’equilibrio nt = moli iniziali moli equilibrio PV 2.40 · 30 = = 0.34 RT 0.082 · 2573 2H2 O ni ni − 2ne ¿ 2H2 0 2ne + O2 0 ne le moli totali saranno nt = ni − 2ne + 2ne + ne = n1 + ne ∴ ne = 0.34 − 0.27 = 0.07 nH2 O = 0.38 nt nH = 2 = 0.41 nt nO2 = = 0.21 nt xH2 O = xH2 xO2 M. Rustici, Chimica di base ne = nt − ni 122 Equilibrio chimico Avremo quindi Kp = P xO2 x2H2 = 0.59 x2H2 O Esercizio Una certa quantità di un gas biatomico A2 viene posto in un recipiente di capacità V e temperatura T . Dopo un certo tempo si raggiunge l’equilibrio A2 ¿ 2A Misurando le moli di A all’equilibrio si osserva che esse sono il 30% delle moli iniziali del gas biatomico. La pressione misurata in queste condizioni risulta P = 0.65 atm. Calcolare la Kp della reazione. Le moli di A sono nA = 0.3nA2 (i) A2 ni ni − x moli iniziali moli equilibrio ¿ 2A2 0 2x i dati del problema ci dicono allora che 2x = 0.3nA2 (i) ∴ 2x = 0.3n( i) x = 0.15ni le moli totali saranno nt = ni − 0.15ni + 0.3ni = 1.15ni possiamo allora calcolare le frazioni molari 0.3ni 0.3 nA = = = 0.26 nt 1.15ni 1.15 = 1 − 0.26 = 0.74 xA = xA2 M. Rustici, Chimica di base 123 Equilibrio chimico Avremo quindi Kx = x2A = 0.092 xA2 inoltre Kp = Kx P ∆ν ma ∆ν = 1 quindi Kp = 0.092 · 0.65 = 0.060 Esercizio 4.91 g di acqua vengono posti in un recipiente del volume V = 30 l e la temperatura viene portata a 25730 K. Una volta stabilito l’equilibrio 2H2 O ¿ 2H2 + O2 la pressione totale misura P = 2.4 atm. Si determini il valore della costante di equilibrio Kp e Kc per la reazione di equilibrio in questione. Le moli iniziali dell’acqua sono nH2 O (i) = 4.91 = 0.27mol 18 attraverso la legge dei gas possiamo valutare le moli totali all’equilibrio nt = moli iniziali moli equilibrio PV 2.40 · 30 = = 0.34 RT 0.082 · 2573 2H2 O ni ni − 2ne ¿ 2H2 0 2ne + O2 0 ne le moli totali saranno nt = ni − 2ne + 2ne + ne = n1 + ne ∴ ne = 0.34 − 0.27 = 0.07 M. Rustici, Chimica di base ne = nt − ni 124 Equilibrio chimico nH2 O = 0.38 nt nH = 2 = 0.41 nt nO2 = 0.21 = nt xH2 O = xH2 xO2 Avremo quindi Kp = P xO2 x2H2 = 0.59 x2H2 O Esercizio In un recipiente a volume costante e ad una certa temperatura si instaura per l’ammoniaca il seguente equilibrio 2NH3 ¿ 3H2 + N2 Ad equilibrio raggiunto la pressione totale misura P = 4 atm e la pressione parziale dell’ammoniaca risulta di 1.2 atm. Si determini il valore della costante di equilibrio Kp per la reazione di equilibrio in questione. Applicando la legge di Raoult abbiamo PNH3 = xNH3 Pt da cui risulta che xNH3 = 1.2 PNH3 = = 0.3 Pt 4 dalla stechiometria della reazione risulta che nH2 = 3nN2 ∴ xH2 = 3xN2 ricordando che la somma delle frazioni molari è uguale all’unità possiamo scrivere che xH2 + xN2 + xNH3 = 1 3xN2 + xN2 + 0.3 = 1 quindi M. Rustici, Chimica di base 125 Equilibrio chimico 1 − 0.3 = 0.175 4 = 3xN2 = 3 · 0.175 = 0.525 xN 2 = xH 2 xNH3 = 0.3 allora Kx = xN2 x3H2 = 0.536 x2NH3 inoltre Kp = Kx P ∆ν ma ∆ν = (1 + 3) − 2 = 2 quindi Kp = 0.536 · 42 = 8.57 Esercizio In un recipiente di volume incognito vengono inserite 2 moli di PCl5 . Il sitema viene portato alla temperatura di 5730 K e una volta raggiunto l’equilibrio PCl5 ¿ PCl3 + Cl2 la kp = 14 atm. Sapendo che in queste condizioni il pentacloruro di fosforo è dissociato per il 50% calcolare il volume del recipiente moli iniziali moli equilibrio PCl5 ni ni − x ¿ 2PCl3 0 x + Cl2 0 x per cui nt = ni − x + x − x = ni + x = 2 + 1 = 3 Dato che il PCl5 è dissociato per il 50% possiamo scrivere che x = 0.5 · n1 = 0.5 · 2 = 1 M. Rustici, Chimica di base 126 Equilibrio chimico da cui risulta che nPCl3 = nCl2 = x = 1 e nPCl5 = ni − x = 2 − 1 = 1 quindi xPCl3 = xCl2 = xPCl5 = 1 = 0.333 3 possiamo calcolare ora la costante di equilibrio relativa alle frazioni molari allora xCl2 xPCl3 0.333 · 0.333 = = 0.333 xPCl5 0.333 Kx = inoltre Kp = Kx P ∆ν ma ∆ν = (1 + 1) − 1 = 1 quindi Kp = Kx P ∴ P = kp 14 = = 42.42 kx 0.333 Applicando l’equazione di stato dei gas possiamo valutare il volume finale V = 10.2 3 · 0.082 · 573 nRT = = 3.32 l P 42.42 Equilibri eterogenei implicanti fasi gassose Un equilibrio è detto eterogeneo quando i reagenti e i prodotti si trovano in fasi diverse. Quando la fase gassosa è in equilibrio con la fase condensata possiamo applicare le leggi incontrate nel precedente paragrafo. Consideriamo ad esempio l’equilibrio eterogeneo relativo alla decomposizione del carbonato di calcio M. Rustici, Chimica di base 127 Equilibrio chimico CaCO3 À CaO + O2 (10.14) Questa reazione avviene intorno a 8000 C , possiamo pensare di scrivere la costante di equilibrio nella forma KP = pCaO pO2 pCaCO3 (10.15) tenendo però presente che la tensione di vapore parziale dei solidi è costante a temperatura costante in realtà tali tensioni di vapore sono inglobate nella costante di equilibrio e pertanto possiamo esprimere la costante di equilibrio come KP = pO2 10.3 Equilibri di solubilità Gli equilibri di solubilità coinvolgono in genere soluzioni acquose in presenza di sali parzialmente o poco solubili. I sali si solubilizzano parzialmente in soluzione dissociandosi nei rispettivi ioni costituenti il sale. Dopo un po’ di tempo si stabilisce un equilibrio tra il sale non disciolto e gli ioni in soluzione. Si dice che una soluzione è satura quando si è raggiunta la concentrazione massima degli ioni in soluzione oltre la quale gli ioni precipitano sotto forma di sale. In altre parole quando, a temperatura costante, si osserva una soluzione in presenza del corpo di fondo (del sale non disciolto) siamo in condizioni di saturazione. Consideriamo ad esempio un sale poco solubile come il Cloruro di Argento esso si dissocia in soluzione secondo la reazione AgCl À Ag+ + Cl− (10.16) per il quale possiamo definire la costante di equilibrio [Ag+ ][Cl− ] K= [AgCl] dove le parentesi quadre stanno ad indicare la concentrazione molare. Se teniamo presente che [AgCl] è costante a temperatura costante possiamo inglobarla nella costante di equilibrio e scrivere Ks = [Ag+ ][Cl− ] M. Rustici, Chimica di base 128 Equilibrio chimico che prende il nome di prodotto di solubilità. Tale costante è ovviamente adimensionale analogamente alla KP e alla KC . Nel caso ad esempio di una soluzione satura di Cloruro di piombo il prodotto di solubilità sarà: Ks = [Pb2+ ][Cl− ]2 Le concentrazioni molari degli ioni espresse nel prodotto di solubilità sono collegate alla solubilià del sale, cioè al numero di moli di sale che passa direttamente in soluzione. Indichiamo S la solubilità espressa in mol/l. Supponiamo allora di voler risolvere il seguente questito: Esercizio Calcolare quanti grammi di PbCl2 si solubilizzano in 500 ml di acqua sapendo che il suo prodotto di solubilità è pari a 1.7 · 10−5 Se con S indichiamo la solubilià del sale allora possiamo evincere dalla stechiometria della reazione PbCl2 À Pb2+ + 2Cl− che [Pb2+ ] = S e [Cl− ] = 2S allora applicando la definizione del prodotto di solubilità Ks = [Pb2+ ][Cl− ]2 possiamo scrivere che Ks = S · (2S)2 = 4S 3 da cui S = (Ks /4)1/3 = [(1.7 · 10−5 )/4]1/3 = 1.62 · 10−2 mol/l Tenendo presente che vogliamo sapere quanti grammi di sale si sciolgono in 500 ml possiamo scrivere che S= n ∴ n = S · l = 1.62 · 10−2 · 0.5 = 8.1 · 10−3 l Essendo il peso formula del PbCl2 =278.11 i grammi del sale che possono disciogliersi nella soluzione saranno: massa disciolta in 500 ml di soluzione = 278.16 · 1.03 · 10−3 = 0.286 g M. Rustici, Chimica di base 129 Equilibrio chimico È interessante osservare inoltre come la solubilità di un sale diminuisca per l’aggiunta di uno ione comune. Supponiamo ad esempio di confrontare la solubilità del cloruro di argento in acqua pura e in una soluzione 1 M di HCl. In acqua pura √ la solubilità del AgCl sarà certamente espressa dalla relazione Ks dato che [Cl− ] = [Ag+ ] = S, inoltre tenendo presente che il Ks = 1.7 · 10−10 otteremo che S = 1.3 · 10−5 . In una soluzione 1 M di HCl l’uguaglianza [Cl− ] = [Ag− ] perde la sua validità dato che la Cl− dovrà ritenersi molto maggiore della concentrazione [Ag+ ] e praticamente uguale a quella della concentrazione dell’acido cloridrico. Se volessimo essere rigorosi dovremmo dire che [Cl− ]totale = [Cl− ]AgCl + [Cl− ]HCl (10.17) ma essendo [Cl− ]AgCl ¿ [Cl− ]HCl possiamo scrivere che [Cl− ]totale ' [Cl− ]HCl Conseguentemente possiamo scrivere che KS = 1.7 · 10−10 = [Cl− ][Ag+ ] = [Cl− ] · S = 0.1 ∗ S da cui S = 1.7 · 10−10 /0.1 = 1.7 · 10−9 Si osserva pertanto che la solubilità del sale è diminuita drasticamente sotto l’effetto dello ione a comune. Ovviamente si dovrà tener conto della relazione non approssimata 9.16 nel momento in cui la concentrazione dello ione in comune è dello stesso ordine di grandezza della solubilità del sale in acqua pura. 10.4 Equilibri acido base In chimica, le definizioni di acido e base hanno subito diverse modifiche nel tempo, partendo da un approccio empirico e sperimentale fino alle più recenti definizioni, sempre più generali, legate al modello molecolare ad orbitali. • Teoria di Arrhenius: un acido è una sostanza che dissociandosi in acqua produce ioni H+ . Una base , invece, è una sostanza che dissociandosi in acqua produce ioni OH− HCl → H+ + Cl− NaOH → OH− + Na+ M. Rustici, Chimica di base 130 Equilibrio chimico Le proprietà acido base di una soluzione acquosa sono connesse ad un eccesso di ioni H+ eo di ioni OH− . Un acido si dice forte se è completamente dissociato, debole quando è parzialmente dissociato. Lo stesso vale per le basi. L’HCl è un acido forte e l’NaOH è una base forte viceversa l’acido acetico CH3 COOH è un acido debole. Una caratteristica essenziale degli acidi e le basi è quella che una volta mescolati questi si neutralizzano formando acqua secondo lo schema di reazione H+ + OH− → H2 O Ci sono sostanze che non posseggono direttamente protoni od ossidrili ma possono essere a loro volta chiamati acidi o basi se sono in grado di produrre tali ioni quando vengono mescolati con acqua. Ad esempio l’ammoniaca NH3 benchè non contenga direttamente ioni ossidrili è una base. Infatti a contatto con acqua dà luogo alla reazione NH3 + H2 O À OH− + NH+ 4 La teoria di Arrhenius non è valida per le dissociazioni che non avvengono in acqua. Possiamo pertanto introdurre una teoria più generale che comprende la vecchia teoria di Arrhenius ma risulta più generale. Si tratta della teoria di Brönsted-Lowry. • Teoria di Brönsted-Lowry: un acido è una sostanza capace di cedere ioni H+ ad un’altra specie chimica detta base. La teoria di Brönsted-Lowry estende la definizione di acido a quelle sostanze di cui non è possibile o non è pratico valutare il comportamento in acqua, come di fatto succede nella definizione data da Arrhenius. Introduce anche il concetto di complementarietà tra acido e base , dato che l’acido non è tale se non in presenza di una controparte cui cedere il proprio ione H+ . Secondo Brönsted e Lowry, quindi, anche composti che non presentano un carattere evidentemente acido nella quotidianità, come ad esempio gli alcoli, possono avere un comportamento acido quando sono in presenza di una base sufficientemente forte. Un esempio è la reazione tra metanolo e idruro di sodio, in cui il metanolo si comporta da acido, secondo la definizione di Brönsted e Lowry, cedendo allo ione idruro (la base) uno ione H+ CH3 OH + NaH → CH3 O− + H2 + Na+ Secondo questa teoria non esistono quindi acidi e basi a sé stanti, ma solo coppie di acido e base coniugati. Una coppia acido/base coniugata è una M. Rustici, Chimica di base 131 Equilibrio chimico coppia di specie chimiche che differiscono soltanto per uno ione H+ . Quando un acido cede uno ione H+ si trasforma nella sua base coniugata; quando una base acquista uno ione H+ si trasforma nel suo acido coniugato. Qualunque reazione che comporta il trasferimento di uno ione H+ da un acido a una base è una reazione acido-base secondo Brönsted e Lowry. Un acido può, in determinate circostanze, comportarsi da base e viceversa. • Teoria di Lewis: un acido è una sostanza capace di accettare un doppietto elettronico da un’altra specie chimica (detta base). Simile alla teoria di Brönsted-Lowry, sostituisce al trasferimento dello ione H+ il trasferimento in senso inverso di un doppietto elettronico. Secondo Lewis sono quindi acidi anche composti come il cloruro di alluminio ed il borano, che presentano nella loro struttura un orbitale vuoto capace di alloggiare un doppietto elettronico proveniente da una molecola donatrice, la base e legarsi quindi ad essa tramite un legame dativo. Il legame dativo non rappresenta altro che un legame covalente che nasce quando una doppietto elettronico viene ceduto ad un orbitale vuoto di un atomo accettore. Nell’esempio qui riportato, l’ammoniaca è la base ed il trifluoruro di boro è l’acido, secondo Lewis. NH3 + BF3 → H3 NBF3 Esercizio Supponendo di mescolare 80 ml di una soluzione 1 M di NaOH con 30 ml di una soluzione 1.2 M di H2 SO4 dire se la soluzione finale sarà acida o alcalina e calcolare la concentrazione finale. la reazione che ha luogo è la seguente 2NaOH + H2 SO4 → Na2 SO4 + 2H2 O Calcoliamo allora le moli dei due componenti reagenti ricordando che M = n/V n(NaOH) = M V = 1 · 0.08 = 0.08 n(H2 SO4 ) = M V = 1.2 · 0.03 = 0.036 osservando i rapporti stechiometrici della reazione chimica di neutralizzazione si osserva che 2 moli di idrossido di sodio necessitano una mole di acido solforico per avere una completa neutralizzazione. Allora avendo M. Rustici, Chimica di base 132 Equilibrio chimico 0.036 molti a H2 SO4 avremo bisogno per la completa neutralizzazione del sale nNaOH necessarie per neutralizzare l’acido = 0.036 · 2 = 0.072 avendo a disposizione 0.08 moli di NaOH è chiaro che rimarrà un eccesso di base e la soluzione risultante sarà basica. L’eccesso di base sarà allora nNaOH in eccesso = 0.08 − 0.072 = 0.008 Il volume finale risulta essere di 110 ml (80+30). Conseguentemente la concentrazione finale della base sarà pari a MNaOH = 10.4.1 n 0.008 = = 0.73 mol/l V 0.11 Prodotto ionico dell’acqua L’acqua pura allo stato liquido è un debole elettrolita soggetto alla seguente dissociazione 2H2 O À OH− + H3 O+ per tale equilibrio vale la legge di azione di massa per la quale [H3 O+ ][OH− ] K= [H2 O]2 Il valore della costante è molto minore di 1 e praticamente l’acqua risulta quasi completamente indissociata. Possiamo pertanto inglobare la concentrazione dell’acqua nella costante in modo tale da definire il prodotto ionico dell’acqua mediante una nuova costante Kw cosı̀ definita Kw = [H3 O+ ][OH− ] = 1.0 · 10−14 (10.18) a 250 C il prodotto ionico dell’acqua è pari a 1.0 · 10−14 . Nell’acqua la concentrazione degli ioni ossidrili è identica a quella dei protoni. Pertanto possiamo scrivere che [H3 O+ ] = [OH− ] quindi possiamo a sua volta scrivere che Kw = [H3 O+ ]2 = 1.0 · 10−14 M. Rustici, Chimica di base 133 Equilibrio chimico e quindi [H3 O+ ] = [OH− ] = 1.0 · 10−7 (10.19) Le concentrazioni ioniche risultano estremamente piccole rispetto alla concentrazione dell’acqua che risulta essere dell’ordine di 55.5 mol/l. L’introduzione del prodotto ionico dell’acqua ci permette di introdurre un’utile scala dell’acidità per le soluzioni acquose. Possiamo per prima cosa osservare che la condizione di neutralità è rappresentata dalla relazione 9.18. Nel caso di una soluzione di HCl 1M, applicando la relazione 9.17, si ricava che la concentrazione ionica degli ossidrili è 1·10−14 essendo quella degli idrogenioni pari a 1 M Viceversa per una soluzione 1 M di NaOH la concentrazione degli ossidrili sarà 1 M mentre quella idrogenionica sarà 1 · 10−14 . In altre parole per le soluzioni acquose la concentrazione idrogenionica che per semplicità inizieremo ad indicare con [H+ ] benchè sappiamo che tale ione si trova in realtà sotto forma di ione ossonio [H3 O+ ] sarà compresa nell’intervallo 1 ≤ [H+ ] ≤ 1 · 10−14 Possiamo tuttavia utilizzare una descrizione più comoda per la scala dell’acidità eliminando le potenze del 10 utilizzando una scala logaritmica. A tale proposito conviene definire il pH di una soluzione come il logaritmo in base 10 della concentrazione idrogenionica cambiato di segno. pH = − log[H+ ] (10.20) Ovviamente ciò può essere fatto solo se assumiamo che le concentrazioni idrogenioniche siano adimensionali, dato che l’operatore logaritmo è applicabile solo a quantità adimensionali. Tuttavia ricorderemo che tutte le concentrazioni espresse nelle costanti di equilibrio sono quantità adimensionali pertanto possiamo facilmente applicare tale operatore alla relazione 9.17. In questo modo possiamo scrivere che − log[H+ ] − log[OH− ] = − log Kw = − log(1.0 · 10−14 ) = 14 quindi pH + pOH = 14 (10.21) dove abbiamo definito pOH = − log[OH− ]. In questo modo la nuova scala dell’acidità sarà esprimibile come 0 ≤ pH ≤ 14. Le soluzioni con pH < 7 sono acide e quelle con pH > 7 sono alcaline. Attraverso questa definizione proviamo M. Rustici, Chimica di base 134 Equilibrio chimico a risolvere risolvere l’esercizio precedente chiedendo però di calcolare il pH della soluzione Esercizio Supponendo di mescolare 80 ml di una soluzione 1 M di NaOH con 30 ml di una soluzione 1.2 M di H2 SO4 dire se la soluzione finale sarà acida o alcalina e calcolare il pH della soluzione risultante. Il procedimento è identico fino al calcolo della concentrazione molare dell’idrossido di sodio. Ricordiamo che avevamo ottenuto che MNaOH = n 0.008 = = 0.73 mol/l V 0.11 Applicando allora la definizione di pOH possiamo scrivere pOH = − log[OH] = − log[0.73] = 0.137 applicando la relazione 9.20 otteniamo pH = 14 − 0.137 = 13.863 Pertanto il pH della soluzione è nettamente alcalino. 10.4.2 Acidi e basi deboli Il calcolo del pH o del pOH si complica leggermente quando dobbiamo valutarlo nel caso di acidi e basi deboli. Come abbiamo visto un acido o una base è detto debole quando non è completamente dissociato. La forza della dissociazione verrà valutata sulla base della costante di equilibrio. In generale se supponiamo di avere un acido debole di formula generica HA che si si dissocia secondo l’equazione HA À H+ + A− possiamo a sua volta scrivere la costante di equilibrio dell’acido come [H+ ][A− ] Ka = [HA] Nel caso siamo interessati a conoscere il pH di una soluzione acquosa di tale acido dobbiamo tener presente che per prima cosa è necessario calcolare la concentrazione idrogenionica totale la quale risulterà esprimibile come dovuta alla somma degli idrogenioni provenienti dall’acqua più quelli provenienti dall’acido. In altre parole dobbiamo scrivere che M. Rustici, Chimica di base 135 Equilibrio chimico [H+ ]tot = [H+ ]H2 O + [H+ ]HA che a sua volta possiamo riscrivere come [H+ ] = Kw Ka [HA] − + [OH ] [A− ] Questa equazione tuttavia in generale può essere enormemente semplificata a causa del fatto che in genere si tratta di valutare il pH di una soluzione di un acido debole con una costante di acidità nettamente superiore a quella dell’acqua. Se allora ci troviamo nell’assunzione in cui Ka À Kw il primo termine è trascurabile e l’equazione si riduce [H+ ] = Ka [HA] [A− ] Allora se con Ca definiamo la concentrazione dell’acido osservando la reazione di dissociazione possiamo anche scrivere che [HA] = Ca − [H+ ] e inoltre che [A− ] = [H+ ] Quindi [H+ ] = Ka (Ca − [H+ )] [H+ ] (10.22) questa espressione risulta allora facilmente risolubile, tuttavia si può ulteriormente semplificare quando Ca À [H]+ che costituisce la maggior parte dei casi. Quindi 9.21 si trasforma in una semplicissima formula per il calcolo immediato della concentrazione idrogenionica di un acido debole. [H+ ]2 = Ka Ca (10.23) EsercizioCalcolare il pH di una soluzione 0.1 M di acido acetico sapendo che Ka = 1.8 · 10−5 CH3 COOH À H+ + CH3 COO− Questo è il caso tipico in cui la concentrazione dell’acido Ca À [H+ ] pertanto possiamo risolvere il problema applicando direttamente la relazione 9.22. quindi [H+ ] = p Ka Ca ) = √ 1.8 · 10−5 · 0.1 = 1.34 · 10−3 da cui pH = − log[H+ ] = 3 − log(1.34) = 2.87 M. Rustici, Chimica di base 136 Equilibrio chimico Consideriamo ora un altro esempio relativo ad una base debole Esercizio100 ml di una soluzione 0.1 M di ammoniaca Kb = 1.8·10−5 vengono diluiti con 400 ml di acqua deionizzata. Calcolare il pH della nuova soluzione NH3 + H2 O À OH− + NH+ 4 Per prima cosa è necessario valutare la nuova concentrazione ammoniacale ottenuta dopo la diluizione con acqua. nNH3 = M V = 0.1 ∗ 0.1 = 0.01 dopo la diluizione la nuova molarità sarà M == [OH− ] = 0.01 n = = 0.02 V 0.5 √ p Kb Cb ) = 1.8 · 10−5 · 0.02 = 6 · 10−4 da cui pOH = − log[OH+ ] = 3.22 quindi pH = 14 − 3.22 = 10.78 10.4.3 Acidi poliprotici Gli acidi che possono rilasciare più di un protone si definiscono acidi poliprotici. In questo caso è necessario definire una costante di dissociazione per ogni stadio di dissociazione. Ad esempio per l’acido ortofosforico possiamo scrivere le seguenti dissociazioni. H3 PO4 À H+ + H2 PO− 4 + 2− H2 PO− 4 À H + H2 PO4 + 3− H2 PO2− 4 À H + PO4 le tre costanti di dissociazione acida sono: M. Rustici, Chimica di base 137 Equilibrio chimico [H+ ][H2 PO− 4] pKa1 = 2.12 [H3 PO4 ] [H+ ][HPO2− 4 ] Ka2 = pKa2 = 7.21 − [H2 PO4 ] [H+ ][PO3− 4 ] Ka3 = pKa3 = 12.68 − [H2 PO4 ] Ka1 = L’acido fosforico si comporta cosı̀ come un acido di media forza mentre per quanto concerne la seconda e la terza dissociazione si tratta di acidi debolissimi. In tutti gli acidi poliprotici le costanti acide di dissociazione diminuiscono in modo tale che pKa1 > pKa2 > pKa3 inoltre spesso si osserva che Kai /Ka(i+1) ' 105 questo implica che la concentrazione idrogenionica è data solo dalla prima dissociazione mentre le altre dissociazioni risultano trascurabili. Nel caso dell’acido solforico invece la prima dissociazione è quella di un acido forte mentre nella seconda dissociazione abbiamo un acido di media forza con una costante acida dell’ordine di 10−2 . In questo caso non possiamo trascurare la seconda dissociazione. Proviamo ad analizzare il tutto mediante un semplice esempio applicato all’acido solforico. EsercizioCalcolare il pH di una soluzione 0.2 M di acido solforico. Sapendo che l’acido è completamente dissociato nella prima dissociazione mentre mostra una Ka2 = 10−2 H2 SO4 → H+ + HSO− 4 + 2− HSO− 4 À H + SO4 Possiamo risolvere il problema applicando per prima cosa il bilancio di massa, attraverso il quale possiamo scrivere, assumendo che Ca sia la concentrazione analitica dell’acido, che 2− Ca = [HSO− 4 ] + [SO4 ] questo è dovuto al fatto che la concentrazione analitica dell’acido solforico deve coincidere con la somma delle concentrazioni di tutte le specie chimiche contenenti lo zolfo presenti in soluzione. Possiamo inoltre applicare il bilancio di carica. In altre parole per il fatto che la soluzione nel suo complesso debba essere elettricamente neutra possiamo scrivere che [H+ ] = [H+ ]Idissociazione + [H+ ]IIdissociazione + [H+ ]acqua M. Rustici, Chimica di base 138 Equilibrio chimico cioè 2− − [H+ ] = [HSO− 4 ] + 2[SO4 ] + [OH ] Tenendo presente che il prodotto ionico dell’aqua è molto più piccolo rispetto alla costante di dissociazione Ka2 possiamo trascurare gli idrogenioni provenienti dall’acqua e scrivere 2− [H+ ] = [HSO− 4 ] + 2[SO4 ] inoltre Ka2 = [H+ ][SO2− 4 ] = 10−2 − [HSO4 ] Se sottraiamo all’equazione relativa all’elettroneutralità quella del bilancio di massa possiamo scrivere che [H+ ] − Ca = [SO2− 4 ] sostituendo questo risultato nella relazione del bilancio di massa ottengo anche una relazione per [HSO− 4 ]. Cioè 2Ca − [H+ ] = [HSO2− 4 ] sostituendo i risultati ottenuti nella costante di equilibrio abbiamo Ka2 = [H+ ]([H+ ] − Ca ) = 10−2 2Ca − [H+] Abbiamo ottenuto cosı̀ un’equazione ad un’incognita che possiamo riscrivere nella forma [H+ ]2 − [H+ ](Ca − 10−2 ) − 2Ca 10−2 = 0 Dobbiamo pertanto semplicemente risolvere un’equazione di secondo grado e quindi avremo che + [H ] = (Ca − 10−2 ) + p Ca2 + 6 · 10−2 · Ca + 10−4 2 sostituendo il valore della concentrazione Ca otteniamo + [H ] = (0.2 − 10−2 ) + √ 0.22 + 6 · 10−2 · 0.2 + 10−4 = 0.204 2 M. Rustici, Chimica di base 139 Equilibrio chimico quindi pH = − log(0.204) = 0.69 Si osservi comunque che quando la Ca À 10−2 la concentrazione idrogenionica è praticamente identica a Ca . In questo caso si considera solo la prima dissociazione. Quando la Ca ¿ 10−2 allora [H+ ] = 2Ca . Se invece 0.5 < [H+ ] < 2 · 10−4 la concentrazione va calcolata attraverso la formula quadratica. In generale è sempre possibile calcolare la concentrazione idrogenionica di una soluzione acquosa di un acido poliprotico quando si conoscono le successive costanti di dissociazione dell’acido e la sua concentrazione totale. Per risolvere il problema è ovviamente necessario scrivere un sistema di equazioni indipendenti pari al numero delle concentrazioni incognite. Per far ciò è necessario utilizzare l’equazioni per le costanti di equilibrio, l’equazione del bilancio di massa e quella dell’elettroneutralità della soluzione. Di norma tali problemi a parte casi particolari si risolvono per approssimazioni successive. 10.4.4 Equilibri idrolitici Gli equilibri idrolitici sono gli equilibri che interessano le proprietà acido base degli ioni provenienti dalla dissociazione dei sali a seguito della loro reazione con acqua. Ci sono vari tipi di sali che possono dar luogo ad una variazione del pH a causa della loro dissoluzione in acqua. • Sali che provengono da un acido debole e una base forte del tipo KCN, CH3 COONa ecc. Consideriamo ad esempio il caso di un sale di formula generica MA che si dissoci in acqua generando ioni M+ e A− con una concentrazione salina pari Cs . Assumiamo inoltre che il sale derivi da una base forte e un acido debole. Il catione M+ non subirà in acqua nessun effetto se non quello associato alla solvatazione dello ione stesso. Viceversa l’anione A− provenendo da un acido debole in acqua darà luogo ad una tipica reazione di idrolisi. In altre parole provocherà la scissione della molecola di acqua con produzione dell’acido e necessariamente renderà la soluzione alcalina. Il tutto potrà essere schematizzato nel seguente modo A− + H2 O À HA + OH− La reazione di idrolisi sarà ovviamente legata alla costante di idrolisi dello ione associato A− . che possiamo scrivere nella forma M. Rustici, Chimica di base 140 Equilibrio chimico Kb = [HA][OH− ] [A− ] dove abbiamo omesso la concentrazione dell’acqua per il semplice fatto che tale concentrazione possiamo assumere che rimanga costante dato che solo una piccolissima quantità di acqua si idrolizzerà. Possiamo inoltre esprimere la costante di idrosi in relazione alla costante di acidità dell’acido coniugato. Se infatti moltiplichiamo e dividiamo per [H+ ] il numeratore e il denominatore della precedente equazione avremo potremo osservare che Kb = [HA][OH− ][H+ ] Kw = − + Ka [A ][H ] In questo tipo di problemi siamo interessati a conoscere il pH della soluzione risultante. Per ricavare quest’ultimo possiamo semplicemente valutarlo con diversi gradi di approssimazione a secondo della situazione in cui ci troviamo. In molti casi possiamo semplicemente assumere che [A− ] = Cs dato solo una piccola percentuale del sale si idrolizza. Inoltre trascurando la ionizzazione dell’acqua possiamo scrivere che [HA] = [OH− ] Sostituendo allora nella Kb otteniamo Kb = [OH− ]2 Kw = Cs Ka e quindi r − [OH ] = Kw Cs Ka Se invece vogliamo essere più rigorosi, dobbiamo partire dal bilancio di massa e dal bilancio di carica e scrivere che Cs = [A− ] + [HA] e Cs + [H+ ] = [A− ] + [OH− ] Se la concentrazione del sale è sufficientemente alta Cs À 10−6 la concentrazione protonica è sicuramente trascurabile e conseguentemente M. Rustici, Chimica di base 141 Equilibrio chimico Cs = [A− ] + [OH− ] e [A− ] = Cs − [OH− ] Possiamo inoltre ricavare che [HA] = [OH− ] e quindi sostituendo nella costante di idrolisi otteniamo [OH− ]2 Kw − = Ka Cs − [OH ] • Sali che provengono da un acido forte e una base debole del tipo NH4 Cl, AlCl3 ecc. In modo del tutto analogo possiamo ricavare le equazioni che ci permettono di valutare le concentrazioni idrogenioniche per sali di questo tipo e che daranno origine ad una reazione del tipo B+ + H2 O À BOH + H+ Utilizzando lo stesso procedimento possiamo scrivere in prima approssimazione che r + [H ] = Kw Cs Kb o altrimenti [H+ ]2 Kw + = Kb Cs − [H ] • Sali che provengono da un acido debole e una base debole del tipo NH4 CN, CH3 COONH4 ecc. In questo caso sia gli anioni che i cationi danno origine all’idrolisi secondo gli schemi di reazione B+ + H2 O À BOH + H+ A− + H2 O À HA + OH− M. Rustici, Chimica di base 142 Equilibrio chimico Per il bilancio di massa possiamo scrivere che Cs = [AH] + [A− ] = [B+ ] + [BOH] a sua volta per l’elettroneutralità della soluzione possiamo scrivere [H+ ] + [B+ ] = [A− ] + [OH− ] ∴ [H+ ] = [A− ] − [B+ ] + [OH− ] sostituendo in quest’ultima le espressioni ricavabili dal bilancio di massa possiamo scrivere [H+ ] = Cs − [HA] − Cs + [BOH] + [OH− ] = [BOH] − [HA] + [OH− ] Sostituendo i dati relativi alle costanti di equilibrio relativi all’acido e alla base coniugata abbiamo [H+ ] = [B+ ][OH− ] [A− ][H+ ] − + [OH− ] Kb Ka esprimendo tutto in funzione della concentrazione idrogenionica avremo [B+ ]Kw [A− ][H+ ] Kw [H ] = + + + − Ka Kb [H ] [H ] + quindi [H+ ]2 Ka Kb = [B+ ]Kw Ka − [H+ ]2 [A− ]Kb + Kw Ka Kb allora [H+ ]2 (Ka Kb + [A− ]Kb ) = [B+ ]Kw Ka + Kw Ka Kb trascurando l’ultimo termine che risulta essere molto più piccolo degli altri termini. Possiamo scrivere [H+ ]2 = [B+ ]Kw Ka (Ka Kb + [A− ]Kb ) M. Rustici, Chimica di base 143 Equilibrio chimico a sua volta Ka Kb ¿ [A− ]Kb quindi [H+ ]2 = [B+ ]Kw Ka +[A− ]Kb e tenendo inoltre presente che [B+ ] ' [A− ] otteniamo Kw Ka [H ] = Kb + 2 r ∴ + [H ] = Kw Ka Kb Possiamo osservare da questa espressione semplificata che in questi casi il pH praticamente risulta indipendente dalla concentrazione del sale. Inoltre possiamo notare che quando la costante di equilibrio dell’acido e della base sono praticamente identici (Kb ' Ka ) la concentrazione idrogenionica risulta uguale a 10− 7. In altre parole la soluzione risultante è neutra con un pH pari a 7. • Sali che provengono da una base forte e un acido debole poliprotico del tipo NaHCO3 , KHS, Na2 HPO4 ecc. Supponiamo di considerare un sale derivante da una base forte monoprotica BOH e un acido debole diprotico AH2 . In questo caso possiamo avere due tipi di sali BHA e B2 A. Il primo tipo di sale genera dopo la dissociazione in acqua ioni del tipo HA− che si idrolizzeranno secondo lo schema di reazione HA− + H2 O À H2 A + OH− inoltre lo ione HA− potrà agire anche come acido dissociandosi secondo lo schema di reazione HA− À A2− + H+ Se al solito con Cs indichiamo la concentrazione molare totale del sale, per il bilancio di massa possiamo scrivere Per il bilancio di massa possiamo scrivere che Cs = [H2 A] + [HA− ] + [A2− ] = [B+ ] M. Rustici, Chimica di base 144 Equilibrio chimico a sua volta per l’elettroneutralità della soluzione possiamo scrivere [H+ ] + [B+ ] = [HA− ] + 2[A2− ] + [OH− ] = Cs + [H+ ] Sottraendo la penultima equazione dall’ultima, si ha [H+ ] = [A2− ] − [H2 A] + [OH− ] inoltre abbiamo che Ka1 = [HA− ][H+ ] [A2− ][H+ ] e Ka2 = [H2 A] [HA− ] Utilizzando queste due espressioni assieme al prodotto ionico dell’acqua otteniamo [H+ ] = Ka2 [HA− ] [HA− ][H+ ] Kw + + − + Ka1 [H ] [H ] Se la concentrazione del sale non è troppo piccola possiamo trascurare la concentrazione di [A2− ] e [H2 A] rispetto alla concentrazione del sale Cs e scrivere semplicemente che Cs = [HA− ]. Cosı̀ facendo possiamo scrivere che [H+ ]2 = Ka2 Cs + Kw 1 + Cs /Ka1 quest’equazione tuttavia può essere ulteriormente semplificata ogni qual volta si verifica la condizione Cs À Ka1 . Allora in questo caso possiamo scrivere µ + 2 [H ] = Ka1 Kw Ka2 + Cs ¶ Un ulteriore semplificazione potrà essere fatta quando Ka2 À Kw /Cs , in questo caso otterremo [H+ ]2 = Ka1 Ka2 ∴ [H+ ] = p Ka1 Ka2 M. Rustici, Chimica di base 145 Equilibrio chimico Se si verifica la condizione Cs ¿ Ka1 questo implica che praticamente non si verifica l’idrolisi alcalina e quindi la concentrazione di ossidrili è trascurabile e pertanto il pH si calcola in modo da considerare solo la dissociazione acida. La condizione sopracitata implica infatti che Cs [HA− ] = ¿1 Ka1 Ka1 e quindi [HA− ] [H2 A] = ¿1 Ka1 [H+ ] Ossia che la dissociazione acida della specie [H2 A] è trascurabile rispetto a quella idrogenionica, cioò significa che la reazione di idrolisi della specie [HA− ] non avverrà. 10.4.5 Soluzioni tampone Si chiamano soluzioni tampone quelle soluzioni il cui pH non varia sensibilmente per l’aggiunta di un acido forte o una base forte. Consideriamo come esempio una soluzione di un acido debole che contenga contemporaneamente il sale dell’anione dell’acido stesso HA/A− . Un esempio potrebbe essere la coppia CH3 COOH/CH3 COO− . Per il caso specificato possiamo al solito scrivere la costante di equilibrio relativa all’acido, in altre parole Ka = [H+ ][A− ] [HA] La presenza in soluzione dell’anione dell’acido provocato dalla presenza del sale fa si che l’acido sia poco dissociato. Pertanto possiamo assumere che se Ca e Cs sono rispettivamente le concentrazioni dell’acido e del sale allora possiamo scrivere che Ca ' [HA] e Cs ' [A− ] allora la concentrazione idrogenionica sarà [H+ ] = Ka Ca Cs EsercizioCalcolare la variazione di pH associata a 500 ml di soluzione 0.1 M in CH3 COOH e 0.1 M CH3 COONa dopo che sono stati addizionati 100 ml di HCl 0.1 M sapendo che la Ka =1.85 · 10−5 . M. Rustici, Chimica di base 146 Equilibrio chimico Possiamo valutare subito il pH della soluzione iniziale applicando l’equazione relativa alle soluzioni tamponi e dato che il rapporto Ca /Cs = 1 avremo [H+ ] = Ka Ca = 1.85 · 10−5 Cs e quindi pH = − log(Ka ) = 5 − log(1.85) = 4.76 l’aggiunta di un acido forte come l’HCl farà sı̀ che una parte dello ione acetato si trasformi in acido acetico. Ovviamente se il numero di moli di acido forte introdotte nel sistema non supera quelle dello ione acetato la soluzione rimanente sarà ancora costituita dalla coppia CH3 COOH/CH3 COO− e possiamo pertanto supporre che il pH non subisca una grossa variazione. Calcoliamo allora il numero di moli delle singole componenti del sistema ni (CH3 COOH) = ni (CH3 COO− ) = M · V = 0.1 · 0.5 = 0.05 n(HCl) = M · V = 0.1 · 0.1 = 0.01 l’aggiunta dell’acido provocherà la seguente reazione CH3 COO− + H+ → CH3 COOH Allora possiamo scrivere che nf (CH3 COOH) = ni (CH3 COOH) + n(HCl) = 0.05 + 0.01 = 0.06 nf (CH3 COO− ) = ni (CH3 COO− ) = 0.05 − 0.01 = 0.04 allora essendo il volume finale pari a 600 ml o 0.6 l avremo che [CH3 COOH] = n/V = 0.06/0.6 = 0.1(M ) [CH3 COO− ] = n/V = 0.04/0.6 = 0.067(M ) riapplicando l’espressione per le soluzioni tamponi abbiamo [H+ ] = Ka Ca 0.1 = 1.85 · 10−5 = 2.76 · 10−5 Cs 0.067 da cui pH = − log([H+ ]) = 5 − log(2.76) = 4.56 la variazione di pH sarà pertanto ∆pH = 4.76 − 4.56 = 0.2 M. Rustici, Chimica di base 147 Equilibrio chimico 10.4.6 Capacità tamponante L’efficacia di una soluzione tampone può essere misurata in termini della sua capacità tamponante (β) che rappresenta la quantità di acido o base che si deve aggiungere per provocare una variazione unitaria di pH. La definizione formale della capacità tamponante è esprimibile come: β= dCb dCa =− dpH dpH (10.24) Dove Cb rappresenta la concentrazione della base aggiunta e Ca la concentrazione dell’acido aggiunto Se ad esempio in una soluzione tampone aggiungiamo un acido la concentrazione della base diminuirà e analogamente avremo una diminuzione del pH se invece dovessimo aggiungere una base avremo un aumento della concentrazione della base e un conseguente aumento del pH. Quindi la variazione associata a dCb e di dpH avrà sempre lo stesso segno, conseguentemente la capacià tamponante avrà sempre un segno positivo. Sulla base di questa definizione supponiamo di voler calcolare il potere tamponante di un tampone classico costituito da acido acetico e acetato di sodio. Supponiamo , per semplicità, di aggiungere lentamente, ad una soluzione acquosa di acido acetico, una base monobasica come l’idrossido di sodio. Per il principio dell’elettroneutralità delle soluzioni in ogni momento dovrà valere l’equazione seguente [CH3 COO− ] + [OH− ] = [Na+ ] + [H+ ] (10.25) Definiamo inoltre la concentrazione totale del tampone come C = [CH3 COO− ] + [CH3 COOH] (10.26) Ricordando inoltre la costante di dissociazione dell’acido Ka Ka = [CH3 COO− ][H+ ] [CH3 COOH] (10.27) Ricavando allora [CH3 COOH] dalla 10.27 e sostituendolo nella 10.26 otteniamo Ct = [CH3 COO− ][H+ ] + [CH3 COO− ] Ka o ancora M. Rustici, Chimica di base (10.28) 148 Equilibrio chimico [CH3 COO− ] = Ka Ct + [H ] + K (10.29) a Riscrivendo la 10.25 nella forma [Na+ ] = [OH− ] − [H+ ] + [CH3 COO− ] (10.30) Ricordando il prodotto ionico dell’acqua e utilizzando l’equazione 10.29 possiamo esprimere la 10.30 in funzione della concentrazione protonica, in altre parole otteniamo [Na+ ] = Kw Ka Ct − [H+ ] + + + [H ] [H ] + Ka (10.31) In ogni istante la concentrazione dello ione sodio deve essere descritta dall’equazione 10.31, a sua volta la concentrazione dello ione sodio può identificarsi con la concentrazione di base ( es NaOH) aggiunta Cb all’acido debole e quindi l’equazione 10.31 diventa Cb = Kw Ka Ct + − [H ] + [H+ ] [H+ ] + Ka (10.32) Tenendo inoltre presente che l’equazione 10.24 che definisce il potere tamponante può essere riscritta come β= dCb d[H+ ] d[H+ ] dpH (10.33) dove possiamo sostituire il risultato dell’equazione 10.32 e quindi ottenere d β= d[H+ ] µ Ka Ct Kw + − [H ] + [H+ ] [H+ ] + Ka ¶ d[H+ ] dpH (10.34) Per calcolare il potere tamponante espresso dall’equazione 10.34 dobbiamo pertanto calcolare il prodotto di due derivate. La seconda derivata risulta immediatamente valutabile come segue d[H+ ] d[H+ ] d[H+ ] =− = −2.303 = dpH d log[H+ ] d ln[H+ ] ricordando a sua volta che M. Rustici, Chimica di base 149 Equilibrio chimico Z 1 dx = ln x + c x ∴ d ln x = dx x quindi d[H+ ] d[H+ ] = −2.303[H+ ] = −2.303[H+ ] dpH d[H+ ] La 10.34 diventa cosı̀ d β= d[H+ ] µ Kw Ka Ct − [H+ ] + + + [H ] [H ] + Ka ¶ (−2.303d[H+ ]) (10.35) (−2.303[H+ ]) (10.36) derivando anche il primo termine otteniamo µ β= Kw Ka Ct − + 2 −1− + ([H ]) ([H ] + Ka )2 ¶ quindi µ β = 2.303 Ka Ct [H+ ] Kw + + [H ] + [H+ ] ([H+ ] + Ka )2 ¶ (10.37) I primi due termini non dipendono dalla presenza o meno di una soluzione tampone essi però ci dicono che nel caso ci trovassimo di fronte a soluzioni ad alti valori di pH (soluzioni fortemente basiche) o a bassi valori di pH (soluzioni fortemente acide) il potere tamponante della soluzione risulterebbe alto. In altre parole soluzioni fortemente acide o fortemente basiche sono resistenti alle variazioni di pH. L’ultimo termine invece è caratteristico delle soluzioni tamponi. Se riportiamo in un grafico il potere tamponante in funzione del pH (fig 10.1) osserviamo che l’equazione 10.37 mostra un massimo coincidente con il pKa dell’acido. M. Rustici, Chimica di base Figura 10.1. Potere tamponante del sistema tampone CH3 COOH 1M/CH3 COONa 1M in funzione del pH. Il massimo della curva si trova a pH 4.76 che corrisponde al valore del pKa Capitolo 11 Processi elettrochimici e reazioni redox 11.1 Processi elettrochimici e reazioni redox L’elettrochimica è lo studio dei processi che implicano una trasformazione di lavoro chimico in lavoro elettrico e viceversa. Se immergiamo una lamina di zinco metallico in una soluzione contenente ioni 2+ Cu , dopo un po’ di tempo possiamo osservare che la superficie della lamina, venuta a contatto con la soluzione, si è ricoperta di un sottile strato di rame metallico, mentre nella soluzione assieme agli ioni Cu2+ saranno presenti anche gli ioni Zn2+ . In altre parole è avvenuta la reazione Cu2+ + Zn Zn2+ + Cu (11.1) la quale non è altro che una reazione di ossidoriduzione che viene ottenuta dalla somma di due semireazioni: una di ossidazione, nella quale una specie chimica perde elettroni e una di riduzione, nella quale una specie chimica acquista elettroni. Possiamo schematizzare il tutto nella forma Zn Zn2+ + 2e 2+ Cu +2e Cu (11.2) (11.3) La somma di queste due equazioni ci fornisce la reazione complessiva. Questa reazione si verifica spontaneamente e questo implica che la reazione liberi una certa quantità di energia. Per una legge universale tutti i sistemi spontaneamente evolvono verso stati aventi un contenuto di energia minore e pertanto essi nel corso delle loro trasformazioni spontanee liberano energia. Se ad esempio facciamo avvenire questa reazione in un calorimetro (uno strumento capace di misurare le quantità di calorie messe in gioco) vediamo che se utilizziamo 31.77 g di CuSO4 e una quantità equivalente di polvere di Zn si svilupperanno 25700 cal. M. Rustici, Chimica di base 152 Processi elettrochimici e reazioni redox Figura 11.1. Questa stessa reazione può tuttavia essere fatta avvenire in un modo completamente diverso in modo tale da sviluppare, invece che energia chimica sotto forma di calore, energia elettrica. Possiamo realizzare un dispositivo, noto come pila Daniell, formato da due recipienti separati da un ponte salino (ponte che permette ai due recipienti di essere in contatto elettrico tramite ioni) contenenti l’uno una soluzione acquosa di ioni Zn2+ nella quale è immersa parzialmente una lamina di Zn metallico, e l’altro una soluzione acquosa di ioni Cu2+ nella quale è immersa parzialmente una lamina di rame metallico (Figura 10.1). Se colleghiamo le due lamine metalliche mediante un conduttore metallico nel quale è inserito un amperometro (capace di misurare il passaggio di una corrente elettrica), si potrà osservare che questo strumento misurerà il passaggio di elettricità. Se andiamo a verificare lo stato del sistema dopo che abbiamo osservato l’erogazione dell’energia elettrica, possiamo rilevare che sono avvenute le due reazioni di ossidoriduzione 10.2 e 10.3. Osserveremo infatti che la lamina di rame aumenterà di peso e viceversa quella di zinco diminuirà di peso. Le due reazioni sommate genereranno la reazione 10.1. Ognuno dei due elementi che costituiscono la pila sono detti semielementi. Praticamente tutte le reazioni redox spontanee possono generare energia elettrica. Se invece di sfruttare le reazioni per ottenere energia elettrica, fornissimo noi l’energia elettrica, invertendo la direzione del flusso elettronico, potremmo far avvenire la reazione inversa. È possibile perciò far avvenire anche reazioni non M. Rustici, Chimica di base Processi elettrochimici e reazioni redox 153 Figura 11.2. spontanee (elettrolisi). Chiamiamo catodo l’elettrodo sul quale avviene la riduzione, anodo quello su cui avviene l’ossidazione (esattamente come nell’elettrolisi). La ddp (differenza di potenziale) generata (a circuito esterno interrotto, altrimenti non la potremmo misurare poiché cambierebbe continuamente) è una misura della tendenza della reazione ad avvenire. In realtà non siamo in grado di misurare il potenziale assoluto di un singolo elettrodo, tuttavia possiamo assegnare per convenzione un potenziale di riferimento in modo da calcolare tutti gli altri. Per questo motivo viene scelto come potenziale di riferimento quello relativo alla semireazione 2H+ + 2e H2 (11.4) al quale assegnamo potenziale uguale a zero a tutte le temperature. L’elettrodo standard ad idrogeno è formato da una soluzione acquosa di ioni H+ in concentrazione 1 M (HCl 1M) in cui pesca una lamina di platino platinato sul quale gorgoglia idrogeno gassoso con pressione di 1 atmosfera (figura 10.2). Si può ricavare, mediante considerazioni termodinamiche, che il potenziale dell’elettrodo relativo ad una generica reazione di riduzione aOx + ne → bRid è esprimibile mediante la relazione di Nerst M. Rustici, Chimica di base (11.5) 154 Processi elettrochimici e reazioni redox E = E0 + RT [OX]a ln nF [Rid]b (11.6) Dove E 0 è il potenziale dell’elettrodo riferito all’elettrodo di idrogeno, n è il numero di elettroni scambiati nella semireazione, F il numero di Faraday cioè la carica elettrica totale uguale a 96500 C trasportata da un grammo equivalente di ioni. Un grammo equivalente o semplicemente un equivalente di ioni monovalente è numericamente uguale ad una mole di atomi, e cioè a un numero di Avogadro di atomi. Un equivalente di ioni monovalenti trasporta una carica elettrica totale di 96500 C. Nel caso di ioni bivalenti, un equivalente di essi è numericamente uguale alla metà di una mole, e cioè alla metà del numero di Avogadro. Infatti ogni ione bivalente trasporta una carica doppia di quella dell’elettrone. Pertanto la carica elettrica totale trasportata da un grammo equivalente di ioni, qualunque ne sia la valenza ionica, è sempre uguale a 96500 C. Questa quantità è denominata Faraday (F). Infine a e b sono i coefficienti stechiometrici della equazione di ossidoriduzione. Consideriamo ad esempio, il potenziale di riduzione di un semielemento galvanico relative alla reazione 2+ + MnO− + 4H2 O 4 + 8H + 5e Mn (11.7) allora il suo potenziale di riduzione sarà esprimibile come E = E0 + + 8 0.059 [MnO− 4 ][H ] ln 5 [Mn2+ ] (11.8) se invece avessimo considerato la reazione inversa cioè quella relativa al potenziale di ossidazione avremmo avuto che E = E0 − 11.1.1 + 8 0.059 [MnO− 4 ][H ] ln 5 [Mn2+ ] (11.9) Serie dei potenziali normali Collegando l’elettrodo standard di idrogeno con un elettrodo, nei quali le concentrazioni di equilibrio delle specie chimiche partecipanti alla reazione elettrodica siano unitari, e cioè nei rispettivi stati standard, e misurando la f.e.m. della pila cosı̀ formata è possibile determinare il potenziale standard E 0 di molte reazioni elettrodiche. Seguendo il criterio dei potenziali di riduzione della I.U.P.A.C. assegnamo per convenzione un potenziale negativo a quelle reazioni che tendono ad ossidarsi rispetto alla reazione dell’elettrodo standard ad idrogeno. Consideriamo M. Rustici, Chimica di base Processi elettrochimici e reazioni redox 155 ad esempio di costruire un pila utilizzando la semireazione relativa alla riduzione dello ione Zn+ Zn2+ + 2e → Zn (11.10) accoppiata a quella della riduzione dello ione H+ secondo lo schema 10.4. In valore assoluto la f.e.m. misurata è pari a 0.76 V. Sperimentalmente osserviamo che la semireazione 10.10 andrà in senso opposto a quello indicato cioè andrà nel senso dell’ossidazione mentre quello della reazione 10.4 andrà nel senso indicato cioè nel senso della riduzione. Assegneremo pertanto alla semireazione 10.10 un potenziale di riduzione negativo pari a -0.76. Da ciò si evince che se lo zinco metallico viene trattato con un acido come l’HCl questo subirà un attacco acido con la dissoluzione del metallo stesso e produzione di idrogeno gassoso. In altre parole i metalli con potenziale di riduzione negativo vengono attaccati (dissolti) dagli acidi. Se viceversa considerassimo la pila costituita dalla semireazione Cu2+ + 2e → Cu (11.11) e la reazione 10.4. Osserveremo una f.e.m pari a 0.34 V. In questo caso però la semireazione 10.11 avverrà nel senso indicato cioè secondo la riduzione mentre sarà la reazione 10.4 ad avvenire in senso opposto cioè secondo l’ossidazione. Assegneremo allora al ptetenziale elettrodico 10.11 un potenziale positivo paria a + 0.34 V. Questo implica che il rame metallico non subisce ossidazione da parte di un acido come l’HCl. In altre parole se trattiamo il rame metallico con l’acido cloridrico non succede nulla non si ha cioè dissoluzione del metallo stesso. Tutti i metalli con potenziale positivo rispetto all’idrogeno non subiscono ossidazione da parte degli acidi. La figura 10.3 mostra i potenziali standard di riduzione per una serie di comuni semireazioni a partire da potenziale più positivo a quello più negativo. Ricordiamo che le semireazioni con potenziale più positivo hanno la capacità di ossidare quelle con potenziale più basso. Dalla tabella vediamo ad esempio che la cop2+ pia MnO− ha un potenziale di +1.507 mentre quella del Fe3+ /Fe2+ ha un 4 /Mn potenziale di + 0.771. Questo ci porta a concludere lo ione MnO− 4 in ambiente 2+ acido ha una capacità ossidante rispetto allo ione Fe . Ci aspettiamo pertanto che abbia luogo la seguente reazione 2+ MnO− + 8H+ Mn2+ + 5Fe3+ + 4H2 O 4 + 5Fe (11.12) I potenziali standard di riduzione ci permettono cosı̀ di prevedere l’andamento delle reazioni chimiche. Questo ovviamente vale in generale perchè non sempre viene rispettato quello che possiamo prevedere. M. Rustici, Chimica di base Figura 11.3. Capitolo 12 Cinetica chimica 12.1 Velocità di reazione Consideriamo una generica reazione del tipo AP (12.1) e supponiamo di voler esaminare la velocità del processo di reazione. Possiamo pertanto misurare le concentrazioni del reagente A in due istanti successivi di tempo (t1 e t2 con t2 > t1 ) che possiamo indicare con [A]1 e [A]2 . Possiamo definire la velocità media nell’intervallo considerato come [A]2 − [A]1 ∆[A] = t2 − t1 ∆t (12.2) poiché [A]2 < [A]1 affinché si possa assegnare alla velocità un valore positivo mettiamo un segno negativo quindi possiamo esprimere la velocità v come v=− ∆[A] ∆t (12.3) se volessimo esprimere la velocità della reazione in funzione del prodotto di reazione allora dovremmo scrivere v= ∆[P] ∆t (12.4) in questo caso con il segno positivo dato che [P]2 > [P]1 . La velocità che abbiamo indicato corrisponde ovviamente ad una velocità media mentre noi vogliamo conoscere la velocità istantanea che potremmo valutare cercando di rendere il ∆t sempre più piccolo. In termini matematici quando M. Rustici, Chimica di base 158 Cinetica chimica ∆t → 0 il limite del rapporto incrementale definito dalla relazione 11.3 e 11.4 diventa una derivata. possiamo, cosı̀, esprimere la velocità della reazione come v=− d[A] d[P] = dt dt (12.5) Ovviamente, data una generica reazione, la velocità può essere espressa per qualunque componente a nostra scelta. La situazione si può leggermente complicare quando la stechiometria della reazione, che stiamo considerando, non è espressa mediante rapporti unitari. Se ad esempio consideriamo una generica reazione del tipo aA + bB cC + dD dove A,B,C,D rappresentano i reagenti e i prodotti mentre a, b, c e d rappresentano i coefficienti stechiomentrici possiamo chiederci quale sia il modo più conveniente per definere la velocità di reazione, tenendo ben presente che essa deve essere la stessa per qualunque specie chimica che vogliamo considerare. Per tale motivo è necessario definire la velocità di reazione come v=− 1 d[A] 1 d[B] 1 d[C] 1 d[D] =− = = a dt b dt c dt d dt Cosı̀ facendo la velocità di reazione è la stessa per qualunque specie chimica considerata all’interno della reazione Supponiamo, ad esempio, di voler esprimere la velocità di reazione per i rispettivi componenti per la reazione di ossidazione dell’anidride solforosa 2SO2 + O2 SO3 (12.6) scriveremo in questo caso v=− 12.1.1 1 d[SO2 ] d[O2 ] 1 d[SO3 ] =− = 2 dt dt 2 dt (12.7) Le leggi base della cinetica Si osserva sperimentalmente che la velocità di reazione, a temperatura costante, è funzione delle concentrazioni delle sostanze presenti nel sistema di reazione. I prodotti di reazione possono a sua volta influire sulla velocità aumentando (effetto autocatalitico) o diminuendo la velocità (inibizione). Quando invece la velocità è influenzata da sostanze esterne alla reazione e che rimangono inalterate al termine M. Rustici, Chimica di base 159 Cinetica chimica del processo chimico parliamo di catalisi. In generale, comunque, non è possibile esprimere l’equazione di velocità sulla base della stechiometria della reazione, la dipendenza della velocità dalle concentrazioni può essere determinata solo sperimentalmente. Possiamo osservare, ad esempio, come reazioni aventi la stessa stechiometria possono avere una dipendenza dalle concentrazioni totalmente diversa. La reazione tra idrogeno e vapori di bromo o vapori di iodio decorre con una diversa cinetica benché la stechiometria sia la stessa H2 + I2 2HI H2 + Br2 2HBr d[HI] = k[H2 ][I2 ] dt d[HBr] [H2 ][Br2 ]1/2 =k dt 1 + k0 [HBr] [Br]2 La differenza evidenziata nell’equazione cinetica implica un diverso meccanismo di reazione, da ciò segue come lo studio sperimentale della cinetica chimica sia usato per determinare i meccanismi attraverso i quali le reazioni avvengono. La dipendenza della velocità di reazione dalle concentrazioni è complessa e viene determinata sperimentalmente. La velocità di ogni reazione è ad ogni istante proporzionale al prodotto delle concentrazioni dei reagenti elevate ad una potenza uguale al numero di molecole di ogni specie partecipanti al processo Consideriamo la seguente reazione A + B → Prodotti (12.8) e supponiamo che la stechiometria corrisponda alla molecolarità della reazione stessa,cioè che la reazione avvenga attraverso l’urto diretto di una molecola A con una molecola B. Allora, se questo è il caso, possiamo esprimere la velocità di formazione del prodotto come v = k[A][B] Assumeremo cosı̀ che questa reazione sia del secondo ordine. Dove definiamo per ordine di reazione la somma degli esponenti della [A] e [B]. Dato che ogni concentrazione è elevata a 1 l’ordine di reazione sarà 1+1=2. Non dobbiamo tuttavia confondere gli esponenti delle concentrazioni con i coefficienti stechiometrici. Questi ultimi si identificano con gli esponenti solo quando la stechiometria della reazione corrisponde alla molecolarità della reazione. Consideriamo ad esempio una tipica reazione organica che conduce alla formazione di un alcol partendo da un alogenuro alchilico per trattamento con un idrossido. La stechiometria della reazione può essere riassunta nella forma M. Rustici, Chimica di base 160 Cinetica chimica RCl + OH− → ROH + Cl− (12.9) Considerando la stechiometria della reazione noi dovremmo immaginare che la velocità di reazione del prdotto (alcool) sia del secondo ordine e sia esprimibile come v = k[RCl][OH− ] Sperimentalmente si osserva che a secondo delle proprietà del solvente, in cui viene fatta avvenire la reazione, e in relazione alle proprietà del gruppo alchilico (R) la reazione può essere del primo, del secondo ordine o intermedia. Proprio lo studio della cinetica sperimentale ci permette infatti di capire quale sia il meccanismo della reazione e quindi la sua molecolarità. Nel caso la reazione sia del secondo ordine possiamo pensare che la reazione abbia luogo tramite gli urti tra le molcecole del’alcol con quello degli iono ossidrili e in questo caso la reazione prosegua con un molecolarità indicata dalla stechiometria della 12.9. Quando viceversa la reazione procede con ordine 1 dobbiamo postulare un meccanismo alternativo. Ad esempio si possiamo assumere il seguente meccanismo RCl→ R+ + Cl− R+ +OH− → ROH Il primo processo è lento e favorito da solventi che facilitano la separazione di cariche e a sua volte è possibile quando il carbiocatione che si forma è sufficientemente stabile. Il secondo processo risulta invece un processo velocissimo. É ovvio che la velocità di reazione sia influenzata solo dalla stadio lento della reazione e allora essendo il primo stadio quello determinante, la velocità dipenderà solo dalla concentrazione dell’alogenuro alchilico. In altre parole possiamo scrivere v = k[RCl] cioè abbiamo una reazione del primo ordine Questi due casi che abbiamo indicati costituiscono solo dei casi limite e pertanto è anche possibile ottenere situazioni in cui la velocità di reazione risulta essere intermedia ai due casi esaminati e questo si verificherà tutte quelle volte che entrambi i meccanismi sono plausibili. Lo studio della cinetica chimica permette cosı̀ di studiare il meccanismo di reazione. Quest’ultimo può essere a sua volta utilizzato per costruire il modello che a sua volta genererà un ordine di reazione. L’ordine teorico dovrà essere con buona approssimazione uguale al valore sperimentale cosı̀ che sia possibile individuare il modo con cui la reazione avviene. M. Rustici, Chimica di base 161 Cinetica chimica Raramente una reazione si compie nel modo suggerito dall’equazione chimica bilanciata. In genere, la reazione complessiva è la somma di diversi stadi; la sequenza degli stadi con la quale avviene una reazione è detta meccanismo della reazione. Conoscere il meccanismo della reazione significa conoscere il modo in cui le molecole si avvicinano l’una all’altra durante una collisione, il modo in cui si rompono e si formano legami chimici, il modo in cui si trafersicono le cariche e cosı̀ via. 12.1.2 Cinetica del primo ordine Le cinetiche del primo ordine rappresentabili secondo uno schema del tipo A→P sono comuni dinamiche che caratterizzano sistemi chimici, fisici o biologici. per mezzo dell’equazione 11.5 e per la definizione di processo del I ordine possiamo scrivere d[A] = −k[A] dt (12.10) d[A] = −kdt [A] (12.11) e separando le variabili questa equazione può essere immediatamente integrata conducendoci al risultato [A] = [A]0 e−kt ∴ [A] = e−kt [A]0 (12.12) L’equazione 11.11 mostra cosı̀ che la concentrazione del componente che si consuma secondo una cinetica del primo ordine diminuisce esponenzialmente nel tempo. I decadimenti radioattivi sono tipici esempi con cinetica del primo ordine. L’isotopo 14 6 C è un isotopo instabile e viene sfruttato per la datazione di reperti archeologici. La reazione nucleare di decadimento è cosı̀ schematizzabile 14 6 C →14 7 N+β M. Rustici, Chimica di base 162 Cinetica chimica dove l’emissione β si riferisce ad un elettrone. L’emissione β si ha quando un neutrone si trasforma in un protone e ciò comporta l’emissione di un elettrone. Gli isotopi che hanno un rapporto tra protoni e neutroni vicino ad 1 sono molto stabili mentre quelli che superano 1 sono instabili. L’isotopo 14 6 C ha un rapporto ha un rapporto pari ad 8/6 cioè di 1.333 che è al di fuori del rapporto di stabilità e pertanto tende a disintegrarsi. Al contrario l’isotopo più abbondante in natura il 12 6 C ha un rapporto pari a 1 ed è quindi stabile. In generale si osserva che la zona di stabilità è intorno ad 1 per gli elementi leggeri mentre per gli elementi pesanti il rapporto di stabilità si aggira intorno a 1.5-1.6. Negli strati superiori 14 dell’atmosfera il 14 6 C tende a riformarsi a partire dal 7 N in questo modo la concentrazione del 14 6 C rimane pressoché costante nel tempo e viene incorporato nella anidride carbonica e attraverso la fotosintesi, negli organismi viventi, pertanto, finché gli organismi rimangono in vita la concentrazione del 14 6 C rimane costante. Invece dopo la morte inizia a decadere radioattivamente e la concentrazione del 14 14 6 C diventa via via più piccola. Il tempo di dimezzamento t1/2 del 6 C, cioè il tempo necessario affinché la sua concentrazione diventi la metà è di 5715 anni. Possiamo allora sfruttare questa conoscenza per risalire all’età di un determinato reperto archeologico. Supponiamo che un determinato reperto archeologico mostri una radiattività pari al 40% rispetto a quello di un organismo vivente. Se allora indichiamo con N il numero di isotopi di 14 6 C del reperto archeologico e N0 quello di un organismo vivente, allora N/N0 = 0.4. Per la 11.12 possiamo scrivere [N] = 0.4 = e−kt [N]0 (12.13) al tempo di dimezzamento possiamo il rapporto [N]/[N]0 deve necessariamente essere 1/2. Pertanto 1 = e−kt1/2 2 ∴ k= ln(2) t1/2 (12.14) nel caso specifico sostituendo il valore del tempo di dimezzamento si trova che k = 1.21 · 10− 4. Utilizzando questo dato nella 11.13 otteniamo che l’età del reperto è intorno a 7555 anni. 12.2 Effetto della temperatura sulla velocità di reazione Come è noto la maggior parte dei processi chimici, con rare eccezioni, aumenta rapidamente con la temperatura. É esattamente per questa ragione che il riscaldamento è ampiamente usato nella pratica chimica. Ricordando che la velocità di reazione è esprimibile come M. Rustici, Chimica di base 163 Cinetica chimica v = kCAp CBq · · · (12.15) la temperatura può, in principio, avere un effetto modificando, le concentrazioni, gli esponenti p, q, . . . e infine la costante di velocità k. Gli esperimenti mostrano che i primi due fattori sono insignificanti per la variazione della velocità, viceversa la costante di velocità subisce rilevanti cambiamenti rispetto alla variazione della temperatura. Questa è la ragione per cui quando parliamo di effetto della temperatura sulla velocità di reazione è implicito una variazione della costante di velocità. Se definiamo il coefficiente di temperatura come l’inverso del rapporto tra la costante di velocità ad una data temperatura T rispetto a quello di una temperatura T + 100 (kT +10 /kT ) possiamo scrivere la regola empirica per la quale i coefficienti di temperatura per le reazioni chimiche sono nell’intervallo compreso tra 2 e 4. In altre parole un incremento della temperatura di 100 implica che la velocità può variare da 2 a 4 volte. La dipendenza della costante di velocità dalla temperatura è ben espressa dall’equazione di Arrhenius esprimibile nella forma ln k = − B +C T (12.16) dove i termini B e C sono assunti costanti specifiche per una determinata reazione e indipendenti dalla temperatura. L’equazione 12.16 derivata da Arrhenius è giustificata da un grande insieme di dati sperimentali. Questa equazione può essere derivata teoricamente sulla base di certe premesse termodinamiche attraverso le quali possiamo ottenere che ln k = − EA +C RT (12.17) passando all’esponenziale, otteniamo k = e−EA /RT+C ∴ k = eC e−EA /RT (12.18) definendo A = eC come fattore preesponenziale si ottiene k = Ae−EA /RT (12.19) dove EA viene definita come energia di attivazione. Da qui si osserva che, fissata la temperatura, tanto più piccola è l’energia di attivazione e tanto maggiore sarà la velocità alla quale avviene la reazione. Questa considerazione porto Arrhenius a interpretare il processo di reazione come il risultato di collisioni tra due M. Rustici, Chimica di base 164 Cinetica chimica o più molecole durante le quali alcuni legami si indeboliscono mentre altri iniziano a formarsi. Possiamo allora ipotizzare che prima dell’effettiva formazione dei prodotti si possa immaginare l’esistenza di un intermedio, detto complesso attivato. L’energia di attivazione può allora essere interpretata come l’energia richiesta affiché si possano raggiungere collisioni efficaci capaci di portarci alla formazione di tale complesso. Solo le molecole che posseggono questa energia o un energia superiore possono avere la possibilità di dar luogo al complesso attivato e quindi alla formazione dei prodotti. In particolare le sostanze che hanno la capacità di abbassare l’energia di attivazione prendono il nome di catalizzatori. In altre parole essi sono sostanze che non modificano l’equilibrio ma permettono di raggiungere prima la condizione di equilibrio aumentando la velocità di reazione nei due sensi. 12.3 Reazioni catalizzate da enzimi Gli enzimi sono grandi molecole proteiche, con un peso molecolare compreso nell’intervallo tra 104 -105 , che presentano un elevato effetto catalitico per un ampia varietà di reazioni di importanza biologica. La dimensione degli enzimi rispetto alla dimensione delle piccole molecole coinvolte nella catalisi enzimatica ci induce a chiederci se tale processo catalitico può essere annoverato tra le reazioni omogenee o eterogene. In realtà la distinzione è arbitraria e le reazioni enzimatiche possono essere associate ad entrambi i tipi di catalisi omogenea ed eterogena. Per gli enzimi che hanno dimensione inferiore a 100 Å non è irragionevole trattare questi come grandi molecole in soluzione. Si assume generalmente che gli enzimi abbiano una o più regioni, detti siti attivi, dove i reagenti sono assorbiti e sono soggetti all’attività catalitica. L’equazioni cinetiche per le attività enzimatiche furono sviluppate sopratutto da Michaelis e Menten, le equazioni per un dato enzima dipenderanno ovviamente dal tipo di reazione chimica coinvolta. Nel caso più semplice in cui si consideri una semplice reazione unimolecolare del tipo S→P dove S è la molecola reagente chiamata comunemente, dagli enzimologi, substrato e P è il prodotto della reazione. Il più semplice meccanismo ipotizzabile per la reazione catalizzata dall’enzima è il seguente E + S À ES ES → E + P Dove ES è il complesso costituito tra l’enzima (E) e la molecola del substrato. Naturalmente l’enzima accelera la reazione in intrambi i sensi ma la rimozione del M. Rustici, Chimica di base 165 Cinetica chimica prodotto (P) fa si che la reazione proceda nella direzione dei prodotti. Definendo con k1 e k−1 la costante di associazione e dissociazione dell’enzima con il substrato e con k2 la kostante di velocità per la reazione che porta al prodotto possiamo esprimere la velocità di scomparsa di ES come d[ES] = k1 [E][S] − k−1 [ES] − k2 [ES] dt (12.20) L’enzima è tipicamente presente in piccole concentrazioni cosı̀ che la concentrazione ES raggiungerà uno stato stazionario rendendo la concentrazione ES costante. In altre parole la concentrazione del complesso ES non dipenderà dal tempo e la sua derivata sarà nulla, di conseguenza la 13.20 assumerà la forma k1 [E][S] − k−1 [ES] − k2 [ES] = 0 (12.21) e quindi [ES] = k1 [S] [E] k−1 + k2 (12.22) Supponendo che la concentrazione iniziale dell’enzima sia [E]0 , [E] rappresenti quella dell’enzima libero ed infine [ES] quella dell’enzima legato allora il bilancio di massa impone [E]0 = [ES] + [E] quindi [E] = [E]0 − [ES] (12.23) sostituendo la 13.23 nella 13.22 otteniamo [ES] = k1 [S] ([E]0 − [ES]) k−1 + k2 (12.24) k1 [S][E]0 k−1 + k2 + k1 [S] (12.25) da cui [ES] = Possiamo allora esprimere la velocità di reazione, per quanto concerne la formazione del prodotto P, come M. Rustici, Chimica di base 166 Cinetica chimica v= d[P] = k2 [ES] dt (12.26) Sostituendo nella 13.26 il risultato ottenito nella 13.25 possiamo scrivere v= k1 k2 [S][E]0 k−1 + k2 + k1 [S] (12.27) dividendo numeratore e denominatore per k1 otteniamo v= k2 [S][E]0 [S] + (k−1 + k2 )/k1 (12.28) Definiamo allora km = k−1 + k2 k1 (12.29) come la costante di Mikaelis-Menten e riscriviamo la 13.28 come v= k2 [E]0 [S] [S] + km (12.30) L’equazione 12.30 è l’equazione di un iperbole rettangolare, un equazione analoga si ottiene per il legame tra ossigeno e mioglobina. Matematicamente questa equazione presenta due asintoti, uno parallelo all’asse [S] nel punto v0 = vmax e l’altro parallelo all’asse v0 nel punto [S]=−km . Questa espressione è in accordo con le osservazioni sperimentali. In particolare si osserva che per alti valori del substrato [S] >> km ] e la 12.30 assume la forma di un’equazione del primo ordine vmax = k2 [E]0 (12.31) Possiamo pertanto risecrivere la 13.30 come v= vmax [S] [S] + km (12.32) in questo caso la velocità di reazione non dipende più dalla concentrazione del substrato e k2 [E0 ] rappresenta la velocità massima ottenibile che si verifica quando l’enzima è saturato, in altre parole quando tutte le molecole sono legate con il substrato S. Numerosi fenomeni biologici esibiscono cinetiche saturanti e l’espressione 13.32 manifesta proprio questa proprietà caratteristica. M. Rustici, Chimica di base Capitolo 13 Stechiometria esercizi tipici 13.1 Mole Ricordiamo che la mole rappresenta la quantità di sostanza che contiene un numero di molecole, ioni atomi o particelle pari al numero di Avogadro (6.022 · 1023 ). 1. Consideriamo la seguente reazione chimica AgNO3 + NaCl → AgCl + NaNO3 Quanti grammi di NaCl e di AgNO3 sono necessari per preparare 10 grammi di AgCl? Per prima cosa calcoliamo il numero di moli (n) associate a 10 g di AgCl. Tenendo presente che il Peso Formula (PF) del AgCl è pari a 143.5 avremo che n= g 10 = = 0.70 PF 143.5 Dalla stechiometria della reazione vediamo che i rapporti stechiometrici dei rispettivi componenti sono di 1:1:1:1 in altre parole per preparare 1 mole di AgCl sono necessarie 1 mole di AgNO3 e una mole di NaCl. Allora nel caso specifico saranno necessarie 0.7 moli di AgNO3 e 0.7 moli di NaCl. pertanto avremo: g(AgNO3 ) = n · PF(AgNO3 ) = 0.7 · 170 = 119g g(NaCl) = n · PF(NaCl) = 0.7 · 58.5 = 40.95g M. Rustici, Chimica di base 168 Stechiometria esercizi tipici 2. Consideriamo la seguente reazione chimica H2 SO4 + 2NaOH → Na2 SO4 + 2H2 O Calcolare quanti grammi di NaOH sono necessari per neutralizzare completamente 20 g di H2 SO4 ? Per prima cosa calcoliamo il numero di moli di H2 SO4 . Essendo il peso molecolare PM pari a 98 avremo che nH2 SO4 = g 20 = = 0.2 PM 98 Dalla stechiometria della reazione si osserva che per far reagire completamente 1 mole di H2 SO4 sono necessarie 2 moli di NaOH. In altre parole il numero di moli di NaOH dovrà sempre essere il doppio di quello del H2 SO4 . Nel caso specifico avremo che nNaOH = 2 · nH2 SO4 = 2 · 0.2 = 0.4 allora i grammi necessari di NaOH potranno essere calcolati moltiplicando il numero di moli corrispondenti con il peso formula (PF) dell’idrossido di sodio. gNaOH = n · P F (NaOH) = 0.4 · 40 = 16 g 3. Supponiamo che sia possibile preparare il solfuro ferrico a partire dai suoi elementi secondo la seguente reazione: 2Fe + 3S → Fe2 S3 Supponiamo inoltre di partire da 40 g di zolfo (S) e da 50 g di ferro (Fe). Ci chiediamo, supponendo che la resa della reazione sia del 100%, quanti grammi di solfuro ferrico possiamo ottenere e nel caso se c’è un eccesso di qualche reagente e quanto ne rimane al termine della reazione? Per prima cosa calcoliamo il numero di moli di S e di Fe. Tenendo conto che i rispettivi pesi atomici (PA) sono rispettivamente di 32 e 55.8, il numero di moli sarà dato da: nFe = g 50 g 40 = = 0.89nS = = = 1.25 PA 55.8 PA 32 M. Rustici, Chimica di base 169 Stechiometria esercizi tipici Conviene risolvere il problema costruendo una tabella in cui sotto i rispettivi componenti della reazione scriviamo le moli iniziali e sotto ancora le moli finali. moli iniziali moli finali 2Fe 3S 0.89 1.25 → Fe2 S3 0 Per il calcolo delle moli finali dobbiamo prestare attenzione ai coefficienti stechiometrici e metterci nelle condizioni di cercare, nel caso che questo esista, il componente in difetto. È ovvio che il componente in difetto regola la quantità dei prodotti perché non si può creare un composto a partire dal nulla. Una volta che il componente in difetto è terminato la reazione si arresta. Per valutare il componente in difetto possiamo andare per tentativi. Consideriamo allora le moli iniziali descritte nella tabella e focalizziamoci, ad esempio, sul Fe. Dalla stechiometria della reazione osserviamo che sono necessarie 2 moli di Fe e 3 moli di S per generare una mole di solfuro ferrico. Possiamo altresı̀ osservare che da 1 mole di Fe saranno necessari 3/2 di mole di S per generare 1/2 di mole di solfuro ferrico. La tabella mostra che se abbiamo a disposizione 0.89 moli di Fe allora, affinché il Fe reagisca completamente, saranno necessari (3/2 · 0.89 = 1.335) moli di S. Osservando la tabella vediamo che nel caso da noi indicato abbiamo a disposizione solo 1.25 moli di S. Questo significa che i reagenti non sono espressi in condizioni stechiometriche e dato che 1.25 < 1.335 significa che la quantità di S è in difetto rispetto alla quantità teorica che sarebbe necessaria per far reagire tutto il Fe. Conseguentemente lo S è il componente in difetto e il Fe è il componente in eccesso. A questo punto possiamo chiederci quale sarà la quantità teorica di Fe che necessaria affinché tutto lo S reagisca completamente. Dalla reazione si osserva che 3 moli di S reagiscono che 2 moli di Fe per dar luogo ad una mole solfuro ferrico. Altresı̀ possiamo osservare che per far reagire completamente una mole S saranno necessari 2/3 di mole di Fe. Dalla tabella sappiamo che abbiamo a disposizione 1.25 moli di S, pertanto affinché tutto lo zolfo a disposizione reagisca completamente saranno necessari 1.25 · 2/3 = 0.833 moli di Fe. Dato che la quantità di Fe è in eccesso rispetto allo S ed è pari a 0.89, alla fine della reazione il Fe rimasto sarà esprimibile come la differenza tra la quantità iniziale e la quantità che ha reagito, cioè 0.89-0.833=0.057. Lo S ovviamente reagirà completamente e sparirà dalla miscela di reazione. Ricordando che il prodotto finale è regolato dal componente in difetto, cioè dallo S, possiamo osservare che da 3 moli di S si ottengono 1 mole di solfuro M. Rustici, Chimica di base 170 Stechiometria esercizi tipici ferrico. Pertanto da 1 mole di S si ottengono 1/3 di mole di solfuro ferrico e quindi da 1.25 moli di S si otterranno (1.25/3=0.42) moli di solfuro ferrico. Questi dati possono essere riassunti nella tabella in modo da ottenere moli iniziali moli finali 2Fe 3S 0.89 0.89-0.833=0.057 1.25 0 → Fe2 S3 0 0.42 Moltiplicando le moli di solfuro ferrico per il suo peso formula possiamo ricavare i grammi corrispondenti che si formano dalla reazione. gFe2 S3 = n · PF(Fe2 S3 ) = 0.42 · 207.7 = 87.23 g 4. 3.000 g di una miscela di ossido rameoso e di ossido rameico, trattati con un eccesso di un opportuno riducente, si trasformano in 2.550 g di rame metallico. Determinare la composizione della miscela di partenza , esprimendola come percentuale in peso dei due componenti. Per prima cosa ci troviamo di fronte a due processi chimici che trasformano i nostri due ossidi attraverso una reazione di riduzione in rame metallico. Benché non si conosca la reazione possiamo sempre comprendere quali siano i rapporti stechiometrici tra gli ossidi e il rame metallico. Schematicamente possiamo scrivere che Cu2 O → 2Cu CuO → Cu dai rapporti stechiometrici possiamo scrivere che nCu(totali) = nCu(processo1) + nCu(processo2) possiamo ora esplicitare le moli di rame del processo 1 e del porcesso 2 in funzione delle moli dell’ossido rameoso e dell’ossido rameico. Dalla stechiometria del processo è chiaro che nCu(processo1) = 2nCu2 O e nCu(processo2) = nCuO e quindi M. Rustici, Chimica di base 171 Stechiometria esercizi tipici nCu(totali) = 2nCu2 O + nCuO le moli di rame possono essere direttamente valutate dalla definizione di mole n = g/P M cioè nCu(totali) = 2.550 = 0.0401 63.5 sostituendo questo risultato possiamo scrivere 0.0401 = 2nCu2 O + nCuO Dalla conoscenza del fatto che la miscela di ossidi pesa 3.00 grammi possiamo scrivere che 3.00 = gCu2 O + gCuO ed esprimendo i grammi dei rispettivi ossidi in funzione del peso molecolare e del numero di moli possiamo scrivere che 3.00 = nCu2 O PMCu2 O + nCuO PMCuO sostituendo i rispettivi valori dei pesi molecolari otteniamo 3.00 = nCu2 O 143 + nCuO 79.5 abbiamo cosı̀ due equazioni con due incognite 0.0401 = 2nCu2 O + nCuO 3.000 = nCu2 O · 143 + nCuO · 79.5 la cui risoluzione conduce ai risultati nCu2 O = 0.012 nCuO = 0.016 e passando ai grammi otteniamo che gCu2 O = 0.012 · 143 = 1.7 gCuO = 0.016 · 79.5 = 1.3 possiamo ora determinare la percentuale in peso dei rispettivi composti che saranno esprimibili come %gCu2 O = 1.7 · 100 = 56.7 3 %gCuO = M. Rustici, Chimica di base 1.3 · 100 = 43.3 3 172 13.2 Stechiometria esercizi tipici Soluzioni Ricordiamo che la molarità definisce la concentrazione di una soluzione intesa come il numero di moli di soluto disciolte in un litro di solvente e pertanto definibile matematicamente come: M= numero di moli n = litro di soluzione V con il volume (V) espresso in litri. 1. Calcolare la concentrazione molare di una soluzione di HCl al 36% in peso e densità 1.179 g/ml. Essendo la densità della soluzione pari a 1.179 g/ml questo significa che 1 litro della soluzione pesa esattamente 1179 g. Di questi 1179 g solo il 36% corrisponde all’acido cloridrico. In altre parole possiamo valutare la concentrazione dell’HCl espressa come grammi di acido cloridrico /litro di soluzione moltiplicando la densità espressa in grammi/litro per la percentuale in peso. Cioè C = d · % = 1179 · 0.36 = 424.44 g l Questo risultato significa che solo 424.44 g su un totale di 1179 g sono di HCl. Se allora dividiamo questo risultato direttamente per il peso molecolare dell’acido cloridrico otteniamo la molarità che rappresenta il risultato cercato n l M = C/P M = 424.44/36.5 = 11.63 2. Calcolare quanti ml di acido nitrico HNO3 al 40% in peso e densità 1.247 g/ml occorre prelevare per preparare 200 ml di soluzione 0.5 M di HNO3 Per prima cosa possiamo procedere come nell’esercizio precedente per calcolare la molarità della soluzione più concentrata. Dato che 1 litro della soluzione di partenza pesa 1247 g possiamo moltiplicare questo numero per la percentuale in peso e dividerlo a sua volta per il peso molecolare dell’acido nitrico e immediatamente otteniamo la molarità della soluzione di partenza. M= d·% 1247 · 0.4 = = 7.92 PM 63 n l Dobbiamo ora calcolare quanti ml della soluzione di acido nitrico avente una molarità pari a 7.92 devono essere prelevati per preparare 200 ml di una soluzione 0.5 M di acido nitrico. M. Rustici, Chimica di base 173 Stechiometria esercizi tipici Possiamo quindi chiederci quante moli di acido nitrico dovranno essere presenti in un volume (V) di 200 ml (0.2 l). Ricordando la definizione di molarità possiamo scrivere che n = M · V = 0.5 · 0.2 = 0.1 Queste 0.1 moli di HNO3 possono essere prelevate dalla soluzione concentrata (7.92 M). Applicando allora sempre la definizone di molarità possiamo cercare quale è il volume della soluzione concentrata che contiene un numero di moli pari a 0.1. In altre parole n 0.1 = = 0.0126 l = 12.5 ml M 7.92 Allora se noi preleviamo 12.5 ml dalla soluzione di partenza al 40% in peso e densità pari a 1.247 g/ml e le mettiamo in un matraccio del volume di 200 ml e aggiungiamo tanta acqua fino a raggiungere il volume desiderato (200 ml) otteniamo la soluzione alla concentrazione desiderata (0.5 M). V = 3. Calcolare quanti ml di una soluzione 1 M d idrossido di sodio (NaOH) occorrono per neutralizzare completamente 50 ml acido solforico (H2 SO4 ) 1 M secondo la reazione H2 SO4 + 2NaOH → Na2 SO4 + 2H2 O Possiamo allora ricavare per prima cosa il numero di moli di acido solforico 1 M contenute in 50 ml. Dalla definizone di molarità otteniamo che n = M V = 1 · 0.05 = 0.05 Per neutralizzare 0.05 moli di acido solforico dalla reazione si evince che sono necessarie 2 moli di idrossido di sodio e uindi nel caso specifico saranno necessarie nNaOH = 0.052̇ = 0.1 Queste moli di idrossido di sodio saranno contenute in un volume espresso dalla relazione n 0.1 = = 0.1 l = 100 ml M 1 Quindi per neutralizzare 50 ml di una soluzione 1 M di acido solforico sono necessari 100 ml di idrossido di sodio 1 M V = M. Rustici, Chimica di base 174 13.3 Stechiometria esercizi tipici Gas 1. Supponendo che la pressione massima sopportata da una bombola sia pari a 50 atm. Calcolare quale è la massima temperatura che puo sopportare una bombola con un volume di 50 litri contenente un gas alla pressione di 5 atm alla temperatura di 298 0 K, supponendo che il gas si comporti idealmente. La legge dei gas ideali ci dice che PV = costante T da questo segue che P2 V2 P1 V1 = T1 T2 tenendo presente che il volume rimane costante possiamo allora scrivere che P1 P2 = T1 T2 ∴ T2 = P2 T1 P1 sostituendo i dati T2 = 50 · 298 = 29800 K 5 2. 5 g di Na metallico vengono disciolti in 50 ml di HCl 5 M. Calcolare quanti litri teorici di idrogeno misurati a 25 0 C e 1 atm si possono ottenere, supponendo che la reazione vada a completezza. Per prima cosa scriviamo la reazione chimica 2Na + 2HCl → 2NaCl + H2 e calcoliamo rispettivamente il numero di moli di Na e il numero di moli di HCl nNa = g/P M = 5/23 = 0.217 nHCl = M V = 0.05 · 5 = 0.25 dato che il rapporto stechiometrico tra Na e HCl è di 1:1 osserviamo che nNa < nHCl . Questo implica che il sodio reagisce completamente Inoltre essendo i rapporti stechiometrici tra il Na e l’idrogeno sono di 2:1 possiamo scrivere che nH2 = 21 nNa = 0.5 · 0.217 = 0.11 M. Rustici, Chimica di base 175 Stechiometria esercizi tipici possiamo ora applicare la legge di stato dei gas P V = nRT e calcolare il volume espresso in litri di idrogeno sviluppato. In questo caso possiamo utilizzare la costante universale dei gas espressa come R = 0.0082 atm · l mole ·0 K allora V = 0.11 · 0.082 · 298 nRT = = 2.69 l P 1 3. 1.54 g di una miscela di Mg e Al vengono disciolti in eccesso di acido cloridrico. Dalla reazione si sviluppano 1.9 l di idrogeno misurati alla pressione di 1 atm e temperatura di 25 0 C. Sapendo che le reazioni che hanno luogo sono le seguenti Mg + 2HCl → MgCl2 + H2 2Al + 6HCl → 2AlCl3 + 3H2 Calcolare la percentuale in peso della miscela di partenza nei rispettivi componenti. se con x indichiamo le moli di Mg e con y le moli di Al e ricordando che i n = g/P M possiamo scrivere che xP MMg + yP MAl = x · 24.3 + y · 26.98 = 1.54 dai rapporti stechiometrici osserviamo inoltre che nH2 = nMg per la prima reazione e nH2 = 32 nAl Possiamo allora calcolare le moli totali di idrogeno sviluppate dalla legge di stato dei gas n= PV 1 · 1.88 = = 0.078 RT 0.082 · 298 dobbiamo quindi risolvere le equazioni x · 24.3 + y · 26.98 = 1.54 3 x + · y = 0.078 2 risolvendo il sistema otteniamo allora x = nMg = 0.023 e y = nAl = 0.037 M. Rustici, Chimica di base 176 Stechiometria esercizi tipici moltiplicando per i rispettivi pesi molecolari otteniamo che gMg = 0.54 e gAl = 1.0 e le rispettive percentuali saranno %Mg = 0.54 · 100 = 35.1 1.54 %Al = 100 − 35.1 = 64.9 Calcolare quanti litri di aria (21% in volume di ossigeno), misurati alle condizioni standard (25 0 C e 1 atm), sono teoricamente necessari per bruciare 10 grammi di benzene (C5 H6 ) supponendo che la reazione produca solo anidride carbonica e acqua. Scriviamo per prima cosa la reazione di combustione del benzene 2C6 H6 + 30O2 → 12CO2 + 6H2 O Per prima cosa calcoliamo il numero di moli di benzene nC6 H6 = g 10 = = 0.128 PM 78.1 le moli di ossigeno necessario seguendo la stechimentria della reazione saranno nO2 = 30 nC6 H6 = 15 ∗ 0.128 = 1.92 2 Possiamo calcolare ora il volume teorico di ossigeno dall’equazione di stato dei gas V = nRT 1.92 · 0.082 · 298 = = 46.93 l P 1 tenendo allora conto della quantità di ossigeno presente nell’aria la quantità teorica di aria necessaria alla combustione sarà V (aria) = 13.4 100 · 46.93 = 223.46 l 21 pH 1. 100 ml di acido cloridrico (HCl) 0.1 M vengono mescolati con 30 ml di idrossido di Bario (Ba(OH)2 0.1 M. Supponendo valida l’additività dei volumi calcolare il pH della soluzione finale. M. Rustici, Chimica di base 177 Stechiometria esercizi tipici Dal mescolamento delle due soluzioni segue la reazione acido base cosı̀ schematizzabile 2HCl + Ba(OH)2 → BaCl2 + 2H2 O Calcoliamo rispettivamente le moli iniziali dell’acido e della base nHCl = M · V = 0.1 · 0.1 = 0.01 nBa(OH)2 = M · V = 0.1 · 0.03 = 0.003 Dalla reazione si osserva che 2 moli di acido cloridrico reagiscono con 2 moli di idrossido di bario. Possiamo calcolre immediatamente le moli di acido cloridrico che reagiscono dal componente limitante che in questo caso è l’idrossido di bario. nHCl (consumate) = 0.003 · 2 = 0.006 quindi nHCl (finali) = 0.01 − 0.006 · 2 = 0.004 La soluzione finale è costituita da un acido forte e da un sale (BaCl2 ) proveniente da un acido forte e una base forte che non influenza il pH della soluzione. La concentrazione idrogenionica sarà pertanto regolata solo dalla concentrazione finale di HCl che sarà esprimibile come M= n 0.004 = = 0.031 V 0.13 allora avremo che pH = − log M = −log(0.031) = 1.51 13.5 Solubilità 1. Determinare la solubilità molare dell’acetato di argento, a 25 0 C, sia in una soluzione a pH 2, che in una soluzione a pH 7 sapendo che il prodotto di solubilità del sale insolubile è 4 · 10−3 e Ka = 1.8 · 10−5 . Per risolvere questo tipo di esercizio dobbiamo tenere presente che siamo in presenza di più equilibri che contemporaneamente debbono essere soddisfatti, tali equilibri possono essere schematizzati come M. Rustici, Chimica di base 178 Stechiometria esercizi tipici CH3 COOAg CH3 COO− + Ag+ CH3 COO− +H2 O CH3 COOH + OH− dove abbiamo trascurato l’equilibrio di ionizzazione dell’acqua, essendo la costante di autoprotolisi molto più piccola rispetto alle altre due costanti di equilibrio. Ricordando che la solubilità di un sale è definita come la concentrazione molare del sale in una soluzione satura essa si identifica cone la concentrazione dello ione argento, quest’ultima sarà allora esprimibile come [Ag+ ] = [CH3 COO− ] + [CH3 COOH] in effetti se non ci fosse il secondo equilibrio la concentrazione dello ione argento si identificherebbe solo con quella dello ione acetato dato che il rapporto stechiometrico tra le due specie è di 1:1, tuttavia essendo lo ione acetato una base debole esso, in parte, si trasforma per la presenza dell’acqua in acido acetico. Conseguentemente la conentrazione dello ione argento si identifica numericamente cone la somma delle due specie. ricordando la costante di equilibrio dell’acido acetico Ka = [H+ ][CH3 COO− ] [CH3 COOH] possiamo allora ricavare la concentrazione della specie indissociata e sostituirla nella precedente equazione ottenendo cosı̀ [Ag+ ] = [CH3 COO− ] + [H+ ][CH3 COO− ] Ka mettendo in evidenza la concentrazione dello ione acetato avremo µ ¶ [H+ ] [Ag ] = [CH3 COO ] 1 + Ka + − Ricordando a sua volta che kps = [CH3 COO− ][Ag+ ] possiamo ricavare la concentrazione dello ione acetato e sostituirlo nella precedente equazione ottenendo cosı̀ M. Rustici, Chimica di base 179 Stechiometria esercizi tipici ¶ µ [H+ ] [Ag ] = Kps 1 + Ka + 2 e quindi ¶ µ [H+ ] s = Kps 1 + Ka 2 dove s è la solubilità del sale. Osserviamo pertanto che la solubilità di un sale di un acido debole è direttamente influenzata dal pH della soluzione. É ovvio che a pH 7 il secondo termine è trascurabile e quindi la solubilità è calcolabile direttamente come s2 = p Kps tuttavia a pH 2 la situazione è capovolta e il secondo termine vale 555.56 che certamente non è trascurabile. Sostituendo i dati si trova pertanto che a pH 2 la solubilità è di 1.49 M, mentre a pH 7 è di 6.34·10−2 M M. Rustici, Chimica di base Capitolo 14 libri consigliati 14.1 Libri di testo consigliati • CHIMICA kotz, Treicheil, townsed EdiSES • Elementi di CHIMICA L. Palmisano, M Schiavello EdiSES • CHMICA la scienza della vita P. Kelter, M. Mosher, A. Scott EdiSES • CHIMICA, La natura molecolare della materia e delle sue trasformazioni M.S. Silberberg McGraw-Hill • Elementi di stechiometria P. Giannoccaro, S. Doronzo EdiSES • Fondamenti di stechimetria M. Giomini, e. Balestrieri, M. Giustini EdiSES M. Rustici, Libri consigliati
Scaricare