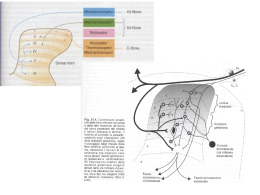
L’affidabilità analitica relazione a cura di: F. Franceschetti L.R. Incorvaia S. Ludovici P. Maltoni P. Mimmi GF. Bolelli Gruppo Controllo Qualità Az. Osp. S.Orsola-Malpighi (BO) e Policlinico (MO). COSA SI INTENDE PER AFFIDABILITÀ L’affidabilità rappresenta la “certezza di corretto funzionamento che un impianto, uno strumento, un dispositivo o un servizio può dare in base alle sue caratteristiche tecniche, di fabbricazione o di organizzazione”. (dal dizionario di lingua italiana “Devoto-Oli” ed. 2000) Trasferendo questo assunto all’indagine di laboratorio, significa che questa deve essere in grado di fornire una risposta corretta a supporto del momento decisionale nei confronti del paziente. CONTROLLO DI QUALITÀ IN CHIMICA CLINICA Nella sua visione tradizionale, il Controllo di Qualità è preposto a garantire che il prodotto “analisi di laboratorio” sia “tecnicamente” conforme ai requisiti fissati. In termini più attuali, questa garanzia “deve” essere allargata a tutti gli elementi dell’intero processo analitico, tra i quali spiccano la corretta modalità di prelievo, l’uso di un adeguato intervallo di riferimento e la stesura di un referto chiaramente esplicativo (qualità totale dell’informazione di laboratorio). TIPOLOGIE DI CONTROLLO IN CHIMICA CLINICA • Controllo di Qualità interno • Controllo di Qualità “tra laboratori” (Valutazione Esterna di Qualità) Le normative sull’accreditamento e la certificazione del laboratorio di analisi stabiliscono l’obbligatorietà di esecuzione di entrambi i controlli (con vincolo di fornire immediata documentazione in caso di visita ispettiva). Controllo di Qualità tra laboratori (Valutazione Esterna di Qualità) Compito istituzionale di questo programma di controllo è quello di fornire ai laboratori uno strumento di autovalutazione. Questa capacità si esplica attraverso la possibilità che ha il singolo partecipante di confrontarsi con le prestazioni di tutti gli altri; ciò vale anche per le Aziende di diagnostici che possono accedere a informazioni statisticamente consistenti sulla qualità del loro prodotto. In questo modo si stimola l’interazione tra produttori e utilizzatori facilitando così un processo continuo di miglioramento dei livelli qualitativi. Questa possibilità del confronto sarà tanto più incisiva quanto più viene allargata ad altri elementi dell’intero processo di analisi. Indicatori di qualità nel processo analitico La precisione è una variabile che deve trovare la sua massima espressione nel monitoraggio, mentre l’accuratezza (esattezza) è il requisito indispensabile per la formulazione di una corretta diagnosi. Quest’ultimo assunto trova la sua piena validità se connesso ad un adeguato intervallo di riferimento (IR). Indicatori di qualità nel processo analitico L’intervallo di riferimento (IR) non dovrebbe essere una variabile (almeno in ambiti territoriali circoscritti); lo potrebbe diventare se le differenze di misura tra i sistemi di analisi sono tali da compromettere la concordanza dell’informazione clinica che si ricava dal confronto tra IR e dato sperimentale. Indicatori di qualità nel processo analitico L’adeguamento degli IR alle differenze sistematiche tra i sistemi di analisi è scientificamente corretto per i dosaggi caratterizzati da una incerta identità tra calibratore e componente da misurare (dosaggi di tipo comparativo), mentre è da considerarsi una esigenza temporanea in quelli dove questo requisito di identità viene soddisfatto (dosaggi di tipo analitico). Classificazione del dosaggio Scarsa identità strutturale tra componente e calibratore. Dosaggio comparativo Con questo dosaggio sono possibili anche accentuate differenze sistematiche tra i diversi sistemi di misura. Identità strutturale tra componente e calibratore. Dosaggio analitico Questo tipo di dosaggio non “dovrebbe” presupporre differenze sistematiche tra i diversi sistemi di misura Obiettivo analitico proposto per l’imprecisione (I) dall’European Group for the Evaluation of Reagent and Analytical Systems in Laboratory Medicine (EGELAB) a) inferiore alla metà della variabilità biologica media intra-individuale (I<0,5·CVw), oppure, quale obiettivo intermedio: b) almeno analoga a quella mostrata in un Programma di VEQ dal quintile di laboratori rappresentativi del miglior stato dell’arte. Obiettivo analitico proposto per l’inesattezza (B) dall’European Group for the Evaluation of Reagent and Analytical Systems in Laboratory Medicine (EGELAB) a) inferiore a 1/4 della variabilità biologica totale [B<0,25·(CV²w + CV²b)½], oppure, quale obiettivo intermedio: b) inferiore a 1/16 dell’intervallo di riferimento (¼ di Tonks). Indici di valutazione di un programma di controllo “tra laboratori” EFFICIENZA + APPROPRIATEZZA + INFORMAZIONE EFFICACIA Regione Emilia Romagna Programma Valutazione Esterna di Qualità Ciclo di controllo: febbraio - ottobre '02 Esempio di calcolo dell'imprecisione media "nel laboratorio" (CVL %) LAB. L7 Profilo analitico: Biomarcatori tumorali Componente: Ca 125 cod. pool sigla camp. data invio ris. (UI/mL) CV% repl. K051 M111 M116 feb '02 mag '02 37,3 46,6 15,7 K052 M112 M117 feb '02 giu '02 40,4 48,2 12,5 K053 M113 M120 mar '02 set '02 47,2 40,1 11,5 K054 M119 M122 set '02 ott '02 24,9 29,2 11,2 CV L medio "nel lab" = miglior decile CV "nel lab" (CV L %) 25 12,7 % peggior decile Ca 125 CVL mediano "tra i lab" = 7,56 % 20 La b. L7 15 10 5 0 10° 50° pe rce ntile 90° Variabilità biologica media intra-individuale (CVW) = 13,6 % Obiettivo analitico (CVB) £ 6,8 % Regione Emilia Romagna (RER) Programma di Valutazione Esterna Qualità Calcolo del limite di accettabilità (L.A.) per l’inesattezza secondo quanto proposto da Tonks*: un dato analitico viene considerato accettabile quando il suo scarto percentuale dal riferimento rientra nel limite definito dal rapporto percentuale tra ¼ dell’ampiezza dell’intervallo di riferimento (IR) e il valore medio dell’IR stesso. Es: IR medio per il glucosio = 62 110 mg/dL (110 – 62) / 4 1 Tonks = ------------------- x 100 = 14.0 % (62 + 110) / 2 ne deriva che: 1/2 Tonks = 0,5 Tonks = 1/8 dell’IR = 7.0 % 1/4 Tonks = 0,25 Tonks = 1/16 dell’IR = 3.5 % * DB Tonks, Clin Chem, 1963; 9:217-233 Regione Emilia Romagna Programma Valutazione Esterna Qualità per le droghe di abuso (ciclo 2001) Andamento dei risultati ottenuti nel dosaggio di "screening" quantitativo per gli oppiacei sostanza aggiunta: morfina, 385 ng/mL media di consenso: 267 ng/mL CV = 11,2 % (36 ris.) D038 (mar 2001) Oppiacei valore soglia 600 ng/mL 500 400 300 200 LU G2 F7 JA T5 AN CD N8 HC FE M5 L9 Z9 FS 0 H2 100 cod. lab I dati sperimentali sono raggruppati per gruppi omogenei e visualizzati contestualmente al "valore soglia" adottato dai laboratori. Si osserva una eccellente omogeneità di risposta e l'esito dell'accertamento è prevalentemente negativo ad eccezione di 9 laboratori. Per 6 di questi ultimi (indicati dalle frecce) la causa non deriva dal fattore analitico bensì da una soglia di positività fissata a livelli inferiori a quella di altri. REGIONE EMILIA ROMAGNA PROGRAMMA VALUTAZIONE ESTERNA QUALITA’ PER LE DROGHE DI ABUSO DOSAGGI IMMUNOLOGICI DI “SCREENING” Confronto tra i “valori soglia” adottati dai laboratori Parte qualitativa (A1) Parte (semi)quantitativa (A2) Derivati cocaina Derivati cocaina Oppiacei Oppiacei Metadone Metadone Amfetamine Amfetamine Cannabinoidi Cannabinoidi Benzodiazepine Benzodiazepine 0 400 800 1200 1600 2000 0 400 800 ng/mL n. lab Intervallo escursione Derivati cocaina Oppiacei Metadone Amfetamine Cannabinoidi Benzodiazepine 46 46 33 40 43 37 150 – 500 50 - 1000 200 - 500 300 - 1000 20 – 100 80 - 2000 1600 2000 ng/mL Parte qualitativa (A1) Sostanze 1200 Parte (semi)quantitativa (A2) Val. Freq. Val. modale Modale (%) 300 300 300 1000 50 200 87.0 82.6 78.8 77.5 72.1 54.1 Sostanze n. lab Intervallo Escursione Derivati cocaina Oppiacei Metadone Amfetamine Cannabinoidi Benzodiazepine 63 64 47 56 61 57 30 - 300 25 - 300 16 -300 100 - 1000 13 - 100 40 - 500 Val. Freq. Val. modale Modale (%) 300 300 300 1000 50 200 88.9 62.5 55.3 53.6 57.4 54.3 Confronto tra i “valori soglia” adottati dai laboratori nelle due procedure analitiche contemplate per lo “screening. Nella parte superiore tale confronto viene rappresentato in forma grafica mentre in quella inferiore viene espresso più dettagliatamente in termini numerici. Si osserva l’accentuato intervallo di escursione di questo “valore soglia”, ma è soprattutto la frequenza modale che denota il sensibile grado di disomogeneità anche tra partecipanti che utilizzano il medesimo sistema analitico. REGIONE EMILIA ROMAGNA PROGRAMMA VALUTAZIONE ESTERNA QUALITA’ PER LE DROGHE DI ABUSO Confronto tra le frequenze modali (%) dei valori soglia adottati dai partecipanti in due periodi di controllo Val. modale ng/mL parte A2 - determinazioni quantitative Benzodiazepine 2002 200 Metadone 1997 300 Am fetam ine 1000 Cannabinoidi 50 Derivati cocaina 300 Oppiacei 300 0 20 40 60 frequenza m odale (%) 80 100 Regione Emilia Romagna Programma Valutazione Esterna di Qualità Profilo Chimica Clinica Variabili considerate nella valutazione della affidabilità analitica • Imprecisione “nel laboratorio” (CVL%) • Risultati compresi entro il limite di accettabilità • Risultati aberranti • Congruenza dell’intervallo di riferimento (IR) verso l’inesattezza relativa del sistema analitico
Scaricare