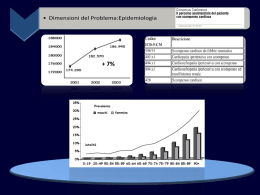
Aggiornamento in Malattie Cardiovascolari Scompenso cardiaco cronico: diagnosi e terapia Giovanni Pulignano I UO Cardiologica/UTIC Ospedale S.Camillo Roma 1 Introduzione Lo scompenso cardiaco è una sindrome clinica complessa caratterizzata da disfunzione ventricolare sinistra, segni di congestione venosa sistemica e/o polmonare e attivazione compensatoria dei sistemi neurormonali. Le principali manifestazioni sono rappresentate da ridotta tolleranza allo sforzo, ritenzione di liquidi e diminuita spettanza di vita (M. Packer) 2 Classificazione ACC/AHA dell’IC • Fase A: pazienti ad alto rischio di sviluppare IC – 60 milioni di pazienti con Coronaropatia Aterosclerotica (CAD), Ipertensione (HTN) Diabete Mellito (DM) • Fase B: pazienti con malattia cardiaca strutturale (bassa Frazione di Eiezione) – 10 milioni di pazienti 3 Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 Classificazione ACC/AHA dell’IC • Fase C: pazienti con disfunzione ventricolare sinistra e sintomi che rispondono al trattamento terapeutico • 5 milioni di pazienti • Fase D: pazienti con sintomi che non rispondono alla terapia massimale • 200.000 pazienti Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 4 Classificazione funzionale dello Scompenso Cardiaco Classe NYHA Grado di Weber I Nessuna limitazione Asintomatico nelle abituali attività quotidiane A MVO2 > 20 ml/Kg/min II Limitazione lieve Sintomi lievi nelle abituali attività quotidiane B MVO2 16-20 ml/Kg/min III Limitazione moderata Sintomi avvertiti per attività minime C MVO2 10-15 ml/Kg/min IV Limitazione severa Sintomi anche a riposo D MVO2 <10 ml/Kg/min 5 Fisiopatologia • Alterazioni emodinamiche • Anomalie Neuro-ormonali • Rimodellamento • Malattia aterosclerotica coronarica 6 Lesione cardiaca-disfunzione miocardica Ridotta gittata cardiaca Sistema adrenergico AVP Cardiotossicità diretta Prostaglandine ANP Sistema RAA Aumento frequenza e contrattilità Vasocostrizone ET+ NO - Ritenzione sodio e acqua Vasodilatazione Sovraccarico di volume Aumento MVO2 Aumentato stress parete Danno miociti BNP Ipertrofia Riduzione della contrattilità 7 Scompenso cardiaco : Epidemiologia Incidenza di SC nello studio di Framingham in rapporto all’età Prognosi severa dello SC in rapporto a pazienti con CAD stabile e buona funzione Vsx 8 Storia naturale dell’insufficienza cardiaca Fonte: Linee Guida nello scompenso cardiaco ANMCO/SIC 9 Storia naturale dell’insufficienza cardiaca 100%- Progressione Stress della parete % di sopravvivenza 0%- Danno da ischemia Attivazione neuro-ormonale Morte improvvisa IC progressiva Altro Asintomatica Lieve Fattori periferici Forte Severa 10 Fonte: Massie, 1990, Am J Cardiol Diagnosi di Scompenso Cardiaco secondo le LineeGuida ESC 1) sintomi e segni di scompenso (criterio soggettivo) 2) dimostrazione obbiettiva di disfunzione ventricolare (criterio obbiettivo) 3) reversibilità del quadro clinico dopo terapia (criterio retrospettivo, accessorio). 11 Scompenso sistolico vs diastolico Lo scompenso può essere causato da: • Anormalità della funzione sistolica, determinante una ridotta gittata (s.sistolico) • Anormalità della funzione diastolica che causa un difetto nel riempimento ventricolare (s. diastolico) Fonte: Linee Guida nello scompenso cardiaco ANMCO/SIC 12 13 Mortalità a 1 anno nel Registro ANMCO-IN-CHF (11,070 pts) 36.7% Sudden death 24.8% Non sudden mortality 11.7% 18.4% 13.0% 4.1% 2.8% NYHA I 1 Adjusted RR 95%CI 6.4% NYHA II 2.14 [1.33-3.44] NYHA III 3.77 [2.32-6.12] NYHA IV 5.54 [3.23-9.48] 14 Severità dello scompenso e modalità di morte NYHA II NYHA III 12% 15% NYHA IV 11% 33% 24% 64% 26% 59% 56% N = 103 Sudden death HF Other N = 232 N = 27 MERIT-HF Study Group et al. Lancet 199915 Storia naturale dell’insufficienza cardiaca Fonte: Linee Guida nello scompenso cardiaco ANMCO/SIC 16 Pathophysiology of Heart Failure: Left Ventricular Remodeling Left-ventricular (LV) remodeling is defined as a change in LV geometry, mass and volume that occurs over a period of time Obiettivi nella diagnosi di scompenso cardiaco 1. 2. 3. 4. 5. 6. 7. 8. E’ presente scompenso cardiaco? Quali sintomi sono presenti? Quali segni sono presenti? E’ possibile identificare l’eziologia? E’ presente disfunzione sistolica o diastolica? Sono presenti patologie associate? Sono presenti fattori precipitanti?. Quale è la severità dello scompenso? Fonte: Linee Guida nello scompenso cardiaco ANMCO/SIC 18 Diagnosi: sintomi ed esame obiettivo SINTOMI ESAME OBIETTIVO * Dispnea * Attivazione simpatica * Tosse * Aumento ponderale * Intolleranza allo sforzo * Astenia * Edemi e stasi polmonare * Cianosi * Polso arterioso * Polso venoso * Sudorazione * Sintomi gastrointestinali * Sintomi neurologici * Reflusso addomino-giugulare * Obiettivita’ cardiaca-Galoppo * Cachessia cardiaca Fonte: Linee Guida nello scompenso cardiaco ANMCO/SIC 19 Sensibilita’ e specificita’ dei reperti clinici dello scompenso cardiaco Segni e sintomi Dispnea Ortopnea Disp.par.Nott. Storia di edemi FC a riposo >100 Rantoli Riscontro edemi Terzo suono card Dist.vene collo Sensiblita’% 66 21 33 23 7 13 10 31 10 Specificita’% 52 81 76 80 99 91 93 95 2 20 H.Krumholz et al, Ann.Intern.Med., 1977 Dispnea di origine cardiaca e polmonare: diagnosi differenziale Pneumopatia cronica Asma bronchiale Cardiopatia Storia di dispnea Lunga Lunga e ricorrente breve Cardiopatia Di solito assente Di solito assente Presente Insorgenza Lenta e graduale Periodica Acuta/subacuta Sudorazione Modesta/assente Modesta/assente Presente Percussione torace Iperespansione Iperespanso Non iperespanso Ascoltazione Ronchi/sibili Sibili esp/ronchi Rantoli/ronchi Cianosi Presente/marcata Modesta Assente Impegno mm respiratori Presente Marcato Modesto Rx torace Rinforzo trama Enfisema Edema interst/alveo Efficacia broncodilatatori Si Si No Efficacia diuretici possibile No si 21 Criteri di Boston per la diagnosi di Scompenso Cardiaco Criteri Categoria I: Anamnesi Dispnea a riposo / ortopnea Dispnea parossistica notturna Dispnea camminando in piano Dispnea camminando in salita Categoria II: Esame obiettivo Anormalità della frequenza cardiaca (FC 91-110, 1; FC>110 b/m, 2) Aumento della pressione venosa giugulare Rantoli polmonari (basali, 1; medio-basali/diffusi,2) Sibili Terzo tono Categoria III: Radiografia del Torace Edema alveolare Edema interstiziale Versamento pleurico bilaterale Rapporto cardiotoracico >0.50 Ridistribuzione del flusso Punti * 4 3 2 1 1-2 2-3 1-2 3 3 4 3 3 3 2 22 Diagnosi: esami cardiologici strumentali * Elettrocardiogramma * Radiografia del torace * Ecocardiografia * Test cardiopolmonare Fonte: Linee Guida nello scompenso cardiaco ANMCO/SIC 23 Diagnosi: esami cardiologici strumentali Elettrocardiogramma Fonte: Linee Guida nello scompenso cardiaco ANMCO/SIC 24 Diagnosi: esami cardiologici strumentali * Radiografia del torace Fonte: Linee Guida nello scompenso cardiaco ANMCO/SIC 25 Diagnosi: esami cardiologici strumentali PA >Pa>Pv Pa >PA >Pv Pa >Pv>PA PA= Pressione alveolare 26 Diagnosi: esami cardiologici strumentali * Ecocardiografia Fonte: Linee Guida nello scompenso cardiaco ANMCO/SIC 27 Diagnosi: esami ematochimici •Dosaggio dei peptidi natriuretici (ANP/BNP) * Esame emocromo-citometrico completo * Esame delle urine * Creatinina sierica (Creatinina clearance) * Albumina sierica * FT3, FT4, TSH Fonte: Linee Guida nello scompenso cardiaco ANMCO/SIC 28 1 of 4 Using brain natriuretic peptide (BNP) to diagnose congestive heart failure 97 subjects referred for echocardiography BNP levels were significantly lower in subjects with normal heart function than in those with dysfunction (p <0.001) BNP levels (pg/mL) Normal heart function Diastolic dysfunction Systolic dysfunction 38 4 416 31 480 48 Koon and colleagues, 49th Annual Scientific Session of the American College of Cardiology 29 Classificazione funzionale dello Scompenso Cardiaco in base al test cardiopolmonare Classi di Web MVO2 ml/Kg/m Soglia anaerobica(ml/min/Kg) A > 20 >14 B 16-20 11-14 C 10-15 8-11 D <10 <8 30 Eziologia dello Scompenso Cardiaco Ischemica Non ischemica Eziologia imprecisata Eziologia nota Idiopatica Valvolare Ipertensiva Alcoolica Virale Post-partum Amiloidosi Altra/non specificata % 50,3 49,7 13,3 36,4 18,2 4,0 3,8 1,8 0,4 0,4 0,1 7,6 Teerlink et al 31 Scompenso cardiaco: Cause precipitanti • Aritmie 24% » » » » Tachiaritmie (FA, aritmie ventricolari) Bradicardia Perdita della coordinazione AV Anomalie della conduzione IV • Infezioni • Ischemia • Farmaci 23% 14% 10% » Alle norme igienico-dietetiche » Ai farmaci • Altro (anemia, Embolia polmonare, Disfunzione tiroidea, 5% Infarto cerebrale, Disfunzione di protesi, 15% • Ridotta compliance 9% • Non definito 32 Prognosi 1 • • • • • • • Fattori demografici: età, sesso, razza Sintomi (CF NYHA) Segni (FC>100, ipotensione, BMI ridotto, T3) Aritmie (TVS, FA) e sincope Eziologia (ischemica) Comorbidità (Diabete, arteriopatia periferica, ipertensione?) Terapia farmacologica (idralazina+ISDN, ACE-i, betabloccanti, spironolattone, amiodarone?) • ICD (AVID, MADIT I e II) • Iponatriemia (<130 mEq/l), linfocitopenia (<1000) • Noradrenalina, ANP-BNP, endotelina-1, ICAM-1, TNF-a 33 Sinergia terapeutica ACEi - Beta-Bloccanti SOLVD death (%) 20 CIBIS II MERIT+HF † *** 19.6 10 13.6* 11.9 7.4 0 Diuretic Digoxin McMurray J Circulation 2002 Diuretic Digoxin ACEI Diuretic Digoxin ACEI Diuretic Digoxin ACEI Betablocker 34 Prognosi 2 • – – – – – – ECG: Ipertrofia Vsx-donne; BAV e BBS Potenziali tardivi Dispersione del QT Ridotta variabilità RR TVS, TVNS (?) Ridotta sensibilità barocettoriale • Rx torace (RCT>50) • Ecocardiogramma :FEVs, Disfunzione-dilatazione VDx, Pattern restrittivo persistente con TDE<140 msec; FE<25%+TDE<130 prognosi peggiore=sopravvivenza 35% a 2 anni 35 Prognosi 3 • Cardiologia nucleare: FE con scintigrafia all’equilibrio; decremento o mancato incremento da sforzo; • Test da sforzo cardiopolmonare: VO2 max <14 ml/Kg/min o VO2<50% del valore predetto • Test del cammino per 6 min (<150 m grave; 150-425 m moderato) • Variabili emodinamiche/CVG – Pressione wedge>16 mmHg nonostante vasodilatatori; – Resistenze polmonari >2,5 U Wood nonostante vasodilatatori (NTP) – ridotta FE e malattia trivasale: indicazione cardiochirurgica 36 Sopravvivenza in funzione della classe NYHA Placebo Terapie convenzionali (diuretici, digossina) Classe NYHA IV (CONSENSUS) Mortalità (%) 100 90 80 70 60 50 40 30 20 10 0 Classe NYHA II–III (SOLVD Treatment Trial) 0 6 12 18 24 Mesi CONSENUS Trial Study Group. N Engl J Med. 1987; 316: 1429 The SOLVD Investigators. N Engl J Med. 1991; 325: 293 The SOLVD Investigators. N Engl J Med. 1992; 327: 685 30 Classe NYHA I–II (SOLVD Prevention Trial) 36 42 48 37 38 39 Terapia dello Scompenso Cardiaco Obiettivi Prevenire l’insorgenza e la progressione dello scompenso cardiaco Migliorare i sintomi e migliorare la qualita’ di vita Migliorare la sopravvivenza 40 Terapia dello scompenso cardiaco The cardiovascular continuum NYHA Risk factor Class 0 I II III LV dysfunction Prevention ASA Statins blockers ACE inhibitors Ca antagonists Heart Failure Treatment Diuretics ACE inhibitors blockers AT-1 blockers Potassium-sparing Spironolactone Digitalis IV Time Mild Moderate Severe 41 Modelli interpretativi dell’insufficienza cardiaca e Terapia Modello • Disordine cardiorenale • Depressione contrattile • Disordine cardiocircolatorio Disordine neuroormonale • Malattia infiammatoria Terapia diuretici, digitale inotropi vasodilatatori ACE-inibitori beta-bloccanti spironolattone sartani BNP inibitori endotelina anti-TNF, IgG, immunoadsorbimento 42 Suggested Pharmacological Treatments for Symptomatic CHF: ESC Guidelines For Symptoms NYHA I NYHA II reduce / stop diuretic +/- diuretic depending on fluid retention For Survival/Morbidity mandatory therapy For Symptoms if Intolerance to ACE inhibition or -blockade continue ACE inhibitor if asymptomatic, add -blocker if post MI ACE inhibitor as first-line treatment add -blocker if still symptomatic NYHA III + diuretics + digitalis if still symptomatic + nitrates / hydralazine if tolerated ACE inhibitor and -blockade add spironolactone NYHA IV diuretics + digitalis + nitrates / hydralazine if tolerated + temporary inotropic support ACE inhibitor -blockade spironolactone ARB if ACE inhibitor intolerant or ACE inhibitor + ARB if -blocker intolerant ARB if ACE inhibitor intolerant or ACE inhibitor +ARB if -blocker intolerant ARB if ACE inhibitor intolerant or ACE inhibitor +ARB if -blocker intolerant 43 ACC / AHA Guidelines Stage B Structural heart disease No CHF symptoms Stage A High risk for CHF No structural heart disease or CHF symptoms Structural heart failure eg, Patients with: hypertension, coronary artery disease, diabetes mellitus, or patients using cardiotoxins or with FHx CM Therapy: treat hypertension, encourage smoking cessation, treat lipid disorders, encourage regular exercise, discourage alcohol intake and illicit drug use, ACEinhibition in appropriate patients Stage C Structural heart disease Prior or current CHF symptoms Development of Stage D Refractory CHF requiring special interventions Refractory symptoms CHF symptoms eg, Patients with: previous MI LV systolic dysfunction asymptomatic valvular disease Therapy: All measures under Stage A, ACE inhibitors in appropriate patients, blockers in appropriate patients of CHF at rest eg, Patients who have marked eg, Patients with: symptoms at rest despite known structural maximal medical therapy (eg, heart disease, those who are recurrently shortness of breath hospitalised or cannot be and fatigue safely discharged from the reduced exercise tolerance hospital without specialised interventions) Therapy: All measure under stage A, drugs for routine use (diuretics, ACE inhibitors, blockers, digitalis), dietary salt restriction Therapy: All measures under Stages A, B and C, mechanical assist devices, heart transplantation, continuous iv inotropic infusions for palliation, 44 hospice care Fase A Classe I • Livello di evidenza A – Controllare l’ipertensione • Livello di evidenza B – Trattare le dislipidemie – Usare ACE-inibitori nei pazienti con DM, HTN, associati a fattori di rischio cardiovascolari e storia di malattia aterosclerotica vascolare – Controllare la frequenza ventricolare nel caso di tachiaritmie sopraventricolari 45 Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 Fase B Classe I • Evidenze di livello A (in pazienti con storia di IMA) – ACE-inibizione e bloccanti • Evidenze di livello B - ACE-inibizione e -bloccanti nei pazienti con ridotta IC – Sostituzione o riparazione valvolare in pazienti con stenosi o insufficienza valvolare Raccomandazione di Classe I per la Fase A • Gli agenti antiaritmici NON dovrebbero essere prescritti nel caso di aritmie ventricolari asintomatiche • La Digitale NON dovrebbe essere somministrata nei pazienti in ritmo sinusale 46 Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 Fase C Classe I • Livello di evidenze A – Diuretici nei pazienti con ritenzione di fluidi – ACE-inibizione, a meno di controindicazioni -bloccanti in pazienti stabili, a meno di controindicazioni – Digitale, a meno di controindicazioni • Livello di evidenze B – Sospensione di farmaci responsabili di possibili effetti avversi sullo status clinico del paziente Raccomandazioni di Classe I per le Fasi A e B 47 Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 Fase C Classe IIb • Livello di evidenza B – Aggiunta del blocco recettoriale dell’inibizione dell’ACE – Aggiunta di un nitrato (solo o in combinazione con idralazina) all’ACE-inibizione nei pazienti che già ricevono -bloccanti, digitale e diuretici 48 Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 Fase C Classe IIa • Livello di evidenza A – Allenamento fisico nei pazienti ambulatoriali – Antagonisti recettoriali dell’Angiotensina possono essere somministrati nei pazienti che ricevono -bloccanti, diuretici e digitale, ma non in chi riceve ACEinibitori (per tosse severa ed angioedema) • Livello di evidenza B – Spironolattone nei pazienti con funzione renale preservata, normale concentrazione di potassio e recente o attuale classe sintomatologica NYHA IV – Combinazione di Idralazine e di nitrati in pazienti che hanno ricevuto -bloccanti, diuretici e digitale ma che non possono assumere ACE- inibitori (a causa di ipotensione o insufficienza renale) 49 Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 Fase D Classe I • Livello di evidenza A – Inviare il paziente ad uno specialista per il trattamento di IC refrattaria • Livello di evidenza B – Seguire attentamente eventuale ritenzione di fluido – Inviare i pazienti elegibili alla valutazione per trapianto cardiaco Raccomandazioni di Classe I per le Fasi: A B e C 50 Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 Diuretici 1. Riduzione del volume telediastolico e della PCWP 2. Riduzione delle resistenze vascolari sistemiche 3. Aumento dello stroke volume e della portata 4. Miglioramento della capacità di esercizio e dei sintomi causati dalla congestione polmonare o periferica Indicazioni: pazienti con sintomi e segni di sovraccarico di volume Principali diuretici: tiazidici (idroclorotiazide, clortalidone metolazone) diuretici dell’ansa (furosemide, torasemide) Effetti collaterali : ipotensione posturale, iperuricemia, ipokaliemia, ipoglicemia, disturbi della sfera sessuale 51 Abraham and Schrier. 1994 Diuretici • Diuretici dell’Ansa nei pazienti con CrCl < 30 • Dovrebbero essere somministrati 2 volte al giorno per evitare il rebound di assorbimento del Na • Si può ricorrere ai tiazidici se CrCl > 30 • Bisognerebbe usare combinazioni di farmaci (come furosemide + metolazone), per somministrazione in bolo o continua endovena • Metolazone ha una lunga emivita: può essere usato una volta al giorno o anche una volta ogni due o tre giorni 52 Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 Digitale 1. Effetti sull’inotropismo cardiaco 2. Riduzione della frequenza ventricolare media in corso di fibrillazione o di flutter atriale 3. Effetti extracardiaci a livello della muscolatura liscia vascolare e del sistema nervoso autonomo Indicazioni Possono essere candidati tutti i pazienti con scompenso cardiaco sintomatico dovuto a disfunzione sistolica e specificatamente in corso di fibrillazione atriale a risposta ventricolare rapida Controindicazioni Bradicardia, sick sinus syndrome, WPW Blocchi AV II o III grado Ipokaliemia, ipercalcemia Digossina: DIG Study 54 N Engl J Med 1997; 336:525-33 Lesione cardiaca Disfunzione miocardica Sovraccarico cardiaco Ridotta perfusione sistemica Segnali neuro-ormonali, infiammatori, Meccanici- stiramento Alterazione dell’espressione dei geni Tossicità, Ischemia, Deplezione energetica Crescita e Rimodellamento Apoptosi Necrosi Morte Cellulare 55 ACE-inibitori 1. modulazione dell’attivazione neurormonale 2. riduzione della ritenzione idrosalina 3. effetti emodinamici favorevoli 4. effetti su morbilita’ e mortalita’ 5. effetti su sintomatologia e tolleranza allo sforzo Indicazioni: Pazienti con scompenso cardiaco da disfunzione Vsx in assenza di controindicazioni all’uso (es. potassio>5,5 mEQ/L, ipotensione sintomatica) e che non siano intolleranti al farmaco (storia di reazioni avverse) CONSENSUS Probabilità cumulativa di morte Mortalità cumulativa nel gruppo placebo e nel gruppo enalapril pazienti >70 anni in CF avanzata (prevalentemente IV ) 0.7 0.6 31% 0.5 Placebo* 40% Riduzione N=126 0.4 Riduzione del rischio del rischio Enalapril* 0.3 N=127 0.2 0.1 0 0 1 2 3 4 5 6 7 8 9 10 11 12 Placebo 102 78 63 59 53 47 42 34 30 24 18 17 Enalapril 111 98 88 82 79 73 64 59 49 42 31 26 *In Concomitanza con Terapia Convenzionale Mesi The CONSENSUS Trial Study Group, N Engl J Med,57 1987 SOLVD trattamento Pazienti prevalentemente in II-III CF NYHA Mortalità per tutte le cause % di mortalità 50 40 16 % 30 Riduzione del rischio Placebo (n=1284) Enalapril 20 (n=1285) 10 p=0,0036 0 0 6 12 18 24 mesi 30 36 42 48 58 SOLVD Treatment Trial, N Engl J Med, 1991 ATLAS All-Cause Mortality + Hospitalisation for Any Reason % Event-Free Survival 100 75 p=0.002 50 High-dose lisinopril 25 Low-dose lisinopril 0 0 6 12 18 24 30 36 42 48 Months 59 La “Triplice terapia”: PROVED AND RADIANCE TRIALS Modificazioni nella durata massima di esercizio 40 20 Triple Dig+Diur Diur ACE+Diur nS 0 -20 0 2 6 12 P<0.01 P<0.01 -40 -60 -80 -100 -120 Weeks post randomization Young JB, et al J Am Coll Cardiol 1998; 32: 686-92 60 ACE-Inibitori • I pazienti non dovrebbero essere troppo ”asciutti” • Iniziare a bassa dose, usare ACE-I a breve emivita, raggiungere la dose target o la massima dose tollerata • Se vi è bassa pressione arteriosa, controllare le variazioni ortostatiche. Se non vi sono cambiamenti, OK per somministrazione di ACE-I • Bassa pressione arteriosa ed insufficienza renale cronica non sono controindicazioni per gli ACE-I • Se l’azotemia e la creatinina aumentano, modificare la dose del diuretico • La maggior parte dei pazienti tollera gli ACE-I 61 Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 Betabloccanti 1.Effetti favorevoli a livello miocardico (tossicità catecolamine) 2. Effetti antiaritmici 3. Effetti a livello neuroendocrino 4. Effetti a livello emodinamico 5. Effetti su sintomi, morbilita’ e mortalita’ 6. Effetto antiossidante (carvedilolo) Indicazioni: da pazienti con SC sintomatico in CF NYHA II-III (e anche IV secondo i criteri COPERNICUS) che siano stabili in terapia con digitale, diuretici e ACE-inibitori e che non abbiano controindicazioni all’uso blockade in HF – All-cause mortality US Carvedilol Programme Survival 1.0 Carvedilol (n=696) 0.9 Placebo (n=398) 0.8 Risk reduction = 65% p<0.001 0.7 Survival CIBIS-II 1.0 0.6 Bisoprolol 0.5 0 50 100 150 200 250 300 350 400 Days 0.8 Packer et al (1996) Mortality % 20 Risk reduction = 34% p<0.0001 0.6 0 0 200 400 MERIT-HF Placebo 600 Placebo 15 Metoprolol CR/XL 800 10 Time after inclusion (days) Risk reduction = 34% p=0.0062 5 CIBIS-II Investigators (1999) 0 0 3 6 9 12 15 18 21 Months of follow-up The MERIT-HF Study Group (1999) 63 COPERNICUS trial Pz con Sc severo (NYHA IV) All-cause mortality 100 % Survival 90 80 Carvedilol 70 Placebo p=0.00013 35% risk reduction 60 0 0 3 6 9 12 Months 15 18 21 Packer, NEJM 200064 –Bloccanti • Usare solo farmaci approvati: bisoprololo, carvedilolo e metoprololo CR/XL • Iniziare a basse dosi, aumentare ogni 2 settimane fino alla dose target o alla dose massima tollerata • Non iniziare la terapia in chi è in trattamento con inotropi positivi • Possibilità di iniziare il trattamento in pazienti ospedalizzati purchè in assenza di congestione sistemica (IMPACT) • Non interrompere i BB nei pazienti ospedalizzati che sono in trattamento cronico con BB (l’IC potrebbe peggiorare) • Bassa pressione arteriosa e IC severa non sono controindicazioni per i BB 65 Hunt SA et al. J Am Coll Cardiol. 2001; 38: 2101 Antagonisti Recettoriali dell'AII: razionale ANGIOTENSINOGEN (LIVER) CHYMASE RENIN INHIBITOR ANGIOTENSIN I BRADYKININ PEPTIDES ACE INHIBITOR ANGIOTENSIN II AT1 RECEPTOR BLOCKER AT1 AT2 66 ELITE II Evaluation of Losartan In The Elderly trial II Trattamento:Losartan 50 vs. captopril 150 ( digitale e diuretici) 3.152 pazienti classe NYHA II-IV, FE 40%,Età 60 anni (media 74) Probabilità di sopravvivenza Pazienti: Mortalità per tutte le cause 1.0 0.8 0.6 Captopril Losartan (N=1.574) (N=1.578) 250 eventi 280 eventi 0.4 Captopril / Losartan RR (95% C.I.): 0.88 (0.75, 1.05) p=0.16 (NS) 0.2 0.0 0 100 200 300 400 500 Giorni di follow-up Pitt B et al Lancet 2000;355:1582-1587 600 700 67 Val-HeFT: Valsartan in Heart Failure Trial mortalità totale mortalità totale/ospedalizzazioni 1.0 P = 0.8 (ns) 13.3% RISK REDUCTION P= 0.009 0.9 0.8 0.7 0 VALSARTAN PLACEBO 3 6 9 12 15 18 21 24 27 0 TIME(MONTHS) VALSARTAN PLACEBO 3 6 9 12 15 18 21 24 27 TIME (MONTHS) 68 Cohn J et al NEJM 2001 VASODILATATORI NON ACE-INIBITORI • IDRALAZINA (Hy-C trial) • NITRATI (V-HeFT I e II) Efficacia vs placebo di 2^ linea vs ACE-inibitori • AMLODIPINA (PRAISE) e • FELODIPINA (V-HeFT III) = nessun effetto sulla mortalità 69 POTENTIALLY ADVERSE EFFECTS OF ALDOSTERONE IN CHF ALDOSTERONE Baroreceptor dysfunction Loss of magnesium Potentiation of Catecholamines Ventricular arrhyrhmias Myocardial fibrosis 70 ANTIALDOSTERONICI STUDIO RALES • 1663 p età media 65+12; 73% maschi; NYHA III-IV • dose SPIRONOLATTONE 12.5- 25 mg 1.00 0.95 Randomized Aldactone Evaluation Study (RALES) 0.90 0.85 0.80 Probability of survival 0.75 Spironolactone 0.70 0.65 0.60 0.55 Placebo 0.50 Risk reduction 30% p<0.001 0.45 0.00 0 3 6 9 Pitt 24 B et27 al. N Med 1999;10:709–717 12 15 18 21 30Engl 33 J 36 Months Riduzione rischio di Morte 30%; ospedalizzazioni 35% 71 ANTICOAGULANTI orali INDICAZIONI CERTE •PREGRESSI EVENTI EMBOLICI •FIBRILLAZIONE ATRIALE(mantenere INR 2.5-3.5) INDICAZIONI POSSIBILI •FE SEVERAMENTE DEPRESSA (<20-25%) •TROMBI VENTRICOLARI •ANZIANI: > RISCHI >BENEFICI (mantenere INR 1.8-2.0) : problemi: stato cognitivo, problemi logistici, interazioni farmacologiche... 72 Randomised trial of low-dose amiodarone in severe congestive heart failure Grupo de Estudio de la Sobrevida en la Insuficiencia Cardiaca en Argentina (GESICA) Controllo pz Amiodarone Rid.rischio (95%CI) 260(100) 260(100) Morti 106(41,4) Morti e osped. per CHF 149(58,2) 119(45,8) 87(33,5) 28(4-24) p 0.024 31(13-46) 0.0024 Morte improvvisa 39(15,2) 32(12,3) 27(-17-54) 0.16 Scompenso ingravescente 44(16,9) 23(-15-48) 0.16 52(20,3) Miglioramento della sopravvivenza e riduzione delle ospedalizzazioni in pazienti con scompenso severo. 73 Doval HC et al. Lancet 1994;344:493-98 Amiodarone in patients with congestive heart failure and asymptomatic ventricular arrhythmia Survival Trial of Antiarrhythmic Therapy in Congestive Heart Failure (CHF-STAT) Non miglioramento della sopravvivenza e dell'incidenza di morte improvvisa nonostante una soppressione delle AIV e un miglioramento della funzione VS (trend non significativo in pz con eziologia non ischemica) . 74 Singh SN et al. NEJM 1995;333:77-82 TERAPIA CHIRURGICA dello scompenso • RIVASCOLARIZZAZIONE CORONARICA • CORREZIONE MITRALICA • CARDIOMIOPLASTICA • DISPOSITIVI DI ASSISTENZA MECCANICA PORTATILI (LVAD) • TRAPIANTO CARDIACO (FE < 20%, VO2 max < 14 ml/kg/min, età < 60aa) • TRAPIANTO DI CELLULE STAMINALI • DEFIBRILLATORE IMPIANTABILE • RESINCRONIZZAZIONE CARDIACA 75 Rivascolarizzazione miocardica • 60-80% dei pz con SC hanno una cardiopatia coronarica • Occorre valutare la presenza di ischemia miocardica, miocardio vitale e il potenziale beneficio della rivascolarizzazione • La sopravvivenza è migliorata, rispetto alla terapia medica da sola, anche in assenza di angina (Duke database) 76 ICD: studio MADIT 1 0.78 0.69 0.69 P=0.007 (probabilityofofsurvival) survival) (probability 77 Trials con ICD Hazard Ratio N=196 MADIT-I [EF<0.35, NSVT, EP+] 0.46 1996 N=1016 AVID [Aborted Cardiac Arrest] 0.62 1997 N=704 MUSTT [ EF<0.40, NSVT, EP+] 0.45 1999 N=1232 MADIT-II [Prior MI & EF<0.30] 0.69 2002 0.4 0.6 0.8 1.0 1.2 1.4 1.6 1.8 78 ICD Better Resincronizzazione cardiaca : MIRACLE STUDY Miglioramento di Classe NYHA con TRC P < 0.001 100% 13% 27% 80% 60% 90% 93% 40% 52% Class I II III IV 64% 20% 32% 0% Baseline 6-Months Control (N = 117) Baseline 6-Months CRT(N = 124) Chi-square test 79 Effetto della Resincronizzazione sulla Mortalità nei pazienti con ICD • ICD indication • Cardiac arrest • VT/VF • MADIT/MUSTT • NYHA Class III • Optimal medical therapy • Sinus rhythm 80 2000 Contak CD/Ventak CHF Study - NASPE Trapianto cardiaco • • • Sopravvivenza 60%-90% at 1 anno, 70% at 5-anni Criteri Inclusione: – escludere ischemia miocardica curabile – Scompenso cardiaco refrattario a terapia medica ottimizzata – EF <20% – VO2 max 14 mL/kg/min Problemi: – rigetto , aterosclerosi del graft, neoplasia, costo/ disponibilità 81 Terapia non farmacologica dell’insufficienza cardiaca Educazione sanitaria e counselling Esercizio fisico * Migliore efficacia della terapia farmacologica * Migliore adesione del paziente allo schema terapeutico * Migliore qualita’ della vita Terapia dell’insufficienza cardiaca avanzata 83 Prospettive • • • • • Terapia antiinfiamatoria Terapia genica Cellule staminali Devices Terapia metabolica 84 Conclusioni 1 •Lo SC rappresenta uno dei maggiori problemi di sanità pubblica e interessa prevalentemente soggetti di età avanzata, in cui è la prima causa di ricovero ospedaliero •Incidenza e prevalenza sono in aumento per l’invecchiamento della popolazione e per il miglioramento della sopravvivenza dopo IMA e altre cardiopatie •La diagnosi di SC è un processo dianmico e complesso in cui un ruolo importante è svolto dalla identificazione della disfunzione ventricolare e di una eziologia potenzialmente curabile •Una percentuale consistente (30-50%) dei soggetti con SC presenta una FE conservata e disfunzione prevalentemente diastolica 85 Conclusioni 2 •La terapia deve essere individualizzata in base alle caratteristiche del paziente, l’eziologia, lo stato di progressione della malattia e deve essere organizzata in un piano di cura strutturato e continuativo, che coinvolge diverse strutture e professionalità •Gli ACE-inibitori rimangono la base della tp farmacologica, con un effetto sinergico con i betabloccanti •Gli antagonisti recettoriali dell’AII rappresentano una alternativa agli ACE-i (quando questi non sono tollerati) e possono essere associati in assenza di trattamento betabloccante in atto •Lo spironolattone è efficace in associazione con ACE-i + BB •Gli anticoagulanti orali sono indicati in caso di rischio embolico, previa una accurata valutazione del rischio emorragico nel singolo paziente. •L’amiodarone rappresenta l’unico antiaritmico efficace e sicuro in pazienti con SC •I tattamenti non farmacologici (chirurgia, ICD, stimolazione biventricolare) si sono dimostrati efficaci in pazienti selezionati 86
Scaricare