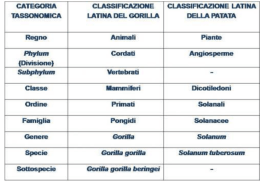
Come i neuroni, le cellule muscolari rispondono a stimoli: elettrici, meccanici e chimici potenziale d’azione contrazione muscolare Nei vertebrati il sistema muscolare è rappresentato dal muscolo scheletrico, cardiaco e liscio Il tessuto cardiaco e la muscolatura liscia sono controllati dal sistema nervoso vegetativo Il tesuto del muscolo scheletrico è costituito da cellule allungate contenenti più nuclei (poliploidi) localizzati alla periferia del citoplasma Le cellule del tessuto cardiaco e della muscolatura liscia sono mononucleate Circa il 90-95% del peso secco dei miociti è costituito da proteine Proteine miofibrillari: Proteine contrattili Proteine regolatrici Proteine strutturali Proteine ad attività biologica: mioglobina, citocromi, enzimi glicolitici, enzimi del ciclo di Krebs ecc. Il contenuto di H2O e circa 70-80% del peso bagnato di cui il 20-25% è nel liquido extra-cellulare La quota intra-cellulare è prevalentemente H2O di solvatazione delle proteine L’elettrolita a concentrazione maggiore è il K+ ~ (150 mM) seguito dal Na+ ~ (10 mM) e dal Mg2+ ~ (10 mM) Istologicamente il tessuto muscolare è classificabile in: striato scheletrico striato cardiaco liscio Metabolicamente e funzionalmente le fibre dei muscoli scheletrici si suddividono in: rosse (fibre tipo I) bianche (fibre tipo II) Fibre di tipo I Elevate quantità di mioglobina Riccamente vascolarizzate Attivo metabolismo ossidativo Numerosi mitocondri Maggiore capacità di ossidare gli acidi grassi, il piruvato, i corpi chetonici Dovuta in parte all’alto rapporto H/M degli isoenzimi della lattico deidrogenasi: L’isoenzima H è inibito da NAD+ e piruvato + NADH + H+ LDH (lattato deidrogenasi) + NAD+ Fibre di tipo II alte concentrazioni di enzimi glicolitici basso numero di mitocondri elevata produzione di acido lattico maggiore [PCr] rispetto alle fibre I debito di ossigeno contrazione in anaerobiosi BIOENERGETICA MUSCOLARE BIOENERGETICA MUSCOLARE BIOENERGETICA MUSCOLARE La reazione che produce direttamente energia utilizzabile per la contrazione muscolare è catalizzata dalla miosina-ATPasi: ATP + H2O ADP + Pi (1) DG°’ = - 30.5 kJ/mol Tuttavia, la quantita' di ATP presente nel muscolo è sufficiente per sostenere una attivita' contrattile solo per un periodo limitato di tempo CK PCr + ADP + H+ ATP + Cr (2) DG°’ = - 43 kJ/mol FOSFORILAZIONE OSSIDATIVA NADH + H+ + 3ADP + 3Pi + 1/2O2 = NAD+ + 3ATP + H2O La somma di (1) e (2): PCr + H2O + H+ Cr + Pi per effetto dell’adenilico cinasi ADP + ADP ATP + AMP e per successiva deaminazoione ad opera dell’adenilico deaminasi AMP + H2O IMP + NH3 per effetto della xantina ossidasi IMP ipo-xantina xantina acido urico actina miosina MIOSINA E’ una molecola di cicrca 160 nm di pm ~ 470 mila La coda e’ formata da due catene polipeptidiche ad a-elica di pm di ~ 200 mila (catene pesanti) Le estremità globulari della molecola contengono 4 catene peptidiche dette catene leggere MIOSINA Le catene leggere possono esseredi tre tipi: LC1, LC2, LC3 hanno pm leggermente diversi Ciascun lobo della testa della miosina contiene due catene leggere: una è sempre LC2 l’altra LC1 o LC3 LC2 sono le uniche ad essere fosforilate reversibilmente MIOSINA Gli enzimi proteolitici tripsina e chimotripsina scindono la molecola in due frammenti: meromiosina leggera e meromiosina pesante La meromiosina pesante è ulteriormente scissa dalla papaina in due sub-frammenti globulari S1 e un frammento a bastoncino S2 MIOSINA I punti in cui la miosina è scissa dagli enzimi proteolitici, sono quelli a maggiore flessibilità (cerniere) che consentono alle teste di flettersi durante la contrazione MIOSINA LC2 Ogni frammento S1 della testa della miosina ha due regioni: il collo che è in continuità con la coda che contiene le catene leggere il dominio motore la parte globulare che contiene i domini che legano l’actina MIOSINA Un filamento è formato da ~ 400 molecole di miosina raggruppate in due fasci contrapposti di ~ 200 molecole aventi le teste che emergono ogni 43 nm I due fasci sono separati da uno spazio centrale senza teste emergenti di ~ 1500 Å L’attività ATPasica è concentrata nella porzione globulare delle teste detta: dominio motore miosina-ATP + H2O -ADP-Pi + actina actomiosina-ADP-Pi Actomiosina-ADP + ATP -ADP-Pi actomiosina-ADP-Pi actomiosina-ADP + Pi actina + miosina-ATP + ADP MIOSINA Nel muscolo scheletrico: nelle fibre di tipo I: bassa attività ATPasica nelle fibre di tipo II: alta attività ATPasica Nel muscolo cardiaco: nel miocardio atriale: alta attività ATPasica nel miocardio ventricolare: bassa attività ATPasica Nel miocardio ventricolare dei mammiferi sono state identificate tre isoforme di miosina con diversa attività ATPasica le cui proporzioni variano in funzione della taglia dell’animale Isoforme delle proteine miofibrillari ACTINA E’ una proteina globulare di pm ~ 43 mila E’ costituita da 376 aminoacidi E’ detta actina G ed è il costituente dei singoli monomeri I singoli monomeri polimerizzano a formare actina F due catene di actina F si avvolgono in forma elicoidale formando un filamento di 1 mm di lunghezza ogni spira contiene 13-14 molecole di monomero ACTINA sono presenti 4 domini: 1,2 sulla superficie esterna responsabili del legame con la miosina; 3-4 partecipano al legame con gli altri monomeri ACTINA n(Actina-G) + nATP + nCa2+ n(Actina-G)-nATP-nCa2+ n(Actina-G)-nATP-nCa2+ Actina-F(ADP)n +nPi + nCa2+ Forma il complesso acto-miosina aumenta di 200 volte l’attività ATPasica della miosina Proteine regolatrici Le proteine che regolano l’attività contrattile sono: tropomiosina e troponina Tropomiosina (~ pm 68 mila): costituita da due catene a e b avvolte a spirale Giace nei solchi formati dai filamenti di actina Funzione regolatrice della formazione del complesso acto-miosina Troponina pm complessivo ~ 76 mila è formata da tre sub-unità è legata alla tropomiosina TnC (pm 18 mila) lega il Ca2+ TnI (pm 21mila) inibisce l’ATPasi dell’acto-miosina TnT (pm 37 mila) lega la tropomiosina legame debole non si forma il complesso legame forte miosina-ATP + H2O -ADP-Pi + actina actomiosina-ADP-Pi Actomiosina-ADP + ATP -ADP-Pi actomiosina-ADP-Pi actomiosina-ADP + Pi actina + miosina-ATP + ADP Proteine strutturali Proteine della linea Z: a-actinina, b-actinina, desmina (abbondante nel cuore) Proteine della linea M: tengono in registro i filamenti di miosina Proteina C: si lega alla coda della miosina (ruolo ignoto) Nebulina, Connettina: legano linee Z opposte impedendone l’eccessiva distensione DISTROFINA Disponendo delle proteine contrattili purificate si è potuto studiare in vitro il complesso proteico actomiosina verificando che: Ca2+ Mg2+ stimolano l’attività ATPasica Na+, K+ inibiscono l’attività ATPasica inibiscono l’interazione tra le due proteine ATP favorisce l’interazione actina-miosina 10-4 < [ATP] < 10-2 un impulso nervoso arriva alla placca neuromuscolare si genera potenziale d’azione il sarcolemma si depolarizza il segnale elettrico arriva alle cisterne del ret. sarcoplasm. rilascio di Ca2+ saturazione dei siti di legame di TnC modificazioni conformazionali del complesso regolatrice liberazione dei siti attivi di legame dell’actina legame tra la testa della miosina e actina miosina-ATP + H2O -ADP-Pi + actina actomiosina-ADP-Pi Actomiosina-ADP + ATP -ADP-Pi actomiosina-ADP-Pi actomiosina-ADP + Pi actina + miosina-ATP + ADP In ogni ciclo avviene uno slittamento di 10 nm verso la linea M Una contrazione comporta circa 5 cicli al secondo Il Ca2+ che entra nel sarcolemma dal tubulo a T non è sufficiente per attivare il sistema contrattile, ma promuove il rilascio di Ca2+ dalle cisterne terminali Il Ca2+ che realmente attiva il sistema contrattile è quello immagazzinato nel reticolo sarcoplasmatico Il rilassamento del muscolo avviene per richiamo del Ca2+ nelle cisterne per mezzo di un enzima ATPasi Mg2+/Ca2+ dipendente presente nella membrana del reticolo sarcoplasmatico Il trasferimento di Ca2+ nelle cisterne del reticolo sarcoplasmatico comporta il trasporto di due Ca2+ per ogni ATP idrolizzato Si fosforila un residuo di acido aspartico di una subunità La fosforilazione determina un cambiamento conformazionale che disattiva i due siti di legame del Ca2+ ad alta affinità rivolti verso il citoplasma, mentre si attivano i siti a bassa affinità rivolti verso il lume del reticolo
Scaricare