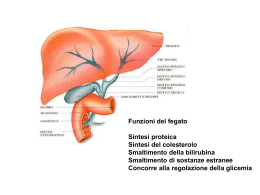
Il fegato è diviso in: lobo destro, lobo sinistro, lobo quadrato e lobo caudato. I primi due sono attraversati da un legamento falciforme, una membrana sierosa attraverso la quale passano i nervi e i vasi sanguigni a esso destinati, come l’arteria epatica e la vena porta. La struttura interna del fegato è lobulare, ovvero costituita da ulteriori suddivisioni tutte uguali e con simili funzioni. All’interno di ogni lobulo, che ha una struttura prismatica, vi è una ricchissima rete di vasi, nei quali scorre il sangue proveniente dalla vena porta, ricco delle sostanze nutritive assorbite dall’intestino durante la digestione. Essi convergono in una vena centrolobulare, che a sua volta confluisce in vene sempre più grandi fino a originare le vene sopraepatiche, tributarie della vena cava inferiore. Sempre all’interno dei lobuli corrono i capillari biliari, che hanno la funzione di raccogliere la bile, e si riuniscono in vasi di dimensioni sempre maggiori, originando il dotto epatico dal quale la bile si riversa nella cistifellea. Il fegato gioca un ruolo fondamentale nel mantenimento dell’omeostasi metabolica Funzioni biochimiche fondamentali: - METABOLISIMO DEI CARBOIDRATI (mantenimento della gluconeogenesi) glicemia attraverso glicogenesi, glicogenolisi, glicolisi, - METABOLISIMO LIPIDICO (secrezione di VLDL, HDL, catabolismo LDL) - METABOLISIMO GLI AMINOACIDI E DELLE PROTEINE (sintesi e catabolismo delle proteine) - BIOTRASFORMAZIONE E DETOSSIFICAZIONE (composti liposolubili ed ormoni vengono convertiti in composti meno attivi ed idrosolubili) - METABOLISIMO DELLA BILIRUBINA (deriva dalla degradazione dell’eme) LA VALUTAZIONE LABORATORISTICA INCLUDE NUMEROSI PARAMETRI IN GRADO DI VALUTARE LE DIVERSE FUNZIONI EPATICHE TESTS DI CITOLISI (Valutano il danno dell’epatocita con fuoriuscita dei componenti cellulari che vengono liberati nel sangue (TRANSAMINASI, cioè ALT, AST) TESTS DI SECREZIONE BILIRUBINA DIRETTA e INDIRETTA, ACIDI BILIARI TEST DI ESCREZIONE AMMONIACA TESTS CHE VALUTANO LA CAPACITA’ DI SINTESI PROTEICA ALBUMINA, FATTORI DELLA COAGULAZIONE, COLESTEROLO, COLINESTERASI ENZIMI DI COLESTASI FOSFATASI ALCALINA (ALP), GAMMAGLUTAMILTRANSPEPTIDASI (GGT) CIRROSI EPATICA E ’ la conseguenza di una continuata risposta cicatriziale ad un danno epatico cronico (che induce necrosi cellulare). Il risultato finale è la distruzione della normale architettura del fegato che viene sostituito da fibrosi (con cicatrici e setti ) e formazione di noduli epatici. Insorge in seguito al progredire di alcune malattie che agiscono come stimoli infiammatori cronici sulle cellule del fegato. La trasformazione dell'organo in tessuto fibroso interferisce con le normali funzioni del fegato. PATOGENESI DELLA FIBROSI: l’attivazione delle cellule stellate è seguita da proliferazione dei fibroblasti e deposito di collagene La cirrosi trasforma il fegato in una massa dura e nodulare. In questo caso i noduli hanno un diametro maggiore di 3 mm e quindi si parla di cirrosi macronodulare; è di tipo micronodulare se i noduli hanno diametro minore di <3 mm. CAUSE DI CIRROSI: - VIRUS -Abuso di alcool (etilismo):. Metà dei casi di cirrosi è provocata dall'alcool. -Cirrosi biliare primitiva: è una malattia rara, che colpisce soprattutto le donne. In questi pazienti, per motivi ancora sconosciuti, lo stesso organismo sferra un attacco contro il proprio fegato -Epatite attiva cronica autoimmune: è un'altra condizione rara, in cui il sistema immunitario attacca e distrugge le cellule epatiche. -Farmaci e altre sostanze chimiche: diversi farmaci e sostanze chimiche possono danneggiare il fegato ma pochi provocano cirrosi. La somministrazione di alcuni farmaci deve essere comunque controllata perché essi influiscono sul fegato. Fra i farmaci ad azione lesiva sul fegato devono essere citati il metotrexate e l'amiodarone -Ostruzione del deflusso venoso del fegato: malattia veno-occlusiva, sindrome di Budd- Chiari, pericardite costrittiva - Disturbi metabolici ed ereditari: condizioni rare in cui si verifica un accumulo di tossine nel fegato. La più diffusa è l'emocromatosi, che causa un deposito eccessivo di ferro in questo organo. morbo di Wilson, deficit di alfa-1 antitripsina, diabete mellito, glicogenosi di tipo IV, galattosemia, tirosinosi congenita. Virus dell'epatite B (HBV) •Negli adulti la cronicizzazione si osserva in ~ 7% dei casi •La cronicizzazione dell'infezione può associarsi: alla condizione di portatore asintomatico del virus, con malattia epatica assente) oppure ad epatiti croniche con possibile evoluzione in cirrosi (in ~ 10 anni) e successivo sviluppo di epatocarcinoma. La cirrosi da HBV è prevalente in età relativamente giovane (~ 40 anni). Nei soggetti sottoposti a trapianto epatico la reinfezione con HBV determina una malattia epatica aggressiva e rapidamente progressiva in cirrosi. Esiste una elevata associazione epidemiologica tra infezione cronica da HBV e sviluppo di carcinoma epatocellulare. Il rischio di sviluppo di epatocarcinoma in portatori di HBsAg è 30-100 volte maggiore che non nella popolazione generale Virus dell'epatite C (HCV) La malattia epatica HCV-indotta evolve in cirrosi in almeno il 20% dei casi. Evoluzione rapida e grave in 2-5 anni nel 10% dei casi, in 6-15 anni nel 30% ed in 16-30 anni nel 60%. La cirrosi epatica da HCV è caratterizzata da scarsi sintomi e da buon compenso per molti anni. Esistono comunque rari casi che presentano una rapida insorgenza di scompenso e spesso si complicano con lo sviluppo di un epatocarcinoma primitivo epatico (HCC). L'HCC presenta una incidenza annua del 3-5% nei pazienti con cirrosi da HCV. Non sembra che il paziente con cirrosi HCV-indotta abbia un rischio di sviluppare la neoplasia maggiore di quelli con cirrosi da HBV o da alcool. La coesistenza di infezione cronica da HBV ed HCV aumenta considerevolmente il rischio di sviluppo di HCC. Il ruolo di HCV nell'eziopatogenesi dell'epatocarcinoma nelle nostre aree geografiche non sembra dipendere da un effetto diretto del virus su oncogeni o sulla regolazione genica della moltiplicazione cellulare, ma dalla sua capacità di indurre l' evoluzione in cirrosi, che è condizione quasi indispensabile per lo sviluppo di HCC. Virus dell'epatite Delta (HDV) •Possibili 2 forme di epatite acuta da HDV: •Coinfezione: inoculum contemporaneo di HBV + HDV in soggetto recettivo con conseguente epatite acuta Delta, spesso autolimitante, con elevati valori di transaminasi e doppio picco di citolisi (il primo da HBV ed il secondo da HDV); possibili anche forme fulminanti. •Superinfezione: inoculum di HDV in portatore cronico di HBsAg con epatite acuta Delta e successiva cronicizzazione; costante l'aggravamento della malattia epatica preesistente alla superinfezione. •Evolvono in epatite cronica il 10% delle forme da coinfezione e quasi tutte le forme da superinfezione. •L'evoluzione in cirrosi avviene nell'80% dei casi di epatite cronica. EPATOPATIA ALCOOLICA dalla steatosi epatica (conseguenza reversibile dell'ingestione acuta di alcool), sino alla cirrosi irreversibile. circa 20% progredisce verso l'epatite alcoolica o la cirrosi. Fattori di rischio per lo sviluppo di queste sequele più gravi: - Durata ed entità dell'ingestione alcoolica E’ stato stimato che sia necessario per lo sviluppo della cirrosi un introito totale medio di 80 grammi di etanolo al giomo per 20 anni, ma il rischio relativo di malattia epatica cronica aumenta sostanzialmente già con 40-60 grammi/die (80 grammi di etanolo equivalgono a 8 birre da 330 ml, ad un litro di vino o a mezza pinta di superalcoolici). La progressione viene influenzata solo dalla quantità totale e non dal tipo di bevanda o modalità di ingestione. - Sesso femminile - Infezione da epatite B o C. accelerante del danno epatico nel pz che beve in eccesso. - Fattori genetici esiste una predisposizione ereditaria all'alcoolismo. L'aumentata suscettibilità al danno dell'organo può anche essere legata a certi isoenzimi dell'alcool deidrogenasi, il principale enzima metabolizzante dell'etanolo. -Stato nutrizionale La malnutrizione non è dovuta solo al ridotto introito, ma anche ad un anomalo metabolismo dei nutrienti. La scarsa nutrizione può contribuire all'evoluzione della malattia epatica alcoolica, ma una nutrizione adeguata non ne previene lo sviluppo. ANATOMIA PATOLOGICA La steatosi (gocce di grasso negli epatociti), è una conseguenza rapida e reversibile della tossicità da alcool. Non è patognomonica di patologia epatica alcoolica; può essere osservata nella patologia epatica da farmaci, nell'obesità, nell'ipertrigliceridemia, nel diabete mellito, nella malnutrizione La steatosi epatica è associata ad epatomegalia moderata-severa ed occasionalmente, a dolorabilità a livello del quadrante superiore destro e disturbi epigastrici. Gli esami di funzionalità epatica sono solitamente normali o solo lievemente alterati, l'ittero è insolito. La lesione si può sviluppare in seguito ad un unico abuso alcoolico. Affinchè si sviluppi epatite alcoolica sono necessarie in genere molte settimane o mesi di abusi alcoolici. Gli esami evidanziano un rialzo della AST e della ALT <500, che diminuiscono dopo molti giorni e sono seguite da un rialzo più prolungato ed a volte severo della bilirubina (fino a 20 volte i valori normali). L'uso concomitante di paracetamolo, in particolare può provocare un danno epatico severo . L'evidenza di una disfunzione epatica nei pazienti con epatite alcoolica suggerisce l'eventualita di una concomitante cirrosi. Aspetti tipici includono rialzi del tempo di protrombina che non rispondono alla vitamina K, ipoalbuminemia, ascite e/o encefalopatia. Conseguenze cliniche della cirrosi: dalla completa assenza di sintomi all'insufficienza epatica dipendono sia dalla natura e severità della sottostante patologia epatica che dalla estensione della fibrosi. Le manifestazioni cliniche possono essere grossolanamente classificate A- derivanti da una ridotta funzionalità epatocellulare (es. ittero e coagulopatia), B- derivante da un’ alterazione fisica del parenchima epatico (es. varici esofagee ed ascite). I sintomi Nelle prime fasi, i sintomi possono anche essere assenti e la malattia viene individuata durante indagini che sono state fatte per altri motivi. Con il progredire della malattia, possono manifestarsi affaticabilità, debolezza, mancanza di forze, perdita dell'appetito, nausea e dimagrimento. Nelle fasi più avanzate, il fegato fatica a compiere tutte le sue funzioni e possono comparire alcuni o tutti i seguenti sintomi. Ittero: ingiallimento della pelle e delle sclere degli occhi per l'incapacità del fegato di eliminare la bilirubina dal sangue. Ascite e edemi agli arti inferiori: sono frequenti con l'aggravarsi della malattia. Una funzione importante del fegato è contribuire a liberare il corpo dei liquidi in eccesso attraverso i reni e, quando ciò non avviene, questi liquidi si accumulano nell'addome (ascite) o nelle gambe (edema). Splenomegalia (aumento del volume della milza) e di varici venose della parete addominale indicano che si è instaurato un quadro di ipertensione portale; Emorragia digestiva (ematemesi): Encefalopatia: confusione, sonnolenza e, alla fine, coma. Predisposizione alla formazione di ematomi, di ecchimosi, di "porpora" e di "petecchie": il naso può sanguinare e si formano facilmente ematomi e ecchimosi a causa di una insufficiente produzione di fattori della coagulazione da parte del fegato e della riduzione del numero di piastrine; Spider nevi (angiomi stellati o aracnoidei che si formano sulla pelle, in particolare quella della schiena come piccole macchie circondate da sottili vasi sanguigni) dovuti ad alterazioni dei vasi periferici. È frequente anche l'arrossamento del volto. Alterazioni delle unghie: possono cambiare la forma e l'aspetto delle unghie. Alterazioni della pelle: in circa un quarto dei pazienti, la pelle si scurisce. Ginecomastia (Ingrossamento delle mammelle negli uomini): il fegato distrugge gli ormoni sessuali femminili; nella cirrosi, essi si accumulano provocando l'ingrossamento delle mammelle e l'atrofia (restringimento) dei testicoli negli uomini. Malnutrizione e perdita dei muscoli: I pazienti cirrotici malnutriti mostrano una rallentata produzione di energia che dipende in gran parte dall'ossidazione del grasso endogeno. La perdita di tessuto muscolare si correla alla ridotta sintesi di proteine muscolari, con una riduzione complessiva del turnover di proteine di tutto il corpo. L'ulcera peptica è frequente in associazione alla cirrosi alcoolica. Come si fa la diagnosi di cirrosi? Se l'esame clinico fa sorgere il sospetto di trovarsi di fronte a una cirrosi, la diagnosi può essere confermata con le analisi del sangue. Esami del sangue: non è raro che si faccia diagnosi di malattia cronica epatica e di cirrosi perché vengono rilevati nel sangue livelli elevati di transaminasi (GOT e GPT o AST e ALT). I pazienti cirrotici presentano abitualmente anche altre alterazioni negli esami del sangue: - aumento della bilirubina (perché il fegato non riesce più a depurarla dal sangue in maniera ottimale); - riduzione dei fattori della coagulazione, in particolare dell'attività protrombinica (per un difetto dell'utilizzazione della vitamina K nel fegato) - riduzione dei livelli di albumina (il fegato non ne produce in quantità adeguata) - riduzione del numero di piastrine (per il sequestro che avviene all'interno della milza, la quale si ingrossa a causa dell’epatopatia cronica) Il cambiamento dell'aspetto del fegato: visualizzazione diretta, per esempio durante una laparotomia (apertura della cavità addominale) o alla laparoscopia (visualizzazione dell'interno della cavità addominale attraverso micro-telecamere). In genere questi sistemi sono però inapproriati per arrivare alla diagnosi di cirrosi e oggi non vengono più usati. L'ecografia suggerisce la diagnosi di cirrosi quando evidenzia aree dense riflettenti a distribuzione irregolare ed aumentata ecogenicità. Il lobo caudato è aumentato di volume relativamente al lobo destro. Tuttavia, l'ecografia non è una metodica affidabile per la diagnosi di cirrosi a meno che non siano già presenti quadri eclatanti. La diagnosi della cirrosi e delle sue complicanze con la Tomografia assiale computerizzata (TAC) ha un buon rapporto costo-beneficio. Può essere valutata la grandezza del fegato e osservata la superficie nodulare irregolare. Se non esistono controindicazioni, come l'ascite o un deficit della coagulazione, la biopsia può fornire indicazioni sull'eziologia e l'attività. La prognosi La prognosi e il trattamento dipendono dall'entità dei sintomi. L'insufficienza epatica viene valutata in base alla presenza di segni quali - l'ittero, - l'ascite, - l'encefalopatia, - i bassi livellli di albumina, - le transaminasi aumentatate ed - il deficit di protrombina che non si corregge dopo somminstrazione di vitamina K. Il metodo più comune per determinare il grado di insufficienza del fegato è quello di Child-Pugh, che calcola la classe di appartenenza del paziente partendo da pochi dati clinici. La cirrosi è comunque una condizione grave. Solo il 30 per cento dei pazienti sopravvive per più di 5 anni dopo la diagnosi e la prognosi è ancora peggiore se la cirrosi è provocata dall'alcool e il paziente non cessa di bere. La terapia La progressiva distruzione del fegato può essere arrestata, o almeno rallentata, eliminando la causa che l'ha provocata. È necessario smettere l'assunzione di bevande alcoliche. -L'epatite B e l'epatite C croniche possono essere curate con cure specifiche, in base alle condizioni cliniche. - Il sovraccarico di ferro può essere eliminato attraverso prelievi regolari di sangue. - L'epatite attiva cronica autoimmune può essere trattata con corticosteroidi. A parte l'eliminazione della causa, la cirrosi epatica non può essere curata. Quindi, è importante trattare e cercare di alleviare le complicazioni. Anche se il danno non può essere riparato, è comunque possibile alleviare i sintomi e tenerli sotto controllo. Se la terapia viene iniziata tempestivamente, il malato può condurre una vita quasi normale. Se invece la causa non viene eliminata, la formazione di tessuto cicatriziale e la distruzione della struttura dell'organo continuano, provocando alla fine insufficienza epatica. I rimedi più comuni sono: Diuretici per la terapia della ritenzione idrica agli arti inferiori (edema) o nell'addome (ascite). Integrazioni di vitamine e sali minerali Integrazioni caloriche (in genere, bevande dolcificate) per rafforzare l'alimentazione Lassativi (di solito, lattulosio, una soluzione sciropposa) per prevenire la stitichezza e ridurre la possibilità che le tossine intestinali "scavalchino" il fegato e raggiungano il cervello provocando sonnolenza, confusione e coma (encefalopatia epatica). Ad alcuni pazienti con emorragie per rottura di varici nella parte inferiore dell'esofago può essere prescritto il propranololo, un farmaco che abbassa la pressione in queste vene riducendo l'eventualità di un nuovo sanguinamento. Il trapianto di fegato è oggi la terapia migliore per il trattamento della cirrosi. Contrariamente a quello che veniva affermato fino a qualche anno fa, devono oggi essere considerati per il trapianto quei pazienti che non sono ancora arrivati allo stadio più grave della malattia. Quindi, è bene valutare subito per questo intervento quei pazienti che, pur ancora in buone condizioni generali, hanno già avuto almeno uno dei sintomi che identificano la cirrosi scompensata (ascite, encefalopatia, ittero, emorragia digestiva da rottura delle varici esofagee). Per tutti questi pazienti devono essere valutati, oltre che anche il trapianto di fegato da donatore vivente. L’epatocarcinoma (tumore del fegato) può essere curato in diversi modi, includendo l'asportazione chirurgica di una parte del fegato qualora il fegato del paziente funzioni ancora abbastanza bene e non vi sia né ascite né ipertensione portale. COMPLICANZE DELLA CIRROSI IPERTENSIONE PORTALE si verifica quando la pressione della vena porta supera la pressione delle vene addominali non-portali (es. vena cava inferiore) di almeno 5 mm Hg, portando alIa formazione di vasi collaterali porto-sistemici nel tentativo di eguagliare la pressione tra questi due sistemi venosi. Questi vasi collaterali, o varici, si sviluppano più comunemente nell'esofago e nello stomaco prossimale e possono provocare sanguinamenti clinicamente significativi. L'incremento della pressione portale nella cirrosi è principalmente il risultato della resistenza al flusso ematico attraverso il fegato fibrotico e duro. ASCITE è un accumulo di fluidi in eccesso nell'addome. La cirrosi è la causa principale per almeno l'80% dei pazienti Patogenesi: -Ipertensione sinusoidale: si instaura a causa di un'aumentata resistenza al flusso legata al deposito di matrice; con la progressione della fibrosi, solo i fluidi senza proteine riescono ad attraversare i sinusoidi, entrando nei linfatici epatici. L'accumulo continuo di linfa supera le capacita di drenaggio linfatico e l'eccesso di fluido "trasuda" dal fegato nella cavità peritoneale. –Ipoalbuminemia: peggiora con l'avanzare della disfunzione epatica e riduce la pressione oncotica che richiama il fluido verso l’interno del vaso. -Aumentato riassorbimento di sodio da parte dei reni, legato probabilmente a fattori umorali. -Vasodilatazione arteriolare splancnica, che può stimolare in modo indipendente la ritenzione di sodio e di acqua libera TRATTAMENTO: -La maggior parte dei pz risponde alla restrizione dietetica di sodio e al diuretico. Lo spironolattone dovrebbe essere iniziato ad un dosaggio di 100 mg/die fino a 400 mg per ottenere una perdita di peso di circa 500 – 700 gr/die. -Paracentesi SINDROME EPATORENALE Conosciuta anche come insufficienza renale funzionale, un'insufficienza renale associata a grave malattia epatica senza anomalie intrinseche del rene. E’ tipicamente presente ascite. Aspetti tipici sono la riduzione dl flusso renale, della perfusione corticale e del filtrato glomerulare. Un ruolo importante è giocato dagli elevati livelli circolanti di endotelina-1, un potente vasocostrittore. La diagnosi viene posta in un paziente cirrotico documentando sodio urinario molto basso 10 mEq/litro) ed oliguria senza deplezione del volume intravascolare. La prognosi della sindrome epatorenale è molto scadente, in parte perchè la comparsa della sindrome denota una malattia epatica alI'ultimo stadio. ENCEFALOPATIA EPATICA (coma epatico o encefalopatia porto-sistemica) una sindrome neuropsichiatrica reversibile che può accompagnare la patologia epatica avanzata scompensata di qualsiasi natura e/o lo shunt porto-sistemico esteso. L'encefalopatia è almeno in parte attribuibile ai materiali tossici derivanti dal metabolismo dell’azoto degli aminoacidi formati nell'intestino che by-passano il fegato attraverso shunts anatomici o funzionali. Per questo motivo, viene usato il termine encefalopatia porto-sistemica. L'ammonio ed i mercaptani vengono prodotti rispettivamente dalla degradazione dell'urea o delle proteine e dai composti contenenti zolfo e probabilmente la presenza dei mercaptani nell'aria espirata di alcuni pazienti è responsabile del caratteristico odore dolciastro definito fetor hepaticus. Gli esami di laboratorio evidenziano un aumento dell’ammoniemia. MANIFESTAZIONI NEUROLOGICHE. I pazienti con encefalopatia epatica manifestano un caratteristico spettro di alterazioni mentali e motorie.
Scaricare