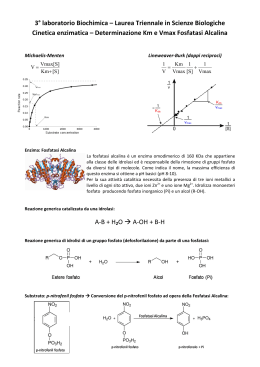
6WDQGDUGL]]D]LRQH LQWUDRVSHGDOLHUDGHL PHWRGLDQDOLWLFL /DIRVIDWDVLDOFDOLQD $XWULFH &KLDUD6LODFFL Anno scolastico 2003-2004 Lavoro pubblicato il 1° giugno 2004 Lavoro di diploma per l’ottenimento del diploma di ODERUDWRULVWDPHGLFR svolto presso il Laboratorio ospedaliero dell’Ospedale Regionale Bellinzona e Valli Responsabile del posto di stage: Tutor: Roberto Francesconi Luigi Fraschini ,QGLFH pag. Riassunto 3 1. Introduzione 4 2. Materiali e metodi 8 1.1 2.1 2.2 2.3 2.4 La fosfatasi alcalina Reflotron Sprint Pipetta Eppendorf (32 mL) Hitachi 912 Trattamento dei campioni 3. Risultati 3.1 3.2 Calibrazione della pipetta Eppendorf (32 mL) Riproducibilità degli apparecchi 3.3 Test per il fattore di conversione 3.2.1 Hitachi 912 3.2.2 Reflotron Sprint 5 8 10 10 13 14 14 15 15 16 17 4. Discussione 20 5. Conclusioni 22 6. Ringraziamenti 23 7. Bibliografia 24 Allegato 1 - Risultati dei test eseguiti Allegato 2 - Morbo di Paget 5LDVVXQWR Nei laboratori dell’ORBV (Bellinzona, Acquarossa, Faido) alcune analisi vengono svolte con apparecchi diversi. Per lo stesso paziente vengono rilevati dei valori che presentano delle differenze soprattutto dovute al fatto che gli apparecchi sono di generazioni diverse e lavorano con princìpi diversi. A Bellinzona l’attività della fosfatasi alcalina (fosfoidrolasi di un monoestere fosforico) viene misurata con l’Hitachi 912, mentre ad Acquarossa con il Reflotron Sprint. L’obiettivo del presente lavoro è stato quello di determinare un fattore di conversione che permettesse di rendere le analisi, svolte nell’uno e nell’altro laboratorio, comparabili. Mediante una serie di test effettuati sui medesimi campioni nei laboratori di Bellinzona e di Acquarossa è stato possibile definire un fattore di conversione di 2.18 per la fosfatasi alcalina. I valori ottenuti ad Acquarossa devono essere divisi per questo fattore di conversione, mentre, ovviamente, quelli di Bellinzona devono essere moltiplicati. Il medico avrà perciò a disposizione un valore calcolato come se l’analisi fosse avvenuta con i criteri, con i quali egli è abituato a formulare una diagnosi. L’analisi dell’attività della fosfatasi alcalina è quella che dava maggiori problemi di comparabilità. I risultati ottenuti a Bellinzona, e considerati nella norma, potevano essere, se l’analisi veniva effettuata con l’apparecchio di Acquarossa, patologici. Per questa ragione è stata scelta per questo lavoro di ricerca. In seguito lo stesso tipo di lavoro dovrà essere svolto anche con altri tipi di analisi. 3DUROHFKLDYH analisi – diagnosi – conversione – test – comparabile – fosfatasi alcalina. 2 ,QWURGX]LRQH Ho scelto di approfondire il tema “Standardizzazione intraospedaliera dei metodi analitici: la fosfatasi alcalina.” perché nell’istituto (ORBV) dove ho svolto il mio lavoro di diploma, costituito da tre sedi (Bellinzona, Acquarossa e Faido), si è potuto constatare che vi sono delle importanti differenze nella determinazione di diversi parametri, eseguiti su apparecchi differenti e con tecniche differenti. Lo scopo del lavoro è quindi quello di determinare se è possibile applicare dei fattori di conversione dei risultati dell’uno o dell’altro test, affinché i dati ottenuti possano diventare comparabili. I test scelti per lo sviluppo del lavoro sono eseguiti con due apparecchi: - Hitachi 912 - Reflotron Sprint. Il primo viene utilizzato a Bellinzona, mentre il secondo è in uso ad Acquarossa. Le analisi comuni svolte con questi due apparecchi sono: Glucosio Urea Creatinina JOXWDPLOWUDVIHUDVL *7 Fosfatasi alcalina (ALP) Aspartato-aminotrasferasi (ASAT) Alanina-aminotrasferasi (ALAT) Creatinchinasi (CK) Amilasi Bilirubina Potassio In tutte le analisi indicate vi sono dei problemi di corrispondenza dei risultati. Per ragioni diagnostiche invece i risultati dovrebbero essere facilmente confrontabili. L’analisi che pone maggiori problemi è la fosfatasi alcalina. Per questa ragione ho deciso, in accordo con il sig. Luigi Fraschini, tutor per il mio lavoro di diploma, di concentrarmi sulla determinazione di un fattore di conversione per quest’ultima. Come mai i risultati di queste analisi ottenuti su un apparecchio semi-automatico, il Reflotron Sprint (pipettaggio manuale) non possono essere confrontati con i risultati ottenuti su un apparecchio automatico, l’Hitachi 912? Questa è la domanda che mi sono posta quando ho conosciuto il tema del mio lavoro di diploma. Ho dapprima supposto che ci fossero degli errori in fase di preparazione dell’analisi, ossia nella preanalitica. Nell’apparecchio semi-automatico la preparazione è manuale: l’operatore esegue il pipettaggio del campione e quindi è possibile che una manipolazione non perfetta possa comportare degli errori. Si trattava perciò di eseguire l’analisi adottando con la maggiore precisione possibile le tecniche di laboratorio apprese. Naturalmente la possibilità di errore in questa manipolazione non è esclusa, soprattutto se le analisi vengono effettuate da più persone. 3 La seconda ipotesi è che la pipetta sia imprecisa, cioè che ad un valore nominale non corrisponda l’effettiva quantità di sostanza pipettata. Ho perciò eseguito una calibratura della pipetta, secondo le indicazioni contenute nelle modalità d’uso della pipetta, prodotta dalla ditta Eppendorf 1. Con la tecnica della riproducibilità (20-30 misurazioni dei risultati ottenuti sullo stesso campione) ho verificato che gli apparecchi fossero precisi. Verificata l’assenza di problemi in queste tre prime ipotesi ho pensato che fosse possibile determinare un fattore di conversione. Questo dovrebbe facilitare i medici a meglio comprendere i valori ottenuti in un ospedale piuttosto che in un altro. Per ragioni di lettura immediata del testo ho preferito introdurre le abbreviazioni in corrispondenza della prima citazione dell' elemento di testo a cui si riferiscono, invece di aggiungere un lessico finale. /DIRVIDWDVLDOFDOLQD Figura 1: modello molecolare della fosfatasi alcalina2 La fosfatasi alcalina è un enzima non organo-specifico, che interviene nel metabolismo dei composti fosforici organici presenti in tutti i tessuti e particolarmente abbondanti nel fegato, nelle ossa, nell’intestino e nei reni, catalizzando l’idrolisi a pH alcalino di parecchi fosfomonoesteri. È associata a membrane citoplasmatiche e microsomi delle cellule della mucosa dell’intestino tenue, del tubulo convoluto prossimale del rene, degli osteoblasti, degli epatociti e del sinciziotrofoblasto placentare. L' esatto ruolo fisiologico dell' enzima non è stato stabilito ma si pensa che esso intervenga nel processo di calcificazione dell' osso. Utilizzata per la prima volta nella diagnostica delle malattie ossee da Robinson nel 1923, la AP venne in seguito largamente studiata ed applicata. Una svolta essenziale per l' interpretazione del significato clinico di questo enzima fu il riconoscimento della sua eterogeneità molecolare e la possibilità di applicare l' analisi isoenzimatica per identificare le varie forme in cui può presentarsi nel siero in diverse e specifiche situazioni anatomo-cliniche. Si sa ora che tale eterogeneità è in parte dovuta a fattori genetici (DNA) ed in parte a modificazioni post-translazionali. Nel siero è composta da quattro genotipi strutturali: il tipo fegato-ossa-reni, il tipo intestinale, il tipo placentare e la variante derivante dalle cellule germinali. Il tipo fegato-ossa-reni è 1 2 Eppendorf-Netheler – Hinz GmbH, Hamburg Research Collaboratory for Structural Bioinformatics (RCSB) - Protein Data Bank - http:/ / www.rcsb.org/ pdb/ 4 particolarmente importante per le numerose patologie riscontrate in caso di variazione rispetto ai valori normali. Figura 2: Modalità di detezione dell’attività dell’enzima fosfatasi alcalina nei tessuti3 3 Constance Cepko, Elizabeth Ryder, Donna M. Fekete, and Suzanne Bruhn, Harvard Medical School and the Howard Hughes Medical Institute Boston, MA 02115 - DETECTION OF ß-GALACTOSIDASE AND ALKALINE PHOSPHATASE ACTIVITIES IN TISSUE - http:/ / axon.med.harvard.edu/ ~ cepko/ protocol/ xgalplap-stain.htm 5 La tabella seguente4 indica le variazioni della fosfatasi alcalina per diverse patologie: ',0,18=,21( $80(172ILQRDYROWHL YDORULQRUPDOL $80(172ILQRDYROWH $80(172ILQRDYROWHL LYDORULQRUPDOL YDORULQRUPDOL Iperparatiroidismo Cirrosi biliare primitiva Cachessia Epatiti virali Metastasi ossee Acondroplasia Epatiti croniche Rachitismo, osteomalacia Atresia congenita delle vie biliari Colestasi extraepatica Scorbuto Cirrosi epatiche Morbo di Paget 5 Sarcoma osteogenico Plasmocitoma Osteite deformante Ipotiroidismo Epatite alcolica Ipofosfatasia ereditaria Mononucleosi infettiva (3a sett.) Carenza di Mg Colangite Anemie gravi Fratture ossee Morbo di Cushing Ittero ostruttivo incompleto Intossicazione da vitamina D Displasia fibrosa Gravidanza Colestasi iatrogena Nei bambini e nei giovani (16-18 anni), l’aumento considerevole della fosfatasi alcalina è causata dall’aumento dell’attività osteoblastica in seguito ad una crescita ossea accelerata. Inoltre nella donna in gravidanza la fosfatasi alcalina aumenta in seguito alla crescita del feto e alla formazione della relativa placenta. Figura 3: sito attivo dell’AP. Per attivarsi la molecola di AP deve avere in corrispondenza del sito attivo due atomi di zinco (azzurre) 4 5 Laboratorio di analisi chimiche Brusca, Roma, http:/ / web.tiscali.it/ labanalisibrusca/ Negli allegati è inserito un testo di presentazione che ho utilizzato per le lezioni di inglese ALP su Hitachi 912 (U/ L) 6 0DWHULDOLHPHWRGL Come già anticipato i due apparecchi a confronto sono il Reflotron Sprint, che viene utilizzato presso il Laboratorio ospedaliero dell' Ospedale di zona di Blenio ad Acquarossa e l’Hitachi 912, che viene invece utilizzato presso il Laboratorio ospedaliero dell' Ospedale San Giovanni di Bellinzona. In questo capitolo li presenterò, aggiungendo un capitolo importante per il Reflotron, ossia la pipetta utilizzata, prodotta dalla ditta Eppendorf. 5HIORWURQ6SULQW Figura 4: Reflotron Sprint Il sistema Reflotron Sprint utilizza la tecnologia della dry chemistry (chimica secca), ossia una tecnica che permette la determinazione dei parametri senza utilizzare reagenti allo stato liquido. L' operatività è facilitata dalla presenza dei reagenti già essiccati sulla striscia reattiva e dal codice magnetico per la trasmissione allo strumento dei dati relativi all' analisi da effettuare e al lotto di reagenti utilizzati. Vantaggi: - può effettuare analisi singole o in piccole serie direttamente su sangue intero può essere utilizzato anche da personale non specializzato, grazie alla semplicità d’uso fornisce risultati affidabili in tempi brevi (3 minuti ca.). Applicando una goccia di sangue intero (non centrifugato) sulle cartine che vengono utilizzate per le analisi di chimica secca, gli eritrociti vi si depositano sopra, mentre il plasma si diffonde (per capillarità) nello strato sottostante zona di raccolta del plasma. Questa zona si trova sotto i due strati contenenti i reagenti. La parte magnetica presente sulla striscia reattiva contiene le seguenti informazioni: tipo di test tempo di incubazione e momento di inizio della reazione lunghezza d’onda utilizzata per la misura numero di misure e intervalli tra le misure metodo per il calcolo dei risultati fattori di conversione tra unità SI e unità convenzionali I risultati delle analisi possono variare leggermente da lotto a lotto a causa delle piccole differenze nel materiale usato per ogni zona reattiva. Per questa ragione viene eseguito un accurato controllo di qualità (CQ) e il calcolo dei risultati viene ripetuto diverse volte per ciascun lotto. Questo assicura dei risultati sempre più affidabili. 7 La procedura di lavoro con l’apparecchio, una volta pipettato il campione, è la seguente: inserire la striscia reattiva e chiudere lo sportello mentre la striscia viene portata in posizione di misura, lo strumento esegue automaticamente la prima funzione: lettura del codice. Questa lettura permette l’esecuzione del procedimento analitico e del calcolo dei risultati mettere in incubazione Durante l’incubazione viene separato il plasma e la temperatura deve raggiungere 37°C. In uno stadio successivo la testina di misura preme i reagenti contro la zona sottostante, contenente il plasma, in modo da mettere a contatto i campioni di plasma con i reagenti del test. inizio della reazione. Il colore sviluppato viene registrato attraverso una pellicola trasparente dal sistema ottico. La lunghezza d’onda viene scelta fra le tre differenti sorgenti luminose, a seconda del tipo di test (567 nm, 642 nm, 951 nm). La zona reattiva viene illuminata dalla luce diffusa emessa dai LED e riflessa dalle pareti bianche della sfera di Ulbricht. Questo tipo di misura elimina ogni possibilità di errore. Figura 5: Schema della striscia reattiva Valori di riferimento6: Pz þ: 106-265 U/L Pz : 83-223 U/ L CQ: 133-163 U/ L 6 Per la fosfatasi alcalina 8 Principio del test 7 Il campione applicato sulla striscia reattiva, penetra nella zona di reazione. La fosfatasi alcalina (ALP) idrolizza il fosfato di o-cresoftaleina in o-cresolftaleina trasferendo il gruppo fosfato alla molecola di metilglucamina. Il prodotto colorato derivato dall’idrolisi o-cresoftaleina è prodotto per unità di tempo in ambiente alcalino in quantità direttamente proporzionale dell’attività delle fosfatasi alcaline. o-cresoftaleina fosfato + metilglucamina ALP o-cresolftaleina+ metilglucamina fosfato Ad una temperatura di 37°C il colore sviluppato dalla reazione viene misurato cineticamente a 567 nm ed il risultato appare sul display dopo circa 135 secondi. Il campione viene preparato manualmente, con l’ausilio della pipetta Eppendorf, che descrivo. 3LSHWWD(SSHQGRUIm/ Figura8 6 La gamma di produzione a cui appartiene la pipetta utilizzata (32 L). La pipetta Eppendorf (32 mL) è uno strumento che permette di misurare con precisione dei piccoli volumi, cioè anche il quantitativo necessario per le analisi con il Reflotron Sprint. Queste pipette funzionano con un sistema a stantuffo. Se lo stantuffo non è in posizione corretta, il volume sarà sbagliato e quindi l’analisi potrebbe dare dei risultati non corretti. È per questo che bisogna calibrare le pipette Eppendorf con una certa frequenza, ogni 6 mesi (ca.). Per farlo è sufficiente avere una bilancia analitica, e un po’ di acqua. Calibrare significa pesare il volume che può misurare la pipetta. In questo caso si peseranno 32 mL. +LWDFKL 9 Figura 7: Hitachi 912 Hitachi 912 è un sistema analitico che utilizza la tecnologia della CHIMICA LIQUIDA, ossia per la determinazione dei parametri chimico-clinici vengono utilizzati esclusivamente dei reagenti allo stato liquido. L’affidabilità, il consolidamento analitico, la flessibilità e l’elevata produttività ne fanno il sistema ideale per piccole-medie routine. Sono possibili 100 analisi diverse. 7 idem Eppendorf-Netheler – Hinz, Amburgo: http:/ / www.eppendorf.com/ en/ index.php 9 Roche Diagnostics – Laboratorio – Prodotti: http:/ / roche-diagnostics.it/ prodotti/ Laboratorio/ 8 9 Vantaggi: - esecuzione di 720 test all’ora 32 canali in linea autocalibrazione prediluizione automatica pronto all’uso 24 h su 24 h lettura codice a barre dei campioni lettura codice a barre dei reagenti punto finale, cinetica enzimatica e chimica isoenzimatica ISE bianco campione automatico 115 posizioni per la routine, per i calibratori, per i CQ e per le soluzioni di lavaggio Inoltre l’Hitachi 912 presenta le seguenti altre caratteristiche: - robustezza delle parti meccaniche affidabilità continua gestione efficiente minima manualità di gestione software operativo Windows NT riconoscimento positivo di campioni e reagenti mediante codice a barre caricamento di provette primarie e secondarie aiuto in linea avviamento entro tre minuti dalla condizioni di stand by possibilità di selezionare campioni urgenti con esecuzione prioritaria sulla routine L’Hitachi 912 viene calibrato una volta al giorno (a mezzogiorno, presso l’OSG). Malgrado lo strumento sia molto affidabile la calibrazione viene controllata una seconda volta, a mezzanotte. La calibrazione avviene nel modo seguente: - - lo strumento deve essere in situazione STOP a questo punto viene spento in seguito vengono aperti i due vani portareagenti refrigerati (1, 2 nella figura a lato) e sostituiti o rabboccati i reagenti consumati vengono chiusi i due vani e lo strumento viene riavviato lo strumento legge automaticamente i codici a barre dei reagenti Figura 8: Visione della zona operativa dell’Hitachi 912 sullo schermo del computer viene controllato dall’operatore che i barcode siano stati letti in modo corretto. In caso contrario appare sullo schermo quale analisi non può essere effettuata 10 - nell’anello interno refrigerato (3 nella figura sopra) viene immesso uno standard alto, uno basso e un compensatore per la modalità ISE. Inoltre viene aggiunto un MT (calibratore) per tutte le altre analisi quando appare sul monitor del PC “Start up calibration”, allora cliccando si avvia la calibrazione dello strumento Immediatamente dopo la calibrazione avvengono i controlli (ripetuti a mezzanotte) con la seguente procedura: - nell’anello delle urgenze (4 nella figura sopra) viene messo un campione con NaCl sul monitor si clicca sul pulsante con la scritta corrispondente al campione inserito (NaCl) e compaiono tutte le analisi che lo strumento deve fare viene cliccato “Accept/ next” e si passa al campione successivo (PU = Precinorm, controllo) viene aggiunto un campione NaCl per l’analisi CK-MB10 per evitare le interferenze con le altre si clicca su PU e su “Accept/ next”, come precedentemente, aggiungendo anche in questo caso il campione PU per l’analisi CK-MB si prosegue con NaCl due volte, la prima selezionando il pulsante corrispondente, la seconda selezionando l’analisi PCR11 a questo punto vengono selezionate i due controlli “C1” e “C2” della PCR si continua con un campione NaCl per l’analisi HDL12 e si seleziona l’analisi corrispondente per finire si selezionano i pulsanti corrispondenti MQ113 e MQ3 Valori di riferimento14: Pz þ : 40-129 U/ L Pz : 35-104 U/ L CQ1 : 36-42 U/ L CQ3 : 303-318 U/ L CQ4 : 82-101 U/ L Principio del test 15 Test colorimetrico conforme ad un metodo standardizzato. R1: tampone/ attivatori R2: substrato p-nitrofenilfosfato + H2O ALP fosfato + p-nitrofenolo 10 CK-MB = Creatinfosfochinasi per muscoli e cervello CRP = proteina C-reattiva 12 HDL = High Density Lipoprotein 13 MQ = Multi Qual 14 Per la fosfatasi alcalina 15 idem 11 11 In presenza di ioni magnesio e di zinco, il p-nitrofenilfosfato viene scisso dalle fosfatasi in p-nitrofenolo e fosfato. Il p-nitrofenolo rilasciato, proporzionale all’attività della fosfatasi alcalina, viene misurato fotometricamente. 7UDWWDPHQWRGHLFDPSLRQL Per il test della riproducibilità16 degli apparecchi, ho preso tre sieri di pazienti del giorno prima (in frigo da 24h), con valori della fosfatasi alcalina attorno al 90 U/ L, e li ho mescolati tra di loro per fare in modo che ci fosse siero a sufficienza per fare 20 misurazioni. Dopo aver misurato la riproducibilità dell’Hitachi 912, ho congelato il siero (-30°C). Un mese dopo circa ho eseguito questo test con il Reflotron Sprint ad Acquarossa. La sera prima di andare ad Acquarossa, ho preso il campione e l’ho messo in un frigobox in grado di mantenere la temperatura di congelamento costante per 24h. Arrivata ad Acquarossa l’ho scongelato (scongelamento spontaneo: circa 90 minuti a temperatura ambiente- 22°C) ed ho eseguito il test della riproducibilità del Reflotron Sprint. Per determinare il fattore di conversione ho invece preso campioni di 30 pazienti con dei valori della fosfatasi alcalina tra 80-300 U/ L. Ho cercato di prendere dei pazienti del giorno stesso, ma purtroppo, essendo giovedì, ne ho trovati ben pochi. Ho quindi deciso di prendere dei campioni del giorno prima. Poiché la fosfatasi alcalina rimane stabile per la durata di 7 giorni a TA (temperatura ambiente) o in frigorifero (4-8°C) (Vedi libretto Roche) ho potuto prendere questa decisione. Il giorno seguente sono andata ad Acquarossa per eseguire il test di confronto. Per il trasporto i campioni sono stati messi in una scatola di polistirolo con all’interno un “frigobox” avvolto nella carta da cucina, in modo da non congelare i prelievi. Ho così eseguito il test, ottenendo i risultati che descrivo nel capitolo seguente. 16 I risultati dei test di riproducibilità per l’Hitachi 912 e per il Reflotron Sprint sono presentati nel capitolo seguente 12 5LVXOWDWL &DOLEUD]LRQHGHOODSLSHWWD(SSHQGRUIm/ Per questo test ho eseguito 20 misurazioni. Pesata (g) Pesata (g) 1 2 0.032 0.032 Media 0.032 11 12 0.032 0.032 3 4 0.033 0.032 DS 0.0004588 13 14 0.032 0.032 5 6 7 8 9 10 0.032 0.032 0.032 0.031 0.031 0.033 CV 1.4338483 15 16 17 18 19 20 0.032 0.032 0.032 0.032 0.032 0.032 Per questa operazione ho usato una bilancia Mettler Toledo PB 153, n° serie 1118011563, con numero di inventario EOC IOS000249. Per la calibrazione della pipetta viene usata acqua alla temperatura di 24°C (temperatura rilevata con un termometro a mercurio immerso nell' acqua). &DOLEUD]LRQHSLSHWWD 9DORULRWWHQXWL 0.034 0.033 0.032 0.031 0.03 0.029 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 QPLVXUD]LRQL 13 5LSURGXFLELOLWjGHJOLDSSDUHFFKL +LWDFKL Questo test è stato ripetuto 20 volte, per avere dei risultati a sufficienza da confrontare. $/3VX+LWDFKL 8/ 1 93 2 91 3 93 4 92 5 6 7 8 9 10 92 92 93 92 93 92 Media 92.3 DS 0.7327 CV 0.7938 $/3VX+LWDFKL 8/ 11 93 12 91 13 92 14 92 15 92 16 17 18 19 20 92 92 92 93 94 5LSURGXFLELOLWj+LWDFKL 9DORULULVFRQWUDWL 95 94 93 92 91 90 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 QPLVXUD]LRQL 14 5HIORWURQ6SULQW Questo test è stato ripetuto 30 volte perché i risultati ottenuti dopo 20 misurazioni non erano soddisfacenti. Per una mia maggiore sicurezza, ho pensato che fosse meglio ripetere questo test più volte. Ho così potuto escludere un mio errore di pipettaggio. $/3VX5HIORWURQ 6SULQW 8/ Canale 1 193 C1 2 189 C2 3 187 C3 4 188 C2 5 6 7 8 9 10 11 12 13 14 15 185 187 188 184 180 173 186 195 184 188 193 C3 C1 C2 C3 C1 C2 C3 C1 C2 C3 C1 Media 16 188.77 DS 6.4256 CV 3.4040 $/3VX5HIORWURQ 6SULQW 8/ Canale 188 C2 17 183 C3 18 204 C1 19 192 C2 20 187 C3 21 22 23 24 25 26 27 28 29 30 190 184 196 195 185 187 198 185 186 203 C1 C2 C3 C1 C2 C3 C1 C2 C3 C1 5LSURGXFLELOLWj5HIORWURQ3OXV 200 190 180 Serie1 170 160 29 27 25 23 QPLVXUD]LRQL 21 19 17 15 13 11 9 7 5 3 150 1 9DORULULVFRQWUDWL 210 15 7HVWSHULOIDWWRUHGLFRQYHUVLRQH Il test è stato effettuato su 30 campioni. Nella tabella riassuntiva ho indicato, come elemento di influenza sul valore normale della fosfatasi alcalina, anche l’età dei pazienti, sui quali sono stati effettuati i prelievi. Per ogni campione sono stati registrati due valori, soprattutto per verificare la precisione della misurazione e quindi per lavorare su un valore medio. Si noti come con l’apparecchio Hitachi 912 i valori delle misurazioni doppie sono molto simili, mentre la variabilità dei risultati con il Reflotron Sprint è molto sensibile fino a una differenza di + 30 U/ L. Queste differenze stanno alla base della necessità di trovare un fattore di conversione diverso, ma basato sull’esperienza pratica, da quello fornito dal costruttore. Hitachi 912 1° valore Pazienti Età (U/ L) 1 51 92 2 62 164 3 40 138 4 88 154 5 49 86 6 81 131 7 95 111 8 32 250 9 91 129 10 65 94 11 88 170 12 41 101 13 69 174 14 33 121 15 67 87 16 71 96 17 95 116 18 75 95 19 92 114 20 72 93 21 73 181 22 67 99 23 66 112 24 71 139 25 67 112 26 72 86 27 33 81 28 40 173 29 49 119 30 58 135 Media 125.1 2° valore (U/ L) 94 167 140 155 87 132 111 256 131 96 176 107 180 128 92 100 121 98 119 96 186 102 116 144 115 89 83 161 124 139 128.2 Media (U/ L) 93.0 165.5 139.0 154.5 86.5 131.5 111.0 253.0 130.0 95.0 173.0 104.0 177.0 124.5 89.5 98.0 118.5 96.5 116.5 94.5 183.5 100.5 114.0 141.5 113.5 87.5 82.0 167.0 121.5 137.0 Reflotron Sprint 1° valore (U/ L) 212 404 274 316 245 280 215 509 256 228 321 215 321 225 189 217 241 197 248 232 450 204 216 253 223 240 177 291 236 271 263.5 2° valore (U/ L) 211 419 257 305 244 262 218 527 277 233 331 204 331 217 159 204 236 193 241 220 443 197 207 261 218 231 182 293 246 288 261.8 Media (U/ L) 211.5 411.5 265.5 310.5 244.5 271.0 216.5 518.0 266.5 230.5 326.0 209.5 326.0 221.0 174.0 210.5 238.5 195.0 244.5 226.0 446.5 200.5 211.5 257.0 220.5 235.5 179.5 292.0 241.0 279.5 16 Sulla base di questi dati è stato realizzato, con il software Method Validator (1999 by Philip Marquis, Metz, Francia, [email protected]), il grafico della pagina seguente. Con questo grafico è possibile determinare il fattore di conversione, che risulta essere di . I risultati dell’apparecchio Reflotron Sprint sono quindi da dividere per il fattore di conversione determinato per essere confrontabili con i valori ottenuti con l’Hitachi 912. 17 600 Reflotron 500 400 300 200 100 0 0 Hitachi 912 100 200 300 400 500 600 &RQIURQWRIRVIDWDVLDOFDOLQD Unweighted Deming regression N = 30 Slope : 2.177 [ 1.678 to 2.676 ] Intercept : -12.96 [ -71.14 to 45.22 ] 18 'LVFXVVLRQH La prima constatazione da fare è che la pipetta Eppendorf (32 mL), utilizzata nello svolgersi dell’esperienza, è molto accurata e precisa. Ho potuto verificarlo con un accurato controllo della calibrazione. L’errore di pipettaggio dovuto alla strumentazione è praticamente da escludere17 (v. tabella a pagina 14) con un buon margine di sicurezza. La media trovata è di 0.032 g e il coefficiente di variazione (CV) è 1.43 %, l’errore è praticamente nullo. Ho in seguito controllato la precisione degli apparecchi, facendo ripetutamente delle misurazioni di un campione i cui valori erano conosciuti. Come si può vedere dalle tabelle e dai grafici, Hitachi 912 è molto preciso (CV= 0.79%), mentre la stessa cosa non si può dire del Reflotron Sprint (CV= 3.40%). Vi possono essere delle spiegazioni: il Reflotron Sprint è un apparecchio manuale. Quindi tutte le volte che viene effettuata una misurazione potrebbe essere presente un errore di pipettaggio da parte dell’operatore, oppure un difetto della pipetta, oppure ancora un errore dell’apparecchio stesso, che malgrado sia abbastanza nuovo (acquistato circa 2 anni orsono) può presentare un’imprecisione intrinseca. Per questa ragione ho cercato di curare al massimo la precisione e la concentrazione, in funzione della costanza del modo d’uso, nel pipettare il campione. Un’altra ragione dell’imprecisione” del Reflotron Sprint è da ricercare nel numero dei canali di lettura, che sono tre. In un canale, piuttosto che in un altro, potrebbero esserci dei problemi che finirebbero per far deviare il risultato apparso dal valore effettivo del campione. Grazie a questo primo test, ho potuto constatare che è necessario determinare un fattore che semplifichi la comprensione dei risultati e che ne permetta una lettura più o meno uniforme. Si tratta cioè di trovare un IDWWRUHGLFRQYHUVLRQH, per far sì che i valori ottenuti ad Acquarossa, possano essere convertiti nei valori di Bellinzona e quindi confrontati con quelli ottenuti con uno strumento diverso. Per estrapolare il fattore di conversione ho quindi deciso di eseguire 30 analisi in doppio sia a Bellinzona (Hitachi 912) che ad Acquarossa (Reflotron Sprint). Per far questo ho utilizzato il metodo di Deming18, che mi permette di vedere, grazie ad un grafico, qual è il fattore risultante, che posso perciò utilizzare con un buon margine di sicurezza. Questo fattore verrà utilizzato dal laboratorio di Acquarossa. Naturalmente, come previsto negli obiettivi del mio lavoro, il fattore di conversione può essere applicato unicamente alla determinazione della fosfatasi alcalina. In futuro verranno poi eseguiti i test per trovare i fattori di conversione di tutte le analisi che vengono eseguite con il Reflotron Sprint. L’applicazione del fattore di conversione dovrebbe facilitare i medici a meglio comprendere i valori di laboratorio e quindi a elaborare delle diagnosi corrette, sulla base di valori che non devono prima di tutto essere rielaborati. 17 L’errore è possibile solo in caso di manipolazione imprecisa da parte, soprattutto, di personale non qualificato o poco abituato all’uso della pipetta. 18 Si tratta di un metodo di analisi di dati applicati in ambito scientifico, anche detta analisi di regressione di Deming, in casi analoghi a quello trattato in questo lavoro, quando cioè per un identico campione analizzato con due sistemi diversi è necessario poter rendere i dati comparabili 19 Il fattore di conversione che ho trovato per la fosfatasi alcalina è di 2.18 (2,177 per la precisione). Questo significa che per confrontare i valori di Acquarossa con i valori di Bellinzona bisognerà dividere il valore ottenuto con il Reflotron Sprint ad Acquarossa per il fattore di conversione. Al contrario i valori ottenuti a Bellinzona, per essere paragonabili a quelli di Acquarossa, dovranno essere moltiplicati per il fattore di conversione. Questo fattore verrà, molto probabilmente, inserito nel sistema informatico19 dell’EOLAB. 19 Cortex Quality Software 20 &RQFOXVLRQL Dunque l’ipotesi iniziale è stata confermata. È cioè possibile trovare un fattore di conversione che permetta il confronto tra sue sistemi analitici differenti e quindi rendere i risultati ottenuti con un sistema confrontabili a quelli ottenuti con un altro sistema. Il lavoro svolto per giungere a questo risultato non è stato facile. Prima di tutto, come già illustrato nei capitoli precedenti, la precisione di un sistema e la relativa “imprecisione” dell’altro rendono le analisi non semplici. Inoltre riuscire a garantire le condizioni ottimali di analisi non è scontato. La disponibilità di campioni, il loro trasporto, la disponibilità dei sistemi analitici, l’abitudine a lavorare con uno piuttosto che con l’altro, la tensione determinata dalla necessità di procedere con la maggior cura possibile al pipettaggio (per esempio), per evitare ogni possibile fonte di minimo errore hanno reso il lavoro nel contempo impegnativo e molto istruttivo. Ciò che più di ogni altra cosa ritengo importante nel lavoro svolto è di essere riuscita a dimostrare la necessità di rendere le analisi confrontabili. Mi sono resa conto che era importante poter dare ai medici un supporto uniforme e soprattutto penso che sia importante ripetere questa esperienza con tutte le altre analisi che vengono svolte dai due sistemi. Analogamente credo che per altre analisi svolte da altri apparecchi esista lo stesso problema. Purtroppo non è sufficiente affidarsi ai valori indicati dai fornitori, occorre verificare con esperienze la possibilità di determinare questi fattori di conversione. Infatti per valori normali (fino a 265 U/ L il valore è considerato nella norma per analisi fatte ad Acquarossa) il fornitore dà un fattore di conversione di 2.05. L’esperienza dimostra che il fattore di conversione è diverso, in modo sensibile (+ 6.34%). Per la qualità delle diagnosi è necessaria una maggiore accuratezza nelle analisi. Applicando il fattore di conversione da me stabilito il valore normale calcolato sarebbe di 281,80, cioè patologico. Mi sono chiesta come mai questi fattori segnalati dai fornitori non siano sufficientemente corretti. Volendo provare a dare una risposta, che dovrebbe essere però verificata, credo che i motivi possano essere: - l’”invecchiamento” dell’apparecchio - il fatto che il valore determinato dal fornitore sia stato determinato in condizioni ottimali e non di laboratorio (un solo operatore, temperatura costante, procedura con campioni preparati in modo ottimale e standardizzati, ecc.) - l’evoluzione tecnologica. 21 5LQJUD]LDPHQWL Desidero ringraziare, al termine di questo lavoro: - il signor Luigi Fraschini, che mi ha sostenuto nel corso di tutto il periodo, leggendo e correggendo le diverse versioni che gli ho consegnato e stimolandomi al rigore scientifico - il signor Roberto Francesconi, capo Laboratorio a Bellinzona, per il tempo messomi a disposizione e per gli utili consigli - il signor Alberto Dellamora, perito chimico presso il Laboratorio di Bellinzona che mi ha spiegato con dovizia di particolari l’apparecchio Hitachi 912 - le signore Michela Lomazzi e Pamela Vigilante, laboratoriste, che mi hanno aiutato nel lavoro pratico sia a Bellinzona, che ad Acquarossa - tutto il personale dei Laboratori di Bellinzona e di Acquarossa per il sostegno - il signor Andrea Boffini, le signore Daniela Marcacci e Sonja Marci, della Scuola cantonale superiore medico-tecnica, per l’aiuto nell’allestimento del testo. 22 %LEOLRJUDILD ALP, Foglietto illustrativo, Roche Diagnostics GmbH, Mannheim (D), 5-2001 Constance Cepko, Elizabeth Ryder, Donna M. Fekete, and Suzanne Bruhn, Harvard Medical School and the Howard Hughes Medical Institute Boston, MA 02115 DETECTION OF ß-GALACTOSIDASE AND ALKALINE PHOSPHATASE ACTIVITIES IN TISSUE - http:/ / axon.med.harvard.edu/ ~ cepko/ protocol/ xgalplap-stain.htm Cortex Quality Software, Manuale d' istruzione per Lab/ 400, capitolo 2.1 Eppendorf-Netheler – Hinz GmbH, Hamburg Eppendorf-Netheler – Hinz, Amburgo: http:/ / www.eppendorf.com/ en/ index.php Laboratorio di analisi chimiche Brusca, Roma, http:/ / web.tiscali.it/ labanalisibrusca/ Research Collaboratory for Structural Bioinformatics (RCSB) - Protein Data Bank http:/ / www.rcsb.org/ pdb/ Roche Diagnostics – Laboratorio – Prodotti: http:/ / roche-diagnostics.it/ prodotti/ Laboratorio/ 23 Chiara Silacci, FLM3 may, 2004 24 ,QGH[ 1. Introduction 1.1 1.2 Why this topic? History of the disease 2. What is Paget’s Disease? 3. What caused Paget’s Disease? 4. Who is affected? 5. Symptoms 6. Diagnosis 7. Alkaline Phosphatase 8. Treatment 9. Exercise and diet 10. Bibliography 25 ,QWURGXFWLRQ 1.1 Why this topic? I have choose this topic, because in my diploma work, I speak about the alkaline phosphatase, an enzyme that in the Paget’s disease is elevated. My diploma work is not easy to explain, it is to technical. So I choose to explain a disease, where the alkaline phosphatase is increase. 1.2 History of Paget’s Disease Paget’s Disease was recognized by Sir James Paget approximately 100 years ago. Initially it was a rather mysterious disease, which caused a variety of deformities as well as fractures. This is a collage of pictures from Sir James Paget paper on osteitis deformans published in 1876. The condition is characterized by uncontrolled osteoclastic bone resorption coupled with increased bone formation. The net result is an increase in bone mass that is functionally and structurally defective bone. 26 :KDWLV3DJHW¶V'LVHDVH" The bones commonly affected by Paget’s disease. Paget’s disease is a disease of the bones. I t is a chronic disorder and typically produces deformities and enlargement of the bones due to the excessive bone breakdown and also bone formation. It creates density of the bone and makes the bone rather fragile and tender. Clinically, this disease can create severe pain, followed by deformities and sometimes fractures. Almost every bone of the body can be involved. The major part of the involvement concentrates and localizes on the long bones; thibia (shin bone), femur (the thigh bone) and pelvic bones, skull and spinal column. When the skull is involved, the patient may experience difficulties with vision and the nerves of the eyes are affected. Also, when the neural canal bones of hearing are involved, the tightness of canal will also create nerve deafness and loss of hearing results. This can involve both side and both ears or can involve only one. It is said that Beethoven, the great musician, had Paget’s disease which involved his skull and also his neural canal of hearing and he came deaf. While the skull is showing the involvement of Paget’s disease, the effect of that can also be observed on the facial bones and disturbances of the chewing mechanism may occur when the disease affect the teeth in the upper and lower jaws. A severe case of Paget’s disease which has caused the right leg to become bowed. 27 :KDWFDXVHG3DJHW¶V'LVHDVH" A possible slow virus infection of the bone way be the cause. Also, others factors such as hereditary appears strong since Paget’s disease has been seen in different members of a family. The hereditary factor may lead to susceptibility among family members. Isolation of this slow virus and exact nature has not been totally understood or explained. Research is still being done on this subject. In regard to Paget’s being in families, it is suggested that after the age of 40, it may be advisable for the siblings and children of a person with Paget’s disease to have a standard blood test checking for alkaline phosphatase (an enzyme produced by bone cells) done every two or three years. If the blood levels of this chemical are high, further tests such as bone scanning and other tests in regards to the urine need to be initiated. :KRLVDIIHFWHG" Paget’s disease is rarely diagnosed in people under 40 years of age. Men and women are affected equally. Prevalence of Paget’s disease ranges from 1.5 to 8 percent depending on age and country of residence. Prevalence of familial Paget’s disease (where more than one family member has the disease) ranges from 10 to 40 percent in different parts of the world. Because early diagnosis and treatment is important, after age 40, siblings and children of someone with Paget’s disease may wish to have an alkaline phosphatase blood test every 2 or 3 years. If the alkaline phosphatase level is above normal, other tests such as a bone-specific alkaline phosphatase test, bone scan, or x-ray can be performed. 6\PSWRPV Many patients do not know they have Paget’s disease because they have a mild case of the disease with no symptoms. Sometimes, symptoms may be confused with those of arthritis or other disorders. In other cases, the diagnosis is made only after complications have developed. Symptoms can include: %RQHSDLQ: the most common symptom. Bone pain can occur in any bone affected by Paget’s disease. It often localizes to areas adjacent to the joints. +HDGDFKHVDQGKHDULQJORVV: may occur when Paget’s disease affects the skull. 3UHVVXUHRQQHUYHV: may occur when Paget’s disease affects the skull or the spine. ,QFUHDVHGKHDGVL]HERZLQJRIOLPERUFXUYDWXUHRIVSLQH: may occur in advanced cases. 28 +LSSDLQ: may occur when Paget’s disease affect the pelvis or thighbone. 'DPDJHWRFDUWLODJHRIMRLQ: may lead to arthritis. 'LDJQRVLV Paget’s disease may be diagnosed using one or more of the following test: ;UD\V: Pagetic bone has a characteristic appearance on x-rays. $ONDOLQHSKRVSKDWDVHEORRGWHVW: An elevated level of alkaline phosphatase in the blood can be suggestive of Paget’s disease %RQHVFDQ: Useful in determining the extent and the activity of the condition. If a bone scan suggests Paget’s disease, the affected bone(s) should be x-rayed to confirm the diagnosis. The structure of normal bone. This diagram shows a cross section through part of the thigh bone (femur). 29 $ONDOLQHSKRVSKDWDVH Alkaline phosphatase is an enzyme found throughout the body. Like all enzymes, it is needed, in small amounts, to trigger specific chemical reactions. When it is present in large amounts, it may signify bone or liver disease or a tumor. Medical testing of alkaline phosphatase is concerned with the enzyme that is found in liver, bone, placenta, and intestine. In a healthy liver, fluid containing alkaline phosphate and other substances is continually drained away through the bile duct. In a diseased liver, this bile duct is often blocked, keeping fluid within the liver. Alkaline phosphatase accumulates and eventually escapes into the bloodstream. The alkaline phosphatase of the liver is produced by the cells lining the small bile ducts (ductoles) in the liver. Its origin differs from that of other enzymes called aminotransferases. If the liver disease is primarily of an obstructive nature (cholestatic), i.e. involving the biliary drainage system, the alkaline phosphatase will be the first and foremost enzyme elevation. If, on the other hand, the disease is primarily of the liver cells (hepatocytes), the aminotransferases will rise prominently. Thus, these enzymes are very useful in distinguishing the type of liver disease- cholestatic or hepatocellular. Growing bones need alkaline phosphatase. Any condition of bone growth will cause alkaline phosphatase levels to rise. The condition may be normal, such as a childhood growth spurt or the healing of a broken bone; or the condition may be a disease, such as bone cancer, Paget’s disease, or rickets. During pregnancy, alkaline phosphatase is made by the placenta and leaks into the mother’s bloodstream. This is normal. Some tumors, however, start production of the same kind of alkaline phosphatase produced by the placenta. These tumors are called germ cell tumors and include testicular cancer and certain brain tumors. Alkaline phosphatase from the intestine is increased in a person with inflammatory bowel disease, such as ulcerative colitis. 30 7UHDWPHQW Paracetamol and/ or non-steroidal anti-inflammatory drugs (NSAIDs) help the pain in some people although they may not always be very helpful or effective. Simple physical measures are sometimes useful. For example, in a case where one leg has effectively been shortened because the thigh and shin bones have grown curved, a built-up insole in the shoe can make a great difference to the feeling of “lopsidedness”. Once the diagnosis has been made, most patients will be referred to a specialist clinic for assessment and treatment. There is a choice of 3 main forms of treatment. Etidronate (“Didronel”) Etidronate is a bisphosphonate drug – one of the earlier ones of this type produced. I t is taken by mouth in courses of up to 6 months. There are usually no side effects, although minor stomach upsets can occur. One course of etidronate can sometimes start a remission in the disease for up to several years. If it is taken in a high dose for too long etidronate can further weaken the bone. However, if you are prescribed this drug your doctor will be aware of this risk and pay special attention to it. Newer bisphosphonates Newer, more powerful bisphosphonates have now been developed which act without the risk of weakening the bone. Pamidronate is the most widely udes of these. Pamidronate has to be given as an injection, either as a series of 6 weekly injections or, more usually, as a series of 3 injections given at intervals of 2 weeks. Some doctors give an additional reduced dose before the series of 3 full doses. Such courses can be repeated if necessary. The pain in the bone is often relieved and sometimes more quickly than this. Pamidronate is well tolerated and side-effects are usually mild and do not require treatment. Tiludronate and risedronate are alternatives, effective treatments. Both these drugs can be taken by mouth. Calcitonin Calcitonin in an hormone which is produced naturally from glands in the neck. Large doses have been found to reduce the turnover of bone cells and reduce the pain in Paget’s disease. However, at present it is only available by injection (although it may become available as a nasal spray in the future). Many patients learn to give their own injections and have intermittent courses of calcitonin for up a year. Calcitonin has no serious side effects but can often cause relatively minor side effects such as a flushed face, nausea, vomiting and diarrhoea. 31 ([HUFLVHDQGGLHW In general, patients with Paget’s disease should receive 1000-1500 mg of calcium, adequate sunshine, and at least 400 units of vitamins D daily. This is especially important in patients being treated with bisphosphonates. Patients with a history of kidney stones should discuss calcium and vitamin D intake with their physician. Exercise is very important in maintaining skeletal health, avoiding weight gain, and maintaining joint mobility. Since undue stress on affected bones should be avoided, patients should discuss any exercise program with their physician before beginning. %LEOLRJUDSK\ 1. http:/ / www.osteo.org/ pdibone.html 2. http:/ / www.aanos.org/ edctn_paget.htm 3. http:/ / www.arc.org.uk/ about_arth/ booklets/ 6031/ 6031.htm 32
Scaricare