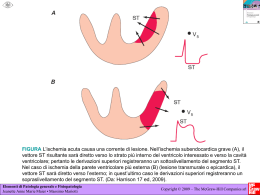
ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio - Settembre 2006 Direttore FRANCO SALVATI Comitato di redazione ALFONSO ALTIERI, FRANCESCO BELLI, MAURO CALVANI, GIUSEPPE CARDILLO, PAOLO MATTIA, GIOVANNI MINARDI, MAURIZIO MORUCCI, FABRIZIO NESI, BRUNO NOTARGIACOMO, SERGIO PILLON, ELIO QUARANTOTTO, MAURIZIO RUSSO, PIETRO SACCUCCI, MICHELE SCOPPIO, GIAN DOMENICO SEBASTIANI, MARIO VALLE Segreteria di redazione: RITA VESCOVO, ALMERINDA ILARIA Comitato scientifico-editoriale Coordinatore ROBERTO CANOVA LOREDANA ADAMI, MARIO GIUSEPPE ALMA, CATERINA AMODDEO, MARCELLO ASSUMMA, GIANLUCA BELLOCCHI, FRANCO BIANCO, PIETRO BORMIOLI, PIO BUONCRISTIANI, ALESSANDRO CALISTI, ILIO CAMMARELLA, ALBERTO CIANETTI, MASSIMO CICCHINELLI, ENRICO COTRONEO, FRANCESCO CREMONESE, ALBERTO DELITALA, EUGENIO DEL TOMA, FILIPPO DE MARINIS, LORENZO DE MEDICI, CARLO DE SANCTIS, SALVATORE DI GIULIO, GIUSEPPE DI LASCIO, CLAUDIO DONADIO, ALDO FELICI, MARIA ANTONIETTA FUSCO, ALFREDO GAROFALO, LAURA GASBARRONE, GIAMPIERO GASPARRO, CLAUDIO GIANNELLI, EZIO GIOVANNINI, LUCIA GRILLO, MASSIMO LENTINI, IGNAZIO MAJOLINO, CARLO MAMMARELLA, LUCIO MANGO, EMILIO MANNELLA, LAURO MARAZZA, MIRELLA MARIANI, MASSIMO MARTELLI, ANTONIO MENICHETTI, GIOVANNI MINISOLA, CINZIA MONACO, FRANCESCO MUSUMECI, GIULIO CESARE NICOTRA, MICHEL VOINO ORANSKY, REMO ORSETTI, PAOLO ORSI, GIOVACCHINO PEDICELLI, GIUSEPPE PIAZZA, ROBERTO PISA, LUIGI PORTALONE, COSIMO PRANTERA, GIOVANNI PUGLISI, GIORGIO RABITTI, SANDRO ROSSETTI, ENRICO SANTINI, ALESSANDRO SCHIRRU, GIOVANNI SCHMID, CIRIACO SCOPPETTA, FABRIZIO SOCCORSI, CORA STERNBERG, GIUSEPPE STORNIELLO, PIERO TANZI, ROBERTO TERSIGNI, ANNA RITA TODINI, CLAUDIO TONDO, MIRELLA TRONCI, ROBERTO VIOLINI Segreteria: GIOVANNA DE PAOLA NUOVA EDITRICE GRAFICA Azienda Ospedaliera San Camillo-Forlanini Roma Direttore Generale: Luigi Macchitella Direttore Sanitario: Fulvio Forino Direttore Amministrativo: Roberto Noto NUOVA EDITRICE GRAFICA Abbonamenti 2006: istituzionali 100, privati 73 Per la richiesta di abbonamenti e per la richiesta di inserzioni pubblicitarie rivolgersi a Nuova Editrice Grafica srl, Via Francesco Donati, 180 - 00126 Roma Tel. 065219380 - Fax 06 5219399 Internet: www.negeditrice.it E-mail: [email protected] Garanzia e riservatezza per gli abbonati L’editore garantisce la massima riservatezza dei dati forniti dagli abbonati e la possibilità di richiederne gratuitamente la rettifica o la cancellazione scrivendo a: Nuova Editrice Grafica srl, Via Francesco Donati, 180 - 00126 Roma. Le informazioni custodite nell’archivio elettronico della Nuova Editrice Grafica srl verranno utilizzate al solo scopo di inviare agli abbonati vantaggiose proposte commerciali (legge 675/96). Direttore responsabile: Franco Salvati Iscrizione al registro della Stampa n. 176/98 con ordinanza del Tribunale di Roma in data 6/5/1998 © Copyright Nuova Editrice Grafica srl Finito di stampare nel mese di marzo 2007 nella tipografia della NUOVA EDITRICE GRAFICA srl - Roma I diritti di traduzione, di riproduzione e di adattamento, totale o parziale, con qualsiasi mezzo (compresi i microfilm e le copie fotostatiche), in lingua italiana, sono riservati per tutti i paesi. ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 Contenuto EDITORIALE Influenza aviaria C. CARVELLI Avian influenza FOCUS SU: L’ISCHEMIA CRITICA DEGLI ARTI INFERIORI L’ischemia critica degli arti inferiori: una sfida per il chirurgo vascolare L. PEDRINI The critical lower limb ischemia: a challenge for the vascular surgeon La diagnostica ultrasonografica nell’ischemia critica degli arti inferiori P. M. NICOSIA Non invasive diagnosis in critical lower limb ischemia Diagnostica radiologica TC e RM nella ischemia critica degli arti inferiori V. BUFFA, G. REGINE, V. MIELE, L. ADAMI MR and CT in diagnosis of lower extremity arterial disease Procedure endovascolari di rivascolarizzazione del distretto femoro-popliteo nel paziente critico M. MORUCCI, P. AGRESTI, L. DE’ MEDICI Endovascular revascularization in critical patients Analisi dei fattori che influenzano l’outcome R. BARTOLUCCI, F. NESI Analysis of the factors influencing on outcome L’ischemia critica nelle lesioni aorto-iliache F. SPEZIALE, M. RUGGIERO, A. PALMIERI, D. MENNA Critical limb ischemia in patients with aorto-iliac disease Le procedure “ibride” di rivascolarizzazione G. BERTOLETTI, M. MASSUCCI, A. VARRONI, V. GENOVESE, H. A. RACHED, G. IANNI, F. NAPOLI, G. MARTINELLI, L. CAPOCCIA, E. NOTARIANNI, R. CIANNI Hybrid revascularization procedures Il chirurgo vascolare e l’ischemia critica: le opzioni endovascolari S. RONCHEY, E. SERRAO, P. COSTA, C. CAVAZZIN, C. IOVINO. N. MANGIALARDI The vascular surgeon and critical lower limb ischemia: the endovascular options L’ischemia critica non rivascolarizzabile: ruolo della neurostimolazione midollare tecnica d’impianto E. D’AVINO Non-reconstructable critical leg ischemia: role of spinal cord stimulation Implantation technique L’ischemia critica non rivascolarizzabile: ruolo della neurostimolazione midollare. Indicazioni F. DI CESARE Non-reconstructable critical leg ischemia: role of spinal cord stimulation - Indications 5 • 9 • 18 • 22 • 26 • • 29 33 • 35 • 39 • 42 • 49 ARTICOLO ORIGINALE Indicazioni particolari all’impiego della TCms toracica nell’ambulatorio per la terapia del tabagismo R. PRINCIPE, F. QUAGLIARINI, G. MANCINI Special indications to the use of the CTms in the outpatient’s department for the smoking cessation 53 CASO CLINICO Captazione del 99MTC-MDP in un caso di amiloidosi cardiaca A. ANNOVAZZI, G. VENTRONI, E. PICCHIO, C. AMIDEI, C. TORRINI, L. MANGO 99MTC-MDP uptake in a case of heart amylodosis 57 GESTIONE E ORGANIZZAZIONE SANITARIA Psicoterapia di gruppo per pazienti con sclerosi multipla: specificità e metodologia M. SPARVOLI - E. PODRASKY Group psychotherapy for patients with multiple sclerosis: specificity and methodology 60 RECENSIONE “Sessantesimo Anniversario 1946-2006” F. SALVATI 64 ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 Editoriale INFLUENZA AVIARIA AVIAN INFLUENZA CHIARINA CARVELLI U.O. Infezioni Ospedaliere Azienda Ospedaliera San Camillo-Forlanini - Roma Parole chiave: Influenza aviaria, Virus H5N1. Key words: Avian influenza, H5N1 avian influenza virus. STATO DELL’ARTE In Asia, in questi ultimi anni, si è manifestata una nuova influenza epizootica aviaria da virus A (H5N1), che ha provocato milioni di abbattimenti selettivi di pollame finalizzati al controllo della diffusione della malattia. Nell’uomo l’influenza aviaria, fino alla metà del 2005, ha causato circa 50 morti attribuibili direttamente al virus H5N1, ma la possibilità che si verifichino mutazioni in una forma più contagiosa per l’uomo con le caratteristiche di pandemia rappresenta il motivo di maggior preoccupazione dell’OMS e delle autorità sanitarie internazionali, che sono al lavoro per programmare piani di prevenzione veterinaria e medica finalizzati al contenimento di questo possibile evento. Tutti i tipi di virus dell’influenza aviaria (AI), che appartengono alla famiglia delle Orthomyxoviridae, sono virus influenzali di tipo A e sono suddivisi in sottotipi basati sulle differenze nelle proteine di superficie emagglutinina (H) e neuraminidasi (N), che hanno un’importante funzione nel ciclo replicativo virale e soprattutto nello stimolare la risposta immune dell’organismo. All’interno dell’involucro esterno (envelope) è contenuto il genoma la cui segmentazione in caso di coinfezioni virali permette il riassortimento genetico attraverso lo scambio di materiale genetico e l’emergenza di ibridi virali potenzialmente pandemici. Esistono 16 tipi di H, ognuno dei quali può supportare una delle 9 variazioni della N, rendendo possibile un totale di 144 diverse combinazioni. Tutti gli AI-virus si suddividono in ulteriori due tipi: bassa (LPAI) e alta (HPAI) patogenicità. Gli uccelli selvatici ed in particolare i volatili acquatici degli ordini Anseriformi e Charadriformi sono sensibili all’infezione, che decorre generalmente in forma asintomatica, mentre le specie aviarie domestiche, come polli e tacchini, possono presentare quadri clinici molto gravi con conseguenti vaste e fulminee epidemie per infezione da parte di sottotipi virali ad alta patogenicità. Dei 16 tipi H conosciuti solo i sottotipi H5, H7, e H9 sono capaci di passare dagli uccelli alla specie umana. Il Virus H5N1 si trasmise da uccelli ad esseri umani nel 1997 a Hong Kong: 18 persone furono infettate e ne morirono 6 (tasso di letalità superiore al 30%). La diffusione fu limitata a Hong Kong. Tutti i polli nel territorio furono abbattuti. Nel gennaio 2004 una nuova e maggiore diffusione di questo tipo di virus apparve in Vietnam e Thailandia e in poche settimane si diffuse in una decina di regioni asiatiche, comprese Indonesia, Corea del Sud, Giappone e Cina. Più di 40.000 polli furono abbattuti e la diffusione fu contenuta, ma morirono 23 persone in Vietnam e in Thailandia. 6 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 Nel febbraio 2004 fu individuato anche nei maiali in Vietnam. Il 18 Marzo 2004 il New England Journal of Medicine pubblicava un articolo in cui veniva riportata la conferma di influenza aviaria, in Vietnam, in dieci pazienti ricoverati dal dicembre 2003 al gennaio 2004. Nove di essi avevano una storia di contatti diretti con pollame. Nel luglio 2004 nuove segnalazioni provenivano dalla Thailandia e dalla Cina. Nell’agosto 2004 l’influenza aviaria compariva in Malaysia, nel gennaio 2005 molte città del Vietnam venivano colpite dalla diffusione del virus per cui erano abbattuti circa 1.200.000 polli; ma si ritiene fossero morti, a causa del virus, oltre 140 milioni di uccelli. Nel maggio 2005 un caso di malattia si riscontrava nei maiali anche in Indonesia. Altri focolai si registravano in Russia, in Croazia, in Slavonia, in Turchia, in Iraq, in Azerbaijan e quindi in Egitto. Nel luglio 2005 si contavano 60 persone morte, la maggior parte in Vietnam. In totale, dalla fine del 2003 al novembre del 2006, sono stati riportati da dieci Paesi 258 casi umani di influenza aviaria di cui 153 sono stati letali (59,3%). La Commissione di Consulenza sull’Influenza Umana dell’OMS (Commitee of the World Health Organization [WHO]. Consultation on Human Influenza A/HS) pubblicava sul NEJM un documento che formalizzava le conoscenze sull’influenza aviaria e forniva una serie di raccomandazioni suscettibili di modifica, in considerazione dei molti interrogativi aperti sul problema. È recentissima la notizia, pubblicata su Proceedings of the National Academy of Sciences, dell’identificazione di una nuova linea differenziata di virus H5N1 nel pollame, denominata Fujian, che sembra essere diventata la linea dominante di virus aviario che circola attualmente in parte dell’Asia. La distribuzione geografica dell’infezione da A.I. indica comunque che la popolazione umana è a rischio. MODALITÀ DI TRASMISSIONE Gli uccelli infetti eliminano il virus con la saliva, le secrezioni nasali e le feci, trasmettendo l’infezione attraverso il contatto con le escrezioni, con le superfici e con l’acqua contaminate. La causa del contagio nell’uomo, per la maggioranza dei casi, è stato il contatto diretto con volatili da cortile malati o morti. La trasmissione avviene sia attraverso le mani, con il trasporto agli occhi, al naso o alla bocca di materiale contaminato, sia per aerosol di origine fecale. I clusters familiari verificatisi sono stati attribuiti ad una comune fonte di infezione, date le scarse condizioni igieniche e la promiscuità con volatili infetti. La diffusione da uomo a uomo non è stata confermata totalmente, risultando probabilmente avvenuta solo in due casi, rispettivamente in Tailandia e in Vietnam: in un caso la madre di un paziente, che morì per influenza aviaria, si ammalò e poi morì. In un altro caso, nel marzo 2005, due infermiere che assistettero pazienti affetti da influenza H5N1 si ammalarono. La trasmissibilità interumana, con l’eventuale conseguente pandemia di portata mondiale, è subordinata alla ricombinazione fra il virus aviario e quello stagionale e alla capacità del nuovo virus di adattarsi all’uomo. Ciò è tanto più probabile quanto maggiore è l’estensione dell’epizoozia e maggiore il numero di passaggi dall’animale all’uomo, che permettono il riassetto genetico e il superamento della barriera di specie. La dimostrazione di tale possibilità di mutazione è data dal fatto che il virus è stato isolato dai maiali. Finora sono state individuate due mutazioni aminoacidiche che possono favorire la capacità di trasmissione interumana: una è la sostituzione di serina con asparagina nella HA, l’altra di acido glutammico con lisina in una subunità della polimerasi virale. In particolare quest’ultima caratterizza la specificità di ospite nei mammiferi e si ritrova nei virus isolati dall’uomo. Il controllo di contatti di pazienti, attraverso il test RT-PCR (reverse-transcriptase polymerase-chain-reaction), ha portato alla scoperta di casi subclinici oltre che di un maggior numero di infezioni in adulti più anziani e di clusters familiari nel Nord Vietnam; ciò suggerisce che i ceppi locali del virus si stanno adattando all’uomo ma con relativamente scarsa contagiosità. Anche il rischio di trasmissione nosocomiale è basso con l’utilizzo delle precauzioni di isolamento. 7 C. Carvelli: Influenza aviaria La scarsa contagiosità associata all’alta virulenza dell’H5N1 è stata correlata al tropismo per i recettori polmonari più che per quelli delle alte vie respiratorie. penia moderata, oltre che un incremento lieve delle transaminasi. MANIFESTAZIONI CLINICHE Gli studi effettuati sul virus H5N1 hanno indicato, sin dal 1997, una sua continua evoluzione con cambiamento antigenico; la specie ospite è aviaria, ma esso ha dimostrato la capacità di infettare i felini e i suini; l’infezione sperimentale nei topi e nei furetti ha aumentato la patogenicità virale e la sua stabilità ambientale. La replicazione virale è prolungata, si sono ottenuti isolamenti nei tamponi nasofaringei per circa una settimana (range 116), ma più bassa che nell’influenza umana. La maggior parte dei campioni fecali testati sono risultati positivi per RNA virale (7 su 9), accanto alla negatività delle urine. L’alta frequenza di diarrea nei soggetti affetti e la presenza di RNA virale nei campioni di feci fanno supporre la replicazione virale a livello del tratto gastroenterico. L’ipotesi diagnostica di influenza da H5N1 dovrebbe essere considerata in tutti i soggetti con una malattia respiratoria grave ed acuta nei paesi con presenza di influenza aviaria, in particolare in coloro che hanno avuto contatti con pollame. Il quadro clinico dell’influenza H5N1 nell’uomo è stato definito sulla base dei dati sui pazienti ospedalizzati e non è possibile descrivere con precisione le manifestazioni subcliniche e le presentazioni atipiche ma solo gli elementi reperibili nei singoli report. Il periodo di incubazione potrebbe essere più lungo rispetto a quello di altri virus influenzali. Nel 1997 la maggior parte dei casi si manifestò dopo 2-8 giorni dall’esposizione e i report più recenti documentano intervalli simili, ma con range fino a 8 giorni. L’esordio era caratterizzato da febbre (>38°C) e sintomi simil-influenzali con interessamento delle basse vie respiratorie (94-100% dei casi), mentre solo a volte erano interessate le alte vie (25-71%). Diversamente dai soggetti con influenza aviaria H7 quelli con influenza H5 raramente hanno manifestato congiuntivite. Erano presenti diarrea (17-70%), vomito (10-33%), dolori addominali (17-50%) e sanguinamento dal naso e dalle gengive; in particolare una diarrea profusa senza sangue si manifestava con una frequenza maggiore rispetto a quanto avviene nella normale influenza e precedeva le manifestazioni respiratorie. Il decorso era correlato all’infezione delle basse vie respiratorie con dispnea e tachipnea che potevano evolvere verso un’insufficienza respiratoria e una sindrome da distress respiratorio (ARDS) che nei casi della Thailandia si evidenziava dopo 6 giorni (range 4-13). Molti soggetti hanno richiesto una ventilazione assistita in Unità di Terapia Intensiva per la comparsa di un deficit multiorgano (MOF) e ipotensione. La mortalità nei soggetti ospedalizzati era alta con un’ampia variabilità (33-100%). Rispetto al 1997, quando le morti erano prevalenti in giovani >13 anni, i casi più recenti di influenza aviaria hanno causato un’alta percentuale di mortalità nei bambini. La morte è intervenuta dopo 9-10 giorni dall’esordio per insufficienza respiratoria. I dati di laboratorio più significativi evidenziavano: leucopenia con linfocitopenia, trombocito- PATOGENESI DIAGNOSI E TRATTAMENTO Sono disponibili test diagnostici antigenici che hanno una scarsa specificità. La determinazione dell’ RNA virale in campioni di secrezioni respiratorie offre una maggiore sensibilità ma essa dipende dai Laboratori e dai metodi utilizzati. La conferma della diagnosi di laboratorio richiede uno o più dei seguenti esami: una coltura virale positiva, una RNA-PCR per H5N1 positiva, un test all’ immunofluorescenza per antigeni virali con l’uso di anticorpi monoclonari anti-H5 positivo ed almeno un aumento di quattro volte il titolo anticorpale specifico per H5 in campioni di siero appaiati. Il test di microneutralizzazione richiede virus vivi che interagiscono con gli anticorpi del paziente ed è effettuato solo in poche strutture apposite. Ulteriori test diagnostici rapidi sono necessari anche per le forme di presentazione atipica della malattia. 8 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 TRATTAMENTO L’uso di inibitori della neuraminidase, zanamivir e oseltamivir, sono indicati in caso di diffusione interumana di H5N1. Dati epidemiologici dimostrativi di un evento epidemico nella comunità o la positività di test di laboratorio rapidi o la presenza dei tipici sintomi influenzali sarebbero sufficienti per iniziare il trattamento con tali farmaci negli adulti, soprattutto se ad alto rischio. Gli inibitori della neuraminidasi si devono usare entro 48 ore o, meglio, entro 12 ore dall’inizio dei sintomi. Una eccezione può essere fatta in caso di malattia grave in pazienti ospedalizzati nei quali la terapia può essere considerata anche oltre le 48 ore dall’inizio dei sintomi. In caso di bambini con febbre, tosse e altri segni respiratori, poiché è possibile la coinfezione con altri patogeni virali respiratori, è necessaria una rapida diagnosi di laboratorio ma, se ciò non fosse realizzabile, soprattutto un rapido inizio della terapia. PREVENZIONE Poiché la maggior parte dei casi di influenza aviaria negli uomini è avvenuta a causa della promiscuità con pollame infetto, l’OMS ha emanato precise raccomandazioni per i Paesi in cui è stato riscontrato il virus, tra cui le più importanti sono di evitare il contatto diretto con pollame vivo e con tutto ciò che è venuto a contatto con esso, di vaccinare il pollame, di implementare la vaccinazione anti-influenzale nell’uomo e di consumare i cibi, a base di pollame, previamente cotti. In Italia sono stati elaborati, per 350.000 medici, due opuscoli; uno sulla vaccinazione contro la normale influenza stagionale, per sensibilizzare sulla sua utilità, ed uno contenente informazioni sull’influenza aviaria. La strategia primaria per la prevenzione è l’immunizzazione ma non è ancora disponibile un vaccino per l’influenza H5. I precedenti vaccini sono scarsamente immunogeni e per determinare una risposta anticorpale richiedono due dosi con l’aggiunta dell’adiuvante MF59. La terza iniezione del vaccino H5-1997 ha determinato anticorpi che hanno una cross reazione variabile con quelli isolati nel 2004. Pertanto sono in corso studi per approntare un vaccino specifico efficace. In mancanza del vaccino, attualmente l’oseltamivir è indicato per uso profilattico per tutti i contatti con pazienti o con sorgenti infette (es. pollame). Per quanto riguarda il personale sanitario sono indicate le mascherine di protezione e, in caso di esposizione non protetta, la chemioprofilassi con 75 mg di oseltamivir una volta al giorno per 7-10 giorni. I contatti di pazienti infetti o sospetti tali devono monitorizzare la loro temperatura ed altri sintomi e per loro è suggerita una contumacia per un periodo di una settimana dopo l’ ultima esposizione. Nei bambini di età inferiore ad un anno di vita non è stata stabilita la non tossicità dell’oseltamivir, infatti alcuni studi hanno evidenziato alte concentrazioni del farmaco nel SNC per superamento della barriera emato-encefalica. In conclusione si può affermare che al momento il virus H5N1 non ha acquisito capacità di trasmissione interumana, per la quale sono necessarie importanti mutazioni. Pianificazioni di interventi, nell’eventualità di una pandemia, devono essere sicuramente predisposti ma ci si augura possano rimanere nell’ambito di pure esercitazioni teoriche. BIBLIOGRAFIA ESSENZIALE Ciccozzi M, Campitelli L, Rezza G. Influenza aviaria. Epidemiologia ed evoluzione di H5N1. Not Ist Super Sanità 2006; 19(7-8):9-11 Commitee of the World Health Organization [WHO] Consultation on Human Influenza A/H5. N Engl J Med 2005; 353:1374-85. Hien TT, Liem NT, Dung NT, et al. Avian influenza (H5N1) in 10 patients in Vietnam. N Engl J Med 2004;350:1179-88. Moscona A. M.D. Neuraminidase Inhibitors for Influenza. N Engl J Med 2005; 353:1363-73. Ungchusak K, Auewarakul P, Dowell SF, et al. Probabile person-to person transmission of avian influenza A (H5N1). N Engl J Med 2005;352:333-40. Per richiesta estratti: Dott.ssa Chiarina Carvelli U.O. Infezioni Ospedaliere Azienda Ospedaliera S. Camillo - Forlanini Via Portuense, 332 - 00149 Roma ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 Focus su: L’ischemia critica degli arti inferiori INTRODUZIONE La malattia aterosclerotica è una patologia in costante aumento nei paesi occidentali, in assoluto ma anche per un aumento di incidenza nel sesso femminile. L’innalzamento dell’età media, determinando un invecchiamento della popolazione, causa un aumento delle patologie degenerative quali quelle cardiovascolari. I pazienti con arteriopatie periferiche hanno una mortalità a 5 anni del 30-35% a causa di importanti e coesistenti morbilità associate. Nell’ambito della patologia obliterante aterosclerotica degli arti inferiori l’ischemia critica è definita come quadro clinico caratterizzato da dolore a riposo che impedisce il sonno e richiede analgesici da almeno quattro settimane, pressione arteriosa alla caviglia inferiore a 50 mmHg e/o pressione all’alluce < 30 mmHg, e/o presenza di lesioni trofiche tissutali; essa deve essere considerata una entità nosologica separata; rispetto alla arteriopatia obliterante periferica caratterizzata da claudicatio intermittens presenta differenti problematiche cliniche e peculiari indirizzi terapeutici; anche le indicazioni chirurgiche differiscono poiché la rivascolarizzazione anche con bypass distali rappresenta a volte l’unica possibilità di salvataggio dell’arto; tali pazienti, inoltre, hanno una morbi-mortalità superiore rispetto ai pazienti con arteriopatia obliterante ad uno stadio meno avanzato. Nei paesi occidentali, l’ischemia critica degli arti inferiori si presenta con un’incidenza valutata tra i 300 ed i 500 casi / milione / anno. Il decorso clinico di tale patologia è caratterizzato da un’evoluzione che spesso, se non trattata, può portare all’amputazione. Le opzioni chirurgiche, d’altro canto, sono spesso complesse, ripetute ed, a volte, infruttuose. Per ottenere dei successi clinici rilevanti è necessaria una collaborazione specialistica multidisciplinare; l’accuratezza diagnostica, l’integrazione tra terapia medica e chirurgica, le terapie di supporto sono momenti fondamentali nella gestione di tali pazienti. Importante, inoltre, è la collaborazione del medico curante che dovrà essere in grado di individuare precocemente l’esordio della malattia aterosclerotica; solo così potrà essere esercitato un ruolo di prevenzione primaria andando ad agire, laddove possibile, sui fattori di rischio modificabili (abitudine di vita, tabagismo,dieta ecc.); egli potrà inoltre seguire l’andamento clinico controllando anche l’efficacia delle terapie mediche eventualmente intraprese; dovrà essere in grado di indirizzare al chirurgo vascolare i pazienti che possono beneficiare di un intervento di rivascolarizzazione. La costante interazione tra specialista e medico di base gioca un ruolo determinante nel garantire un’alta percentuale di successo clinico. In base a tali premesse, nell’ incontro monotematico svoltosi presso l’Ordine dei Medici di Roma il giorno 26 gennaio 2006 presieduto dal Prof. Giorgio Rabitti, specialisti di rilievo hanno dibattuto sulle possibili modalità diagnostico-terapeutiche di tale patologia:questo Focus ne è l’espressione. FABIO DI CESARE Unità Operativa di Chirurgia Vascolare dell’Azienda Ospedaliera San Camillo-Forlanini - Roma Direttore: Prof. G. Rabitti ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 A) L’ISCHEMIA CRITICA DEGLI ARTI INFERIORI: UNA SFIDA PER IL CHIRURGO VASCOLARE THE CRITICAL LOWER LIMB ISCHEMIA: A CHALLENGE FOR THE VASCULAR SURGEON LUCIANO PEDRINI Struttura Complessa di Chirurgia Vascolare – Ospedale Maggiore di Bologna Parole chiave: Ischemia critica degli arti inferiori, Malattie arteriose periferiche. Key words: Critical limb ischemia, Peripheral arterial disease. I pazienti con arteriopatie periferiche sono di per sé pazienti ad elevato rischio per la gravità delle co-patologie vascolari e sistemiche, tanto da avere una mortalità a 5 anni del 32%,1 superiore a quella delle neoplasie della prostata (8%), del M. di Hodgkin (18%), e del tumore della mammella (23%).2 I pazienti con ischemia critica presentano spettanza di vita e rischio di amputazione estremamente più elevati legati ad una maggiore complessità clinica e a fattori di rischio maggiori, che verranno esaminati singolarmente. Il problema è particolarmente rilevante se si considera che l’ischemia critica ha una prevalenza dell’1% nei soggetti ultra 55enni, superiore nei diabetici e nei fumatori, che presentano lesioni vascolari di più difficile trattamento e maggior incidenza di fattori di rischio associati (esempio policitemia). Un approccio “aggressivo”, in molte esperienze porta a ridurre l’incidenza di amputazione primaria per ischemia critica al 16% o meno, e a tentare in almeno due terzi un intervento di rivascolarizzazione;3,4,5 queste percentuali non sono tuttavia riscontrabili in tutti i paesi ed in tutti i modelli organizzativi sanitari. SEDE ED ESTENSIONE DELL’ARTERIOPATIA L’ischemia critica generalmente si realizza per la concomitanza di stenosi o di ostruzioni in più segmenti dello stesso arto, anche se in una minima percentuale di casi la concomitanza di una occlusione del tratto aorto-iliaco, quando è possibile una ricostruzione aorto-femorale, rende più semplice il trattamento con una probabilità di pervietà della rivascolarizzazione dell’87.5% a 5 anni e con una elevata percentuale di salvataggio d’arto.6 La coesistenza di lesioni multisegmentarie può richiedere, nel paziente con ischemia critica, un trattamento sia delle ostruzioni prossimali che di quelle distali al fine di riportare una buona ossigenazione al piede. La combinazione più comune7 è rappresentata dalla PTA iliaca associata ad una ricostruzione chirurgica del tratto femoro-distale, ma in alcuni casi si può eseguire un trattamento endovascolare del tratto femoro-distale in associazione ad una rivascolarizzazione aorto-femorale. Le arteriopatie ostruttive del tratto femoro-popliteo sono state il “banco di prova” dei chirurghi vascolari degli anni ’70, che per lungo tempo hanno trattato i pazienti allo stadio della claudicazione intermittente. I risultati non entusiasmanti, sia in termini di pervietà delle rivascolarizzazioni, sia per l’incidenza di amputazioni, emersi dalla valutazione dei follow-up a lungo termine, hanno consentito di identificare numerosi fattori responsabili della trombosi della rivascolarizzazione e fra questi lo stato del run-off, ed hanno portato a rivedere le indicazioni restringendo il trattamento prevalentemente a pazienti con claudicazione invalidante o con ischemia critica. I pazienti con ischemia critica presentano prevalentemente lesioni nel distretto femoro-distale, più sfavorevole, con frequenti associazioni di lesioni steno- L. Pedrini: L’ischemia critica degli arti inferiori: una sfida per il chirurgo vascolare ostruttive delle arterie tibiali e delle arterie del piede. I risultati di pervietà e salvataggio a questo livello sono decisamente peggiori e sono fortemente correlati al tipo di protesi innestata. ALTERAZIONI EMOCOAGULATIVE Una diatesi trombotica è stata evidenziata da numerosi anni nei pazienti affetti da arteriopatie ostruttive degli arti inferiori.8 Le alterazioni più frequenti sono rappresentate da deficit dell’Antitrombina III, mutazione del fattore V Leiden, mutazione della protrombina, bassi livelli di proteina C e di Proteina S, presenza di Lupus Anti Coagulant (LAC),9 anomalie del plasminogeno o alterazioni della funzionalità piastrinica, che probabilmente consentono di giustificare parte delle occlusioni protesiche precoci.10,11 Il problema è particolarmente rilevante nelle rivascolarizzazioni femoro-distali che nell’esperienza di Ray9 hanno presentato una incidenza di riocclusioni precoci del 27% nei pazienti con alterazioni emocoagulative, rispetto all’1.6% dei controlli. Questo stato ipercoagulativo, nei pazienti che necessitano di una rivascolarizzazione, presenta una incidenza variabile nelle varie casistiche, da valori abbastanza bassi, fino a percentuali del 40%9 ed oltre, rilevata nei pazienti rivascolarizzati. L’incidenza di anticorpi antieparina supera il 3%.12 Donaldson et al.13 riportano una attivazione piastrinica indotta dall’eparina in un 5% dei casi; questi anticorpi sono associati ad una aumentata incidenza di trombosi durante successive somministrazioni del farmaco. Attualmente anche l’omocisteina viene considerata fra i fattori di rischio delle arteriopatie periferiche; elevati livelli di omocisteina sono correlati con fenomeni trombotici, sia arteriosi che venosi.14 La disidratazione, tipica dei pazienti anziani, che costituiscono buona parte del campione dei p. con ischemia critica, aumenta l’ispissatio sanguinis ed il conseguente rischio trombotico. Questi fattori, associati alla tendenza a tenere l’arto declive per ridurre la sintomatologia dolorosa, favoriscono anche l’insorgenza di una trombosi venosa profonda, che può complicare la scelta terapeutica, per l’impossi- 11 bilità di utilizzare la vena safena in questi casi. STADIO DELLA MALATTIA La riduzione dell’indicazione al trattamento della claudicazione intermittente ha portato in molte sedi ad una dilazione estrema del trattamento tanto che in molte chirurgie vascolari attualmente i pazienti giungono di rado allo stadio della claudicazione severa, e quelli con ischemia critica arrivano prevalentemente con lesioni trofiche o gangrena, anziché al primo comparire del dolore a riposo. Uno stadio più avanzato della malattia è associato a peggiori risultati, ma soprattutto a lunghi tempi di guarigione, e può portare a escludere dal trattamento i pazienti più compromessi, o viceversa può comportare ripetuti trattamenti chirurgici vascolari, demolitivi e di chirurgia plastica. DIABETE Il diabete aumenta l’incidenza di ulcere, dovute agli effetti combinati della neuropatia e dell’ischemia nella genesi delle cosiddette ulcere neuroischemiche, che rappresentavano circa il 34% in uno studio trasversale dove le ulcere puramente ischemiche in diabetici erano presenti nel 10% del campione.15 La clinica nel paziente diabetico è spesso mascherata dalla neuropatia e questo favorisce la tardività del trattamento e l’errata valutazione della gravità dell’ischemia. La tipologia delle lesioni del paziente diabetico è fondamentalmente diversa da quella del paziente aterosclerotico ed in molti casi più idonea ad un trattamento endovascolare. Alcuni autori16 riportano ottimi risultati dopo angioplastica, ed una sorprendentemente bassa incidenza di ristenosi, mentre per altri occorrono ripetuti interventi per ottenere una elevata pervietà assistita. PROBLEMI TECNICI NEI PAZIENTI RIVASCOLARIZZABILI – ENDARTERECTOMIA. – La tecnica della tromboendarterectomia a cielo semichiuso con anello di Vollmar, presentava frequenti insuccessi per la persistenza di difetti tecnici o per una rapida ristenosi e per ta- 12 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 le motivo è stata praticamente abbandonata. La ripresa di questa tecnica è stata favorita sia dall’utilizzazione di controlli intraoperatori più attendibili dell’angiografia, sia soprattutto per il possibile completamento endovascolare rappresentato prima dalla tecnica di Moll, sia a livello prossimale17 che distale,18 poi dalla applicazione di stent distali, o di endoprotesi nel segmento disostruito.19 I risultati di questi trattamenti non erano comparabili a quelli di un bypass in vena safena; i risultati con i nuovi materiali sembrano essere migliorati.20 – VENA INVERTITA. – L'utilizzazione della safena invertita consente una semplice ed efficace rivascolarizzazione di lesioni brevi quali quelle per ostruzione della femorale superficiale fino al canale di Hunter (eseguite prevalentemente per claudicatio intermittens) o per aneurismi poplitei trombizzati, ma raramente queste occlusioni sono responsabili di una ischemia critica, salvo non siano associate ad occlusioni prossimali o distali. Nelle ostruzioni femoro-poplitee sottogenicolari l’utilizzo della safena invertita può richiedere incisioni maggiori per la sua preparazione, con maggiori complicanze post-operatorie, inoltre in molti casi la disparità fra i diametri dell’arteria e della vena rendono difficoltose o critiche alcune anastomosi. – VENA IN SITU. – La tecnica del bypass in situ, comparsa per la prima volta in letteratura nel 1962 ad opera di Hall,21 consente un ottimo accoppiamento fra i calibri dell’arteria e della vena nelle sedi anastomotiche, ed inoltre, la sua preparazione può essere effettuata con incisioni limitate, riducendo la deafferentazione vascolare e nervosa alla vena stessa. Una delle maggiori casistiche sui bypass con safena in situ, in pazienti con claudicazione o ischemia critica, riporta una pervietà cumulativa del 91% ad 1 anno e dell’85% a 5 anni, con risultati peggiori nell’ischemia critica.22 La preparazione a cielo semichiuso con la ricerca angiografica o eco-Doppler delle collaterali comporta la persistenza di fistole arterovenose (FAV) in numerosi casi che richiedono un trattamento postoperatorio.23 La valvulotomia è sicuramente uno dei punti critici di questa tecnica; i valvulotomi disponibili sono molti ed ognuno presenta vantaggi e svantaggi: il valvulotomo di Mills è forse uno dei meno traumatici, ma richiede una valutazione endoscopica che comporta ugualmente una possibile lesione endoteliale, oltre che numerosi approcci per raggiungere le varie sedi valvolari. Altri valvulotomi come il Cartier e l’Hall erano maggiormente responsabili di lacerazioni della vena, mentre col valvulotomo di Samuel alcune valvole rimanevano intatte. Il valvulotomo di LeMaitre autocentrante assicura una valvulotomia più completa, ma non è utilizzabile nelle vene di minor calibro (peraltro poco adatte ad una rivascolarizzazione) e comporta qualche lacerazione della parete vascolare. Anche la valvulotomia è responsabile del maggior numero di reinterventi, rispetto al bypass con vena invertita, per la persistenza di lembi valvolari incompletamente strappati, per la formazione di stenosi in corrispondenza delle valvole residue e per altri problemi tecnici insiti nella metodica. Ciò nonostante i risultati sono superiori in molte casistiche; Gupta et al.5 riportano una pervietà primaria a 3 anni dell'85% nei bypass in situ, del 62% negli ex situ (non invertiti ma spostati di sede) e del 57% nei bypass con safena invertita ed una maggior incidenza di revisioni/trombosi nei bypass con safena invertita rispetto a quelli in situ. Opposte altre esperienze, con pervietà primaria a 4 anni del 77% per la safena invertita e del 68% per la vena in situ,24 per altri la differenza fra le due tecniche non è statisticamente significativa.25 Sembra esperienza comune che i bypass con vene di diametro inferiore a 4 mm diano risultati significativamente peggiori.26 – VENE DEL BRACCIO. – Anche le vene del braccio vengono utilizzate per i bypass infrapoplitei con pervietà ad un anno variabili dal 49%27 al 67%28 ed anche migliori. – PROTESI ALLOPLASTICHE. – Le ricostruzioni con protesi in poliestere nel tratto femoro-popliteo sono state generalmente abbandonate e sostituite dalle rivascola- L. Pedrini: L’ischemia critica degli arti inferiori: una sfida per il chirurgo vascolare rizzazioni in PTFE; tuttavia anche questo materiale ha evidenziato una pervietà primaria particolarmente bassa nelle ricostruzioni sotto il ginocchio (33% a 5 anni) o sopra il ginocchio (47% a 5 anni)6. Visti gli scarsi risultati, soprattutto nelle rivascolarizzazioni infrapoplitee, sono state tentate molte tecniche, in particolare per cercare di ridurre l’iperplasia intimale a livello dell’anastomosi distale; fra queste le più note sono la cuffia di Miller ed il patch di Taylor. In un trial controllato e randomizzato la cuffia di Miller ha portato ad una pervietà primaria significativamente migliore nelle rivascolarizzazioni della poplitea sottogenicolare (52% versus 29% p=0.03), ma non ha modificato la pervietà secondaria (59% vs 35%, p= 0.14) e il salvataggio d’arto (84% vs 62%, p= 0.08).29 Il Taylor patch30 e lo “stivale” di Wolfe31 sono altre due configurazioni che hanno consentito risultati comparabili alla cuffia di Miller, ma necessitano conferma da trial randomizzati e controllati.32 L’interposizione di una vena nei bypass femoro-poplitei sottoarticolari e femorotibiali aumenta la pervietà delle protesi alloplastiche.33 Le protesi in PTFE precuffiato presentano vantaggi teorici; le pervietà a 1, 234 e 3 anni35 sono risultate simili a quelle dei bypass con la cuffia in vena. La realizzazione di una FAV a livello dell’anastomosi distale è un’altra tecnica utilizzata per ridurre l’incidenza di trombosi protesica. Hingorani36 nei pazienti senza adeguato patrimonio venoso propone una tecnica mista, con creazione di FAV e con interposizione di un segmento venoso, con un salvataggio d’arto del 79% ad 1 anno e del 74% a 5 anni e con una pervietà primaria del 51% ad un anno. – HOMOGRAFT CRIOCONSERVATI. – Dopo gli iniziali entusiasmi, anche le vene crioconservate hanno evidenziato una elevata incidenza di ostruzioni37 ed ora si preferisce utilizzare le arterie di donatore, anche se i risultati tardivi non sono ancora consolidati. – PTA - STENTING. – Anche l’angioplastica percutanea del tratto femoropopliteo non è seguita da buoni risultati, con pervietà primarie inferiori al 50%38 ad un anno e 13 con pervietà secondarie di circa il 50%. Recenti lavori riportano un salvataggio d’arto del 66% nei pazienti con ischemia critica. La percentuale di ristenosi intrastent, ad 1 anno varia dal 20 al 46%; a questo problema si devono aggiungere le fratture degli stent40 in percentuale variabile in funzione del tipo di stent, con conseguente deterioramento clinico. Le terapie con inibitori della glicoproteina IIb/IIIa aumentano la pervietà dei trattamenti vascolari, ma sono di frequente complicate da una maggior morbilità e mortalità. L’angioplastica sottointimale secondo Bolia ha dato buoni risultati a livello femoropopliteo nei pazienti con claudicazione;41 le prime esperienze di trattamento delle occlusioni delle arterie tibiali per ischemia critica hanno portato a buoni risultati ad 1 anno, con una pervietà primaria cumulativa del 53% e con un salvataggio d’arto dell’ 81%;42 per alcuni questi risultati comunque non hanno una evidenza conclamata.43 I trattamenti endovascolari aggiuntivi all’angioplastica si basano su strumenti o tecniche quali l’aterectomia, l’uso del rotablator, la trombolisi o la tromboaspirazione. Tutte queste tecniche danno buoni risultati in casi selezionati, ma non sono supportati dalla evidenza di trials rigorosi.44,45 Il trattamento endovascolare, nei pazienti con lesioni trofiche, riduce il rischio di infezioni protesica. – INNESTI MIO-CUTANEI. – Gli innesti muscolo-cutanei peduncolati o liberi sono eseguiti da molti anni,46 dopo il trattamento di rivascolarizzazione, quando le lesioni sono particolarmente estese o quando il bypass innestato risulta parzialmente esposto. Il problema maggiore in questi casi è rappresentato dalle lesioni vascolari delle arterie su cui impiantare gli innesti, che differenzia i risultati rispetto a quelli ottenibili nei traumatizzati e per questo motivo vengono eseguiti raramente. TERAPIA NEI PAZIENTI NON RIVASCOLARIZZABILI – PROSTANOIDI. – La terapia con prostanoidi, già raccomandata nella TASC6 nei pazienti con ischemia non rivascolarizzabile, 14 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 è risultata efficace nel ridurre le dimensioni dell’ulcera anche con trattamento topico in un RCT.47 Alcuni studi prospettici e randomizzati avevano dimostrato la superiorità dell’iloprost verso il placebo,48 mentre una metanalisi non aveva evidenziato gli stessi risultati con la PGE1 e con altri farmaci vasoattivi.49 Diversi i risultati riportati dal gruppo ICAI, che comunque ha anche evidenziato che i benefici a breve con questo tipo di trattamento tendono a regredire facilmente.50 Con le prostacicline non sono comunque state dimostrate modificazioni in acuto (3 giorni) del livello di glucosio e di lattato nei tessuti ischemici, ma una verosimile risposta metabolica più tardiva.51 – STIMOLAZIONE SPINALE. – Questo particolare trattamento, nato per il controllo del dolore, ed efficace nel 94% di un gruppo di 38 pazienti, si rivelò utile anche per la guarigione delle ulcere vascolari in circa la metà dei casi.52 Da allora molti studi hanno evidenziato miglioramenti con un incremento della microcircolazione alla capillaroscopia,53 e con un aumento della tcpO2, anche nei pazienti diabetici con e senza ulcere.54 Una revisione della Cochrane Collaboration,55 valutando 6 studi comprendenti quasi 450 pazienti con ischemia critica non rivascolarizzabile trattati con stimolazione midollare o con terapia medica, ha evidenziato un salvataggio d’arto a 12 mesi ed una riduzione del dolore significativamente più alti nel gruppo degli SCS rispetto al trattamento conservativo senza significativa differenza fra i due trattamenti per quanto riguarda la guarigione delle ulcere. Questa revisione inserisce la stimolazione midollare fra i trattamenti da utilizzare nell’ischemia critica non rivascolarizzabile non considerati dalle linee guida TASC. – ALTRE TERAPIE CONSERVATIVE. – Non ancora validati i nuovi trattamenti quali: la terapia genica o l’impianto di monociti, utilizzati sperimentalmente nel trattamento delle ischemie critiche con lesioni trofiche su base aterosclerotica, diabetica ed arteritica. TRATTAMENTO DELLE LESIONI CUTANEE E DELLE INFEZIONI Le infezioni protesiche rappresentano una complicanza importante nelle rivascolarizzazioni femoro-distali ed inoltre, le infezioni sono un fattore favorente l’amputazione anche nei pazienti con rivascolarizzazione funzionante e pertanto devono essere trattate prontamente ed efficacemente.56 Nei pazienti con ulcere neuroischemiche anche apparentemente pulite, con tampone positivo, dovrebbe essere consigliato un trattamento antibiotico precoce.57 Per questi motivi, è opportuno eseguire uno studio batteriologico della lesione ed una detersione chirurgica e/o enzimatica giornaliera, essiccando le ulcere contenenti materiale necrotico fino alla rivascolarizzazione qualora l’asportazione di tessuti necrotici comporti ampie toilette. Le ulcere non necrotiche possono essere ricoperte con medicazioni idrofiliche, alginati ed idrocolloidi. Il ruolo dei fattori di crescita topici, quali quelli derivati dalle piastrine o da equivalenti di cute non è stato ancora completamente definito, pur essendo riportate in letteratura numerose esperienze positive. – OSSIGENOTERAPIA IPERBARICA. – L’ossigenoterapia iperbarica è un’arma aggiuntiva importante nella terapia delle ulcere ischemiche, che presentano una tensione locale di ossigeno inferiore a quella ottimale per la guarigione, perché stimola la proliferazione e la differenziazione dei fibroblasti, aumenta la formazione del collagene, aumenta la neovascolarizzazione e stimola l’azione battericida dei leucociti;58 tuttavia non dovrebbe essere considerate una terapia sostitutiva della rivascolarizzazione. – IMPATTO SOCIO-ECONOMICO. – Le ischemie critiche comportano un impatto socio-economico rilevante correlato alla gravità della malattia, alle comorbidità ed in particolare al tempo intercorso fra l’inizio della sintomatologia ed il trattamento. Spesso questi pazienti giungono tardivamente ad una rivascolarizzazione: quando le ulcere sono complicate da sovrainfezioni o si associano a gangrene delle dita o a lesioni da decubito. L. Pedrini: L’ischemia critica degli arti inferiori: una sfida per il chirurgo vascolare In pazienti con ulcere di grosse dimensioni o con necrosi che richiedono rivascolarizzazioni distali, i tempi di guarigione sono molto lunghi, anche di molti mesi, soprattutto quando le lesioni ischemiche coinvolgono il tallone,59 nonostante la rivascolarizzazione diretta di una arteria del piede. La lunga inattività o il prolungato allettamento comportano, inoltre, una estesa riabilitazione motoria, indispensabile per i pazienti che subiscono amputazioni maggiori, nel tentativo di protesizzarli o di ridurne il grado di dipendenza. A causa dei prolungati periodi di ricovero e dei lunghi periodi di medicazioni, questi pazienti comportano un grosso impegno economico e sociale, sia che i trattamenti vengano effettuati in regime di assistenza domiciliare integrata, sia che costringano il paziente ad un trattamento ambulatoriale. In questo caso spesso al costo della terapia e del materiale di medicazione si sommano i costi indiretti del trasporto e dell’accompagnamento del paziente, che spesso non è autosufficiente. Sotto il profilo psicologico, inoltre, questi pazienti presentano frequenti fenomeni depressivi ed una scarsa sensazione della qualità della vita legata al dolore e alla evidente lentezza della guarigione; questo stato si prolunga ancora qualche mese dopo la completa guarigione delle lesioni trofiche.60 Anche nei pazienti che hanno subito una rivascolarizzazione, i costi continuano nel follow-up, per i frequenti controlli ultrasonografici e per i reinterventi necessari per mantenere elevati il tasso di pervietà della rivascolarizzazione e per ridurre l’incidenza di amputazioni tardive, soprattutto nei pazienti sottoposti a rivascolarizzazioni femoro-distali, che sono le più frequenti. CONCLUSIONI Da quanto sopra esposto, appare chiaro che i fattori che concorrono alla realizzazione di un insuccesso, nella cura dei pazienti con ischemia critica sono numerosi, e costringono il chirurgo vascolare a scegliere fra le possibili terapie e le numerose tecniche quelle che in base alla sua personale esperienza sembrano meglio adattarsi al tipo di lesioni anatomiche, alla se- 15 de e alle dimensioni delle lesioni trofiche, alle caratteristiche del microcircolo. La scelta della tecnica difficilmente può essere supportata pienamente dalle evidenze della letteratura, perchè la comparazione dei risultati non è affatto semplice, soprattutto quando si paragonano i follow-up nei pazienti al 4° stadio di Leriche-Fontaine (stadio III 5-6 della classificazione di Rutherford), in quanto è assolutamente impossibile comparare i pazienti delle varie serie in funzione della gravità delle lesioni trofiche, anche utilizzando le classificazioni più dettagliate quali la Wagner o quella della Texas University, che comunque non contemplano le dimensioni della lesione trofica, la gravità dell’ischemia e lo stato del microcircolo. BIBLIOGRAFIA 1. Criqui MH, Langer RD, Fronek A, Feigelson HS, Klauber MR, McCann TJ, Browner D. Mortality over a period of 10 years in patients with peripheral arterial disease. N Engl J Med 1992;326:381-6. 2. American Cancer Sociey. Cancer Facts and Figures, 2000. 3. Fisher RK, Harris PL. Epidemiological and economic considerations in the critically ischemic limb. In: Branchereau A, Jacobs M. Critical limb ischemia. Futura Publishing Company, inc. Armony, NY, 1999; pp 19-25. 4. Mackey WC, McCullough JL, Conlon TP et al. the cost of surgery for limb-threatening ischemia. Surgery 1986;99:26-34. 5. Gupta SK,Veith FJ. Is arterial reconstruction cost-effective compared with amputation? In Greenhalgh RM et al. (eds) Limb salvage and amputation for vascular disease. WB Saunders, Philadelphia, 1988 pp. 447-452. 6. TASC(TransAtlantic Inter-Society) working group. Consensus. Management of peripheral arterial disease (PAD). J Vasc Surg 2000;31:S1,1-296. 7. Ricco J-B, Camiade C, Mangiacotti N, Ede B, Branchereau A. transluminal angioplasty combined with surgical reconstruction for lower limb ischemia. In: Branchereau A, Jacobs M. Critical limb ischemia. Futura Publishing Company, inc. Armony, NY, 1999: 119-34. 8. Flinn WR, McDaniel MD, Yao JST et al. Antithrombin III deficiency as a reflection of dynamic protein metabolism in patients undergoing vascular reconstruction. J Vasc Surg1984; 1:888. 9. Ray SA, Rowley MR, Loh A, Talbot SA, Bevan DH, Taylor RS, Dormandy JA. Hypercoagulable states in patients with leg ischemia. Br J Surg 1994;81(6):811-4. 16 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 10. Donaldson MC, Weinberg DS, Belkin M et al. Screening for hypercoagulable states in a vascular surgery practice: a preliminary study.J Vasc Surg 1990; 11:825-31. 11. Leijdekkers VJ, Vahl AC, Leenders JJM, Huijgens PC, Gans ROB, Rauwerda JA. Risk factors for premature atherosclerosis. Eur J Vasc Endovasc Surg 1999;17:394-7. 12. Jackson MR, Gillespie DL, Ghang AS, Longenecker EG, Peat RA, Alving BM. The incidence of heparin-induced antibodies in patients undegoing vascular surgery: a prospective study. J Vasc Surg 1998;28:439-45. 13. Donaldson MC, Belkin M, Whittemore AD, Mannik JA, Longtine JA, Dorfman DM. Impact of activated protein C resistance on general vascular surgical patients. J Vasc Surg 1997;25:1054-60. 14. Tazi Z, Cacoub P, Koskas F, Chabanel A, Chadefaux Wekemans B, Horellou MH, Viard JP, Piette JC, Kieffer E, Godeau P.Intérêt d'une exploration biologique approfondie au cours desl thromboses veineuses ou artérielles. Presse Med 1996 25;11:531-6. 15. Uccioli L. Gruppo di Studio Internazionale Piede Diabetico - Gruppo di Studio Piede Diabetico della Società Italiana di Diabetologia. Documento di Consenso internazionale sul Piede Diabetico. Mediserve ed. Milano, 2000 pp 29. 16. Faglia E, Mantero M, Caminiti M et al. L. Extensive use of peripheral angioplasty, particularly infrapopliteal, in the treatment of ischaemic diabetic foot ulcers: clinical results of a multicentric study of 221 consecutive diabetic subjects. J Intern Med. 2002 Sep;252(3):225-32. 17. Smeets L, de Borst GJ, de Vries JP, van den Berg JC, Ho GH, Moll FL. Remote iliac artery endarterectomy: seven-year results of a less invasive technique for iliac artery occlusive disease. J Vasc Surg. 2003 Dec;38(6):1297-304. 18. Teijink JA, van den Berg JC, Moll FL. A minimally invasive technique in occlusive disease of the superficial femoral artery: remote endarterectomy using the MollRing Cutter. Ann Vasc Surg. 2001 Sep;15(5):594-8. 19. Heijmen RH, Teijink JA, van den Berg JC, Overtoom TT, Pasterkamp G, Moll FL. Use of a balloon-expandable, radially reinforced ePTFE endograft after remote SFA endarterectomy: a single-center experience. J Endovasc Ther. 2001 Aug;8(4):408-16. 20. Hartung O, Otero A, Dubuc M, Boufi M, Barthelemy P, Aissi K, Alimi YS. Efficacy of Hemobahn in the treatment of superficial femoral artery lesions in patients with acute or critical ischemia: a comparative study with claudicants. 21. HallKV . The great saphenous vein used in situ as an arterial shunt after extirpation of the vein valves. Surgery 1962; 51: 492-5. 22. Shah DM, Darling RC, Chang BB et al. Longterm results of in-situ saphenous vein bypass. Analysis of 2058 pts. Ann Surg 1995;222:438-46. 23. van Dijk LC, Wittens CHA. Refinements of the in situ vein bypass: towards a more "closed" technique. Eur J Vasc Endovasc Surg 1996; 12: 136-8. 24. Dalman RL, Taylor LM. Basic data related to infrainguinal revascularization procedures. Ann Vasc Surg 1990;4:309-12. 25. Moody AP, Edwards PR, Harris PL. In situ versus reversed femoropopliteal vein grafts: long –term follow-up of a prospective, randomised trial. Br J Surg 1992;79:750-2. 26. Watelet J, Soury P, Menard JF et al. Femoropopliteal bypass: in-situ or reversed vein graft? Ten-years results of a randomised prospective study. Ann Vasc Surg 1997;11:510-9. 27. Sesto ME, Sullivan TM, Hertzer NR et al. Cephalic vein grafts for lower extremity revascularization J Vasc Surg 1992;15:543-9. 28. Harward TRS, Coe D, Flynn TC, Seeger JM. The use of arm in conduits during infrageniculate arterial bypass. J Vasc Surg 1992;16:420-7. 29. Stonebridge PA, Prescott RP, Rukley CV. Randomised trial comparing infrainguinal polytetrafluoroethylene bypass grafting with and without vein interposition cuff at the distal anastomosis. J Vasc Surg 1997;26:543-50. 30. Taylor RS, Loh H, McFarland RJ, Cos M, Chester JF. Improved technique for polytetrafluoroethylene bypass grafting: long term results using anastomotic vein patches. Br J Surg 1992;79:348-54. 31. Tyrrell MR, Wolfe JHN. New prosthetic venous collar anastomotic technique: combining the best of other procedures. Br J Surg 1991;78:1016-17. 32. Wijesinghe LD, McCollum PT. Prosthetic distal bypass for critical leg ischaemia. In: Earnshaw JJ, Murie JA (eds). The evidence for vascular surgery. TFM publishing Limited – JVRG. Shropshire, 1999, pp: 55-9. 33. Fisher RK, Harris PL. Improving patency of femorodistal bypass. In: Earnshaw JJ, Murie JA (eds). The evidence for vascular surgery. TFM publishing Limited – JVRG. Shropshire, 1999, 43-3. 34. Panneton JM, Hollier LH, Hofer JM. Multicenter randomized prospective trial comparing a pre-cuffed polytetrafluoroethylene graft to a vein cuffed polytetrafluoroethylene graft for infragenicular arterial bypass. 35. Oderich GS, Panneton JM, Yagubyan M, et al. Comparison of precuffed and vein-cuffed expanded polytetrafluoroethylene grafts for infragenicular arterial reconstructions: a case-matched study. Ann Vasc Surg. 2005 Jan;19(1):49-55. 36. Hingorani AP, Ascher E, Marks NA, et al. A 10year experience with complementary distal arteriovenous fistula and deep vein interposition for infrapopliteal prosthetic bypasses. Vasc Endovascular Surg. 2005 Sep-Oct;39(5):401-9. 37. Farber A, Major K. Cryopreserved saphenous vein allografts in infrainguinal arterial reconstruction. J Cardiovasc Surg (Torino). 2004 Jun;45(3):213-6. Review. L. Pedrini: L’ischemia critica degli arti inferiori: una sfida per il chirurgo vascolare 38. Soder HK, Manninen HI, Rasanen HT, Kaukanen E, Jaakkola P, Matsi PJ. Failure of prolonged dilation to improve long-term patency of femoropopliteal artery angioplasty: results of a prospective trial. J Vasc Interv Radiol. 2002 Apr;13(4):361-9. 39. Morgan JH 3rd, Wall CE Jr, Christie DB, Harvey RL, Solis MM. The results of superficial femoral, popliteal, and tibial artery stenting for peripheral vascular occlusive disease. Am Surg. 2005 Nov;71(11):905-9; discussion 909-10. 40. Schlager O, Dick P, Sabeti S, Amighi J, Mlekusch W, Minar E, Schillinger M. Long-segment SFA stenting--the dark sides: in-stent restenosis, clinical deterioration, and stent fractures. J Endovasc Ther. 2005 Dec;12(6):676-84. 41. BoliaA, Bell PRF. Femoropopliteal and crural artery recanalisation using subintimal angioplasty. Sem Vasc Surg 1995;8:253-64. 42. Nydahl S, Hatshorne T, Bell PRF, Bolia A, London NJM. Subintimal angioplasty of infrapopliteal occlusions in critically ischaemic leg. Eur J Vasc Endovasc Surg 1997;14:212-6. 43. Ashley S. The role of subintimal angioplasty. In: Earnshaw JJ, Murie JA (eds). The evidence for vascular surgery. TFM publishing Limited – JVRG. Shropshire, 1999, pp:37-41. 44. Coppi G, Silingardi R, Moratto R, Camparini S, Ragazzi G, Gennai S, Pacchioni R. Adjunctive techniques to PTA: thrombolysis, suction embolectomy and rotablator. In: Branchereau A, Jacobs M. Critical limb ischemia. Futura Publishing Company, inc. Armony, NY, 1999; 101-18. 45. Lamont PM. Management of intermittent claudication. In: Earnshaw JJ, Murie JA (eds). The evidence for vascular surgery. TFM publishing Limited – JVRG. Shropshire, 1999, 31-6. 46. McFarland RJ, Taylor RS, Wood F, Mayou B. Free-flap reconstruction of heel pad after femorotibial bypass salvage graft. Br J Surg. 1989 Feb;76(2):158-9. 47. Tondi P, Gerardino L, Santoliquido A, et al. Treatment of ischemic ulcers of the lower limbs with alprostadil (prostaglandin E1). Dermatol Surg. 2004 Aug;30(8):1113-7. 48. Balzer K, Bechara G, Bisler H, et al. Reduction of ischaemic pain in advanced peripheral arterial occlusive disease. A double blind placebo controlled trial with iloprost. Int Angiol 1991;10:229-32. 49. Loosermore TM, Chalmers TC, Dormandy JA. A meta-analysis of randomised placebo control trials in Fontaine stages III and IV peripheral occlusive arterial disease. Int Angiol 1994;13:133-42. 50. The ICAI Study Group. Prostanoids for chronic critical leg ischemia. A randomized, controlled, 17 open-label trial with prostaglandin E1. Ischemia Cronica degli Arti Inferiori. Ann Intern Med. 1999 Mar 2;130(5):412-21. 51. Danielsson P, Metzsch C, Norgren L. Effect of Iloprost infusion on metabolism in critical limb ischemia, utilizing microdialysis. A pilot study. Int Angiol. 2004 Sep;23(3):259-62. 52. Augustinson LE, Carlson CA, Holm J, Jivergard L. Epidural electric stimulation in severe limb ischemia. Pain relief, increased blood flow and possible limb-saving effect. Ann Surg 1985;202:104-10. 53. Jacobs MJ, Jorning PJ, Beckers RCY, et al. Foot Salvage and improvement of microvascular blood flow as a result of epidural spinal cord electrical stimulation. J Vasc Surg 1990;12:354-60. 54. Petrakis IE, Sciacca V. Epidural spinal cord electrical stimulation in diabetic critical lower limb ischemia. J Diabetes Complications 1999;13:293-9. 55. Ubbink DT, Vermeulen H. Spinal cord stimulation for non-reconstructable chronic critical leg ischaemia. The Cochrane Database of Systematic Reviews 2003, Issue 3. Art. No.: CD004001. DOI: 10.1002/14651858.CD004001. 56. Kummer O, Widmer MK, Pluss S, Willenberg T, Vogele J, Mahler F, Baumgartner I.Does infection affect amputation rate in chronic critical leg ischemia? Vasa. 2003;32(1):18-21. Related Articles, Links. 57. Edmonds M, Foster A. The use of antibiotics in the diabetic foot. Am J Surg. 2004;187(5A):25S28S. Review. 58. Niinikoski JH. Clinical hyperbaric oxygen therapy, wound perfusion, and transcutaneous oximetry. World J Surg. 2004 Mar;28(3):307-11. 59. Treiman GS, Oderich GS, Ashrafi A, Schneider PA. Management of ischemic heel ulceration and gangrene: An evaluation of factors associated with successful healing. J Vasc Surg. 2000;31(6):1110-8. 60. Tretinyak AS, Lee ES, Kuskowski MM, Caldwell MP, Santilli SM. Revascularization and quality of life for patients with limb-threatening ischemia. Ann Vasc Surg. 2001;15(1):84-8. 61. Rutherford RB, Baker JD, Ernst C, Johnston KW, Porter JM, Ahn S, Jones DN. Recommended standards for reports dealing with lower extremity ischemia: revised version. J Vasc Surg. 1997;26(3):517-38. 62. Wagner FW: The dysvascular foot: a system of diagnosis and treatment. Foot Ankle 1981, 2: 64–122. 63. Lavery LA, Armstrong DG, Harkless LB: Classification of diabetic foot wounds. J Foot Ankle Surg 1996, 35:528–31. ____ Per richiesta estratti: Prof. Luciano Pedrini Struttura Complessa di Chirurgia Vascolare - Ospedale Maggiore - 40100 Bologna ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 B) LA DIAGNOSTICA ULTRASONOGRAFICA NELL’ISCHEMIA CRITICA DEGLI ARTI INFERIORI NON INVASIVE DIAGNOSIS IN CRITICAL LOWER LIMB ISCHEMIA PIO MAURIZIO NICOSIA U.O.C. Angiologia – Azienda Ospedaliera San Camillo-Forlanini – Roma Parole chiave: Ischemia critica degli arti inferiori, Ultrasonografia. Key words: Critical limb ischemia, Ultrasonography. La valutazione strumentale delle arteriopatia periferiche è essenzialmente quella dell’ecocolorDoppler sia nel primo approccio che nella valutazione più approfondita per l’indicazione di procedure chirurgiche o di radiologia interventistica. VALUTAZIONE CLINICA La valutazione strumentale dell’arteriopatia periferica si avvale dell’ultrasonografia e deve essere guidata da corretti criteri d’orientamento emodinamico e clinico. A questo riguardo è sempre valida la classica suddivisione in stadi clinici di Fontaine: • I stadio asintomatico • II stadio: claudicatio (A>100mt>B) ischemia relativa • III stadio: dolori a riposo • IV stadio: lesioni trofiche ischemia assoluta Il concetto di ischemia critica degli arti è questionabile (qualcuno ha scisso l’ischemia critica come quadro cronico da una ischemia acuta degli arti) ma al di là della sua reale consistenza si deve constatare l’indubbia fortuna del termine vuoi per moda culturale o per intrinseca utilità. Riteniamo di una certa utilità conservare il concetto intendendo l’ischemia critica degli arti come un quadro d’ischemia assoluta d’insorgenza sia acuta che cronica in fase di rapida evolutività e che necessita di un approccio terapeutico medico e interventistico-chirurgico immediato Attribuiamo al termine “critica” il significato non tanto di grave in sé ma piuttosto quello etimologico di richiedente scelta e ciò implica che l’esame va condotto e refertato col proposito di offrire elementi utili alla scelta di una condotta terapeutica Nella visita angiologica anamnesi, ispezione, esame fisico e strumentale Doppler sono intimamente connesse all’uso dell’ultrasonografia Doppler alla luce di elementari regole di emodinamica • Il primo stadio è quello asintomatico che ben prima dell’introduzione dell’ecoDoppler aveva un significato questionabile mentre adesso è di sicura ricognizione ultrasonografica. • Il secondo stadio è quello dell’ischemia relativa all’esercizio con discrimine interno di autonomia di 100 metri nel senso di una più o meno rapida propensione verso il III stadio quando si varchi detta soglia. • Classificazione di Fontaine III stadio: dolore a riposo. Nell’anamnesi il paziente lamenta dolori a riposo (anche se il dolore può mancare nel diabetico). Il dolore si esacerba la notte e in clinostatismo e precorre di poco l’insorgenza di turbe trofiche con assunzione di peculiari posizioni antalgiche quali flessione del ginocchio e arto pendente. All’esame obiettivo ispettivo può essere presente pallore e replezione venosa nelle forme d’ischemia acute recenti per trombosi o embolia oppure eritrocianosi declive e replezione venosa in parti- P.M. Nicosia: La diagnostica ultrasonografica nell’ischemia critica degli arti inferiori colare nelle forme a decorso cronico. Il colore della cute è alterato in relazione alla postura con pallore clinostatico e cianosi dell’arto declive oppure in relazione a manovre (allungamento del tempo di riempimento del plesso subpapillare dopo digitopressione dei polpastrelli). • Classificazione di Fontaine IV stadio: lesioni trofiche. Esame obiettivo ispettivo: distinguiamo un quadro reversibile (pallore, ipotermia con lesioni di continuo iniziali) e un quadro irreversibile (ipossia stagnante, ulcerazioni o necrosi, sepsi, osteomielite, gangrena gassosa) VALUTAZIONE STRUMENTALE • Valutazione del livello emodinamico e della riserva funzionale • Diagnosi di natura dell’affezione • Valutazione di altri distretti • Valutazione del livello emodinamico e della riserva funzionale: non sempre v’è correlazione tra entità di dolore e anomalie ispettive da un lato e gravità ed evolutività del quadro emodinamico dall’altro. Spesso la sintomatologia è una modesta parestesia e i segni sono lievi pallore e ipotermia anche in quadri di severo impegno emodinamico rivelabile soltanto dall’esame Doppler • Diagnosi di natura dell’affezione: elementi ultrasonografici possono essere utili, insieme all’anamnesi e all’esame clinico generale, a stabilire la probabilità di natura embolica o di trombosi locale; la genesi cardiogena o da tromboembolia a partenza da lesioni vascolari di placca o aneurismatiche o da dissecazione • Valutazione di altri distretti: è di vitale importanza per il trattamento una valutazione di condizioni a rischio in altri distretti, in particolare epiaortico, viscerale 19 Winsor permette di valutare l’entità funzionale dell’arteriopatia considerando una forma lieve per un I.W.> 0,8 una forma di media gravità per 0,8>I.W.>0,4 una forma severa per I.W.<0,4 • EcocolorDoppler: Permette una vera e propria “angiografia funzionale” con una valutazione morfologica, di natura, del quadro funzionale e di evolutività clinica delle lesioni. • Aree d’attenzione: le biforcazione arteriose, le arterie con criticità del circolo collaterale (femorale comune, poplitea). L’immagine ecografica di per sé documenta la presenza di aneurismi, trombi, placche, mediocalcinosi (prevalentemente sottopoplitea nel diabetico). La velocimetria Doppler soprattutto se di tipo colorDoppler permette di vagliare i parametri illustrati nelle figg. 1, 2, 3 e 4. ESAMI STRUMENTALI • Doppler a onda continua: è il fonendoscopio dell’angiologo. Permette valutazioni anatomiche e funzionali con la tensiometria segmentale. L’indice di Figura 1 - Valutazione del regime delle resistenze di un distretto, ridotte nell’arteriopatia per la dilatazione dei vasi di resistenza. 20 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 Figura 2 - Valutazione dell’entità della stenosi in base alla velocità di picco. Figura 3 - Valutazione del circolo collaterale (attivazione ed entità). Figura 4 - Valutazione della caduta di energia,subito a valle della lesione (turbolenze, demodulazione). Alcuni quadri specifici di arteriopatia periferica, diversi dall’arteriosclerosi, a frequente esordio acuto ischemizzante sono rappresentati nelle figg. 5, 6 e 7. Figura 5 - Morbo di Buerger. Figura 6 - Malattia polianeurismatica. P.M. Nicosia: La diagnostica ultrasonografica nell’ischemia critica degli arti inferiori 21 3. Valutazione del circolo collaterale 4. Valutazione di lesioni emodinamiche a monte e a valle della principale 5. Coesistenza di lesioni viscerali e sopraortiche BIBLIOGRAFIA ESSENZIALE Figura 7 - Microembolie periferiche, sindrome del dito blu con indennità dei rilievi ecoDoppler sui vasi tronculari. In conclusione lo studio ecocolorDoppler deve appurare: 1. Valutazione della lesione principale (trombo-embolo, placca, dissecazione, emorragia subintimale) 2. Ricerca di aneurisma aortico o in altre sedi (iliache, femoro-poplitee) come focolaio emboligeno Cary NRB. Pathology of peripheral arterial disease. In: Tooke JE, Lowe GDO (Eds). Texbook of vascular medicine. London: Arnold, 1996:143-8. Catalano M. Epidemiology of critical limb ischaemia: north Italian data. Eur J Med 1993; 2: 11-4. Dormandy JA, Ray S. The natural history of peripheral arterial disease. In: Tooke JE, Lowe GDO (Eds). Textbook of vascular medicine. London: Arnold, 1996:162-75. Ruckley CV. Symptomatic and asymptomatic disease. In: Fowkes FGR (Ed). Epidemiology of peripheral vascular disease. London: Springer, 1991:97108. Second European Consensus Document on chronic critical leg ischemia. Eur J Vasc Surg:1992;6(Suppl A):1-32. Stoffers HE et al. Prevalence in general practice. In: Fowkes FGR (Ed). Epidemiology of peripheraI vascular disease. London: Springer, 1991:109-15. Vogt MT et al. Lower extremity arterial disease and the aging process: a review. J Clin Epidemiol 1992;45:529-42. Widmer LK et al. Risk profile and occlusive periphery artery disease (OPAD). In: Proceedings of the 13th International Congress of Angiology; June 1985; Athens, Greece;28. ____ Per richiesta estratti: Dr. P.M. Nicosia U.O.C. Angiologia - Ospedale S. Camillo Circonvallazione Gianicolense - 00152 Roma ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 C) DIAGNOSTICA RADIOLOGICA TC E RM NELLA ISCHEMIA CRITICA DEGLI ARTI INFERIORI MR AND CT IN DIAGNOSIS OF LOWER EXTREMITY ARTERIAL DISEASE VITALIANO BUFFA, GIOVANNI REGINE, VITTORIO MIELE, LOREDANA ADAMI Radiologia Generale - Azienda Ospedaliera San Camillo-Forlanini - Roma Parole chiave: AngioTAC, AngioRMN, Patologie arteriose. Key words: CT angiography, MR angiography, Arterial disease. La valutazione diagnostica strumentale delle arteriopatie periferiche si avvale della Risonanza Magnetica già da alcuni anni e, più recentemente, della Tomografia Computerizzata. Il ruolo di queste metodiche è definire la diagnosi e la localizzazione anatomica delle lesioni vascolari, la selezione dei pazienti ai fini di uno specifico trattamento, la pianificazione preoperatoria, il followup, sostituendo, grazie alla minore invasività, l’angiografia digitale. La Risonanza Magnetica (RM) è metodica matura, ampiamente documentata dalla Letteratura scientifica. Attualmente vengono usati magneti ad alto campo (1 3 T) e sequenze specifiche (3D-SPGR) che rilevano il segnale proveniente dal mdc paramagnetico all’interno dei vasi. L’acquisizione dei dati riguarda un volume corporeo, di norma l’addome e gli arti inferiori inclusi i piedi, attraverso 3 diverse fasi in cui viene studiata l’aorta e le arterie iliache, i vasi di coscia e quelli di gamba e piede attraverso lo spostamento del lettino all’interno del magnete. Le immagini dei vasi ottenute sono visualizzate su workstation di elaborazione e possono essere ruotate per evidenziare i punti di interesse. La rappresentazione vascolare è analoga a quella ottenuta dall’angiografia tradizionale, con un’accuratezza nell’identificazione delle stenosi che è stata definita da alcune metanalisi del 94-96%.1,2,6 È possibile inoltre effettuare uno studio dinamico di uno specifico segmento arterioso, tecnica detta time-resolved, con visualizza- zione del passaggio del bolo di mdc. Questa tecnica fornisce informazioni sul flusso ematico, in maniera analoga all’angiografia tradizionale, consentendo una valutazione soggettiva di quantità e velocità di flusso e elimina la sovrapposizione delle immagini provenienti dalle vene. La RM consente quindi principalmente la valutazione del lume vasale (la luminografia). La valutazione morfologica delle pareti vasali richiede l’impiego di ulteriori sequenze e per motivi tecnici è limitata alle pareti dei vasi di maggior calibro (aorta, arterie iliache: figg. 1 e 2) in quanto lo studio dettagliato dei vasi di minor calibro richiederebbe un tempo molto maggiore e l’impiego di bobine dedicate. Anche le calcificazioni sono scarsamente visualizzabili con la RM. Complessivamente la scarsa esplorabilità delle pareti vasali e delle calcificazioni è un limite della metodica. La TC viene utilizzata da pochi anni ed è quindi metodica recente rispetto alla RM. L’uso della TC è stato reso possibile dall’introduzione della tecnica di acquisizione multistrato e dalla diffusione di programmi informatici di ricostruzione d’immagine. L’aumento di risoluzione spaziale (vengono ottenute immagini di risoluzione sottomillimetrica) e la possibilità di rappresentare in maniera panoramica i vasi degli arti inferiori, di piccolo calibro e a decorso tortuoso, hanno reso la TC uno strumento molto accurato, versatile e scarsamente invasivo.3,4,5 L’esame TC necessita della somministrazione di mdc iodato in quantità di- V. Buffa et al.: Diagnostica radiologica (TC e RM) nella ischemia critica degli arti inferiori screta (100-120 cc) per consentire la visualizzazione arteriosa di tutto l’addome e degli arti inferiori; la scansione è molto rapida (20-30 secondi) e con l’impiego di programmi di riduzione automatica della dose l’esposizione del paziente è contenuta e considerata inferiore a quella dell’angiografia tradizionale. A fronte di una breve durata di scansione e di uno scarso periodo di permanenza del paziente in sala TC, il tempo di elaborazione delle immagini multiplanari e tridimensionali angiografiche (figg. 3, 4 e 5), indispensabili per la diagnosi e la corretta rappresentazione dei vasi, può essere relativamente lungo. Il vantaggio della TC rispetto alla RM è la possibilità di visualizzare sia il lume del vaso, producendo con i programmi suddescritti immagini angiografiche, sia la parete vasale, consentendo una valutazione diretta delle placche ateromasiche di cui può essere misurata la lunghezza, lo spessore e le caratteristiche strutturali essendo la metodica in grado di identificare le parti molli (fibrolipidiche), le calcificazioni e le irregolarità superficiali. In particolare la densità delle parti fibrolipidiche e della trombosi di parete è molto bassa ed è ben differenziabile dall’elevata densità del sangue circolante, iperdenso 23 per la presenza del mdc. Sono quindi riconoscibili facilmente, anche in relazione alla elevata risoluzione spaziale, le piccole irregolarità e le ulcerazioni superficiali delle placche. Le calcificazioni hanno densità molto elevata e possono, quando molto diffuse e grosse, ridurre la visibilità del lume vasale. Inoltre la documentazione delle dimensioni, dell’estensione e delle caratteristiche strutturali degli aneurismi è agevole e molto accurata. Le raccomandazioni delle società scientifiche (ACC/AHA, TASC, SIAPAV) (Tab. 1, 2, 3), disponibili attualmente, affidano a queste metodiche un ruolo complessivamente meno rilevante della angiografia. Tuttavia bisogna tener presente che le innovazioni tecnologiche che hanno riguardato le apparecchiature diagnostiche, e particolarmente la TC, sono di introduzione molto recente. È verosimile quindi che le stesure successive delle linee guida possano tenere conto di una maggiore quantità di lavori scientifici e studi di metanalisi decretando per queste metodiche un ruolo più incisivo nella diagnostica. È già opinione comune tuttavia che queste metodiche siano in grado di sostituire l’angiografia, nel futuro a breve da utilizzare solo nell’ambito di procedure interventistiche. Tabella 1. - Linee guida ACC/AHA sull’impiego di TC e RM nelle arteriopatie periferiche. Recommendations CT ANGIOGRAPHY Class IIB 1. 2. CTA of the extremities may be considered to diagnose anatomic location and presence of significant stenosis in patients with lower extremity PAD. (Level of Evidence: B) CTA of the extremities may be as a substitute for MRA for those patients with contraindications to MRA. (Level of evidence: B) MR ANGIOGRAPHY Class I 1. 2 3. MRA of the extremities is useful to diagnose anatomic location and degree of stenosis of PAD. (Level of Evidence: A) MRA of the extremities should be performed with Gadolinium enhancement. (Level of Evidence: B) MRA of the extremities is useful in selecting patients with lower extremity PAD as candidated for endovascular intervention. (Levl of Evidence: A) Class IIb 1. 2. MRA of the extremities may be consider to select patients with lower extremity PAD as candiddated for sugical bypass and to select the istes of surgical anastomosis. (Level of Evidence:B) MRA of the extremities may be consider for postrevascularization (endovascular and surgical bypass) surveillance in patients with lower extremity Pad. (Level of Evidence: B) 24 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 Tabella 2. - Linee guida TASC sull’impiego di RM e TC nelle arteriopatie periferiche. Magnetic Resonance Angiography (MRA). The other possible future scenario is that MRA may become the preferred imaging technique, as a pratical compromise between duplex imaging and angiography, although with current techniques it tends not to distinguish well between tight stenoses and complete occlusion. However, for at least aortoiliac disease, some studies have shown that the best MRA techniques are adequate for stenosis qualification and discriminating between stenosis and occlusion. In some cases MRA (especially with contrast enhancement) may be as good as conventional angiography. Further studies are needed to determine to what extent Mra may replace angiography. Spiral Computed Tomography (CT) Spiral CT is also being used for the noninvasive evaluation of proximal, that is, aortoilliac occlusive, disease. CRITICAL ISSUE 4: Alternative investigations to angiography Further studies are needed to determine to what extent duplex scanning, magnetic resonance angiography, or other new imaging modalities may replace angiography for many applications in the future. Tabella 3. - Linee guida SIAPAV relative alla diagnostica radiologica. La diagnostica radiologica Raccomandazione 10: L’angiografia deve essere riservata ai pazienti nei quali, sulla base della sintomatologia clinica, dell’esame obiettivo e degli accertamenti non invasivi, si ipotizzi un trattamento chirurgico o una terapia endovascolare. La presenza di stenosi renali emodinamiche in pazienti con arteriopatia degli arti inferiori, per le quali è prevista una terapia farmacologica trova giustificato uno studio angiografico, per un eventuale trattamento percutaneo o chirurgico. Nei pazienti con assenza di lesioni significative dei tronchi sovraortici, documentata da uno studio con ecodoppler, non risulta indicato procedere ad una panangiografia. Raccomandazione 11: Lo studio vascolare con angio-TC o con angio-RMN è indicato nei pazienti con associazione di arteriopatie ostruttive ed aneurismatiche, nei pazienti con difficoltoso accesso vascolare e nei pazienti con sospettata dissecazione. L’angio-RMN è indicata nei pazienti con controindicazione all’uso di mezzi di contrasto iodati. Figura 2 - AngioRM. Si evidenzia occlusione dell’iliaca comune di sinistra e stenosi severa dell’iliaca comune destra. Figura 1 - AngioRM aorto-iliaca e delle arterie degli arti inferiori (sequenza GE con mdc paramagnetico). Occlusione dell’iliaca comune sinistra all’origine. V. Buffa et al.: Diagnostica radiologica TC e RM nella ischemia critica degli arti inferiori 25 Figura 5 - Angiografia TC, immagine tridimensionale. Occlusione della femorale superficiale destra con evidenza di circoli collaterali. Figura 3-4 - Angiografia TC (stesso caso), immagini tridimensionali. Si evidenziano chiaramente le stenoocclusioni e i circoli collaterali. BIBLIOGRAFIA 1. Koelemay MJK, Lijmmer JG, Stoker J, et al. Magnetic Resonance Angiography for the evaluation of lower extremity arterial disease. A metanalisys. JAMA 2001; 285:1338-45. 2. Visser K, Hunink MGM. Peripheral arterial disease: gadolinium- enhanced MR Angiography vs Color-Guided Duplex US- A metanalisys. Radiology 2000; 216:67-77. 3. Catalano C, Fraioli F, Laghi A, et al. Infrerenal aortic and lower-extremity arterial disease: diagnostic performance of multi-detector row CT angiography. Radiology 2004; 231:555-63. 4. Ofer A, Nitecki SS, Linn S et al. Multidetector CT angiography of peripheral vascular disease. AJR 2003; 180: 719-24. 5. Willman JK, Mayer D, Banyai M et al. Evaluation of peripheral arterial bypass grafts with multidetector row CT angiography: comparison with duplex US and digital subtraction angiography. Radiology 2003: 229: 465-74. 6. Assessment of critical limb ischemia in patients with diabetes: comparison of MR angiography and digital subtraction angiography. AJR 2005, 185:1641-50. ____ Per richiesta estratti: Dr. Vitaliano Buffa - Radiologia Centrale Ospedale S. Camillo - Circonvallazione Gianicolense - 00152 Roma ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 D) PROCEDURE ENDOVASCOLARI DI RIVASCOLARIZZAZIONE DEL DISTRETTO FEMORO-POPLITEO NEL PAZIENTE CRITICO ENDOVASCULAR REVASCULARIZATION PROCEDURES OF BELOW-THE-KNEE ARTERIES IN CRITICAL PATIENTS MAURIZIO MORUCCI, PAOLO AGRESTI, LORENZO DE’ MEDICI U.O.C. di Radiologia Vascolare ed Intervensitica Azienda Ospedaliera San Camillo-Forlanini - Roma Parole chiave: Ischemia critica, Procedure endovascolari, Rivascolarizzazione. Key words: Critical Ischemia, Endovascular procedure, Revascularization. La Malattia Aterosclerotica (MA) è una patologia sempre più frequente, soprattutto in conseguenza dell’odierno stile di vita e per il maggiore protrarsi dell’età media della popolazione. La MA può presentarsi sia in modo solo distrettuale o segmentario (segmenti aorto-iliaco e femoro-popliteo, rami tibio-poplitei, tronchi sopra-aortici, circolo cerebrale, aa renali, aa coronarie) che pluridistrettuale. L’interessamento contemporaneo di più distretti, pone problematiche terapeutiche spesso difficilmente risolvibili, ovvero ai limiti delle classiche terapie sia mediche che chirurgiche ed anche interventistiche. Ciò è particolarmente vero quando i distretti interessati sono posti sullo stesso asse vascolare, come nel caso degli arti inferiori. Ulteriore elemento di aggravamento è la frequente presenza di patologie associate, fra le quali assume particolare importanza la presenza di diabete, patologia che agisce anch’essa sul territorio vascolare (periferico).1,2 Fra le altre patologie associate di particolare importanza, ricordare le coagulopatie, l’ipertensione ed il tabagismo.1,2 Generalmente la sola correzione dell’inflow prossimale iliaco-femorale può essere sufficiente per ristabilire un adeguato flusso periferico, anche nei pazienti critici.1,3,4,5 Ma in alcuni casi questo può non bastare e deve essere associato ad un trattamento anche del segmento sotto-popliteo.3,6,7 La storica classica divisione fra trattamento squisitamente chirurgico “a cielo aperto” o con le metodiche “interventisti- che” è stata ultimamente superata, anche a livello semantico, con la individuazione di quella che è stata chiamata “terapia endovascolare”. Un ulteriore evoluzione pratica è stata conseguita dalla presa di coscienza del fatto che la terapia chirurgica a cielo aperto ed il trattamento endovascolare non sono necessariamente alternativi, ma possono essere spesso utilizzati in associazione combinata (procedure “ibride”),8 per ottenere un trattamento “su misura” per ogni paziente, in rapporto alle specifiche esigenze di ogni singolo caso. 2,4,7 Questo consente, inoltre, di limitare in modo significativo la morbilità e la mortalità riducendo al minimo lo stress per il paziente.2 La terapia interventistica (o endovascolare), più della terapia chirurgica a cielo aperto, ha beneficiato in questi ultimi anni di una notevole spinta innovativa, dovuta principalmente ad una formidabile evoluzione tecnologica dei materiali a disposizione (in primo luogo degli “stent” vascolari, nelle loro ormai innumerevoli varianti, dei palloncini da angioplastica e di nuove “guide” angiografiche idrofiliche e con supporto rigido, introduttori vascolari dedicati, etc).8,9,10 Ma molta importanza ha avuto anche lo sviluppo di nuove tecniche di ricanalizzazione, fra le quali riveste particolare importanza pratica, la tecnica di ricanalizzazione periferica sotto-intimale secondo Bolia.11,12 Altro capitolo altrettanto importante è la terapia fibrinolitica selettiva loco-regionale. Questa metodica è in grado di ottenere spesso M. Morucci et al.: Procedure endovascolari di rivascolarizzazione del distretto femoro-popliteo nel paziente critico gli stessi risultati della embolectomia chirurgica a livello iliaco-femorale (ma utilizzabile anche nei pazienti con alterazioni aterosclerotiche), e con risultati spesso sorprendenti nei segmenti sotto-poplitei, area spesso problematica per la chirurgia. Da menzionare anche la notevole evoluzione tecnologica nel campo degli Aterotomi,13 Laser,14 Trombolizzatori e Tromboaspiratori15 e l’introduzione dei “Cutting Balloon”8,16 e della Crioplastica (angioplastica effettuata con palloncino morfologicamente simile a quelli usuali, ma con temperatura superficiale di circa meno 50-60°C15. Queste metodiche, di notevole complessità tecnica (che richiedono una notevole esperienza specifica) e di alto costo economico, vanno considerate inevitabilmente di secondo livello rispetto alle metodiche di angio-plastica stent e di fibrinolisi locoregionale. La ricanalizzazione sub-intimale, introdotta da Bolia ed il suo gruppo negli anni ’90,11 è stata accolta inizialmente da forti perplessità, se non scetticismo, ma in breve tempo si è imposta come una metodica preziosa, in particolare nei pazienti critici12,17. In questi pazienti, la complessità e molteplicità delle lesioni, generalmente multiple ed estese a gran parte dell’albero arterioso presenta grandi difficoltà sia per la chirurgia tradizionale che per la rivascolarizzione endovascolare classica trovando nella scarsità del run-off la principale causa di insuccesso. La ricanalizzazione sub-intimale può essere invece abilmente estesa sino in sede molto periferica (tibio-peroneale, se non più distale).11,12 La base teorica e pratica è data dalla possibilità offerta dalla media “rovesciata” di creare un by-pass “vivente” in situ, in qualche modo vergine, ovvero non ancora interessato dalle alterazioni aterosclerotiche.11 La metodologia di “entrata” all’interno della media è tanto ingegnosa quanto semplice: creare intenzionalmente una estesa dissezione nel vaso da trattare. Dopo aver dissecato il vaso (o i vasi) da ricanalizzare in tutta la sua-loro estensione, si dovrà “rientrare” all’interno dell’albero arterioso in un tratto sano e con adeguato run-off. Il tramite virtuale creato andrà poi ampliato con adeguata angioplastica su tutto il percorso da trattare, possi- 27 bilmente, senza uso di stent.11 Quanto esposto, pur nella apparente semplicità, richiede una notevole perizia tecnica ed una adeguata esperienza specifica. Alla abilità necessaria per le manovre di “entrata” subintimale e “rientro”, si aggiunge la perizia di “navigare” nella media senza uscire dal vaso (rottura esterna), ma soprattutto la capacità di gestire le non rare ed inevitabili complicanze immediate (embolia distale, rottura vascolare, etc.). Per trattare con successo queste complicanze è necessaria la più ampia conoscienza e consuetudine con le altre procedure di rivascolarizzazione quali la fibrinolisi locoregionale e la tromboaspirazione. I risultati di medio termine possono essere ritenuti molto buoni, trattandosi di pazienti generalmente critici e spesso altrimenti destinati all’amputazione. Le casistiche importanti cominciano ad essere numerose, con successo tecnico immediato di oltre il 95%, risultati di pervietà primaria a 2 anni ben oltre il 50%, con punte del 70-80% e salvataggi d’arto di oltre l’80%.12,17 Molto alta (oltre il 90% dei successi tecnici) è la regressione delle lesioni ulcerative.17 Curiosa constatazione è che questa tecnica ha maggiore successo nei pazienti che presentano ostruzioni cronicizzate, ovvero da almeno 3 mesi,17 in questo assolutamente simmetrica con la angioplastica tradizionale che richiede invece occlusioni recenti, meglio se ricanalizzabili con la fibrinolisi. 6 La restenosi è un annoso problema della angioplastica trans-luminale, e dopo l’introduzione degli stent, forse è la unica problematica ancora non risolta. La ricerca ha battuto le strade più disparate: stent ricoperti da farmaci (anti-trombotici, anti-aggreganti, con azione anti-fibroblastica), stent contenenti materiali radioattivi betaemittenti, stent al carbonio, stent riassorbibili, etc.8,9,10 Ogni strada ha presentato i suoi vantaggi, le sue difficoltà, i suoi limiti. Per il momento l’unica soluzione praticabile è stata lo sviluppo di stent forniti di una piccola lama (cutting-balloon) e quindi capaci di “tagliare” la restenosi, ovvero la superficie fibrosa altrimenti resistente alla dilatazione.16 Anche questi presidi, apparentemente di semplice utilizzo, presentano le loro difficoltà ed i loro tranelli, ed hanno 28 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 quindi le loro specifiche indicazioni ed andranno utilizzati congiuntamente alle altre metodiche endovascolari. Altro curioso aspetto dell’angioplastica-stent nei pazienti critici è la constatazione che il risultato clinico è spesso migliore da quello morfologico. Ovvero l’ottenere quadri morfologici anche imperfetti si associa spesso ad una condizione clinica molto più favorevole.2 Fatto questo ancora più conclamato in caso di re-ostruzione, talora non seguita da un peggioramento clinico significativo o correlato con il peggioramento del quadro iconografico.2,18 Da ricordare, infine, come la comorbidità diabetica, per il coinvolgimento di territori vascolari molto periferici, e spesso in concomitanza con un interessamento cardiaco e renale, faccia di questi pazienti una popolazione ad alto rischio e di grande complessità terapeutica sotto molti punti di vista. Spesso questi pazienti arrivano ad uno stadio clinico particolarmente avanzato, eccezionale nei pazienti non diabetici. Questo accade anche a causa della frequente associazione con una neuropatia, che riducendo la percezione del dolore, porta questi pazienti a ritardare e rimandare l’aiuto del medico. Inoltre, la oggettiva complessità e perifericità delle lesioni (anche queste sconosciute a pazienti non diabetici) pone problematiche tecniche assolutamente proprie solo di questa malattia. Il trattamento di questi pazienti, quindi, costringe gli operatori ad utilizzare sino agli estremi le metodiche di rivascolarizzazione e le terapie mediche, sino ed oltre i loro limiti, ed forzando la loro utilizzazione combinata. I risultati clinici conseguiti sono spesso buoni, per quanto spesso solo, di breve o medio termine. BIBLIOGRAFIA 1. Melliere D. Influence of diabetes on revascularization of the aorta and lower limb arteries. Eur J Endovasc Surg 1999;17:438-41. 2. Faglia E, Mantero M, Caminiti M, et al. Extensive use of peripheral angioplasty in treatment of diabetic foot ulcers: clinical results of multicentric study of 221 consecutive diabetic subjects. J intern Med 2002; 252(3): 225-32. 3. Cynamon J, Marin ML, Veith F, et al. Stent graft repair of aorto-iliac occlusive disease coexisting with common femoral artery disease. J Vasc Interv radiol 1997;8:19-26. 4. Kansal NK, Handman A (in Veves A, Giurini JM, LoGerfo FW): The diabetic foot, HUMANA PRESS, New Jersey, 2002 5. Bosh Jl, Hunnink MGM. Methanalysis of the results of percutaneous transluminal angioplasty and primary stenting of aorto-iliac occlusive disease. Radiology, 1997;204:87-96. 6. Faglia E, Dalla Paola l, Clerici G et al. Peripheal angioplasty as first-choice revascularization procedure in diabetic patients with critical limb ischemia: prospective study of 993 consecutive patients hospitalized and followed between 1999 and 2003. Eur J Endovasc Surg 2005; 29(6):620-7. 7. Aburahma AF, Robinson PA, Cook CC, et al. Selecting patients for combined femoro-femoral by-pass grafting and iliac angioplasty and stenting for bilateral iliac disease. J vasc Surg 2001;33:s93-99. 8. Muller-Hussulbeck S, Oder BM, Jahnke T. Interventions in infrainguinal bypass grafts. Cardiovasc Intervent Radiol 2006;29:17-28. 9. Rand T, Basile A, Cejna M et al. PTA versus carbofilm-coated stents in infrapopliteal arteries : a pilot studies. Cardiovasc Intervent Radiol 2006;29:29-38. 10. Erne P, Schier M, Resnick TJ. The road to bioabsorbable stents: reaching clinical reality. Cardiovasc Intervent Radiol 2006;29:11-6 11. Bolia A, Bell PRF. Femoropopliteal and crural artery recanalization using sub-intimal angioplasty. Sem Vasc Surg 1995;8:253-64. 12. Ingle H, Nasim A, Bolia A, et al. Sub-intimal angioplasty of isolated infragenicular vesselsin lower limb ischemia: long term results. J Endov Surg 2002; 9(4):411-6. 13. Zeller T, Rastan A, Schwarwald A, et al: Midtem results after assisted angioplsty of below-knee arteries with use of siverhawk device. J Vasc Int Rad 2004, 15(12)1391-7. 14. Bosiers M, Hart JP, Deloose K, et al. Endovascular therapy as the primary approach for limb salvage in patients with critical limb ischemia: experience with 443 infrapopliteal procedures.Vascular. 2006;14(2):63-9. 15. Vorwerk D. Mechanical thrombechtomy is an alternative way to go. Cardiovasc Intervent Radiol 2006;29:7-10. 16. Engelke C, Engelke C, Sandhu C, et al. Using 6mm Cutting Balloon angioplasty in patients with resistant peripheral artery stenosis: preliminary results. AJR 2002; 179(3): 619-23. 17. Desgranges P,Bouffy M, Lapeyere M, et al. Subintimal angioplasty: feasible and durable. Eur J endovasc Surg, 2004;28(2):138-41. 18. Soder HK, Manninen HI, Rasanen HT, Kaukanen E, Jaakkola P, Matsi PJ. Failure of prolonged dilation to improve long-term patency of femoropopliteal artery angioplasty: results of a prospective trial. J Vasc Interv Radiol. 2002. ____ Per richiesta estratti: Dr. Maurizio Morucci U.O.C. Radiologia Vascolare e Interventistica Osped. S. Camillo, Roma - E-mail [email protected] ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 E) ANALISI DEI FATTORI CHE INFLUENZANO L’OUTCOME ANALYSIS OF THE FACTORS INFLUENCING ON OUTCOME ROBERTO BARTOLUCCI, FABRIZIO NESI U.O.C. di Chirurgia Vascolare - Dipartimento di Cardioscienze Azienda Ospedaliera San Camillo-Forlanini - Roma Parole chiave: Ischemia critica arti inferiori, Fattori influenzanti i risultati. Key words: Critical limb ischemia, Factors influencing, Outcome. Una maggiore comprensione dei fattori che possono limitare il successo del trattamento chirurgico del paziente affetto da ischemia critica degli arti inferiori (ICAI) comporterebbe necessariamente una migliore selezione dei pazienti ad alto rischio di fallimento dell’ impianto protesico e di perdita dell’arto od addirittura della vita. Nel 1954, Fontaine et al.1 elaborarono una classificazione clinica dei pazienti affetti da AOAI (arteriopatia obliterante arti inferiori), articolata in 4 stadi di gravità crescente, in cui gli stadi III e IV rappresentano rispettivamente quello dei pazienti con dolore a riposo senza lesioni cutanee, e quello dei soggetti con dolore a riposo associato a perdite di tessuto (ulcere o gangrena) a livello degli arti inferiori. In base a tale classificazione clinica i pazienti con ICAI possono essere considerati come appartenenti agli stadi III e IV.2 Tuttavia, si comprende facilmente che negli stadi III e IV di Fontaine può essere compresa un’ampia gamma di pazienti, con quadri clinici assai diversi con differenti prognosi, percentuali di rischio operatorio e possibilità di trattamenti terapeutici. Il termine “ischemia critica” fu coniato a Londra nel 1981 e da oltre venti anni a questa parte, diversi sono stati i tentativi di definire parametri di valutazione univoci ed oggettivi dei pazienti affetti da ICAI.2,3,4 Poiché si avverte sempre più la necessità di identificare e caratterizzare un gruppo di pazienti ad alto rischio di am- putazione d’arto, con valori pressori di perfusione molto bassi, è stato recentemente suggerito di assumere come parametri di riferimento la pressione arteriosa alla caviglia inferiore ai 50-70 mmHg e/o una ridotta pressione all’alluce inferiore a 30-50 mmHg e/o una riduzione della TCPO2 (pressione parziale transcutanea di O2) al di sotto di 30-50 mmHg. 5 È stato chiaramente dimostrato che anche i pazienti con un’età superiore ai 75 anni possono essere sottoposti ad interventi di rivascolarizzazione degli arti inferiori, con risultati, in termini di pervietà dei by-pass e percentuali di salvataggio d’arto, paragonabili a quelli ottenuti in pazienti di classe d’età più giovane.6,7 Alcuni Autori descrivono una percentuale di mortalità, dopo intervento per AOAI (arteriopatia obliterante arti inferioriI) o/e per ICAI (ischemia critica arti inferiori), significativamente più elevata nelle donne rispetto agli uomini (44.5% vs. 29.2%).8,9,10 I risultati di uno studio prospettico, multicentrico e randomizzato13 condotto in Italia su 1560 pazienti con ICAI ha evidenziato come la patologia coronarica rappresenti un importante fattore predittivo della mortalità, a sei e dodici mesi, nei soggetti sottoposti a rivascolarizzazione infrainguinale; allo stesso tempo, essa non condiziona, in maniera statisticamente significativa, i risultati della chirurgia ricostruttiva arteriosa. I pazienti con ICAI, con condizioni generali di salute peggiori ed una più estesa 30 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 patologia aterosclerotica, manifestano forme più avanzate di patologia coronarica e/o cerebrovascolare, associate frequentemente a disordini endocrinologici quali soprattutto il diabete.12,13 È stato dimostrato14 che i pazienti con AOAI sono ad elevato rischio di stroke nel postoperatorio, in particolare coloro che hanno già sofferto di ischemia cerebrale. Una storia clinica di stroke rappresenta un fattore predittivo indipendente della mortalità postoperatoria (2 anni).15 Il diabete è associato ad elevate percentuali di mortalità dopo intervento di rivascolarizzazione degli arti inferiori, così come affermato in alcuni studi, ma in contrasto con quanto riportato in altri.16,17 ll diabete tuttavia non modifica negativamente le percentuali di pervietà protesica; al contrario, alcuni studi riportano i migliori risultati proprio nel gruppo di pazienti affetti da tale disordine endocrino.18,19,20 In relazione all’osservazione di percentuali più alte di amputazione d’arto in soggetti diabetici, è necessario considerare che la causa di tali amputazioni non è riconducibile al fallimento delle protesi impiegate, quanto all’insorgere di importanti stati infettivi, difficilmente controllabili, che evolvono rapidamente verso la necrosi tissutale.21 Una corretta valutazione dell’estensione della lesione ischemica ed, eventualmente, del grado d’infezione a carico dell’arto sembra essere di fondamentale importanza.22 Sfortunatamente, nessun esame clinico o diagnostico sembra in grado di stimare adeguatamente l’entità dell’infezione a carico dei tessuti molli e, soprattutto, dell’interessamento delle strutture ossee ed articolari.23,24 La PCR (proteina C-reattiva) rappresenta un marker di infiammazione acuta e è inoltre riconosciuta come un indice di infiammazione cronica, coinvolta nello sviluppo delle lesioni aterosclerotiche e delle loro complicanze.25 É stato dimostrato che, nel postoperatorio, un aumento della concentrazione sierica della PCR al di sopra dei 50mg/l è predittivo dell’insorgenza di complicazioni in pazienti con ICAI sottoposti ad intervento chirurgico di rivascolarizzazione degli arti inferiori.26 I pazienti candidati a tale procedura chirurgica con livelli preoperatori di PCR uguali o superiori a 100 mg/l hanno un rischio aumentato di perdita d’arto ad un anno.27 Il fallimento dei tentativi di salvataggio d’arto, mediante il confezionamento di bypass distali, in soggetti con elevati livelli sierici di PCR sembra suggerire, così come evidenziato in pazienti con ischemia acuta degli arti inferiori,28,29 l’esistenza di una correlazione tra la PCR e l’entità delle lesioni proprie della ICAI.27 L’insufficienza renale cronica è associata ad un elevato rischio di sviluppo di lesioni aterosclerotiche.30 In particolare, il dismetabolismo del calcio e del fosforo viene ritenuto la causa di una rapida progressione delle lesioni aterosclerotiche con deposizione di calcio lungo le pareti vasali (calcifilassi).31 È stato inoltre suggerito che un aumento della concentrazione sierica di omocisteina, in pazienti uremici, costituisca un importante stimolo metabolico allo sviluppo di lesioni steno-occlusive delle arterie degli arti inferiori.30 In pazienti affetti da insufficienza renale cronica, con lesioni ischemiche e/o infette a carico degli arti inferiori, emerge la tendenza ad una difficoltosa riepitelizzazione ed ad una progressione dello stato infettivo; ciò costituisce la principale causa delle elevate percentuali di morbidità e perdita d’arto registrate in tali soggetti.31 Probabilmente, la ridotta presenza di tessuto di granulazione a livello delle lesioni ulcerate, asssociata ad una carenza di collagene in particolare in pazienti uremici e diabetici, può essere giustificata dalla coesistenza di ipoalbuminemia, malnutrizione, anemia ed eventualmente somministrazione di farmaci steroidei; inoltre, in soggetti uremici si assiste ad una depressione dell’immunità cellulomediata, con linfocitopenia e riduzione dell’attività fagocitica e chemiotattica.32 Tutti questi fattori, in pazienti con ICAI sottoposti a dialisi, spesso determinano il fallimento dei tentativi di salvataggio d’arto.33 R. Bartolucci et al.: Analisi dei fattori che influenzano l’outcome In effetti, se una strategia chirurgica aggressiva di rivascolarizzazione può determinare percentuali di pervietà protesica e salvataggio d’arto all’incirca del 90%,34,35 solamente pochi pazienti sopravvivono oltre il terzo anno di followup.36,37 È sempre più evidente che uno stato ipercoagulativo, spesso misconosciuto, può determinare una trombosi arteriosa od un’accelerazione della PAOP, che richiede il più delle volte un trattamento chirurgico.38,39,40,41 La deficienza di antitrombina III, proteina C ed S, l’iperomocisteinemia, la sindrome da anticorpi antifosfolipidi, rappresentano le principali cause di stati ipercoagulativi ereditari ed acquisiti coinvolti nella patogenesi di lesioni steno-occlusive arteriose e venose.5,40 La maggior parte di tali stati trombofilici costituisce inoltre un fattore predittivo indipendente del possibile fallimento di un impianto protesico di rivascolarizzazione arteriosa38,39,40 ed anche della mortalità postoperatoria39. Diversi studi42,43 hanno evidenziato che l’esperienza del chirurgo riveste un ruolo chiave ai fini dell’ottenimento di buoni risultati nella chirurgia mirata al salvataggio d’arto. Una limitata esperienza nell’utilizzo delle tecniche chirurgiche e soprattutto una scarsa dimestichezza con gli algoritmi decisionali propri del trattamento dei pazienti con ICAI possono essere responsabili del conseguimento di scarsi risultati, in termini di percentuali di pervietà protesica e salvataggio d’arto. In correlazione con quanto affermato, è stato dimostrato che anche le dimensioni ed i carichi di lavoro della struttura ospedaliera di riferimento possono influenzare le percentuali di amputazione d’arto, suggerendo quindi che una centralizzazione dei servizi specialistici di chirurgia vascolare può ottimizzare i risultati conseguiti dopo il trattamento chirurgico dei pazienti affetti da ICAI. BIBLIOGRAFIA 1. Fontaine R, Kim M, Kieny R. Die chirurgische Behandlung der peripheren Durch-blutungsstö- 31 rungen. Helvetia Chirurgica Acta 1954; 5/6: 199-533. 2. Second European Consensus Document. Eur J Vasc Surg 1992; 6(Suppl A): 1-32. 3. Bell PRF, Charlesworth D, DePalma RG et al.. The definition of critical ischaemia of a limb. Br J Surg 1982; 69: 22. 4. Suggested standards for reports dealing with lower extremity ischemia. Prepared by the Ad hoc Committee on Reporting Standards, Society for Vascular Surgery/North American Chapter, International Society for Cardiovascular Surgery. J Vasc Surg 1986; 4: 80-94. 5. TASC Working Group. Management of peripheral arterial disease (PAD). TransAtlantic InterSociety Consensus (TASC). Eur J Vasc Endovasc Surg 2000; 19(Suppl A): 1-250. 6. Luther M, Lepäntalo M. Femorotibial reconstructions for chronic critical leg ischaemia: influence on outcome by diabetes, gender and age. Eur J Vasc Endovasc Surg 1997; 13: 569-77. 7. Luther M, Lepäntalo M. Arterial reconstruction to the foot arteries - a viable option? Eur J Surg 1997; 163: 659-65. 8. Cavillon A, Melliere D, Allaire E et al.. Are femoro-infrapopliteal bypasses worthwhile for limb salvage? J Cardiovasc Surg 1998; 39: 26772. 9. The I.C.A.I. Group. Long-term mortality and its predictors in patients with critical leg ischaemia. Eur J Vasc Endovasc Surg 1997; 14: 91-5. 10. Belkin M, Conte MS, Donaldson MC, Mannick JA, Whittemore AD. The impact of gender on the results of arterial bypass with in situ greater saphenous vein. Am J Surg 1995; 170: 97102. 11. Harris EJ, Taylor LM, Moneta GL, Porter JM. Outcome of infrainguinal arterial reconstruction in women. J Vasc Surg 1993; 18: 627-36. 12. Hultgren R, Olofsson P, Wahlberg E. Gender differences in vascular interventions for lower limb ischaemia. Eur J Vasc Endovasc Surg 2001; 21: 22-7. 13. Bertelè V, Roncaglioni MC, Pangrazzi J, Terzian E, Tognoni G on behalf of the “i.c.a.i.” (CLI) Group. Clinical Outcome and its predictors in 1560 patients with critical leg ischaemia. Eur J Vasc Endovasc Surg 1999; 18: 401-10. 14. L’Italien GJ, Cambria RP, Cutler BS et al.. Comparative early and late cardiac morbidity among patients requiring different vascular surgery procedures. J Vasc Surg 1995; 21: 935-44. 15. Krupski WC, Layug EL, Reilly LM, Rapp JH, Mangano DT and the Study of Perioperative Ischemia Research Group. Comparison of cardiac morbidity rates between aortic and infrainguinal operations: two-year follow-up. J Vasc Surg 1993; 18: 609-17. 16. Limburg M, Wijdicks EFM, Li H. Ischemic stroke after surgical procedures. Clinical features, neuroimaging and risk factors. Neurology 1998; 50: 895-901. 17. The I.C.A.I. Group. A prospective epidemiological survey of the natural history of chronic leg 32 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 ischaemia. Eur J Vasc Endovasc Surg 1996; 11: 112-20. 18. Tyrrell MR, Wolfe JHN, Joint Vascular Research Group. Critical leg ischaemia: an appraisal of clinical definitions. Br J Surg 1993; 80: 177-80. 19 Jeans WD, Cole SE, Horrocks M, Baird RN. Angioplasty gives good results in critical lower limb ischaemia. A 5-year follow-up in patients with known ankle pressure and diabetic status having femoropopliteal dilations. Br J Radiol 1994; 67: 123-8. 20. Gloviczki P, Bower TC, Toomey BJ et al.. Microscope-aided pedal bypasses is an effective and low-risk operation to salvage the ischemic foot. Am J Surg 1994; 168: 76-84. 21. Plecha EJ, Lee C, Hye RJ. Factors influencing the outcome of paramalleolar bypass grafts. Ann Vasc Surg 1996; 10: 356-60. 22. Taylor LM Jr., Edwards JM, Porter JM. Present status of reversed vein bypass grafting: fiveyear results of a modern series. J Vasc Surg 1990; 11: 193-206.. 23. Dietzek AM, Gupta SK, Kram HB, Wengerter KR, Veith FJ. Limb loss with patent infra-inguinal bypasses. Eur J Vasc Surg 1990; 4: 413-7. 24. Carsten CG , Taylor SM, Langan EM III, Crane MM. Factors associated with limb loss despite a patent infrainguinal bypass graft. Am Surg 1998; 64: 33-8. 25. Craig JG, Amin MB, Eyler WR, van Holsbeeck MT, Bouffard JA, Shirazi K. Osteomyelitis of the diabetic foot: MR imaging-pathologic correlation. Radiology 1997; 203: 849-55. 26. Laing P. The development of complications of diabetic foot ulcers. Am J Surg 1998; 176(Suppl.2A): 11S-19S. 27. Tracy RP. Inflammation in cardiovascular disease. Cart, horse, or both? Circulation 1998; 97: 2000-2. 28. Majewski W, Zieliñski A, Laciak M, S et al.. Creactive protein and a-1acid glycoprotein in monitoring of patients with chronic arterial occlusion of the lower limbs. Eur J Vasc Surg 1993; 7: 628-32. 29. Biancari F, Albäck A, Kantonen I, Luther M, Lepäntalo. Predictive factors for adverse outcome of pedal bypasses. Eur J Vasc Endovasc Surg 1999; 18: 138-43. 30. Kuukasjärvi P, Salenius JP, Riekkinen H. Prognostic value of preoperative C-reactive protein concentration and white cell count in acute extremity ischaemia. Eur J Surg 1995; 161: 335-39. 31. Ruiz P, Gomez F, Schreiber AD. Impaired func- tion of macrophage Fcg-receptors in end-stage renal failure. N Engl J Med 1990; 322: 717-22. 32. Reifsneyder T, Grossman JP, Leers SA. Limb loss after lower extremity bypass. Am J Surg 1997; 174: 149-51. 33. Chauveau P, Chadelfaux B, Coude M. Hyperhomocysteinemia, a risk factor for atherosclerosis in chronic uremic patients. Kidney Int 1993; 43(Suppl.41): 72-7. 34. Ascer E, Veith F, White Flores SA. Infrapopliteal bypasses to heavily calcified rock-like arteries: management and results. Am J Surg 1986; 152: 220-3. 35. Simsir SA, Cabellon A, Kohlman-Trigoboff D, Smith BM. Factors influencing limb salvage and survival after amputation and revascularization in patients with end-stage renal disease. Am J Surg 1995; 170: 113-17. 36 Chang BB, Paty PSK, Shah DM, Kaufman JL, Leather RP. Result of infrainguinal bypass for limb salvage in patients with end.stage renal disease. Surgery 1990; 108: 742-7. 37. Harrington EB, Harrington ME, Schanzer H, haimov M. End-stage renal disease. Is infrainguinal limb revascularization justified? J Vasc Surg 1990; 12: 691-96. 38. Hakaim AG, Gordon JK, Scott TE. Early outcome of in situ femorotibial reconstruction among patients with diabetes alone versus diabetes and end-stage renal failure: analysis of 83 limbs. J Vasc Surg 1998; 27: 1049-55. 39. Peltonen S, Biancari F, Lindgren L, Mäkisalo H, Honkanen E, Lepäntalo M. Outcome of infrainguinal bypass surgery for critical leg ischaemia in patients with chronic renal failure. Eur J Vasc Endovasc Surg 1998; 15: 122-7. 40. Donaldson MC. Hypercoagulable states in patients with peripheral vascular disease. In: Whittemore AD, Bandyk DF, Cronenwett JL, Hertzer NR, White RA. Advances in vascular surgery, St. Louis, Mosby-Year Book, 1993; 22742. 41. Girolami A, Simioni P, Scarano L, Girolami B. Venous and arterial thrombophilia. Haematologica 1997; 82: 96-100. 42. Harris PL, da Silva AF, Holdsworth J, McCollum P, Jones SM. Critical limb ischaemia: management and outcome. Report of a national survey. Eur J Vasc Endovasc Surg 1995; 10: 108-13. 43. Luther M, Lepäntalo M. Infrainguinal reconstructions: influence of surgical experience on outcome. Cardiovasc Surg 1998; 6: 351-7. ____ Per richiesta estratti: Dr. Roberto Bartolucci U.O.C. di Chirurgia Vascolare Ospedale San Camillo, Roma Tel: 06 58704535, e-mail: [email protected] ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 F) L’ISCHEMIA CRITICA NELLE LESIONI AORTO-ILIACHE CRITICAL LIMB ISCHEMIA IN PATIENTS WITH AORTO-ILIAC DISEASE FRANCESCO SPEZIALE, MASSIMO RUGGIERO, ARMANDO PALMIERI, DANILO MENNA Scuola di Specializzazione in Chirurgia Vascolare II Università degli Studi La Sapienza - Roma Parole chiave: Ischemia critica degli arti inferiori, Rivascolarizzazione degli arti inferiori. Key words: Critical limb ischemia, Lower extremity revascularization. L’arteriopatia ostruttiva nel segmento aorto-iliaco spesso coesiste con lesioni anche al di sotto del legamento inguinale. Nonostante la natura diffusa della malattia arteriosclerotica questa situazione si presenta di solito con una distribuzione segmentaria delle lesioni, potendo essere suscettibile di un trattamento chirurgico risolutivo. Nei pazienti che presentano lesioni diffuse, a carico del distretto aorto-iliaco e femoro-popliteo la sola correzione delle lesioni prossimali (inflow) dà spesso un miglioramento clinico soddisfacente per quel che riguarda i sintomi ischemici. È di fondamentale importanza, quindi, valutare correttamente l’adeguatezza dell’inflow arterioso. Dall’inizio degli anni ’50, con l’introduzione nella pratica chirurgica dei primi metodi di rivascolarizzazione come la tromboendoarterectomia e, successivamente, la sostituzione protesica omologa, sono stati fatti grandi progressi nel trattamento chirurgico delle arteriopatie periferiche. La ricerca scientifica dei materiali protesici, delle tecniche chirurgiche e del trattamento perioperatorio ha contribuito a migliorare notevolmente i risultati riducendo le complicanze sia in termini di morbilità che di mortalità. Le indicazioni al tipo di intervento al quale sottoporre il paziente sono oggi standardizzate, con la possibilità di effettuare gli approcci chirurgici e le rivascolarizzazioni in maniera diversa a seconda delle varie situazioni. Pertanto, valutando correttamente il rischio del paziente ed eseguendo un’appropriata tecnica chirurgica si può ottenere un buon esito dell’intervento di rivascolarizzazione con un limitatissimo stress per il paziente. La sintomatologia e la storia naturale della malattia aterosclerotica aorto-iliaca e femoro-poplitea è influenzata in modo significativo sia dalla distribuzione delle lesioni, che dalla loro estensione. Classicamente la si può suddividere in tre tipi a seconda delle localizzazioni delle lesioni ateromasiche. Il tipo 1 (5-10%) presenta lesioni ostruttive limitate alla parte distale dell’aorta addominale ed all’origine delle arterie iliache comuni. Raramente si manifesta con una sintomatologia ischemica grave. Il tipo 2 (25%) presenta lesioni più diffuse ma limitate alla regione addominale. Il tipo 3 (65%), invece, presenta una localizzazione molto estesa sia sopra che sotto il legamento inguinale. I pazienti portatori di quest’ultimo tipo con estese lesioni plurisegmentarie sono più anziani, maschi con un rapporto di 6/1, diabetici ed ipertesi. Hanno, inoltre, un interessamento aterosclerotico multidistrettuale (arterie cerebrali, coronarie e viscerali). Si tratta di pazienti che presentano una sintomatologia ischemica a carico degli arti inferiori più grave, con dolore a riposo o con presenza di lesioni tissutali. In questi pazienti l’intervento viene effettuato per il salvataggio d’arto. Si tratta, pertanto, di pazienti con una spettanza di vita minore rispetto a quelli con lesioni localizzate aorto-iliache. I metodi di rivascolarizzazione aorto-iliaca diretta sono quelli che 34 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 presentano una pervietà a distanza maggiore. La tecnica più utilizzata è il bypass aorto-femorale (mono o bi) anche se, in un certo numero di casi, può essere eseguita un’endoarterectomia aorto-iliaca. Gli interventi di rivascolarizzazione extra-anatomica in genere vengono riservati ad un gruppo di pazienti ad alto rischio che non possono essere sottoposti ad una rivascolarizzazione convenzionale. La scelta dell’intervento più idoneo si basa sulle condizioni generali del paziente, sull’estensione della malattia aterosclerotica e sull’esperienza del chirurgo. L’endoarterectomia aorto-iliaca può essere effettuata in un numero cospicuo di pazienti con un’estensione delle lesioni esclusivamente aortoiliaca (tipo 1). Offre dei vantaggi in quanto non viene adoperato materiale sintetico, per cui l’eventualità d’infezione è praticamente inesistente, ma per essere effettuata necessita di una accurata selezione delle lesioni. Dalla fine degli anni ’60 è stato introdotto il bypass che viene utilizzato nella quasi totalità dei pazienti che necessitano di rivascolarizzazione aortofemorale. Questa procedura è ormai ben standardizzata nella sua esecuzione. Per quanto riguarda l’anastomosi prossimale (termino-terminale o termino-laterale), più che il tipo di anastomosi, è di fondamentale importanza il principio di effettuarla il più possibile in vicinanza delle arterie renali perchè questa zona è in genere risparmiata dal processo aterosclerotico. È indispensabile assicurarsi che vi sia un’adeguato outflow prima di effettuare l’anastomosi femorale specialmente nei casi in cui l’arteria femorale profonda presenti una stenosi o l’arteria femorale superficiale risulti ostruita. In questi casi si può effettuare, prima dell’anastomosi, una plastica della femorale profonda con eventuale patch di allargamento. La problematica che ci riguarda più da vicino è quella di valutare se nei pazienti con arteriopatia plurisegmentaria diffusa di tipo 3, con ischemia critica o lesioni trofiche, possa essere sufficiente il solo tratta- mento della lesione aorto-iliaca. Le prime esperienze pubblicate che si riferivano a pazienti con questo tipo di arteriopatia, trattati con rivascolarizzazione aorto-femorale, facevano vedere come nella quasi totalità dei casi la sintomatologia si risolveva solo con la rivascolarizzazione prossimale. Rimane comunque una certa quota di pazienti, anche se di difficile identificazione, che necessitano di una rivascolarizzazione distale combinata. A questo proposito un nostro studio effettuato su 91 pazienti portatori di una arteriopatia aorto-iliaca e femoro-poplitea, operati nel nostro Istituto tra il 1977 ed il 1979, metteva in evidenza come solo in 4 (4%) pazienti fosse stato necessario effettuare un intervento combinato di rivascolarizzazione femoro-poplitea per assicurare una sufficiente irrorazione distale. È quindi necessaria un’accurata valutazione del paziente in funzione del tipo di trattamento da eseguire, considerando che con un’appropriata tecnica chirurgica eseguita correttamente si può prevedere un esito favorevole con un rischio limitato per il paziente, soprattutto in termini di mortalità e morbilità. BIBLIOGRAFIA ESSENZIALE Atti I Congresso Nazionale della Società Italiana di Patologia Vascolare, 1979, Roma. Brewster DC, Darling RC: Optimal methods of aortoiliac reconstruction. Surgery. 1978 Dec; 84(6): 739-48. Crawford ES, Bomberger RA et al: Aortoiliac occlusive disease: factors influencing survival and function following reconstructive operation over a twenty-five-year period. Surgery. 1981 Dec;90(6) 1055-67. Darling RC: Aortoiliofemoral endarterctomy for atherosclerotic occlusive disease. Surgery. 1964 Jan;55: 184-94. Darling RC, Brewster DC et al: Aorto-iliac reconstruction. Surg Clin North Am. 1979 Aug;59(4): 565-79. Malone JM, Moore WS et al: Life expectancy following aortofemoral arterial grafting. Surgery. 1977 May;81(5): 551-5. Moore WS, Cafferata HT et al: In difense of grafts across the inguinal ligament. An evaluation of early and late results of aorto-femoral bypass grafts. Ann Surg. 1968 Aug;168(2): 207-14. ____ Per richiesta estratti: Prof. Francesco Speziale - Chirurgia Vascolare II Università La Sapienza - Viale Policlinico - Roma 00185 ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 G) LE PROCEDURE “IBRIDE” DI RIVASCOLARIZZAZIONE HYBRID REVASCULARIZATION PROCEDURES GIOVANNI BERTOLETTI, MARCO MASSUCCI, ALESSANDRO VARRONI, VINCENZO GENOVESE, HADI ABI RACHED, GIULIA IANNI, FILIPPO NAPOLI, GIACINTO MARTINELLI, LAURA CAPOCCIA, ERMANNO NOTARIANNI1, ROBERTO CIANNI1 U.O.C. di Chirurgia Vascolare U.O.C. di Radiologia Vascolare - Ospedale S. Maria Goretti - Latina 1 Parole chiave: Ischemia critica degli arti inferiori, Rivascolarizzazioni ibride. Key words: Critical limb ischemia, Hybrid revascularizations. INTRODUZIONE L’aterosclerosi è spesso caratterizzata dal contemporaneo interessamento di distretti arteriosi diversi e talvolta a carattere sequenziale. L’ischemia critica in particolare comporta un interessamento sia del distretto aorto-iliaco che di quello femoro-popliteotibiale. La diffusione della chirurgia endovascolare ha comportato la modifica alle indicazioni di trattamento delle lesioni combinate.1,2,3 L’approccio ibrido, endo-vascolare e chirurgico, consente il trattamento di lesioni a più livelli nello stesso tempo o in maniera sequenziale, limita il numero delle vie di accesso da realizzare,permette il risparmio di tempo, mantiene inalterata l’efficacia dell’intera procedura.4 Tale approccio consente la ricanalizzazione di segmenti arteriosi a monte o a valle dell’impianto protesico migliorandone la pervietà.5,6,7 È importante identificare il timing chirurgico in caso di lesioni associate aortoiliache e femoro-poplitee e valutare quali siano le metodiche di trattamento convenzionale o endovascolare più appropiate in questi pazienti. MATERIALI E METODI Tra Dicembre 2002 e Maggio 2005 abbiamo eseguito presso l’Unità Operativa di Chirurgia Vascolare dell’Ospedale Civile S. Maria Goretti di Latina 393 rivascolarizzazioni degli arti inferiori (IIb, III e IV stadio). Di queste 38 (9.6 %) con procedura ibrida. I dati relativi a questa popolazione di pazienti sono riportati nella Tabella 1.L’indicazione all’intervento è stata l’ischemia critica in 32 casi (84,2 %) e una claudicatio invalidante in 6 casi (15,8 %) .Tutti i pazienti sono stati studiati con ecocolordoppler ed angiografia. Nella tabella II sono riportate il tipo e la sede anatomica delle lesioni. Tutti i pazienti hanno ricevuto una anestesia periferica. Il follow-up a 1,3,6,12 mesi è stato clinico e morfologico (ecodoppler e misurazione dell’indice di Windsor). RISULTATI La mortalità peri-operatoria è stata pari a 0. Nel follow-up 2 pazienti sono deceduti per IMA a distanza di 6 e 8 mesi rispettivamente. Un ematoma localizzato in 2 casi e la deiscenza di una ferita inguinale costituiscono il gruppo delle complicanze minori. Il miglioramento dell’inflow è stato ottenuto con metodica chirurgica in 8 pazienti (21,1%) e endovascolare nei rimanenti 30 (78,9 %). Sono stati eseguiti 4 by-pass iliaco-femorali, 10 Tea (tromboendoarteriectomia) + patch d’ampliamento della biforcazione femorale e 21 rivascolarizzazioni periferiche mediante by-pass. In 3 pazienti è sta- 36 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 to confezionato un by-pass femoro-femorale associato a PTA dell’iliaca donatrice. Come procedure endovascolari sono state eseguite 30 PTA (angioplastica percutanea) stent dell’ iliaca, 5 PTA dell’ AFS (arteria femorale superficiale) di cui 3 con stent e 3 PTA delle arterie tibiali. Le tabelle 4, 5 e 6 riassumono i dati sopra elencati. Il follow-up medio è stato di 6 mesi (min 6, max 18). A livello iliaco si è verificata la trombosi di 2 stent (2/30= 6.6%) nel follow-up con pervietà della Tea femorale associata. A livello della AFS si è avuta la trombosi di 2 PTA con stent (Haemobhan) (2/3=66%) nel primo mese con un quadro di grave ischemia e confezionamento di due by-pass femoro-poplitei in VSAI (vena safena autologa invertita). Si è verificata la trombosi precoce di 2 by-pass femoro-poplitei trattati con successo mediante trombectomia. In 2 casi il deterioramento del run-off nel follow up ha comportato il fallimento delle procedure di rivascolarizzazione con esito in amputazioni maggiori. La pervietà primaria delle procedure combinate è stata del 78 %, la pervietà secondaria dell’ 84%. DISCUSSIONE La diffusione delle metodiche endovascolari ha permesso l’utilizzo di un approccio combinato, endovascolare e chirurgico, a estese e complesse lesioni ostruttive aorto-iliache e femoro-poplitee. L’associazione di lesione aorto-iliaca e femoro-poplitea viene riportata frequentemente in letteratura con una incidenza che arriva fino al 70%.8 Naturalmente non tutti i pazienti necessitano di una correzione simultanea ai due livelli ed è quindi necessaria una selezione accurata dei pazienti. Il ruolo delle singole metodiche nelle lesioni aortoiliache resta controverso in quanto sia il trattamento endovascolare che chirurgico presentano indicazioni e controindicazioni che sono in relazione al singolo caso,9 alle sue condizioni generali, allo stato anatomico delle lesioni quali l’estensione o la presenza di calcificazioni. Il trattamento migliore deve essere quindi individualizzato e il successo dipende dall’appropiatezza delle metodiche di indagine e dalla selezione delle lesioni trattabili.10 A sostegno di questo approccio vanno i numerosi report pubblicati negli ultimi anni.1-7 Il by pass aorto-femorale è stato a lungo considerato come la procedura di scelta per ottenere un in-flow ottimale11,12,13 nei pazienti con ischemia critica degli arti inferiori. La mortalità e morbidità associata a questo tipo di trattamento ne restringe tuttavia l’indicazione ai pazienti a basso rischio chirurgico. Nel corso degli ultimi anni hanno trovato larga diffusione le metodiche endovascolari. La PTA isolata non è spesso sufficiente per ristabilire un adeguato in-flow a causa delle complicanze legate alla procedura (dissezione, embolizzazionre o recoil della lesione stessa). L’uso dello stent ha comportato un profondo cambiamento nell’ approccio alle lesioni iliache. Un recente studio retrospettivo su 288 pazienti ha mostrato una pervietà a due anni del 84%,14 e una metanalisi di Bosch sull’utilizzo dello stent nelle lesioni aortoiliache mostra un miglioramento della pervietà primaria e secondaria riducendone i fallimenti tardivi del 39%.15 Brewster nell’89 ha riportato una pervietà a 5 anni del 76% combinando una PTA femorale ad una ricostruzione distale infrainguinale.4 Nelson ha utilizzato questo approccio verso lesioni con morfologia tipo C della classificazione TASC,16 eseguendo una PTA + stent dell’arteria iliaca esterna e una Tea della femorale comune. I risultati evidenziano un miglioramento clinico nel 97% dei pazienti e una pervietà primaria ad un anno dell’84%.10 A fronte di questi risultati promettenti con l’ approccio combinato , un recente lavoro di Timaran evidenzia come la ricostruzione vascolare infrainguinale non migliori la pervietà dello stent iliaco in pazienti in cui le lesioni iliache sono associate a un run-off scarso.17 37 G. Bertoletti et al.: Le procedure “ibride” di rivascolarizzazione Le lesioni aterosclerotiche a più livelli e bilaterali possono essere trattate con una PTA + stenting iliaco associata a bypass femoro-femorale cross-over. Questo tipo di trattamento trova la sua indicazione in pazienti definiti ad alto rischio e con addome ostile. La pervietà primaria per questo tipo di approccio è stata del 96% ad un anno e dell’85% a 2 e 3 anni per lesioni classificate come tipo B, mentre per lesioni di tipo C la pervietà è stata rispettivamente del 46%, 46% e 31% ad 1, 2 e 3 anni. Gli autori ritengono che la PTA percutanea + stenting associato con il by-pass femoro-femorale sia una procedura fattibile e con risultati duraturi se la stenosi dell’asse iliaco donatore è inferiore ai 5 cm (lesione tipo B), mentre nella lesioni di tipo C l’associazione del by-pass non trova utilità. Tale approccio è stato utilizzato in tre casi. Dall’analisi della nostra esperienza il timing tra procedura classica ed endovascolare è influenzato dalla necessità di ottenere come primo atto un adeguato inflow: la correzione primaria di lesioni prossimali è successivamente seguita dalla procedura in grado di ottenere un migliore run-off. Per le lesioni iliache la PTA con stent è stata la metodica utilizzata nel 78% dei casi. La percentuale di complicanze delle procedure endovascolari è stata del 10,5%: due pazienti hanno richiesto la conversione chirurgica in urgenza (trombosi della AFS su Hemobahn), i by-pass realizzati hanno evitato interventi demolitivi. Quattro (4) rivascolarizzazioni chirurgiche sono andate incontro ad occlusione, 2 amputazioni dell’arto inferiore sono state in seguito eseguite in questo gruppo di pazienti con letto vascolare distale deteriorato. Nel loro complesso i dati presentati sono incoraggianti: infatti la pervietà complessiva della metodica ibrida è sovrapponibile alle percentuali di pervietà delle singole metodiche utilizzate nel trattamento di lesioni isolate iliache e femoro-poplitee, come viene riportato in letteratura.12 CONCLUSIONI Il migliore trattamento per lesioni complesse arteriose che interessano più livelli è tuttora oggetto di discussione. Tuttavia, selezionando i pazienti in base alle caratteristiche anatomiche delle lesioni e al quadro clinico, è possibile ottenere il miglior risultato combinando il trattamento tradizionale e quello endovascolare. Tabella 1. - Dati demografici e fattori di rischio Maschi Femmine Età media Cardiopatia ischemica Diabete Ipertensione IRC Fumo 34 (89%) 4 (11%) 72+5,8 27 (71%) 18 (47,3%) 29 (76,6%) 12 (31,5%) 24 (63,3%) Tabella 2. - Indicazione all’intervento chirurgico Ischemia critica Claudicatio invalidante Totale 32 (84,2 %) 6 (15,8 %) 38 Tabella 3. - Sede delle lesioni e caratteristiche anatomiche Iliaca comune Iliaca esterna Femorale comune Femorale profonda Femorale superficiale Popliteo-distale N° 29 8 6 4 19 10 stenosi 22 (75,8 %) 5 (62,5 %) 4 (66,6 %) 4 (100 %) 2 (10,5 %) 7 (70 %) occlusione 7 (24,2 %) 3 (37,5 %) 2 (33,4 %) 17 (89,5 %) 3 (30 %) Tabella 4. - Tipo di intervento chirurgico eseguito By-pass iliaco-femorale By-pass fem-fem Tea femorale By-pass fem-pop-distale Totale 4 (10.5 %) 3 (7.9 %) 10 (26,3 %) 21 (55,3 %) 38 38 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 Tabella 5. - Tipo di intervento endovascolare eseguito PTA e stent iliaco PTA fem. Sup. PTA fem. Sup. e stent PTA vasi infrapoplitei Totale 30 (78,9 %) 2 (5,3 %) 3 (7,9 %) 3 (7,9 %) 38 Tabella 6. - Tipo di trattamento in base alla lesione Iliaca comune Iliaca esterna Femorale comune Femorale profonda Femorale superficiale Popliteo distale N° Trattamento chirurgico 29 4 (13,8%) 8 3 (37,5%) 6 6 4 4 19 14 (73,6%) 10 7 (70%) Trattamento endovascolare 25 (86,2%) 5 (62,5%) / / 5 (26,4%) 3 (30%) P< 0.001 P= NS P<0,001 P<0,001 BIBLIOGRAFIA 1. Ricco JB, Camiade C, Mangiacotti N, Bertrand E, Branchereau A. Transluminal iliac angioplasty with distal by-pass surgery in patients with surgical reconstruction for lower limb ischemia. European Vascular Course 1999; 119-34. 2. Bull PG, Schlegl A, Mendel H. Combined iliac transluminal angioplasty and femoro-popliteal reconstruction for multilevel occlusive disease. Int Surg 1993; 78:332-7. 3. Cynamon J Marin ML, Veith F, et al. Stent graft repair of aorto-iliac occlusive disease coexisting with common femoral artery disease. J Vasc Interv Radiol 1997; 8:19-26. 4. Brewster DC, Cambria RP, Darling RC, et al. Long-term results of combined iliac balloon angioplasty and distal surgical revascularization. Ann Surg 1989;210:324-31 5. Aburahma AF, Robinson PA, Cook CC, Hopkins ES. Selecting patients for combined femorofemoral bypass grafting and iliac balloon angioplasty and stenting for bilateral iliac disease. J Vasc Surg 2001;33:S93-9. 6. Faries PL, Brophy D, LoGerfo FW et al. Combined iliac angioplasty and infrainguinal revascu- larization surgery are effective in diabetic patients with multilevel arterial disease. Ann Vasc Surg 2001;15:67-72. 7. Perler BA, Williams GM. Does donor iliac artery percutaneous transluminal angioplasty or stent placement influence the results of femorofemoral bypass? Analysis of 70 consecutive cases with long-term follow-up. J Vasc Surg 1996;24:363-70. 8. Moneta GL, Yeager RA, Taylor L, Porter JM. Hemodinamic assessment of combined aortoiliac/femoro-popliteal occlusive disease and selection of single or multilevel revascularization. Semin Vasc Surg 1994; 7:3-10. 9. Lorenzi G, Domanin M, Costantini A, Rolli A, Agrifoglio G. Role of bypass, endarterectomy, extra-anatomic bypass and endovascular surgery in unilateral iliac occlusive disease: a review of 1257 cases. Cardiovasc Surg 1994;2:370-3. 10. Nelson PR, Powell R, Schermerhorn ML, et al. Early results of external iliac artery stenting combined with common femoral artery endarterectomy. J Vasc Surg 2002;35:1107-13. 11. Brewster DC; Perler BA, Robinson JG, Darling RC. Aortofemoral graft for multilevel occlusive disease. Predictors of success and need for distal by-pass. Arch Surg 1982; 117: 1593-600. 12. Marin ML, Veith FJ, Sanchez LA, Cynamon J, Suggs WD, Schwartz ML: Endovascular aortoiliac grafts in combination with standard infrainguinal arterial by-pass in the management of limb-threatening ischemia: preliminary report. J Vasc Surg 1995; 22:316-24. 13. Harris PL, Bigley DJ. Aortofemoral bypass and the role of concomitant femoro-distal reconstruction. Br J Surg 1985; 72:317-20. 14. Sullivan TM, Childs MB, Bacharach JM. Percutaneous transluminal angioplasty and primary stenting of the iliac artery in 288 patients. J Vasc Surg 1997; 25: 829-39. 15. Bosch JL, HunninkMGM. Metanalysis of the results of percutaneus transluminal angioplasty and stent placement for aorto-iliac occlusive disease. Radiology 1997; 204:87-96. 16. TransAtlantic Inter-Society Consensus Working Group. Management of peripheral arterial occlusive disease: TASC document. J Vasc Surg 2000; 31 (1Pt 2): 1-296. 17. Timaran CH, Takao O, Gargiulo NJ. Iliac artery stenting in patients with poor distal run-off: influence of concomitant infrainguinal arterial reconstructions. J Vasc Surg 2003; 38:479-85. ____ Per richiesta estratti: Dr. Giovanni Bertoletti Direttore U.O.C. di Chirurgia Vascolare Ospedale S. Maria Goretti Via Guido Reni - 04100 Latina ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 H) IL CHIRURGO VASCOLARE E L’ISCHEMIA CRITICA: LE OPZIONI ENDOVASCOLARI THE VASCULAR SURGEON AND CRITICAL LOWER LIMB ISCHEMIA: THE ENDOVASCULAR OPTIONS SONIA RONCHEY, EUGENIA SERRAO, PIERLUIGI COSTA, CARLO CAVAZZIN, CELESTE IOVINO, NICOLA MANGIALARDI U.O.C. Chirurgia Vascolare – Ospedale San Filippo Neri - Roma Parole chiave: Chirurgia endovascolare, Ischemia critica degli arti inferiori. Key words: Endovascular surgery, Critical limb ischemia. L’ ischemia critica rappresenta una vera e propria sfida per il chirurgo vascolare: il paziente giunge all’osservazione in condizioni gravi, di urgenza terapeutica; è necessario nella gran parte dei casi un approccio multidisciplinare a causa dell’elevata incidenza di comorbidità, per il controllo del dolore ed il trattamento di eventuali infezioni La scelta terapeutica dipende dal bilancio di diversi fattori, primo fra tutti la sede delle lesioni quasi sempre multiple; in secondo luogo bisogna valutare la presenza di procedure pregresse che possono modo ostacolare il successivo trattamento, ma soprattutto il rischio operatorio che è sempre elevato, trattandosi di pazienti con una sopravvivenza del 50% circa fra i 3 ed i 5 anni dalla diagnosi.1-4 MATERIALE E METODO Riportiamo la nostra esperienza relativa a 59 pazienti con ischemia critica trattati inizialmente con successo in modo endovascolare. Tutti i pazienti sono stati valutati con eco-doppler preoperatorio, l’angiografia è stata eseguita intraoperatoriamente al momento della procedura endovascolare. In 20 casi erano presenti importanti lesioni aorto-iliache associate ad ostruzione o stenosi dei vasi a valle. In 39 casi le lesioni arteriose erano localizzate a livello femoro-popliteo e distale; nella gran parte dei pazienti erano pre- senti lesioni associate: 12 pazienti presentavano lesioni della femorale superficiale associate a lesioni delle arterie di gamba; 18 lesioni associate della femorale superficiale e della poplitea; 8 occlusioni complete della poplitea in 3 casi associate a lesioni delle arterie di gamba ed 1 paziente, dializzato, stenosi serrata della poplitea sottoarticolare e lesioni di tutte le arterie di gamba. Il trattamento medico è consistito in una eparinizzazione intraoperatoria e nei primi giorni succesivi all’intervento ed in una doppia antiaggregazione per il primo mese dopo la rivascolarizzazione (ASA+clopidogrel/ticlopidina), quindi in antiaggregazione semplice. I pazienti sono stati controllati intraoperatoriamente con angiografia ed ecodoppler e quindi con eco-doppler ad 1,3,6 e 12 mesi dall’intervento. I successivi controlli sono stati stabiliti sulla base della clinica e dell’eco-doppler. Il follow-up medio è stato di 30 mesi (min. 1 – max. 64). RISULTATI Per quanto riguarda le lesioni aortoiliache in 18 pazienti è stata effettuata una sola ricanalizzazione iliaca mentre in due casi è stata associata una procedura di ricanalizzazione della femorale superficiale. In tutti i casi la procedura ha consentito la risoluzione del quadro clinico. Durante il follow-up si sono verificate 3 occlusioni: in due casi è stato possibile 40 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 eseguire una nuova procedura endovascolare mentre in uno è stato effettuato un bypass femoro-femorale. La pervietà primaria è stata quindi del 81.2%, la pervietà secondaria del 94.4%. Non ci sono state amputazioni a distanza. Nel distretto sottoinguinale sono state effettuate numerose procedure associate (58.9%): sono sempre state trattate le lesioni poplitee associate, in 5 casi sono state eseguite angioplastiche a livello delle arterie di gamba. Durante il follow-up si sono verificati 3 decessi, in 10 casi si è avuta una occlusione (27.7%): in 4 pazienti è stata eseguita una nuova procedura endovascolare, in un caso è stato eseguito un bypass femoro-popliteo ed in 3 un bypass femoro-distale, una paziente non è stata trattata chirurgicamente per l’elevata comorbidità ed un paziente ha rifiutato la chirurgia: entrambi sono stati amputati rispettivamente ad 1 e 3 mesi dalla procedura. La pervietà primaria è stata del 72.2% (26/36), la pervietà secondaria del 77.7% (28/36), il salvataggio d’arto dell’83.3% (30/36). DISCUSSIONE Nonostante la classificazione TASC pubblicata nel 2000 abbia sancito la superiorità del trattamento chirurgico tradizionale rispetto al trattamento endovascolare nei pazienti con lesioni lunghe ed estese, il miglioramento delle tecniche e dei materiali e la maggiore esperienza degli operatori hanno portato sempre più spesso negli ultimi anni a trattare in modo endovascolare queste lesioni soprattutto nei pazienti con ischemia critica. Tali procedure hanno infatti l’indubbio vantaggio di poter essere effettuate in anestesia locale, con minimo trauma chirurgico, minore morbilità e breve ospedalizzazione senza compromettere, almeno nella maggioranza dei casi, un eventuale successivo intervento chirurgico. D’altro canto la chirurgia tradizionale prevede di eseguire nella gran parte di questi pazienti dei bypass estremi, femoro-distali che necessitano di una assoluta perfezione tecnica, che sono gravati da un elevato tasso di morbilità, da una lunga degenza postoperatoria e comunque non sono sempre fattibili per la mancanza in alcuni casi di una vena di lunghezza e calibro adeguati. La selezione anatomica dei pazienti da trattare rimane uno dei punti cardine del trattamento: tanto più lunghe ed estese sono le lesioni, tanto più esiste un rischio di insuccesso e comunque un minor tasso di pervietà a distanza. Quest’ultimo particolare potrebbe non costituire un problema di rilievo significativo in questo particolare gruppo di pazienti che presenta un elevato rischio di mortalità a breve termine. Come per la chirurgia i risultati sono migliori per il trattamento delle lesioni aorto-iliache: Kudo5 in uno studio effettuato su 138 pazienti con ischemia critica trattati in modo endovascolare riporta una percentuale di pervietà secondaria del 97.8% per le lesioni aorto iliache, del 76.4% per le lesioni femoro-poplitee e del 46.1% per le lesioni distali. Nel distretto femoro-popliteo la percentuale di successo e di pervietà a distanza è strettamente legata alla estensione della lesione e, come per la chirurgia, alla presenza di una adeguato run-off. Molloy6, in uno studio condotto su 110 pazienti ha rilevato che la lunghezza media della lesione nei casi trattati con successo era di 19.7 cm mentre era di 28.6 nelle procedure che non erano state seguite da successo e che il run-off medio era di 1.71 vasi nel primo gruppo e di 1.29 nel secondo. Tuttavia in questi pazienti, come del resto avviene anche per quelli trattati mediante bypass, la pervietà non costituisce il parametro fondamentale di valutazione; infatti il salvataggio d’arto a distanza è abitualmente più alto del tasso di permeabilità. La tecnica di ricanalizzazione va eseguita in modo transluminale, questo in realtà nelle occlusioni lunghe si verifica in una percentuale molto limitata dei casi, per cui di fatto circa l’80% delle rivascolarizzazioni avviene per via subintimale. Questa tecnica si rivela particolarmente utile nel trattamento di lesioni lunghe di vecchia data, ove consente di creare e mantenere più facilmente un lume pervio, nelle lesioni particolarmente calcifiche, anche se brevi, in caso di fallimento di S. Ronchey et al.: Il chirurgo vascolare e l’ischemia critica: le opzioni endovascolari una chirurgia di bypass. Essa garantisce comunque in mani esperte una elevata percentuale di successo e di pervietà a distanza. Nella nostra esperienza uno stent viene impiegato quasi sempre per bloccare gli estremi della dissezione; a livello iliaco e lungo il decorso della femorale superficiale utilizziamo abitualmente stent autoespandibili, a livello delle pieghe di flessione preferiamo utilizzare stent elicoidali che sembrano garantire nel tempo una maggiore permeabilità ed un minor tasso di fratture. Il follow-up clinico ed ultrasonografico è fondamentale per individuare precocemente eventuali restenosi in modo da trattarle prima che si arrivi ad una nuova occlusione. In conclusione le tecniche endovascolari hanno risultati a breve e medio termine soddisfacenti anche se a lungo termine la letteratura riporta risultati inferiori rispetto alla chirurgia tradizionale;7 tuttavia un eventuale fallimento non sembra compromettere in modo significativo la possibilità di un successivo trattamento chirurgico e l’occlusione del vaso ricanalizzato non sempre coincide con il ritorno della sintomatologia. Riteniamo quindi che un tentativo di ricanalizzazione endovascolare, anche in considerazione della bassa morbilità di 41 queste procedure, possa essere considerata come prima scelta nei pazienti con ischemia critica. BIBLIOGRAFIA ESSENZIALE Bailey CM, Saha S, Magee TR, Galland RB. A one year prospective study of management and outcome of patients presenting with critical lower limb ischemia. Eur J Vasc Endovasc Surg 2003;25:131-4. Balmer H, Mahler F, Do DD, Triller J, Baumgartner I. Balloon angioplasty in chronic critical limb ischemia: factors affecting clinical and angiographic outcome. J Endovasc Ther 2002;9:403-10. Jamsen T, Manninen H, Tulla H, Matsi P. The final outcome of primary infrainguinal percutaneous transluminal angioplasty in 100 consecutive patients with chronic critical limb ischemia. J Vasc Interv Radiol 2002;13:455-63. Kudo T. Chandra FA, Ahn SS. The effectiveness of percutaneous transluminal angioplasty for the treatment of critical limb ischemia: a 10-year experience. J Vasc Surg 2005;41:423-35. Molloy KJ, Nasim A, London NJM, et al. Percutaneous transluminal angioplasty in the treatment of critical limb ischemia. J Endovasc Ther 2003;10:298-303. SFA angioplasty versus femoro-popliteal bypass: What can we realistically expect? Wolford HY, Surowiec SM, Davies MG. Endovascular today 2005; june:51-3. The I.C.A.I. Group. The study group of critical chronic ischemia of the lower extremities. Long term mortality and its predictors in patients with critical leg ischemia. Eur J Vasc Endovasc Surg 1997;14:91-5. ____ Per richiesta estratti: Dott.ssa Sonia Ronchey - U.O.C. Chirurgia Vascolare Ospedale S. Filippo Neri - Piazza S. Maria della Pietà, 5 - 00135 Roma ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 I) L’ISCHEMIA CRITICA NON RIVASCOLARIZZABILE: RUOLO DELLA NEUROSTIMOLAZIONE MIDOLLARE - TECNICA D’IMPIANTO NON-RECONSTRUCTABLE CRITICAL LEG ISCHEMIA: ROLE OF SPINAL CORD STIMULATION - IMPLANTATION TECHNIQUE EMILIO D’AVINO U.O.C. Anestesia e Rianimazione. Dipartimento Cardiovascolare Azienda Ospedaliera San Camillo-Forlanini - Roma Parole chiave: Neurostimolazione spinale. Ischemia cronica arti inferiori, Dolore ischemico degli arti inferiori, Dolore neuropatico, Mappa di Barolat. Key words: Spinal cord stimulation, Chronic leg ischemia, Ischemic limb pain, Neurophatic pain, Barolat’s map. INTRODUZIONE La soluzione terapeutica del dolore rappresenta una sfida che l’uomo affronta fin dall’antichità e ad esso si correla, ancora oggi, la gran parte dei motivi di richiesta di consulto medico. Anche se qualcosa resta da definire a proposito dei meccanismi anatomo-fisiologici che sottendono al generarsi del dolore, soprattutto di quello cronico, molti sono i passaggi definitivamente chiariti. L’utilizzo delle correnti elettriche a scopo terapeutico ha radici lontane e, molto prima che si arrivasse alla produzione artificiale di energia elettrica, sono state impiegate le torpedini allo scopo più vario con applicazioni su muscoli, apparato uditivo, sistema nervoso, cuore etc. Nel controllo del dolore è stata utilizzata l’elettrostimolazione applicata a vari livelli del sistema nervoso: sui nervi periferici,1 nelle aree subcorticali dell’encefalo2 e naturalmente sul midollo spinale. L’ elettrostimolazione del midollo è stata introdotta per la prima volta in pratica clinica nel 1967 da Shealy3 il quale, basandosi sugli studi precedentemente condotti da Melzack e Wall4 in cui era stata messa a punto la teoria del cancello (Gate Control Theory), ha posizionato a cielo aperto, attraverso una laminectomia, degli elettrodi sul midollo spinale. Il princi- pio era quello di abolire il passaggio dello stimolo doloroso attraverso la stimolazione di fibre mieliniche (Aß) di grosso calibro che avrebbero attivato, appunto, la chiusura del “cancello” alle fibre amieliniche (C) di piccolo calibro. La metodica non ebbe molta fortuna in quegli anni per diversi motivi tra i quali la non adeguatezza dei materiali e l’incostante successo nell’applicazione clinica. D’altra parte c’era ancora molto da rivedere sui meccanismi della trasmissione nervosa che sosteneva i diversi tipi di dolore e sul ruolo dei neurotrasmettitori a livello spinale. Dai primi anni ’80 si è riattivato l’interesse verso la stimolazione anche grazie alla possibilità di introdurre l’elettrodo stimolatore con tecnica percutanea evitando pertanto l’intervento chirurgico5. Ai giorni nostri, dopo diverse migliaia d’impianti (15.000/anno c.ca) eseguiti in ogni parte del pianeta e per numerosi tipi di patologie dolorose, la stimolazione elettrica midollare ed i suoi precisi meccanismi d’azione rimangono ancora in una zona di penombra pur dimostrando in un’elevata percentuale di casi un’efficacia non realizzabile con altri presidi terapeutici. Fisiopatologia della stimolazione cordonale: La stimolazione elettrica dei cordoni posteriori (SCS o Spinal Cord Stimulation), che si è sviluppata come diretta E. D’Avino: L’ischemia critica non rivascolarizzabile: ruolo della neurostimolazione midollare - Tecnica d’impianto conseguenza della teoria del sistema di controllo sull'ingresso spinale, ha seguito l'ipotesi che la iperstimolazione elettrica attivi i sistemi neuronali di inibizione dell' input. Questa ipotesi a sua volta è stata confermata da una discreta quantità di ricerche soprattutto in ambito animale che hanno evidenziato: • Inibizione dei neuroni nocicettori del corno spinale posteriore;6 • Eccitazione degli interneuroni della sostanza gelatinosa del corno posteriore con istituzione di un circuito locale inibitorio per l'ingresso degli stimoli nella via spino-talamica.7 • Inibizione, nell’uomo e nella scimmia, di neuroni nocicettivi del midollo dorsale, in particolare quelli ad ampio spettro dinamico (WDR – wide dynamic range) all’interno della lamina V, con riscontro registrabile tramite potenziali evocati somato-sensoriali.8 Nel 1975 vengono effettuati i primi studi clinici osservazionali per valutare l’effetto della SCS sulla percezione di stimoli dolorosi e non: si realizza, in caso di stimolazione efficace, un aumento della soglia al tatto ed alla vibrazione ma non quella al dolore cutaneo.9 Per avere i primi trial con gruppo di controllo si deve giungere ai primi anni novanta, quando viene documentata, da parte dell’elettrostimolazione, un’attività antalgica quantificabile.10 Sono stati invocati anche meccanismi di attivazione sovraspinale ma che sono carenti nello spiegare il protrarsi dell’analgesia dopo la fine della stimolazione11 e anche la possibile attivazione dei peptidi oppioidi sarebbe da escludere in quanto l’analgesia non viene antagonizzata dal naloxone.12 Secondo le più recenti teorie, che vedono coinvolte nella trasmissione del dolore, numerose sostanze neuromodilatatrici, la SCS ecciterebbe, con meccanismo GABAmediato, la sostanza gelatinosa del corno posteriore istituendo un circuito locale inibitorio per l’ingresso degli stimoli nella via spinotalamica.13 La liberazione di acido gamma-amino-butirrico (GABA) e di glicina (GLY) è uno dei meccanismi di inbizione locale metamerico che intervengono nel 43 complesso meccanismo di neuromodulazione metamerica della trasmissione dolorosa confermato da numerosi studi sperimentali e clinici: l’azione della SCS viene rapidamente annullata da somministrazione, nel ratto, di GABA-antagonisti14 mentre nell’uomo e nel modello animale l’infusione intratecale di Baclofen, agonista GABAB, potenzia l’azione della SCS.15 Ulteriori meccanismi chiamati in causa possono essere: • l’attivazione di vie analgesiche discendenti a partenza dalla sostanza grigia periacqueduttale (PAG)16 e • un rilascio di sostanze neuromodulatrici quali la serotonina (5-HT) e la sostanza P.17 Indipendentemente dai meccanismi coinvolti il dato certo è che la sovrapposizione delle parestesie indotte sulle aree dolorose è un requisito indispensabile per il funzionamento della stimolazione cordonale.18 Altrettanto complessa rimane l'interpretazione fisiologica dell'effetto della SCS sulla vascolarizzazione periferica: sono allo studio diverse ipotesi ma nessuna di queste ha dato ancora un esito sufficientemente esplicativo. Un elemento accertato è l’azione sul bilancio fornitura/fabbisogno di ossigeno a favore del primo ovvero un’effetto ”antischemico”.19 I tipi di dolore predominante nella malattia vascolare periferica sono: • un dolore ischemico profondo con componente “neuropatica” dovuta al danno tessutale nervoso • un dolore superficiale proveniente dall’area delle aree ischemiche, ulcerate e non. Entrambi i tipi di dolore sono sensibili agli oppioidi, il dolore profondo viene alleviato dalla SCS come la gran parte dei dolori neuropatici mentre quello superficiale viene mascherato dalle parestesie. Il primo risponde in alcuni giorni e non riappare immediatamente dopo la sospensione del trattamento mentre il secondo risponde in pochi minuti ma la sua durata è contestuale alla stimolazione. 44 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 Gli impulsi dello stimolatore midollare si distribuiscono sia in senso ortodromico (parestesie) che antidromico (inibizione delle vie nocicettive A-∂ e C). Quest’ultima azione potrebbe interessare, a livello segmentario i tratti autonomici dell’ area grigia periacqueduttale che regolano il tono simpatico periferico e pertanto contrastare l’attività vasocostrittrice. A sostegno di questa interpretazione ci sono evidenze sperimentali (effetto abolito dalla simpaticectomia) che contrastano con dati clinici (effetto mantenuto in pazienti precedentemente simpaticectomizzati). Un secondo effetto di vasodilatazione documentato, in particolare con stimolazione ad alta soglia, è legato al rilascio di sostanze vasoattive, in particolare di Calcitonina-gene related peptide (CGRP) che agirebbe favorendo la produzione locale di ossido nitrico (NO) potente vasodilatatore.20 Le molteplici carenze interpretative hanno determinato, nel passato, un duplice effetto negativo: • ad un iniziale eccessivo entusiasmo circa l'efficacia di questo strumento che ha inevitabilmente comportato un utilizzo esteso e a volte non esattamente congruo, con un’elevata incidenza di insuccessi ha fatto seguito, un diffuso scetticismo al riguardo con un lungo periodo di sottoutilizzo.13 La selezione accurata dei pazienti rimane uno dei momenti cruciali nel realizzare gli obbiettivi della procedura.21 La malattia vascolare periferica non suscettibile di trattamento chirurgico rimane a pieno titolo tra le indicazioni alla SCS soprattutto nei paesi europei dove rappresenta il campo principale di applicazione. Numerosi studi confermano un ottimo recupero delle lesioni trofiche, un documentato aumento della perfusione capillare, una significativa riduzione delle amputazioni ma soprattutto nel 60-100% dei pazienti un deciso miglioramento della sintomatologia dolorosa (pain relief).22 COMPONENTI E METODICA DI POSIZIONAMENTO Lo stimolatore midollare è costituito dall’assemblaggio di più componenti: 1. L’ elettrocatetere che viene alloggiato nello spazio peridurale con la sua estremità fornita di un numero variabile di elettrodi (da 4 a 8) e attraverso il quale si realizza la stimolazione elettrica del midollo spinale. Può essere inserito per via percutanea, attraverso un ago di Thuoy, oppure con accesso chirurgico mediante laminectomia. 2. L’estensione da collegare al catetere, di lunghezza variabile, che verrà tunnellizzata nel fianco del paziente e dalla quale ci si potrà connettere al generatore di impulsi temporaneo o definitivo. 3. Il generatore di impulsi (IPG) che può essere di due tipi: completo di batteria o a radio frequenza. Il sistema completo di batteria è totalmente impiantabile e certamente più comodo per il paziente che può variare alcuni parametri o spegnerlo con sistema telemetrico. L’inconveniente è legato all’esaurirsi della batteria che ne impone la sostituzione entro 3-6 anni. 4. Il sistema Ricevitore/Antenna fa parte solo dei sistemi a radio-frequenza. Il ricevitore, di morfologia simile alle batterie impiantabili e connesso all'elettrocatetere dall'estensione, viene posizionato in una tasca sottocutanea; l'antenna, a sua volta collegata ad un trasmettitore esterno, viene “indossata” dal paziente sulla zona di cute sovrastante il ricevitore. Vengono impiegati in casi in cui si prevede un grosso consumo energetico che richiederebbe frequenti sostituzioni. L'impianto di uno Stimolatore Midollare avviene in tre fasi distinte: • I fase: in camera operatoria, dopo la somministrazione di antibioticoprofilassi, si effettua, in anestesia locale, il posizionamento dell'elettrocatetere. Il paziente viene posizionato prono su tavolo radiotrasparente in modo da poter sopportare la postura per il tempo necessario. La posizione laterale è certamente più comoda per il paziente ma lo è un po’ meno per l’operatore, viene riservata di solito alla puntura del tratto cervicale. Con ago di Thuoy e la tecnica del man- E. D’Avino: L’ischemia critica non rivascolarizzabile: ruolo della neurostimolazione midollare - Tecnica d’impianto drino liquido viene rilevato lo spazio epidurale nel tratto che interessa la stimolazione e, sotto guida fluoroscopica, si fa avanzare il catetere di stimolazione. L’accesso allo spazio epidurale può essere effettuato per via mediana o laterale paramediana, nel primo caso può risultare difficoltosa la guida del catetere verso la regione che interessa stimolare mentre nell’altro approccio, meno agevole, si deve inserire l’ago da uno spazio più in basso a quello che si vuole raggiungere. Nelle vasculopatie degli arti inferiori con dolori e ulcere a carico dei piedi la regione da stimolare (“sweet spot placement”) è di solito tra T11 e L1 con una posizione leggermente spostata dalla linea mediana verso il lato interessato. In caso di malattia estesa ad entrambi gli arti si dovrà optare per la posizione mediana con una possibile perdita di efficacia. Per aver un risultato soddisfacente è indispensabile rifarsi alle indicazioni fornite dal paziente in modo da avere sovrapposizione delle parestesie indotte sulla distribuzione del dolore. In caso di elettrocateteri piatti multipolari, riservati di solito a forme di dolore cronico complesso, si deve ricorrere ad intervento chirurgico. In questo caso, se non è possibile eseguire l’anestesia locale, si dovrà collocare l’elettrodo su indicazioni anatomiche riservandosi di agire sulle possibili combinazioni tra gli elettrodi. Il vantaggio indiscutibile dell’approccio chirurgico sta nella stabilità dell’elettrocatetere. Qualsiasi tipo di catetere (percutaneo o piatto) viene allocato di fronte alle colonne dorsali, con il raggio di azione parallelo alla corda spinale, essendo il target da stimolare le fibre A-ß che ivi decorrono. Oltre che sulle colonne dorsali si può avere una stimolazione a carico delle radici dorsali la quale, oltre a non evocare parestesie segmentarie, può generare sensazioni sgradevoli e contrazioni muscolari riflesse, all’aumentare del voltaggio. Questo voltaggio costituisce una sorta di soglia di di- 45 scomfort e definisce il punto più alto del range terapeutico il quale a sua volta inizia al valore di soglia di percezione delle parestesie. Più è ampio il range terapeutico e migliore è la qualità della stimolazione. Due fattori incidono sull’ampiezza di questo valore: la separazione anodo-catodo nel catetere e la distanza di questo dal cordone midollare. Uno spazio ravvicinato tra i dipoli migliora la precisione della soglia contenendo la dispersione dello stimolo alle radici dorsali: a questo scopo sono stati prodotti cateteri con distanza interpolare di 6-7 mm in aggiunta a quelli più comuni con distanza di 9-10 mm. La distanza tra catetere e midollo ha una grande variabilità intersoggettiva e risente anche della regione anatomica in cui viene posizionato l’elettrodo. Purtroppo non ci sono linee guida in letteratura ma dal lavoro di Law e Miller23 si deriva la necessità di realizzare la parestesia per avere un’efficacia di risultato. Su questa base s’inserisce l’originale ricerca di Barolat24 mirata a costruire una mappa cui far riferimento per posizionare l’elettrodo sulla zona in cui si ricerca l’effetto. È interessante notare, in questo lavoro effettuato su più di cento pazienti sottoposti a SCS, la particolare variabilità anatomica per cui, posizionando un elettrocatetere nello stesso punto in due pazienti diversi, non sempre si possono evocare le stesse parestesie. Dalla frequenza con cui ciò avviene Barolat, dopo aver diviso le aree del corpo in venti sottozone, ha disegnato una “mappa” (Fig.1) con aree di colore diverso corrispondenti alla percentuale con cui si realizza la stimolazione di una determinata zona. Dalla semplice osservazione di questa mappa si può rimanere sorpresi notando che, seppure occasionalmente, con un catetere che stimola a livello toracolombare si può evocare una parestesia del braccio. La sorpresa è decisamente minore in coloro che hanno alle spalle una discreta esperienza nella pratica della SCS. 46 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 Una volta effettuato il test di stimolazione intra-operatorio, l'operatore raccorda con l'elettrocatetere l'estensione temporanea, che viene tunnellizzata nella regione postero-laterale del fianco e collegata ad un generatore esterno. • II fase: Il paziente può essere dimesso in regime di day-hospital dopo avergli fornito alcune raccomandazioni sulla necessità di non effettuare piegamenti, torsioni del busto o sforzi fisici. Questa è la cosiddetta fase di trial provvisorio durante la quale viene monitorizzata la reale efficacia del presidio: durante i controlli si può agire sullo stimolatore esterno modificando l’ampiezza (in genere da 1.0 a 2.5), la frequenza (tra 70 e 120) e la durata della pulsazione (di solito tra 180 e 450 microsec). Si può istruire il paziente in tal senso poiché al variare della posizione, ad esempio da seduto a supino, lo stimolo può aumentare di ampiezza e diventare fastidioso oppure la notte, se il paziente non ha dolore, può decidere di spegnere il device. Il trial può durare da 1 a 4-5 settimane, a seconda delle abitudini del centro di terapia, di solito si preferisce un periodo superiore ai 15 giorni. • III fase: impianto definitivo in quei pazienti che abbiano risposto con successo e soddisfazione alla stimolazione. È fondamentale che il paziente condivida questa soddisfazione ed accetti la convivenza con le parestesie quando queste sono in grado di ridurre od eliminare il consumo di analgesici. L’impianto viene effettuato in camera operatoria in anestesia locale ed eventuale ausilio di una lieve sedazione. Va prestata la massima attenzione durante la manipolazione del cavo temporaneo ad una possibile dislocazione dell’elettrocatetere, verificare che le nuove connessioni siano efficaci e soprattutto eseguire tutta la manovra in una rigorosa asepsi. CONTROINDICAZIONI Fattori che controindicano l'impianto di uno stimolatore midollare possono essere le affezioni psichiatriche (disturbi della personalità, disordini psicologici maggiori, tossico- o farmacodipendenza, i disturbi della coagulazione, le sindromi da immunodeficienza, gli obbiettivi di risarcimento. La presenza di altri stimolatori elettrici quali il PMK cardiaco non è più una controindicazione assoluta se vengono prese alcune misure di cautela. È fondamentale per l'ottimizzazione del trattamento, che la selezione dei pazienti si incentri, oltre che sulla diagnosi e l'esame obbiettivo, anche sulla loro valutazione psicologica25 e che il trattamento a lungo termine preveda anche un follow-up da parte di uno psicologo specializzato in terapia del dolore. Già nel 1981, Long sosteneva che i fattori psicologici costituiscono la principale ragione di insuccesso dello SM26. Spesso nella terapia del dolore cronico, le aspettative del paziente (e, a volte, quelle del medico) possono influenzare profondamente l'esito del trattamento; per questo, fin dall'inizio, deve essere chiaro al paziente e al medico che la SCS non cura la patologia responsabile del dolore, ma mira ad interferire con le anomalie di conduzione e di trasmissione dello stesso; l'obbiettivo può non essere la completa risoluzione della sindrome dolorosa, bensì il raggiungimento di un livello di dolore sopportabile, la possibilità di svolgere le normali attività quotidiane e, se possibile, una riduzione/sospensione del supporto farmacologico. COMPLICANZE La vita media degli impianti varia da Centro a Centro e anche nelle diverse patologie: tra i motivi più comuni di rimozione si annotano le infezioni e l’insuccesso terapeutico per dislocazione del catetere. Quando non si verificano queste due condizioni si può sviluppare un fenomeno descritto come tolleranza. Si parla di tolleranza quando, pur continuando le parestesie nella zona bersaglio, il sollievo del dolore, inizialmente presente in grado soddisfacente, risulta in seguito ridotto o perfino assente. La tolleranza può insorgere dopo i primi 2 anni ma il suo meccanismo fisiopatologico non è ancora stato esaustivamente descritto. E. D’Avino: L’ischemia critica non rivascolarizzabile: ruolo della neurostimolazione midollare - Tecnica d’impianto Kumar13 individua essenzialmente 2 principali processi fisiopatologici: • evoluzione fibrotica del tessuto connettivo intorno alla punta dell'elettrocatetere, che viene così isolata dalla dura; • neuroplasticità delle vie ascendenti nocicettive e riorganizzazione delle vie di percezione del dolore. L'eventuale assunzione di farmaci, di per sé, non depone contro l'efficacia di questa procedura, in quanto una problematica complessa come il dolore cronico necessita di un approccio terapeutico multimodale e l'evidenza clinica di sinergismo fra SM e terapia farmacologica è ormai accettata. CONCLUSIONI Quando si analizza la SCS si tende a semplificare parlando di stimolazione della corda dorsale ma è evidente che quello che si realizza è qualcosa di più complesso. Sulla sua reale efficacia nel trattamento dell’ischemia critica non rivascolarizzabile si esprime una rassegna recente della Cochrane Library26 che conclude affermando un reale vantaggio sulla terapia tradizionale per quel che riguarda il sollievo dal dolore e il salvatag- 47 gio d’arto malgrado ci siano molti studi retrospettivi e pochi trial randomizzati. Sull’altro piatto della bilancia si attestano i costi (che sono più elevati) e gli insuccessi (che sono ancora molto frequenti). Per quello che riguarda questi ultimi il revisore attribuisce una certa responsabilità alla frammentazione della procedura (tanti Centri con casistiche esigue) e consiglia di riservarla a Centri specializzati. BIBLIOGRAFIA 1. Wall PD, Sweet WH: Temporary abolition of pain in man. Science 1967;155:108-9. 2. Adams JE, Hosobuchi Y, Fields HL: Stimulation of internal capsule for relief of chronic pain. J Neurosurg 1974;41:740-4. 3. Shealy CN, Mortimer TJ, Reswick JB: Electrical inhibition of pain by stimulation of the dorsal columns: preliminary clinical report. Anesth Analg 1967;46:489-91. 4. Melzack R, Wall PD: Pain mechanisms: a new theory. Science 1965;150:971-8. 5. Hoppenstein R.: Percutaneous implantation of chronic spinal cord electrode for control of intractable pain, preliminary report” Surg Neurol 1975;4:195-8. 6. Foreman RD, Beall JE, Applebaum HE, Coulter JD, Willis WD. Effects of dorsal column stimu- Figura 1 - (da Barolat G. J.Neurosugery 1993, with permission). 48 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 lation on primate spinothalamic tract neurons. J.Neurophysiol 1976;39:534-46. 7. Dubuisson F. Effect of dorsal-column stimulation on gelatinosa and marginal neurons of cat spinal cord. J.Neurosurg 1989;70:257-65. 8. Larson S, Sances A, Riegel D, Meyer G, Dallman D, Swiontekk T. Neurophysiological effects of dorsal column stimulation in man and monkey. J.Neurosurg 1974;41:217-23. 9. Lindblom U, Meyerson BA. Influence on touch, vibration and cutaneous pain on dorsal column stimulation in man. Pain 1975;1:257-70 10. Marchand S, Bushnell MC, Molina-Negro P, Martinez SN, Duncan GH. The effects of dorsal column stimulation on measures of clinical and experimental pain in man. Pain 1991;45:249-57 11. Campbell JN. Examination of possible mechanisms by which stimulation of the spinal cord in man relieves pain. Appl. Neurophysiol. 1981;44:181-6. 12. Meyerson BA. Electric stimulation of spinal cord and brain. In: Bonica JJ. The management of pain. 2nd edition. Philadelphia,Lea & Febinger, 1990 13. Kumar K, Nath R, Wyant GM: Treatment of chronic pain by epidural spinal cord stimulation: a 10 years experience. J Neurosurg 1991;75:402407. 14. Bennet G. An animal model of neuropathic pain:a review. Muscle Nerve 1993;16:1040-8 15. Meyerson BA Modulation of spinal pain mechanism by SCS and the potential role of adjuvant pharmacotherapy. Stereotact Funct Neurosurg 1997;68:129-40. 16. Stiller CO, Linderoth B Repeated spinal cord stimulationdecrease the extracellular level of gamma-aminobutiric acid in periaqcueductal grey matter of freely moving rats. Brain Res 1995;699:231-41. 17. Linderoth B et al Dorsal column stimulation induces release of serotonin and susbstance P in the cat dorsal horn. Neurosurgery 1992;31:28996. 18. Holsheimer J, Wessenlink WA: Effect of anodecathode configuration on paresthesia coverage in Spinal Cord Stimulation. Neurosurgery 1997;41:654-60. 19. Linderoth B, Herregodts P, Meyerson BA: Sympathetic mediation of peripheral vasodilation induced by spinal cord stimulation: Animal studies of the role of cholinergic and adrenergic receptor subtypes. Neurosurgery 1994; 35:711-9 20. Croom JE, Foreman RD, Chandler MJ, Koss MC, Barron KW: Role of nitric oxide in cutaneous blood flow increases in the rat hindpaw during dorsal column stimulation. Neurosurgery 1997;40:565-70. 21. Tesfaye S, Watt J, Benbow SJ, Pang KA, Miles J, MacFarlane I: Electrical spinal cord stmulation for painful diabetic peripheral neuropathy. Lancet 1996;348:1696-701. 22. Broseta J Spinal cord stimulation in peripheral arterial disease. J Neurosurg 1986;64:71-80. 23. Law JD, Miller LV: Importance of documentation of an epidural stimulating position. AppI Neurophysiol 1982;45:461-4. 24. Barolat G. Mapping of sensory responses to epidural stimulation of the intraspinal neural structures in man. J Neurosurg 1993;78:233-9. 25. Segal R, Stacey Br, Rudy TE: Spinal Cord Stimulation revisited. Neurol Res 1998;20:391-6. 26. Ubbink DT, Vermeulen H Spinal cord stimulation for non-reconstructable chronic critical leg ischaemia. Issue 3 The Cochrane Library 2003. ____ Per richiesta estratti: Dr. Emilio D’Avino - Ospedale S. Camillo - U.O.C. Anestesia e Rianimazione - A.O. San Camillo-Forlanini Circonvallazione Gianicolense - 00152 Roma ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 L) L’ISCHEMIA CRITICA NON RIVASCOLARIZZABILE: RUOLO DELLA NEUROSTIMOLAZIONE MIDOLLARE. INDICAZIONI NON-RECONSTRUCTABLE CRITICAL LEG ISCHEMIA: ROLE OF SPINAL CORD STIMULATION - INDICATIONS FABIO DI CESARE Unità Operativa di Chirurgia Vascolare Azienda Ospedaliera San Camillo-Forlanini - Roma Parole chiave: Ischemia critica arti inferiori, Stimolazione midollare. Key words: Critical leg ischemia, Spinal cord stimulation. INTRODUZIONE Il trattamento dell’ischemia critica degli arti inferiori (CLI) rappresenta un capitolo della chirurgia vascolare molto complesso. I pazienti, affetti da localizzazione pluridistrettuale della malattia aterosclerotica, sono spesso ad alto rischio chirurgico per la presenza di multiple patologie associate, di età avanzata e con quadro anatomo-chirurgico complesso. Il 10-30% dei pazienti con CLI muoiono in media a 6 mesi dalla diagnosi ed un altro 25-35% andrà incontro ad amputazioni maggiori (Trans Atlantic Inter-Society Consensus 2000).1 La terapia di scelta della CLI è la rivascolarizzazione chirurgica, la sola spesso in grado di risolvere la sintomatologia dolorosa invalidante e la guarigione e/o delimitazione delle lesioni ischemiche necrotiche. Esiste una categoria di pazienti per i quali la scelta chirurgica è infruttuosa e la terapia medica non sufficiente ad alleviare la sintomatologia dolorosa; alcuni pazienti, inoltre, non possono essere proposti per l’intervento chirurgico per le estese localizzazioni anche periferiche della malattia aterosclerotica. Per un sottoinsieme di pazienti affetti da ischemia critica apparentemente non è individuabile una valida possibilità terapeutica in grado di liberarli dal dolore profondo per lo più persistente e che possa garantire un buon risultato a medio termine. Un 20% circa di pz con CLI non sono rivascolarizzabili per impossibilità tecnica o per presumibile insuccesso chirurgico.2 La neurostimolazione midollare (spinal cord stimulation – SCS) è stata per prima descritta nel 19653 e successivamente accettata per il trattamento del dolore neurogenico. La prima pubblicazione che riguardava l’uso della SCS per il trattamento della CLI risale al 19764. In seguito diverse esperienze sono state proposte, alcune con rilievi positivi, altre con riscontri meno ottimistici (riduzione nell’assunzione di antidolorifici orali - Spieglmann (1991)5; Mingoli (1993)6; Tesfaye (1996)7; miglioramento nell’autonomia di marcia - Tallis (1983)8; incremento della temperatura cutanea (termografia) Augustisson (1985)9; Broseta (1986)10; miglioramento nella qualità di vita - Fiume (1989)11; Spiegelmann (1991)5; Linderoth (1992)12; Rickman (1994)13; Tesfaye (1996)7. MECCANISMO D’AZIONE DELLA NEUROSTIMOLAZIONE L’uso della SCS si basa più su osservazioni empiriche che su dimostrazioni fisiopatologiche avvalorate da riscontri sperimentali. Il dolore ischemico riconosce due componenti: - dolore profondo, da sofferenza ischemica nervosa sensoriale - dolore superficiale, dalle aree delle zone necrotiche 50 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 Il dolore profondo sarebbe alleviato dalla stimolazione elettrica, quello superficiale mascherato dalle parestesie. L’azione antiischemica della stimolazione midollare sarebbe determinata da un’azione modulante sul sistema nervoso simpatico (vasodilatazione) Una ipotesi è quella del Gate Control: la stimolazione elettrica delle fibre nervose di grande diametro inibirebbe la trasmissione dello stimolo doloroso a livello superiore. Jacobs et al.2 hanno studiato un possibile effetto della SCS sul microcircolo tramite osservazione con la microscopia capillare. - Il numero dei capillari perfusi incrementa notevolmente dopo SCS mentre il diametro dei capillari non varia. - La velocità media dei globuli rossi incrementa in maniera significativa dopo SCS (0,088 mm/sec vs 0,496 mm/sec p<0,001) Gli insuccessi della terapia sono in relazione all’assenza di un letto capillare idoneo; tale situazione non è modificabile dalla SCS. Anche secondo Ubbink et al.14 la stima del microcircolo a livello cutaneo è predittiva della possibilità di un’imminente amputazione nella CLI. I pazienti che possono beneficiare della SCS è il sottogruppo con una circolazione “intermedia”. Il rilievo della ossimetria transcutanea TcpO2 è stata da molti proposta come metodica per la selezione dei pazienti, in particolare da Amann et al.15 I criteri di selezione per SCS sono: - TcpO2 10-30 mmHg; TcpO2 < 10 mmHg ma responsivi al periodo di test stimulation - Positività della risposta clinica dopo periodo di test stimulation Con questa selezione è stato raggiunto un 78% di salvataggio d’arto in pazienti non rivascolarizzabili. La TcpO2 può indicare la presenza di un microcircolo ancora relativamente valido. CRITERI DI INCLUSIONE I pazienti candidati all’impianto di neurostimolatore midollare devono essere affetti da CLI di natura aterosclerotica non rivascolarizzabile; assenza di lesioni ischemiche gangrenose estese; assenza di dipendenza da alcool e droghe; assenza di controindicazioni per l’impianto (sepsi, coagulopatie, ecc.); consenso informato del paziente. Sono esclusi i pazienti con disordini vascolari di natura non aterosclerotica, la presenza di problematiche psichiatriche e/o psicologiche di rilievo, la possibilità di adottare terapie alternative meno invasive e meno costose, l’impossibilità tecnica di impiantare l’elettrodo epidurale, la presenza di patologie quali sepsi, coagulopatie, neoplasie o condizioni che riducano l’aspettativa di vita a meno di un anno, il rifiuto da parte del paziente. Per il raggiungimento di elevate percentuali di successo è importante seguire una corretta metodica d’impianto e un’attenta monitorizzazione durante il periodo di prova. Tale periodo può durare 15-30 giorni e serve a valutare la reale efficacia clinica della SCS; se l’impianto dell’elettrodo sortisce effetti positivi con remissione della sintomatologia dolorosa, si procede all’impianto del neurostimolatore definitivo. È necessario selezionare accuratamente i pazienti agli stadi CLI con ulcere di diametro minore ai 3 cm per attendersi percentuali di successo nel 50 - 70% dei casi trattati e con microcircolo ancora “presente” L’impianto dell’elettrocatetere deve essere corretto (parestesie nella zona algica); bisogna accertarsi che il paziente abbia lo stimolatore esterno di prova sempre acceso. La selezione dei pazienti deve essere accurata; i pazienti devono essere allo stadio di CLI e con ulcere < 3 cm; solo in tal modo è possibile attendersi percentuali di successo nel 50 - 70% dei casi trattati. La riduzione della sintomatologia dolorosa di almeno il 50% con demarcazione delle aree da amputare, con conseguente salvataggio d’arto, può essere considerato un successo terapeutico. RISULTATI Lo studio più significativo è quello della Cochrane review: Spinal cord stimulation for non-reconstructable chronic critical leg ischaemia. Ubbink DT, Vermeulen H – 200316. F. Di Cesare: L’ischemia critica non rivascolarizzabile: ruolo della neurostimolazione midollare. Indicazioni Si tratta di una review su trial randomizzati controllati e trial clinici controllati aventi • Obiettivio primario: salvataggio d’arto; • Obiettivi secondari: riduzione del dolore, guarigione delle ulcere, complicanze dell’SCS, qualità della vita, costi. Il criterio di inclusione è stato la malattia aterosclerotica allo stadio CLI non rivascolarizzabile. U e D > 18 anni. Dalla review dei lavori, di cui 5 studi nazionali (Belgio - Suy 1994, Svezia - Jivegard 1995, Germania - Claeys 1996, Danimarca – 1 ESES 2 Spincemaille 2000) e 1 studio internazionale – SCS EPOS Amann 2003, per complessivi 444 pazienti, i risultati emersi sono stati i seguenti: - Gli studi Svedese, Belga, Tedesco, ESES non hanno rilevato differenze statisticamente significative, nel salvataggio d’arto, dopo 12, 18, 24 mesi di follow-up anche se vi è stata una tendenza positiva vs SCS group. Questa tendenza è risultata più importante nel sottogruppo di pazienti selezionati in base alla TcpO2. - Nello studio SCS-EPOS la differenza cumulativa nel salvataggio d’arto è stata significativamente migliore nell’SCS group (p=0,003); in particolare nel sottogruppo dei pazienti selezionati in base alla TcpO2 e responsivi al periodo di stimolazione di prova (p=0,002) - Il trattamento del dolore è risultato significativamente migliore nell’SCS group. In particolare, l’SCS group ha necessitato di minore quantità di farmaci analgesici narcotici e non narcotici. - Negli studi di Claeys e Suy i pz passati dallo stadio di CLI allo stadio di claudicatio sono risultati più numerosi nell’SCS rispetto al trattamento conservativo (p=0,0014) - Due studi hanno riportato una migliore guarigione delle ulcere ischemiche nell’SCS group (Claeys p=0,013), in particolare nei pz normotensivi. - Costi: - L’ESES studio ha confrontato i costi considerando l’ospedalizzazione, la riabilitazione, lo stimolatore, le procedure chirurgiche di impianto, le medicazioni in 2 anni: 51 - SCS group 36.500 Euro - conservative group 28.600 Euro p<0,009 Le conclusioni dei revisori sono state che c’è evidenza che la SCS è migliore del trattamento conservativo nel ridurre il rischio d’amputazione d’arto, la remissione della sintomatologia dolorosa ed il miglioramento clinico nei pazienti con CLI non rivascolarizzabile. L’effetto positivo della SCS appare essere migliore nei pazienti con accettabile TcpO2 e dopo buona risposta al periodo di stimolazione di prova. In tal senso, la SCS dovrebbe essere limitata ad un sottogruppo ristretto di pazienti con CLI non rivascolarizzabile. In particolare Amann, nel suo SCSEPOS study del 2003 15 ha evidenziato l’importanza della determinazione della TcpO2. Ha trattato 112 pz con CLI; 52% al III° stadio 48% al IV° stadio, non rivascolarizzabili, secondo i seguenti criteri di selezione per SCS: - TcpO2 10-30 mmHg; TcpO2 < 10 mmHg ma responsivi al periodo di test stimulation - Positività della risposta clinica dopo periodo di test stimulation Con questa selezione è stato raggiunto un 78% di salvataggio d’arto in pazienti non rivascolarizzabili. La TcpO2 può indicare la presenza di un microcircolo ancora relativamente valido. CONCLUSIONI In categorie di pazienti non rivascolarizzabili e non rispondenti alla terapia medica può essere presa in considerazione la neurostimolazione midollare. La selezione dei pazienti è fondamentale per ottenere buoni risultati a medio termine. Un criterio di selezione si può basare sulla TcpO2 (valutazione indiretta del letto capillare) in aggiunta alle considerazioni di carattere clinico. L’elettrostimolazione midollare può essere utile nel trattamento di pz selezionati con ischemia critica non candidabili all’intervento di rivascolarizzazione • Non comporta alcuna interruzione temporanea o permanente del percorso nervoso 52 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 • La procedura è reversibile e la risposta del pz può essere verificata prima dell’impianto permanente • I criteri per determinare l’efficacia della metodica sono clinici (scomparsa del dolore e guarigione, anche parziale, delle lesioni trofiche). Di solito si assiste anche ad un miglioramento della TcpO2 BIBLIOGRAFIA 1. Trans Atlantic Inter-Society Consensus (TASC). Management of Peripheral Arterial Disease (PAD). J Vasc Surg 2000;31. 2. Jacobs MJHM, Jorning PJG, Beckers RCY, et al: Foot salvage and improvement of microvascular blood flow as a result of epidural spinal cord electrical stimulation. J Vasc Surg 1990:12(3):354-60. 3. Melzack R, Wall PD. Pain mechanisms: a new theory. Science 1965;150:971-9. 4. Cook AW, Oygar A, Baggenstos P, Pacheco S, Kleriga E. Vascular disease of extremities. Electrical stimulation of spinal cord and posterior roots. NY State J Med 1976;76:366-8. 5. Spiegelmann R, Friedman WA. Spinal cord stimulation: a contemporary series. Neurosurgery 1991;28:65-70. 6. Mingoli A, Sciacca V, Tamorri M, Fiume D, Sapienza P. Clinical results of epidural spinal cord electrical stimulation in patients affected with limb-threatening chronic arterial obstructive disease. Angiology 1993;44:21-5. 7. Tesfaye S, Watt J, Benbow SJ, Mile J, MacFarlane IA. Electrical spinal cord stimulation for painful diabetic peripheral neuropathy. Lancet 1996;348(9043):1698-701. 8. Tallis RC, Illis LS, Sedgwick EM. Spinal cord stimulation in peripheral vascular disease. J Neurol, Neurosurg Psychiatry 1983;46;478-84. 9. Augustinsson LE, Carlsson CA, Holm J, Jivegard L. Epidural electrical stimulation in severe limb-saving effect. Ann Surg 1985;202:104-10. 10. Broseta J, Barbera J, de Vera JA, et al. Spinal cord stimulation in peripheral arterial disease. A cooperative study. Journal of Neurosurgery 1986;64:71-80. 11. Fiume D, Palombi M, Sciacca V, Tamorri M. Spinal cord stimulation (SCS) in peripheral ischemic pain. Pacing Clin Electrophysiol 1989;12:698-704. 12. Linderoth B. Dorsal column stimulation and pain: experimental studies on putative neurochemical and neurophysiological mechanism. Thesis Karolinska Institute, Stockholm 1992. 13. Rickman S, Wuebbels BH, Holloway GA Jr. Spinal cord stimulation for relief of ischemic pain in end-stage arterial occlusive disease. J Vasc Nursing 1994;12:14-20. 14. Ubbink DT, Spincemaille GH, Prins MH, Reneman RS, Jacobs MJ. Microcirculatory investigations to determine the effect of spinal cord stimulation for critical leg ischemia: the Dutch multicenter randomized controlled trial. J Vasc Surg 1999;30:236-44. 15. Amann W, Berg P, Gersbach P, Gamain J, Raphael JH, Ubbink DT. Spinal cord stimulation in the treatment of non-reconstructable stable critical leg ischemia:results of the European Peripheral Vascular Disease Outcome Study (SCS-EPOS): Eur J Vasc Endovasc Surg 2003;26:280-6. 16. Ubbink DT, Vermeulen H. Spinal cord stimulation for non-reconstructable chronic critical leg ischaemia. Issue 3, The Cochrane Library. ____ Per richiesta estratti: Dr. Fabio Di Cesare - U.O.C. di Chirurgia Vascolare Ospedale S. Camillo - Circonvallazione Gianicolense - 00152 Roma ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 Articolo originale INDICAZIONI PARTICOLARI ALL’IMPIEGO DELLA TCms TORACICA NELL’AMBULATORIO PER LA TERAPIA DEL TABAGISMO SPECIAL INDICATION TO THE USE OF THE CTms IN THE OUTPATIENT’S DEPARTMENT FOR THE SMOKING CESSATION ROSASTELLA PRINCIPE, 2FRANCESCO QUAGLIARINI, 3GIORGIO MANCINI 1 III U.O.C. Pneumologia, 2U.O.C. Radiologia Generale, 3U.O.C. Fisiopatologia Respiratoria Azienda Ospedaliera San Camillo-Forlanini - Roma 1 Riassunto. Per valutare l’utilità della TCms(Tomografia Computerizzata multistrato) nella diagnostica delle malattie polmonari, in fumatori con normali indici delle funzioni respiratorie e negatività della radiografia del torace 17 pazienti inseriti nell’ambulatorio per la terapia del tabagismo hanno seguito il corso antifumo per un anno ed al controllo finale hanno ottenuto un’alta percentuale di sospensione (76%): questa percentuale è più alta di quelle presenti in letteratura (approssimativamente 30%). È da ritenere che l’alta incidenza di patologie, anche se in fase iniziale, che la TCms ha permesso di identificare ha rafforzato la motivazione a smettere di fumare. Questa evidenza implica uno studio numericamente ampio per definire il costo-beneficio della TCms, peraltro da destinare soltanto a fumatori decisi a seguire una terapia antifumo. Parole chiave: Fumo, Cessazione dal tabagismo, Tomografia Computerizzata Torace. Summary. To estimate the usefulness of the CTms (Computed Tomography) in the diagnostic assessment of smokers with or without clinical symptoms of pulmonary diseases but with normal indexes of respiratory functionality and X ray thorax negative, 17 patients smokers were introduced to the “ therapy of the tabagism Departement” and followed the antismoking course for 1 year and in follow-up examination they obtained an high percentage of suspension (76.2%); this rate is higher than literature percentages (approximately 30%) . We think that the high incidence of pathologies, even in the early phases, that the CTms has allowed us to identify, has strengthened the patients’ motivation to stop smoking. This evidence deserves a wider numerical study in order to justify the cost-benefit of the CTms: however this exam should be proposed only for smokers confirmed to follow the antismoking therapy. Key words: Smoking, Tobacco-use cessation, Tomography, X-Ray Computed, Chest. INTRODUZIONE Ridurre oggi a metà il consumo di sigarette vuol dire prevenire nell’anno 2020 almeno di 1/3 le morti correlate al fumo: entro il 2050 tali morti verrebbero dimezzate, praticamente evitando fra i 7 ed i 10 milioni di morti previsti per l’anno 2025 in Europa. Aumentare i tassi di disassuefazione dal fumo è perciò l’elemento critico per migliorare la salute della comunità nel breve e medio periodo poiché i fumatori muoiono per malattie fumo-correlate, prevalentemente nell’età compresa fra i 35 ed i 69 anni, calcolata dagli epidemiologi in base all’intervallo di tempo dall’inizio dell’abitudine tabagica e lo sviluppo di una malattia grave, in media 25-30-anni di fumo. Le comuni strategie di sospensione dal fumo si basano solitamente: - rafforzare la motivazione a smettere (il danno alla salute è sicuramente il motivo più frequente riferito dai pazienti); 54 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 - ridurre le manifestazioni di astinenza (terapia farmacologica); - mantenimento della sospensione (idealmente per tutta la vita). PAZIENTI E METODI Al fine di ridurre le percentuali di insuccessi dei pazienti che provano a smettere di fumare abbiamo selezionato 17 fumatori, (10 maschi e 7 femmine) età media 48 anni, afferenti al nostro ambulatorio per la terapia del tabagismo, che fossero ancora negativi ai seguenti esami non invasivi per le malattie cardio-respiratorie fumo-correlate: radiografia del torace, prove di funzionalità respiratoria con broncodilatatore e diffusione al CO, pletismografia, emogasanalisi, elettrocardiogramma. Sei pazienti non riferivano sintomi respiratori, 5 riferivano tosse discontinua, 3 pazienti avevano una dispnea di grado 1 secondo la scala MRC(Medical Research Council modified 2000), 3 pazienti avevano tosse discontinua e dispnea grado 1 MRC. In tali pazienti abbiamo calcolato il Pack/Year (N. sigarette fumate/die x anni di fumo / 20)ottenendo un valore medio di 39 ed abbiamo proposto loro, in presenza di negatività di precedenti esami diagnostici la Tomografia Computerizzata multi strato (TCms) all’inizio della terapia antifumo, al fine di rilevare danni anatomici polmonari non documentabili con i precedenti esami. TCms: Apparecchio Siemens Zoom Volume permette di acquisire l’intero volume polmonare in 25-30 sec. L’esame è stato eseguito in massima inspirazione, in unica apnea. I parametri utilizzati sono stati 120Kv, 100mA con spessore di strato in acquisizione di 5 mm che permette ricostruire sia ad 1,25mm per lo studio in alta risoluzione che a spessori maggiori. Per il calcolo del volume polmonare sono stati inclusi tutti i pixel compresi fra -400 e -1024, mentre i valori soglia utilizzati per quantificare l’enfisema sono compresi fra -900e -1024. Ciò ha permesso di calcolare il volume polmonare totale (CPT) ed il volume occupato da zone patologiche (ipodense) dovute alla presenza di enfisema o ad aree di intrappolamento aereo. Sia nel calcolo del volume polmonare che nel calcolo della percentuale di enfisema non si è evidenziata una significativa differenza fra spessore di strato a 5 mm e spessore di strato a 10mm, mentre rilevante era la differenza se la percentuale di enfisema veniva calcolata utilizzando spessore di strato ad 1,25mm. La radiografia del torace era stata refertata negativamente in tutti i pazienti selezionati ed i valori di alfa1antitripsina controllati a tutti i pz erano nella norma. Il BMI body mass index era molto ridotto in un solo paziente mentre nella media era nella norma. Di tutti i tests respiratori abbiamo selezionato (tabella1) quelli più importanti ai fini diagnostici delle broncopneumopatie croniche ostruttive; il FEV1, nella norma come valore di base, non mostrava variazioni significative dopo l’uso del broncodilatatore; buone erano le correlazioni dei valori di TLC misurati con l’elio, la pletismografia e con la TCms. Il DLCO ha mostrato valori normali nella media. Quindi si sarebbe concluso che tali pazienti fumatori non avevano sviluppato danni all’apparato respiratorio. Tabella 1 Parametri minimo ETÀ 40 Pack/years 20 DispneaMRC 0 BMI (body mass index) 19 DLCO (%t) 66 TI (%) 70 FEF 25-75(%t) 47 RV pl (tot) 37 TLC He (%) 57 TLC PL (%t) 60 TLC ms(ml) 3800 Score-emph% 0 massimo 70 60 1 34 128 85 125 158 127 142 8600 45 media 48,5 39,06 0,1 26,1 97,2 77,2 79,5 112,1 107 107,2 5374,7 20,2 RISULTATI E CONCLUSIONI La possibilità offerta dall’apparecchiatura radiologica di “ricostruire” anche in R. Principe et al.: Indicazioni all’uso della TC ms nell’ambulatorio per la terapia del tabagismo alta risoluzione ha permesso di definire quando presente il tipo di enfisema (e di calcolare anche lo score attraverso il calcolo della TCms), nonché altre patologie, non evidenti alla radiografia standard del torace come bronchiectasie, ispessimenti delle pareti bronchiali, noduli di alcuni millimetri, (questi sono stati ricontrollati a distanza di 3 – 6- e 12 mesi: solo per un nodulo sospetto si è proceduto ad asportazione chirurgica con esame istologico positivo per amartocondroma). Presenti anche frequenti ispessimenti delle pareti bronchiali e lesioni a “vetro smerigliato” (figg. 1, 2 e 3) tipiche delle forme di interstiziopatia polmonare del gruppo RB-ILD (respiratory bronchiolitis with an interstitial lung disease); in un paziente è stato evidenziato e misurato anche Air Trapping. Solo un paziente è risultato completamente negativo alla TCms. (Vedi tab. 2) 55 Figura 1 - Pz con lesione a sin. tipo “ground class”. Tabella 2 – Alterazioni evidenziate alla TCms Pazienti A) ScoreE B)Gro-glas C)Bronch. D)Wall-thic 1 8,5% 3 30% 4 36% 5 20% 6 10% ° * x 10 mm ° ° 16% 9 x x x x 32% Figura 2 - Pz. con enfisema lobi superiori, centrolobulare e parasettale. x x 7 10 F)Air-tra 5 mm 2 8 E)Nodules 3 mm x 11 12 33% 13 45% 14 41% 15 22% x 16 15% x 17 33% ° ° x 8mmAm4m x x ° ° x I pazienti sono stati informati dei danni riscontrati con la TCms ed hanno iniziato tutti il corso antifumo che si articola in un incontro settimanale per due mesi quindi un incontro ogni quindici giorni Figura 3 - Pz con bronchiectasie lobo superiore sinistro. per 2 mesi ed un incontro al mese per un anno dalla cessazione dal fumo (per controllare le eventuali ricadute). Durante 56 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 tali incontri si svolge la terapia comportamentale-farmacologica come da Linee Guida. I farmaci usati sono stati i sostituti della nicotina (nelle diverse formulazioni) e/o il bupropione. Con tali trattamenti si ha una sospensione dal fumo, in media del 30-40% ad un anno (solo il 23% invece quando il pz. affronta il problema da solo), come documentato nella letteratura scientifica e come si ottiene abitualmente anche nel nostro ambulatorio per la terapia del tabagismo. Al contrario nei 17 pazienti sottoposti anche a TCms ad un follow-up a un anno si è ottenuto una sospensione del fumo nel 76,2%, dato molto il più alto rispetto alle percentuali sopra citate, per cui è da ritenere al riguardo che l’alta incidenza di patologie respiratorie, anche se in fase iniziale, che la TCms ha permesso di identificare e quindi di comunicare ai pazienti, ha rafforzato in loro la motivazione di sospensione del tabacco. Questa evidenza necessita certamente di studi numericamente più alti, per giustificare il costo-beneficio della TCms, che comunque andrebbe proposta non a tutti i fumatori ma almeno a coloro che iniziano la terapia del tabagismo con determinazione. I Centri sanitari di II livello per la terapia del tabagismo dovrebbero pertanto insistere, oltre che su una terapia comportamentale – farmacologica anche sulla ricerca diagnostica mirata delle patologie fumo-correlate; poiché questa può essere in molti casi la motivazione più forte per portare alla decisione non solo di iniziare ma anche di proseguire la terapia del tabagismo. ____ Per richiesta estratti: Dott.ssa R. Principe - III U.O.C. di Pneumologia Ospedale Forlanini - Via Portuense, 332 - 00149 Roma BIBLIOGRAFIA ESSENZIALE Barbano G,Bressan MC,Nardini S.Strategie e risultati della disassuefazione dal fumo. Allergy and Respiratory Diseases.2004;2:76-87 Mastora I, Remy-Jardin M,Sobaszek A et al. Thin section finding in 250 volunteers: assessment of the relationship of CT findings with smoking history and polmonary function test results. Radiology 2001; 218:695-702 Muller-Leisse C, Otto A, Berger F, et Al: The recording of parenchimal lung changes in smokers by high resolution computed tomography Rofo Fortschr Geb Rontgenstr Neuen Bildgetb Verfahr 1997; 166:108-14 Nardini S,Bertoletti R,Carrozzi L, Sabato E.Raccomandazioni per la attivazione e la gestione di un ambulatorio per il trattamento della dipendenza da fumo di tabacco in ambito pneumologico. Rass. Patol.App. Resp.2000;15:3Suppl Peto R.Lopez AD.The future worldwide health effects of current smoking patterns.In:Koop CE,Pearson CE,Swarz MR,eds. Critical issues in global health.San Francisco,CA:Jossey-Bass 2000:154-61 Remj-Jardin M, Edme JL, Boulenguez C, et al: Longitudinal follow-up studi of smoker’s lung with thin-secti CT in correlation with pulmonary function test. Radiology 2002 ; 222: 261-70 Spaggiari E, Zompatori M, Verduri A, et Al:Danno polmonare precoce da fumo in soggetti asintomatici. Studio correlativo con TC dinamica ad elevata risoluzione e test di funzionalità respiratoria Rad Med 2005;109:27-39 Swan Ge,McAfee T, Curry SJ, et al. Effectiveness of bupropion sustained release for smoking cessation in a health care setting: a randomized trial.Arch Intern Med 2003;163:2337-44. Webb WR,Muller Nl, Naidich DP High Resolution CT of the lung, third edition. Philadelphia: Lippincott Williams& Wilkins. 2001 : 449-57. Zompatori M, Fasano L, Mazzoli M et al: Valutazione quantitativa dell’enfisema polmonare con Tomografia Computerizzata (TC) spirale a bassa dose Radiol. Med 2005;109:27-39 ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 Caso clinico CAPTAZIONE DEL 99MTC-MDP IN UN CASO DI AMILOIDOSI CARDIACA 99MTC-MDP UPTAKE IN A CASE OF HEART AMYLOIDOSIS ALESSIO ANNOVAZZI, GUIDO VENTRONI, EDO PICCHIO1, CLAUDIA AMIDEI, CLAUDIO TORRINI, LUCIO MANGO Servizio di Medicina Nucleare e Reparto Scompenso-II Cardiologia1 Azienda Ospedaliera San Camillo-Forlanini - Roma Riassunto. Gli autori descrivono un caso clinico di una paziente affetta da carcinoma mammario e amiloidosi cardiaca da accumulo di tiretina, sottoposta a scintigrafia ossea per la ricerca di lesioni metastatiche, in cui si osserva un intenso accumulo cardiaco di 99mTc-Metilendifosfonato (99mTc-MDP). Vengono poi passati in rassegna i principali radiofarmaci utilizzati nello studio dell’amiloidosi. Parole chiave: Amiloidosi, Scintigrafia ossea, 99mTc-MDP. Summary. The authors describe a clinical case of a patient affected by breast carcinoma and heart amyloidosis due to tiretin deposits, who performed a bone scan for the evaluation of bone metastases, in which an intense cardiac uptake of 99mTc-MDP was observed. All the principal radiopharmaceuticals for the study of amyloidosis are discussed in the text. Key words: Amyloidosis, Bone scanning, Technetium Tc 99mMDP. INTRODUZIONE Con il termine amiloidosi ci si riferisce ad un gruppo di patologie diverse, tutte caratterizzate dalla deposizione extracellulare di proteine fibrillari insolubili. Tali proteine mostrano la classica configurazione secondaria a foglietto b e dopo colorazione al Rosso Congo presentano un colore verde al microscopio ottico a luce polarizzata. Si distinguono alcune forme acquisite che possono essere associate ad accumulo delle catene leggere delle immunoglobuline (AL) o della proteina sierica dell’amiloide A (AA). Un’altra forma acquisita è quella legata alla beta microglobulina che si può osservare nei pazienti in corso di trattamento emodialitico. Le forme familiari possono essere dovute a deposito di fibrinogeno, lisozima, apolipo- proteine, transtiretina. L’incidenza dell’amiloidosi è valutata intorno a 8-10 casi/1.000.000 di abitanti1, tuttavia è sicuramente sottostimata, data l’elevata incidenza di forme asintomatiche. La diagnosi definitiva viene ottenuta mediante biopsia dell’organo interessato dalla patologia. I depositi di amiloide possono osservarsi virtualmente in qualsiasi organo o tessuto e generalmente sono più comunemente localizzati in sede peri-vascolare. Il 99mTc-metilendifosfonato (99mTcMDP) è un radiofarmaco utilizzato per la scintigrafia ossea dato il suo elevato tropismo per l’osso in corso di rimodellamento, ma può accumularsi in modo aspecifico nei tumori, nei focolai di infiammazione, nelle calcificazioni distrofiche e metastatiche e nell’amiloidosi. 58 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 CASO CLINICO La paziente D.M. di 55 anni è stata ricoverata presso il nostro nosocomio per il peggioramento di una condizione di scompenso cardiaco da cardiomiopatia restrittiva dovuta ad amiloidosi primitiva familiare da accumulo di transtiretina. La paziente è stata inserita in lista d’attesa per trapianto duplice di cuore-fegato. Un’ecocardiogramma metteva in evidenza un versamento di moderata entità in assenza di segni di tamponamento cardiaco. Nella norma gli indici di funzione sistolica globale e segmentaria, mentre il ventricolo sinistro appariva di ridotte dimensioni con notevole incremento degli spessori parietali ad aspetto granulare. Nel corso del ricovero la paziente è stata sottoposta a scintigrafia ossea total-body con 99mTc-MDP per la ricerca di possibili lesioni metastatiche da recidiva locale di carcinoma mammario dx. Le immagini scintigrafiche non evidenziavano la presenza di localizzazioni ossee metastatiche, mentre è stato osservato un intenso e diffuso accumulo del 99mTc-MDP in corrispondenza dell’aia cardiaca (figura 1). Quale reperto occasionale si è osservata la localizzazione pelvica del rene destro già precedentemente diagnosticata ecograficamente. DISCUSSIONE Il primo lavoro che ha descritto l’accumulo del 99mTc-MDP nell’amiloidosi è da attribuire a VanAntwerp2. Il meccanismo preciso dell’accumulo del 99mTc-MDP nei depositi di sostanza amiloide non è stato identificato, ma l’intensità della captazione nelle sedi interessate non può essere spiegata semplicemente con un meccanismo di accumulo aspecifico, come quello osservato nei tessuti infiammati per iperemia ed aumento del volume interstiziale. La scintigrafia con 99mTc-MDP è stata proposta come tecnica non invasiva per determinare l’estensione dell’amiloidosi in tutti i distretti corporei, in pazienti già diagnosticati3. Dai diversi studi effettuati, emerge tuttavia la bassa sensibilità della metodica rispetto all’ecocardiografia nello studio del coinvolgimento cardiaco. Altri radiofarmaci sono stati efficacemente utilizzati nello studio della amiloido- PIXIE Info Box ID: CARD 2 OSS Acq: 11/3/2005 12:42:42 Whole Body Tc-99m Activity: 18.0 mCi Acq Matrix: 256x1024 Collimator: LEHR-Par Mag: 1.13 File: R2 Image ID: Raw Data Acq ID: WholeBody View: Post Organ: Ossea Slice 2.06 mm Len: 180 cm 14.6 cm/min Win: 83.0% Bas: 0.0% Forlanini Roma Figura 1. Scintigrafia ossea (99mTc-MDP)della paziente in proiezione anteriore. si. La proteina serica dell’amiloide P (SAP) è stata marcata con iodio-131 ed impiegata nello studio di molte forme di amiloidosi. Questo radiofarmaco tuttavia non ha riscosso un grande successo, dato lo scarso accumulo nella amiloidosi cardiaca, che è quella più importante da un punto di vista prognostico. Le non ottimali caratteristiche di questo radiofarmaco sono da ricercare nell’elevato peso molecolare (254.62 KDa), che ne ostacola il passaggio attraverso i capillari endoteliali cardiaci4 e nelle scarse qualità fisiche dello iodio-131 (emissione gamma ad alta energia, 364 KeV). Un radiofarmaco alternativo è rappresentato dalla aprotinina, una piccola proteina di 6.5 KDa estratta dal polmone bovino, marcata con il tecnezio-99m. Questa proteina interagisce con le fibrille della sostanza amiloide attraverso un’interazione tra i foglietti b che caratterizzano entrambe le proteine; on questo radiofarmaco sono stati studiati più A. Annovazzi et al.: Captazione del 99mTc-MDP in un caso di amiloidosi cardiaca di 200 pazienti con diverse forme di amiloidosi5. La 99mTc-aprotinina è in grado di visualizzare il coinvolgimento amiloidosico di tutti i parenchimi, con l’eccezione del rene dove viene eliminato fisiologicamente6. In particolare, nella valutazione del coinvolgimento cardiaco, la 99mTc-aprotinina mostra un’accuratezza diagnostica di 0.96, che è superiore a quella raggiunta dallo studio elettro- ed ecocardiografico7. Questi risultati promettenti sono stati recentemente confermati da un gruppo danese su 23 pazienti con amiloidosi sospetta o già diagnosticata8. In particolare questo radiofarmaco è stato in grado di identificare alcune lesioni occulte in 5 pazienti che successivamente hanno sviluppato la sintomatologia clinica. Altri radiofarmaci sono stati impiegati nello studio dell’amiloidosi, come la beta-2-microglobulina e l’acido dimercaptosuccinico pentavalente (DMSA-V)9,10. Infine, recentemente è stata osservata una intensa captazione del 18F-Fluorodessosiglucosio (18FFDG) in una lesione amiloidosica del polmone nel corso di un esame PET11. Questa recente osservazione potrebbe suggerire l’impiego della PET come tecnica promettente anche nello studio dell’amiloidosi. BIBLIOGRAFIA 1. Falk RH, Skinner M. The systemic amyloidosis: an overview. Adv Intern Med 2000; 45: 107-37. 2. VanAntwerp JD, O'Mara RE, Pitt MJ, Walsh S. 59 Technetium-99m-diphosphonate accumulation in amyloid. J Nucl Med 1975; 16: 238-40. 3. Janssen S, Piers DA, van Rijswijk MH, Meijer S, Mandema E. Soft-tissue uptake of 99mTcdiphosphonate and 99mTc-pyrophosphate in amyloidosis. Eur J Nucl Med 1990; 16: 663-70. 4. Hawkins PN, Aprile C, Capri G, et al. Scintigraphic imaging and turnover studies with iodine-131 labelled serum amyloid P component in systemic amyloidosis. Eur J Nucl Med 1998; 25: 701-8. 5. Cardoso I, Pereira PJ, Damas AM, Saraiva MJ. Aprotinin binding to amyloid fibrils. Eur J Biochem 2000; 267: 2307-11. 6. Aprile C, Marinone G, Saponaro R, Bonino C, Merlini G. Cardiac and pleuropulmonary AL amyloid imaging with technetium-99m labelled aprotinin. Eur J Nucl Med 1995; 22: 1393-401. 7. Aprile C, Merlini G, Saponaro R, et al. Risk stratification of cardiac event in patients with AL/AF amyloidosis by means of 99mTc-aprotinin myocardial scan [abstract]. Eur J Nucl Med 1998; 25: s26. 8. Schaadt BK, Hendel HW, Gimsing P, Jonsson V, Pedersen H, Hesse B. 99mTc-aprotinin scintigraphy in amyloidosis.J Nucl Med 2003; 44: 177-83. 9. Schaffer J, Burchert W, Floege J, et al. Recombinant versus natural human 111In-beta2-microglobulin for scintigraphic detection of Abeta2m amyloid in dialysis patients. Kidney Int 2000; 58: 873-80. 10. Ohta H, Endo K, Kanoh T, Konishi J, Kotoura H. Technetium-99m (V) DMSA uptake in amyloidosis. J Nucl Med 1989; 30: 2049-52. 11. Kung J, Zhuang H, Yu JQ, Duarte PS, Alavi A. Intense fluorodeoxyglucose activity in pulmonary amyloid lesions on positron emission tomography. Clin Nucl Med 2003; 28: 975-6. ____ Per richiesta estratti: Prof. Lucio Mango - Servizio di Medicina Nucleare Ospedale Forlanini - Via Portuense, 332 - 00149 Roma ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 Gestione e organizzazione sanitaria PSICOTERAPIA DI GRUPPO PER PAZIENTI CON SCLEROSI MULTIPLA: SPECIFICITÀ E METODOLOGIA GROUP PSYCHOTHERAPY FOR PATIENTS WITH MULTIPLE SCLEROSIS: SPECIFICITY AND METHODOLOGY MARCO SPARVOLI - ELISABETTA PODRASKY Servizio di Diagnosi e Cura, Ospedale Forlanini. Azienda Ospedaliera San Camillo-Forlanini - Roma Riassunto. Scopo di questo articolo è descrivere come nel trattamento di pazienti con sclerosi multipla le terapie psicologiche, individuali e di gruppo, siano efficaci nel migliorare lo stato emotivoaffettivo del paziente e la capacità di prendersi attivamente cura della malattia. Il lavoro si è basato principalmente sulla possibilità di favorire l’accettazione della malattia da parte del paziente. Questo ha permesso di facilitare la compliance con il sistema medico e un’assunzione di ruolo più responsabile e attivo, con conseguente miglioramento dei sintomi depressivi. L’orientamento psicoterapeutico utilizzato è di tipo analitico, ma prevede delle specifiche variazioni del setting elaborate sulla base della presenza di una patologia organica e agli specifici problemi legati ad essa. Parole chiave: Sclerosi multipla/terapie psicologiche, Psicoterapia, Terapia di gruppo. Summary. The aim of this study is to describe how, in the treatment of multiple sclerosis, psychological individual and group therapy can have good effects on depression and can improve the patient’s capacity of taking actively care of himself. Work was particularly based on the acceptance of the illness by the patient. This has facilitated the compliance with the medical caregiving system and a more responsable and active role, with consequent benefits in depressive symptoms. Psychological treatment was analytically oriented, with specific variations in the setting in agreement with the organic illness and its related problems. Key words: Multiple sclerosis/psychology, Psychotherapy, Psychotherapy group. La sclerosi multipla, malattia organica che minaccia la vita, si ripercuote sull’intera esistenza, cambiandola a volte radicalmente. Nei casi meno sintomatici il paziente deve sottoporsi a continui esami e trattamenti medici e convivere con il fatto di avere una patologia organica attualmente inguaribile. Nei casi più sintomatici il paziente deve abbandonare molte delle attività precedenti alla malattia o cambiare completamente stile di vita (ad esempio lasciare il posto di lavoro o muoversi con la sedie a rotelle). Diversi studi confermano una maggiore prevalenza di disturbi della sfera emotiva-affettiva in pazienti affetti da sclero- si multipla rispetto alla popolazione generale. I pazienti con sclerosi multipla presentano una maggiore frequenza di sintomi depressivi rispetto alla popolazione sana1 ed elevati livelli di ansia2. Una ricerca condotta da Mohr su persone affette da sclerosi multipla evidenzia una prevalenza del 14-57% di sintomi depressivi, 63% di euforia e 19-34% di disturbi d’ansia3. Il modo in cui i pazienti gestiscono lo stress e i problemi sociali sembra influire decisivamente sui sintomi depressivi. Le strategie di evitamento sono infatti correlate con sintomi depressivi più elevati, mentre l’uso di strategie di problem solving e di coping attivo è correlato con sin- M. Sparvoli et al.: Psicoterapia di gruppo per pazienti con sclerosi multipla tomi minori4. Alcuni studi indicano inoltre, che lo stress psicologico può rappresentare un fattore di rischio per l’aggravamento della malattia5. Una buona conoscenza della malattia e una diminuzione dei sintomi sono correlati ad un miglioramento dello stato emotivo6. Da questo studio emerge inoltre, che la soddisfazione rispetto al sistema curante e il coinvolgimento in attività terapeutiche per la cura della sclerosi multipla, influiscono positivamente sullo stato emotivo. Diverse ricerche7,8 hanno evidenziato che le psicoterapie hanno effetti positivi sui pazienti con sclerosi multipla. Da queste ricerche emerge che i pazienti appaiono meno rassegnati, meno disperati, e fisicamente rinvigoriti, riportando la sensazione di avere una maggiore energia fisica a disposizione. La psicoterapia di gruppo in particolare evidenzia cambiamenti significativi nell’area relazionale e in questa sede viene descritto come le terapie psicologiche razionalmente organizzate e condotte possano diminuire i sintomi depressivi e migliorare la compliance con il sistema medico. Scopo della terapia psicologica è favorire l’accettazione della malattia, aiutando il paziente ad affrontare i problemi e i vissuti emotivi legati ad essa. METODOLOGIA PER LA FUNZIONE DI UN GRUPPO TERAPEUTICO Il gruppo per pazienti con sclerosi multipla, ad orientamento gruppoanalitico, deve prevedere la partecipazione di un massimo di 8 - 10 partecipanti. Gli incontri, della durata di un’ora e mezza, si svolgono ogni 15 giorni e sono condotti da uno psicoterapeuta. Nel caso si ritenesse opportuno vengono affiancati incontri individuali. Al gruppo, di tipo monosintomatico, partecipano solo pazienti affetti da sclerosi multipla, senza distinzione in base alla forma o alla gravità dei sintomi. È un gruppo aperto (slow-open), ovvero possono essere inseriti nuovi partecipanti. La durata del percorso non ha un tempo prestabilito, bensì è valutato in base al singolo paziente e nel corso del trattamento. La scelta di un formato terapeutico gruppale, nasce dalla possibilità di offrire 61 in gruppo una maggiore condivisione empatica e cognitiva dei diversi aspetti della malattia. Poter parlare e condividere con altri permette al paziente di sentirsi meno solo, incompreso ed unico. Questo aiuta ad uscire dal senso di isolamento e fa emergere nuove energie che rendono possibile il prendersi attivamente cura di sé. Il paziente sente a volte di dover celare a familiari e conoscenti temi penosi legati alla malattia e emozioni ad essi connessi. Teme di generare preoccupazione, di non essere compreso o di venire giudicato. Le paure e le emozioni negative in questo modo non possono essere liberamente sfogate e vanno affrontate in solitudine. È per questo importante poter disporre di uno spazio nel quale affrontare questi temi senza sensi di colpa e senza il timore di ferire l’altro. Il paziente può sentirsi sollevato dal fatto che gli altri partecipanti del gruppo comprendono il suo stato d’animo e lo condividono. Alcune difficoltà specifiche della malattia (come ad esempio disturbi motori, disfunzioni sessuali, problemi di minzione) sono trattate con riserbo e vergogna e a volte condivisibili solo con persone che stanno vivendo problemi analoghi. La scelta del gruppo nasce anche dalla possibilità di aumentare la conoscenza dei singoli rispetto alla malattia. Ogni partecipante porta infatti la sua conoscenza ed esperienza, ed è in grado di volta in volta di aggiungere qualcosa al sapere dell’altro o di imparare qualcosa dall’altro. La maggiore conoscenza della malattia può aiutare il paziente ad avere un ruolo più attivo e responsabile rispetto ad essa, sia nel rapporto con i medici che nelle possibili terapie da seguire. Inoltre, data la natura ancora sconosciuta della sclerosi multipla e soprattutto della cura, è di sostegno e aiuto poter condividere con gli altri le incertezze che contraddistinguono la patologia. La diagnosi della malattia e le informazioni ad essa connessa possono generare intense reazioni emotive. Il paziente in questa fase può essere incapace di ricevere altre informazioni e di agire conseguentemente. Questo stato emotivo può durare a lungo e diminuire le capacità di 62 Annali degli Ospedali San Camillo e Forlanini 8, 3, 2006 accedere ad un atteggiamento attivo nella cura (in questo caso il paziente adotta uno stile di coping passivo centrato sull’informazione). L’elaborazione dei vissuti interiori e delle emozioni, possibile nel corso di una terapia di gruppo, aumenta la consapevolezza del paziente e la capacità di fronteggiare la situazione in modo più attivo, passando ad uno stile di coping centrato sul problema. Lo stile di coping centrato sul problema viene facilitato in gruppo dalla presenza e degli altri partecipanti, dai quali è possibile osservare modi diversi di reagire e apprendere ad utilizzare quello più utile nelle diverse situazioni e con i quali è possibile confrontarsi. La conoscenza degli altri diventa inoltre un valido aiuto anche nel trovare soluzioni ai problemi materiali e concreti che la sclerosi multipla implica. Il gruppo è un luogo nel quale ricevere informazioni rispetto all’assegno di invalidità, il permesso per la macchina, le strutture provviste delle attrezzature per disabili, etc. È dunque una fonte di informazioni per affrontare meglio i disagi che la malattia può comportare. La terapia di gruppo per pazienti con patologia organica, a differenza del classico setting gruppoanalitico, sollecita il sostegno ed i legami anche fuori dal gruppo. La malattia comporta a volte un ritiro sociale, dovuto allo stato emotivo-affettivo oppure alle difficoltà motorie. Proseguire le relazioni anche fuori dal gruppo può dunque essere un’importante fonte di sostegno. È inoltre importante riportare in primo piano la progettualità in relazione al ciclo di vita. La presenza della malattia va desaturata, per dare spazio ai compiti esistenziali che il ciclo di vita rende necessario affrontare. In altri casi sembra invece che la malattia sia fortemente evitata, con conseguenze pericolose per la vita del paziente. È fondamentale poter fare un’analisi realistica della situazione con il paziente. In questo modo è possibile trovare le soluzioni più utili al suo progetto di vita e all’attuale ciclo di vita. In gruppo il paziente può inoltre sperimentare se stesso come persona capace di aiutare l’altro, scoprendosi quindi possessore di alcune competenze. Questa possi- bilità di assumere un ruolo competente, di Io ausiliario, consente di riappropriarsi degli aspetti positivi e generativi del sé, che spesso la malattia sembra aver distrutto. A dimostrazione di quanto si debba organizzare e gestire al meglio questo settore viene illustrato il caso di G. che partecipa ad un incontro di gruppo. È una donna di 40 anni, sposata, casalinga, con una bambina piccola partorita alcuni anni dopo aver appreso di essere malata di sclerosi multipla. L’esordio della malattia risale ad 8 anni fa. Cammina con difficoltà, aiutandosi con un bastone. Ha smesso di andare dal medico da un anno. “Non mi dava fiducia e comunque le cure non sono state d’aiuto, anzi stavo peggio. Non ho alcuna intenzione di iniziare un nuovo trattamento o di consultare un altro medico.” Parallelamente sembra mancare un investimento generale nelle attività della vita. La stessa gestione della figlia è in parte delegata alla famiglia d’origine. Il suo atteggiamento è contraddistinto da rassegnazione ed apatia. Non torna agli incontri successivi di gruppo e non contatta la terapeuta. Invitata telefonicamente a venire in gruppo, spiega, adducendo varie scuse, che non le è possibile in questo momento. Le si propone un incontro individuale, pensando che questo tipo di setting possa essere più rassicurante e meno esposto al confronto con la malattia. Anche in questo caso G. rifiuta cordialmente. Riflettiamo a lungo con l’equipè terapeutica su cosa sia possibile fare per non perdere G. dal campo terapeutico. Decidiamo di allargare il setting terapeutico ai familiari. In questo modo anche se G. si rifiutasse di venire all’incontro, si avrebbero altri interlocutori con i quali dialogare per comprendere meglio cosa le stia succedendo e come sia possibile aiutarla. Chiamata nuovamente, G. accetta l’incontro. Al primo colloquio appare confusa. Spiega che la malattia la rende molto debole. Appare stanca, meno oppositiva rispetto alle cure mediche, come se questo incontro rappresentasse un primo difficile passo nell’accettazione della malattia e spiega che ha sentito i nostri interventi forti, ma non intrusivi. G. ha percepito l’autentica M. Sparvoli et al.: Psicoterapia di gruppo per pazienti con sclerosi multipla preoccupazione e lo sforzo per non perderla dal campo terapeutico. Dopo questo incontro abbiamo intrapreso un percorso terapeutico. Adesso G. è seguita da un neurologo, per una terapia e segue regolarmente una fisioterapia. Questo diverso atteggiamento nei confronti della malattia ha condotto ad una maggiore cura di sé, dei rapporti sociali e della gestione familiare. Il suo tentativo di fuggire al gruppo e alle cure mediche ha probabilmente rappresentato il suo modo per evitare di entrare realmente in contatto con le emozioni suscitate dalla malattia. Accettare la sclerosi multipla per G. è stato doloroso, ma le ha permesso lentamente di gestire la sua vita in modo più attivo. CONCLUSIONI Diverse ricerche confermano una correlazione tra sclerosi multipla e disturbi della sfera emotiva-affettiva. L’esperienza di un gruppo ad orientamento gruppoanalitico indica che la psicoterapia produce un miglioramento dello stato emotivo-affettivo, al quale corrisponde una maggiore aderenza ai trattamenti medici. Queste due variabili appaiono intimamente connesse. Lo stato affettivo infatti influisce sulla capacità del paziente di prendersi cura di sé e il coinvolgimento in attività terapeutiche soddisfacenti influisce a sua volta positivamente sullo stato affettivo. Appare quindi fondamentale per il paziente poter accettare la malattia e farsi carico della responsabilità di prendersene cura. In questo modo può nuovamente percepirsi come soggetto attivo, nonostante le difficoltà che possono emergere a causa della malattia. La psicoterapia di gruppo può essere uno strumento molto utile nel favorire l’accettazione della malattia e nel migliorare lo stato emotivo, in quanto permette la condivisione con altri dei problemi e delle emozioni legati ad essa. Offre inoltre la possibilità di uscire dal senso di isolamento e di unicità che spesso accompagna una patologia organica. In gruppo è possibile riscoprirsi capace di ricevere e dare aiuto e di essere possessori di competenze. In questo modo le parti del 63 sé, rese fragili dalla malattia, si possono riappropriare degli aspetti positivi. Altro elemento importante per la psicoterapia con pazienti con sclerosi multipla è la possibilità di mantenere un setting variabile, che si possa costruire intorno al paziente e alle sue necessità. Il paziente deve percepire l’autentico interesse del terapeuta al suo stato psicofisico e alla sua responsabilità di prendersi cura di sè. Il terapeuta deve mantenere una certa flessibilità e scegliere, a seconda del caso e del corso della terapia, quale tipo di intervento proporre per mantenere il paziente all’interno del campo terapeutico. BIBLIOGRAFIA 1) Dalton E J, Heinrichs R W. Depression in multiple sclerosis: a quantitative review of the evidence. Neuropsychology 2005; 19: 152-8. 2) Maurelli M. Neuropsychological assessment in MS: clinical neuropsychological and neuroradiological relationships. Acta Neurol Scand 1992; 86: 124-8. 3) Mohr DC, Dick LP. Multiple Sclerosis. In: Camic P., Knight, S. Eds. Clinical handbook of health psychology. Seattle: Hogrefe &Publishers, 1998: 313-48. 4) Mohr DC, Goodkin DE, Van Wende J. Depression, coping and level of neurologic impairment in multiple sclerosis. Mult Scler 1997; 3: 254-8. 5) Nisipeanu P, Korkczyn AD. Psychological stress as risk factor for exacerbations in multiple sclerosis. Neurology 1993; 43: 1311-2. 6) Pavlou M, Conte M. Aspects of coping in multiple sclerosis. Rehabilitation Counselling Bulletin 1982; 25: 138-145. 7) Langenmayr A, Schottes N. Psychotherapy with multiple-sclerosis patients. Psychol Rep 2000; 86: 495-508. 8) Tesar N, Baumhackl U, Kopp M, Guenther V. Effects of psychological group therapy in patients with multiple sclerosis. Acta Neurol Scand 2003; 107: 394-399. Per richiesta estratti: Dott. Elisabetta Podrasky Via G. B. Falcone, 10 - 00149 Roma Tel. 06 5503481 ANNALI DEGLI OSPEDALI San Camillo e Forlanini Volume 8, Numero 3, Luglio-Settembre 2006 Recensione “SESSANTESIMO ANNIVERSARIO” I tre volumi con i quali è stato celebrato il “Sessantesimo Anniversario” (1946-2006) di Recenti Progressi in Medicina (Il Pensiero Scientifico Editore, Roma , ottobre-dicembre 2006, pagg. 294) titolano rispettivamente, “Il Mondo, Il Medico, le Persone”, “Sanità: Ricerca, Tecnologia” e “Medicina Domani”. Nei 39 articoli che si presentano in realtà come veri e propri capitoli, vengono trattati (ad opera di prestigiosi Autori nelle rispettive competenze) argomenti che percorrono sostanzialmente tutto il campo della Sanità, da quello clinico-ospedaliero a quelli della prevenzione, della medicina palliativa, della telemedicina, dell’etica, ecc.. Nel primo Roberto Bertollini, Direttore Programma speciale Salute ed Ambiente, OMS, Ufficio Regionale per l’Europa, sottolinea quanto siano necessarie strategie di sanità pubblica che, oltre ad utilizzare in modo realmente efficace le soluzioni sperimentate per affrontare i problemi ambientali che l’Autore definisce “tradizionali” (il trattamento delle acque di scarico, l’accesso a fonti sicure di acqua potabile, ecc.), si impegnino alla realizzazione di interventi multisettoriali ed efficaci per affrontare i rischi “emergenti” (quali gli effetti a breve e lungo termine dell’inquinamento chimico ambientale diffuso, ecc.), e per riempire di contenuti il Piano di azione per l’infanzia, la salute e l’ambiente delineato sin dal 2004 alla 4ª Conferenza Interministeriale tenutasi a Budapest. Nel secondo degli articoli sopraccitati, Elio Guzzanti già Ministro della Sanità ed attualmente Direttore Scientifico di IRCCS, dopo aver tracciato il lungo percorso degli eventi più significativi delle origini e delle evoluzioni degli ospedali in Italia e in altri paesi industrializzati, sottolinea di poter ravvisare in prospettiva “la tendenza verso l’ospedale quale componente di un complesso e articolato sistema sanitario che sia sicuro, efficace, centrato sul paziente, tempestivo, efficiente ed equo”. A giudizio di un grande esperto quale Guzzanti la risposta migliore per indirizzare con certezza il futuro assetto della sanità è quella di contenere il numero degli ospedali e di costruire i nuovi con criteri che siano rispettosi della centralità del paziente e caratterizzati da adeguata flessibilità mirata ad agevolare la destinazione degli spazi verso le esigenze del futuro. Tutto dovrà essere integrato con i servizi dell’assistenza territoriale attraverso il potenziamento di quella domiciliare e residenziale in modo da ricomporre, utilizzando i progressi della tecnologia, dell’informazione e della comunicazione, quella continuità assistenziale sinora assai sbandierata, ma non altrettanto realizzata. Nell’articolo sulle “false novità della ricerca clinica” le voci congiunte di Silvio Garattini e Vittorio Bertelè dell’Istituto di Ricerche farmacologiche “Mario Negri” sostengono, sulla base di oggettive evidenze che l’area farmacologica non è così ricca di innovazione come possono far credere i clamori mediatico-pubblicitari creando in tal modo una falsa immagine di novità nel settore farmaceutico. Ne consegue che l’obiettivo prioritario dello sviluppo di un farmaco (cioè l’interesse dei pazienti) spesso viene orientato verso quello commerciale delle imprese che, pur legittimo, deve rimanere subordinato a quello della salute pubblica. Sulla base di documentati esempi al riguardo, gli AA. concludono che gli svariati condizionamenti che influenzano il vero ed il falso in medicina (quali conflitti di interesse finanziario e di altra natura, ecc.) trovano un punto nodale nella dipendenza politica ed economica dell’EMEA (European Medicine Agengy), che è l’Agenzia che decide l’autorizzazione, la revoca e quant’altro abbia a che fare con la politica del farmaco in Europa e che attualmente dipende dal Dicastero Europeo dell’Industria e non già da quello della Salute. I tre volumi dedicati al “Sessantesimo Anniversario” – raccolti coerentemente in uno spartano quanto elegante contenitore – rappresentano una preziosa fonte di informazione, di aggiornamento e forzanche di autocritica non soltanto per quanti hanno collaborato per decenni, in diversi ruoli, con l’entourage della prestigiosa Rivista diretta da Francesco De Fiore, ma anche per tutti coloro che hanno a cuore il futuro della salute individuale ed il futuro della sanità pubblica. Franco Salvati
Scaricare