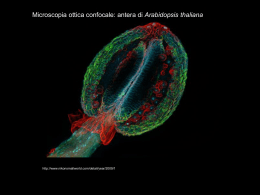
Metodi di studio Il primo microscopio ottico Un microscopio semplice Hooke, 1665 Un moderno microscopio Microscopi ottici da esercitazione Anatomia di un microscopio Fotocamera o telecamera Oculari Stativo Fonte di illuminazione Vite macrometrica e micrometrica Revolver con obiettivi Tavolino traslatore Condensatore Diaframma di campo Anatomia di un microscopio Anatomia di un microscopio Anatomia di un microscopio Microscopia Ottica Microscopia Ottica OSSERVAZIONI A FRESCO • Prime osservazioni • • Il preparato si deteriora velocemente Poco informative • Descrizioni brevi ed inesatte Preparati in campo chiaro a goccia schiacciata Su un vetrino porta-oggetto si pone una goccia di acqua o soluzione fisiologica Il materiale da osservare viene posto sulla goccia ed osservato Preparati in campo chiaro Un batterio Campo chiaro, 1000x Cellul e Microscopia Ottica a Contrasto di fase • Gli oggetti visti in campo chiaro hanno poco contrasto • Per migliorare le immagini è possibile sfruttare le lievi differenze di indice di rifrazione del materiale da osservare rispetto al mezzo circostante • Applicando nel condensatore delle variazioni di fase alla luce che raggiunge il preparato e applicando variazioni opposte nell’obiettivo • I raggi luminosi che sono stati modificati generano fenomeni di interferenza che rendono più chiari o più scuri gli oggetti illuminati Microscopia Ottica a Contrasto di fase Permette, tramite sistema di lenti di osservare le cellule a fresco Le varie parti della cellula appaiono come strutture con diverse tonalità di grigio Un batterio 400x Un lievito (S. cerevisiae) 400x Una muffa (G. candidum) 400x Osservazione in campo scuro Un particolare tipo di condensatore nell’osservazione in campo scuro consente di deviare i fasci di luce in modo che le lenti frontali dell’obiettivo siano attraversati soltanto dai raggi di luce diffratti o diffusi dal preparato. Gli oggetti appariranno chiari su uno sfondo scuro. In questo modo è possibile osservare oggetti anche al di sotto del potere di risoluzione del microscopio ottico Osservazione in campo scuro Uso di colorazioni per migliorare il contrasto dei preparati Utilizzando diverse classi di coloranti è possibile migliorare il contrasto delle immagini al microscopio Coloranti vitali Le cellule possono essere colorate senza fissazione e sono quindi solo minimamente alterate dal trattamento Oggi vengono utilizzati coloranti fluorescenti per colorare selettivamente specie diverse o strutture cellulari diverse Coloranti che richiedono fissazione Le cellule devono essere disidratate prima della colorazione, con possibile alterazione delle strutture cellulari e della forma delle cellule Preparazione di un Campione Biologico per la Microscopia Ottica • Acquisizione del campione e taglio in pezzi • • (1cm3) Biopsia, intervento chirurgico, autospia postmortem Prelevato rapidamente utilizzando strumenti adatti (bisturi) • Fissaggio del campione (immobilizzare, "uccidere" e preservare) • Generalmente per mezzo di aldeidi reattive (formaldeide) • Cross-link delle macromolecole, in particolare le proteine • Si ottiene un effetto indurente sui tessuti "molli" • Deve essere fatto rapidamente per evitare che gli enzimi persenti degradino il tessuto • Disidratazione del campione attraverso passaggi in soluzioni a concentrazione crescente di etanolo • Paraffina (materiale usato per l'inclusione) non è solubile in H2O • Eliminazione dell'etanolo e passaggi in xilene • Paraffina non è solubile nemmeno nell'etanolo • Inclusione del campione in in mezzo appropriato paraffina o resina • Tessuti sono "molli" e fragili • Diversi passaggi in paraffina calda • La paraffina occupa lo spazio precedentemente occupato dall'H2O • La paraffina fredda si indurisce e permette di sezionare il campione Taglio per mezzo di un microtomo, che produce sezioni dello spessore di 1-10 mm Montaggio delle sezioni su vetrini per microscopia Sezione non colorata Colorazione delle sezioni con il metodo più appropriato I coloranti sono a base acquosa, per cui si elimina lo xilene attraverso passaggi in etanolo Colorazione automatizzata Colorazioni • Colorazione • • Con un colore brillante di certe componenti del tessuto Contro colorazione • Del resto del tessuto con un colore contrastante Ematossilina/Eosina • Ematossilina • Ha affinità per le molecole cariche negativamente (DNA, RNA ed alcune proteine) • Eosina • Ha affinità per le molecole cariche positivamente (proteine del citosol) Perchè questa "slide" è blu … • • • Se una porzione di tessuto o di una cellula si colora di blu/porpora, viene detta basofila È colorata dall'ematossilina Nuclei e ribosomi generalmente sono basofili … e questa rossa ? • • • Se una porzione si colora in rosso /arancio/rosa, viene detta acidofila o eosinofila È colorata dall'eosina Sono le proteine del citosol Altre colorazioni • PAS • • (Acido Periodico-Reattivo di Schiff) Per sostanze ricche in zuccheri (muco) Tricromica o HazanMallory • • Adiposo Bianco Per i tessuti connettivi Le fibre si colorano in blu • Con E&E sono rosa Le aree bianche sono lipidi • Osmio o Sudan black • • • Per grasso/lipidi/mielina I lipidi non incorporano coloranti acquosi Mielina Argento ed oro • Per fibre delicate e processi cellulari Cellule nervose • Giemsa • • Per le cellule del sangue Simile ad E&E Cellule del sangue E le aree "bianche"? • I fluidi presenti nei tessuti o negli spazi interstiziali non si colorano con E&E • • • Sangue, linfa etc. Si riconoscono come ampi spazi bianchi Anche i lipidi ed il grasso non si colorano Mesenchima Interpretate il campione !!! • • Dovete pensare in 3 dimensioni Sezioni seriali sono l'ideale per l'interpretazione e la ricostruzione Ricostruzione per mezzo di sezioni seriali “Artefatti” • Shrinkage • • • Lascia dello spazio aggiuntivo Disidratazione e fissaggio Fratture al piano di taglio • • Tagli netti e ben visibili Lama deteriorata • Colorante precipitato • • Tessuto "pinzato" • • • Macchie di colore a "grano di pepe” Strumento per l'excisione deteriorato Durante o dopo il sezionamento Pieghe • Durante il montaggio Microscopia Elettronica Microscopia Elettronica a Trasmissione • Elettroni hanno una lunghezza d'onda corta • • • Alta risoluzione Sezioni molto sottili e coloranti elletrondensi Gli elettroni passano attraverso il campione La maggiore risoluzione del TEM permette di visualizzare strutture non visibili con il microscopio ottico Risoluzione dell'occhio: 0.2 mm = 200 µm Risoluzione del MO: 200 nm = 2,000 Angstroms Risoluzione del TEM: 2 Angstroms 1 mm = 1000 µm 1 µm = 1000 nm 1 nm = 10 Angstroms Pinocitos i Preparazione di Campioni Biologici per TEM • Acquisizione del campione e taglio in pezzi (1cm3) • Fissaggio del campione con glutaraldeide e poi tetrossido di osmio • L’osmio è un metallo pesante che si lega ai lipidi, rendendoli elettrondensi (neri) • Coloranti non legano i lipidi, che nelle sezioni appaiono chiari Disidratazione dei campioni tramite passaggi in soluzioni a concentrazione crescente di etanolo Inclusione dei campioni in piccoli blocchi di resina Taglio dei campioni inclusi con un ultramicrotomo dotato di lama al diamante (a volte vetro) La superfice da analizzare deve essere di circa 0.2 mm Lo spessore della sezione varia da 40 a 100 nm (di solito 65-80 nm) Montaggio delle sezioni su di una griglia Colorazione delle sezioni con nitrato o acetato di uranile e citrato di piombo Visualizzazione al TEM Fotografia, sviluppo ed analisi delle immagini Freeze-fracture • Il tessuto prelevato viene congelato a -140/150 °C • Con un martelletto viene provocata la frattura, secondo le linee di forza del tessuto • Evaporazione e deposizione di metalli pesanti • Eliminazione materia organica Autoradiografia Utilizzando isotopi radioattivi si possono marcare strutture cellulari ben definite e visualizzarle poi tramite microscopia ottica od elettronica Ottico Elettronico Microscopia Elettronica a Scansione SEM fa una scansione della superfice del campione Produce immagini 3-D Preparazione dei campioni per SEM • Acquisizione del campione • Trattandolo con cura in modo da non danneggiare la superficie • Fissazione e disidratazione • Non si include • Poggiato su di un supporto e ricoperto con un metallo • • • • • Oro, cromo, palladio, carbone Deve essere elettronconducente (non elettrondenso) Visualizzato al microscopio Fotografato Si possono analizzare le componenti chimiche tramite raggi X Microscopia a Fluorescenza • Il campione viene colorato con anticorpi oppure sostanze specifiche coniugate con fluorocromi • La luce utilizzata ha lunghezze d’onda specifiche per eccitare i fluorocromi • I fluorocromi emettono radiazione blu, rossa o verde Microscopia a Fluorescenza Microscopia Confocale • • • • • • La luce monocromatica, di lunghezza d’onda breve, è emessa da una sorgente laser, attraverso un diaframma e deviata da uno specchio dicroico, che permette il passaggio di determinate lunghezze d’onda Le lenti dell’obbiettivo focalizzano la luce in un punto del piano ottico del campione I fluorocromi usati per colorare vengono eccitati ed emettono a lunghezza d’onda maggiore, in grado di attraversare lo specchio e focalizzarsi nel piano del diaframma Il foto-moltiplicatore amplifica l’intensità del segnale e lo trasmette al computer che elabora l’immagine La luce che proviene dai piani superiori o inferiori al piano focale non passa attraverso il diaframma e non contribuisce alla formazione dell’immagine Diversi punti dello stesso piano e dei paini consecutivi vengono illuminati e registrati mediante la scansione col laser QuickTime™ and a Motion JPEG A decompressor are needed to see this picture. Metodi analitici Come si analizzano gli organelli o la struttura fine? Metodiche che permettono l’isolamento dei componenti cellulari intatti Centrifugazione, semplice o differenziale Permette l’isolamento sia delle cellule da un tessuto sia delle singole componenti cellulari Centrifugazione Centrifugazione differenziale
Scaricare