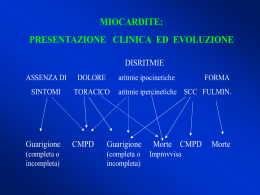
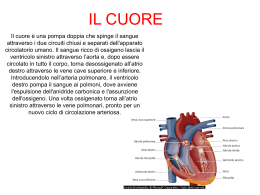
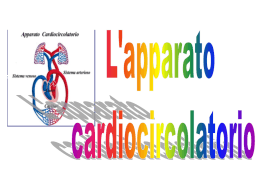
SEZIONE SCIENTIFICA - Patologia in pillole PATOLOGIA IN PILLOLE Nr. 30 D. Soldini, S. Crippa, L. Mazzucchelli Storia clinica Un ragazzo di 17 anni, sportivo di élite, crolla a terra esanime durante una partita di calcio. Tutti i tentativi di rianimazione da parte dello staff tecnico e del personale paramedico presente sul posto sono purtroppo infruttuosi. Dopo oltre un’ora di sforzi viene constatato il decesso del giovane. Le informazioni raccolte dai familiari, dal medico di famiglia, dall’allenatore e dai compagni di squadra non rivelano particolarità. Fino al tragico evento il ragazzo ha goduto di buona salute, al di là di occasionali episodi influenzali, ed ha praticato sport a livello agonistico senza mai accusare sintomi patologici. Il giovane viene sottoposto a riscontro autoptico che, all’esame macroscopico, mostra quale unica alterazione, un quadro di probabile sostituzione fibroadiposa del miocardio ventricolare destro, poi confermato alle indagini istologiche. Il reperto macro- e microscopico è illustrato nelle seguenti immagini. Indica la diagnosi corretta: a b c d e 73 SETTEMBRE 2008 Cardiomiopatia ipertrofica Cardiomiopatia/displasia aritmogena Cardiomiopatia dilatativa Adipositas cordis Nessuna causa di morte evidente (sine materia) TRIBUNA MEDICA TICINESE 399 SEZIONE SCIENTIFICA - Patologia in pillole Diagnosi Cardiomiopatia/displasia aritmogena del ventricolo destro Commento La cardiomiopatia/displasia aritmogena del ventricolo destro (arrhythmogenic right ventricular cardiomyopathy/ dysplasia; ARVC/D) è una malattia del muscolo cardiaco, caratterizzata clinicamente da aritmie ventricolari di origine non ischemica con insorgenza nel ventricolo destro, a rischio di arresto cardiaco (per review vedi ref.1 da cui è tratto questo commento). Essa consiste in una distrofia progressiva del miocardio primariamente del ventricolo destro con sostituzione fibroadiposa e rappresenta una delle maggiori cause di morte istantanea nei giovani e negli atleti. Si stima una prevalenza di circa 1:5000, ma potrebbe essere maggiore in seguito a mancata diagnosi oppure diagnosi errata. Caratteristiche cliniche e decorso naturale della ARVC/D La prima manifestazione della ARVC/D avviene generalmente dopo l’infanzia ed è caratterizzata da palpitazioni e/o sincopi. Possono essere osservati i seguenti quadri clinici: -fase subclinica con anomalie strutturali criptiche: in questa fase non vi sono sintomi e l’arresto cardiaco può rappresentare la prima ed unica manifestazione della malattia. È riconosciuta come la seconda causa di morte improvvisa nei giovani e come seconda causa di morte improvvisa negli atleti agonisti. Sussiste un minimo substrato senza però che si manifestino disturbi di conduzione. -fase con disturbi del ritmo con palpitazioni e sincopi: la presentazione clinica più tipica è rappresentata da aritmie ventricolari sintomatiche con origine nel ventricolo destro, solitamente scatenate da uno sforzo fisico. -insufficienza ventricolare destra: la perdita progressiva di miocardio del 400 TRIBUNA MEDICA TICINESE ventricolo destro ne compromette la funzione meccanica. -scompenso biventricolare: quando la malattia coinvolge il setto interventricolare ed il ventricolo sinistro insorge un’insufficienza cardiaca di tipo congestivo, la quale imita una cardiomiopatia dilatativa. Può verificarsi la formazione di una trombosi murale endocavitaria, specialmente all’interno di aneurismi o appendici atriali, quando la malattia è complicata da fibrillazione atriale. In questi casi la disfunzione contrattile del miocardio può essere seriamente compromessa e richiedere un trapianto cardiaco. Quando il ventricolo sinistro è coinvolto, le aritmie ventricolari possono apparire polimorfe, in quanto hanno origine da regioni cardiache diverse. Il decesso avviene in genere per morte improvvisa con una frequenza di 0.1-0.3% annuale negli adulti affetti da ARVC/D. Tuttavia, la reale frequenza non è nota con certezza e potrebbe essere maggiore in adolescenti e giovani adulti, nei quali la malattia non sia sintomatica ed abbia come prima manifestazione la morte improvvisa. Patologia e patogenesi La malattia consiste nella progressiva sostituzione del miocardio primariamente del ventricolo destro da parte di tessuto adipoconnettivo, inizialmente coinvolgente l’epicardio con possibile estensione fino all’endocardio, diventando così trasmurale (Figura 2). La debolezza della parete libera comporta dunque una dilatazione e la formazione di aneurismi a livello del ventricolo destro, tipicamente in sede inferiore, apicale ed infundibulare (cosiddetto triangolo di displasia). La sostituzione da parte del tessuto fibroadiposo compromette la conduzione intraventricolare e causa un rallentamento (“late potential”, onde epsilon, blocco di branca destro) e la comparsa di fenomeni di “re-entry” che stanno alla base dei meccanismi della aritmie ventricolari. L’infiltrazione di tessuto adiposo nel ventricolo destro non è di per sé una caratteristica morfologica sufficiente per la diagnosi di ARVC/D. Infatti una certa quantità di tessuto adiposo è riscontrabile nella regione anterolaterale ed apicale del ventricolo destro anche in cuori normali, la quale aumenta in genere con l’età e le dimensioni corporee. Inoltre, bisogna distinguere la ARVC/D dall’adipositas cordis. La presenza di fibrosi di tipo sostitutivo e la degenerazione di miociti sono essenziali per la diagnosi, oltre alla sostituzione di tessuto adiposo. Fig. 2: Cuore ottenuto nel corso di trapianto cardiaco. Si nota sostituzione fibroadiposa del miocardio con coinvolgimento biventricolare, A: ventricolo destro; B: ventricolo sinistro con aneurisma apicale (da ref. 1). 73 SETTEMBRE 2008 SEZIONE SCIENTIFICA - Patologia in pillole L’atrofia del miocardio è completamente assente alla nascita ma progredisce con il tempo, a differenza di altre malattie congenite. Nella ARVC/D la perdita di miociti è la conseguenza della morte cellulare dopo la nascita, solitamente nell’infanzia. È stato dimostrato che ciò avviene mediante il meccanismo di apoptosi. Più della metà dei casi studiati postmortem evidenziano un coinvolgimento del ventricolo sinistro, in genere limitato all’epicardio della parete posterolaterale. Il coinvolgimento del setto interventricolare è raro, probabilmente perché non rappresenta una struttura subepicardica. Nei casi più gravi che richiedono un trapianto cardiaco si può osservare la formazione di aneurismi a livello del ventricolo sinistro. L’istologia del miocardio del ventricolo destro mostra una marcata atrofia associata ad una sostituzione da parte di tessuto adipoconnettivo, la quale va interpretata come un meccanismo di riparazione in seguito alla morte dei miociti. Il tessuto connettivo ha un ruolo fondamentale nel rallentamento della conduzione dell’impulso elettrico quale causa delle aritmie. L’esame istologico rivela miociti apoptotici singoli o in gruppi, a volte associati a infiltrato infiammatorio. L’infiammazione cardiaca può essere evidenziata all’autopsia fino nel 75% dei cuori e verosimilmente ha un ruolo importante nello sviluppo delle tachiaritmie ventricolari. Non è noto se l’infiammazione rappresenti un fenomeno reattivo alla morte dei miociti o se sia la conseguenza di infezioni o meccanismi immunitari. In alcuni pazienti affetti da ARVC/D sono stati riscontrati dei virus, ma il loro ruolo appare ancora poco chiaro. Diagnosi clinica Criteri diagnostici sono stati proposti e divisi in criteri maggiori e minori (Tabella 1). La diagnosi di ARVC/D dovrebbe essere posta nel caso di due criteri maggiori, o uno maggiore e due minori o ancora nel caso di quattro criteri minori derivanti da diversi gruppi. Le alterazioni morfologiche sono visibili all’ecocardiografia, all’angiografia, alla risonanza magnetica cardiaca o alla scintigrafia. Una biopsia transvenosa del miocardio può essere di grande aiuto nella dimostrazione morfologica della sostituzione fibroadiposa del miocardio. Le biopsie dovrebbero provenire dalla parete libera del ventricolo destro. Una quantità residua di miocardio inferiore al 45% con sostituzione adipoconnetivale ha una grande accuratezza diagnostica. Genetica L’ARVC/D è una malattia ereditaria in circa il 50% dei casi. La progressiva atrofia miocardica è quindi geneticamente determinata. La forma classica è caratterizzata da trasmissione autosomica dominante a penetranza variabile. Un ruolo fondamentale nella scoperta dei geni coinvolti nella malattia è stato giocato da una forma recessiva di ARVC/D, chiamata malattia di Naxos, la quale causa una sindrome cardiocutanea caratterizzata da cheratosi palmoplantare, capelli lanosi e disturbi cardiaci. Infatti è noto che miociti e cellule epidermiche mostrano 1 Storia familiare Criteri maggiori Malattia familiare confermata da esame autoptico o da espianto/biopsia cardiaca Criteri minori Storia familiare di morte improvvisa prematura (<35 anni) a causa di una sospetta ARVC/D Storia familiare (diagnosi clinica in base agli attuali criteri) 2 Anomalie di depolarizzazione/conduzione all’ECG Criteri maggiori Curve epsilon o prolungamento localizzato (>110 ms) del complesso QRS nelle derivazioni precordiali destre (V1-V3) Criteri minori Potenziali tardivi (signal-averaged ECG) 3 Anomalie nella ripolarizzazione all’ECG Criteri minori Onde T invertite alle derivazioni precordiali destre (V2 e V3) in persone >12 anni in assenza di blocco di branca destro 4 Aritmie Criteri minori Tachicardia ventricolare del tipo “blocco di branca sinistro” all’ECG o all’Holter Extrasistole ventricolari frequenti (>1000/24 h all’Holter) 5 Disfunzioni globali o regionali e anomalie strutturali Criteri maggiori Dilatazione severa e riduzione della frazione di eiezione del ventricolo destro senza o con lieve interessamento del ventricolo sinistro Aneurismi localizzati del ventricolo destro. Severa dilatazione segmentale del ventricolo destro Criteri minori Lieve dilatazione globale del ventricolo destro o frazione di eiezione ridotta con ventricolo sinistro normale Lieve dilatazione segmentale del ventricolo destro 6 Caratterizzazione del tessuto della parete ventricolare Criteri maggiori Sostituzione adipoconnettiva del miocardio evidenziabile in biopsia endomiocardica Tab. 1: Criteri per la diagnosi di ARVC/D (modificata da ref. 1 e 5) 73 SETTEMBRE 2008 TRIBUNA MEDICA TICINESE 401 SEZIONE SCIENTIFICA - Patologia in pillole lo stesso apparato giunzionale (desmosomi e giunzioni aderenti). Questo spiega perché geni codificanti proteine della giunzione intercellulare siano stati considerati potenziali candidati quali responsabili per la ARVC/D. Infatti negli ultimi anni, in pazienti con ARVC/D, sono state identificate mutazioni coinvolgenti geni codificanti proteine di desmosomi e giunzioni aderenti, quali ad esempio placoglobina, desmoplachina, pacofillina 2, desmogleina 2 e desmocollina 2. Le mutazioni in proteine dell’apparato giunzionale causano un rilassamento della connessione intercellulare, apoptosi dei miociti e cambi strutturali, i quali costituiscono il substrato per le aritmie ventricolari. Attualmente sono in corso studi per meglio definire la correlazione tra il tipo di mutazione e la forma clinica di ARVC/D. Rischio e terapie La giovane età al momento della comparsa di sintomi, dispersione >40 ms del complesso QRS, inversione dell’onda T oltre la derivazione V1, coinvolgimento del ventricolo sinistro, tachicardie ventricolari, sincope e pregresso arresto cardiaco sono considerati i maggiori indicatori di una prognosi negativa ed un rischio elevato di morte improvvisa. Inoltre molta attenzione va riservata ad una storia familiare “maligna”. In questo senso, in caso di morte improvvisa di un giovane è essenziale ottenere una diagnosi precisa e discutere con i parenti l’utilità di una consulenza genetica per eventualmente prevenire il ripetersi nella famiglia di un evento tragico di questo tipo. A livello terapeutico possono essere utilizzati degli antiaritmici, quali betabloccanti, amiodarone e verapamil. L’ablazione tramite catetere può essere efficace a breve termine, ma ha un elevato tasso di recidiva. I defibrillatori intracardiaci hanno dimostrato la loro efficacia. In caso di insufficienza cardiaca refrattaria il trapianto rappresenta l’unica opzione terapeutica. 402 TRIBUNA MEDICA TICINESE Prevenzione della morte improvvisa L’arresto cardiaco nella ARVC/D è la conseguenza di una combinazione di diversi fattori (substrato, trigger, aritmie) e le misure preventive dovrebbero focalizzarsi su di essi. Lo scopo di defibrillatori intracardiaci è quello di convertire una fibrillazione ventricolare in un ritmo sinusale. L’apparecchio può essere impiantato in pazienti selezionati. La terapia farmacologica e l’ablazione del substrato hanno un ruolo fondamentale nella prevenzione di aritmie, ma la loro efficacia è purtroppo limitata ed il rischio di recidive è elevato. Sforzi fisici, sovraccarico di volumi e sovraestensione del miocardio del ventricolo destro sono considerati i maggiori “triggers”. L’incremento di attività cardiaca durante pratiche sportive aumenta di 5 volte il rischio di morte improvvisa nei giovani per cui l’identificazione di portatori asintomatici è essenziale. La partecipazione a screening e il divieto di praticare sport in casi selezionati si sono dimostrati efficaci nella riduzione di morte improvvise nei giovani atleti. Una terapia curativa della malattia può essere attualmente raggiunta solo attraverso il trapianto cardiaco che rappresenta anche l’unica forma di prevenzione sicura di morte improvvisa. D. Soldini, S Crippa, L. Mazzucchelli, Istituto cantonale di patologia, Locarno 73 SETTEMBRE 2008 Bibliografia 1 Thiene G, Corrado D, Basso C. Arrhythmogenic right ventricular cardiomyopathy/dysplasia. Review. Orphanet Journal of rare Diseases 2007, 2:45. Articolo ottenibile da http://www.OJRD.com/content/2/I/45 2 Marcus F et al. Right ventricular dysplasia: a report of 24 adult cases. Circulation 1982, 65:384-398 3 Nava A et al. Familial occurrence of right ventricular dysplasia: a study involving nine families. J Am Coll Cardiol 1988, 12: 12221228 4 Thiene G et al. Right ventricular cardiomyopathy and sudden death in young people. N Engl J Med 1988, 318:129-133 5 Basso C et al. Arrhythmogenic right ventricular cardiomyopathy: dysplasia, dystrophy or myocarditis? Circulation 1996, 94:983991 6 McKenna WJ et al. Diagnosis of arrhythmogenic right ventricular cardiomyopathy/dysplasia. Br Heart J 1994, 71:215-219 7 Wichter T et al. Efficacy of antiarrhythmic drugs in patients with arrhythmogenic right ventricular disease. Results in patients with inducible and noninducible ventricular tachycardia. Circulation 1992, 86:29-37 8 Rampazzo A et al. Arrhythmogenic in right ventricular cardiomyopathy/displasia. Advances in genetics: Dominant forms. In Arrhythmogenic right ventricular cardiomyopathy/dysplasia edited by: Marcus FI, Nava A, Thiene G. Milano; Springer; 2007:7-14
Scaricare