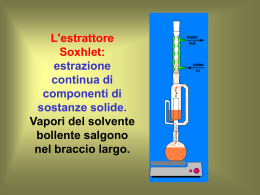
Chimica analitica degli alimenti Scopo dell’analisi sugli alimenti: Aspetti legali Controllo dei limiti di legge Sostanze tossiche (es. aflatossine, mercurio) Pratiche illecite (zucchero nel vino) Aspetti nutrizionali Resveratrolo nel vino Vitamine, principi nutritivi Qualità degli alimenti Importanza dell’analisi degli alimenti Dal punto di vista sanitario, l’l’analisi degli alimenti è l’unica garanzia per la nostra salute relativamente a ciò che mangiamo (a meno che ci si possa fidare ciecamente del produttore). Le frodi alimentari sono infatti alquanto diffuse e non sempre è possibile portarle alla luce. La frode può intervenire su vari livelli: Un alimento è prodotto e commercializzato con materie prime di scarsa qualità qualità Materie prime conservate non correttamente Materie prime contaminate (es (es.. Hg in pesce, pesce, Mucca pazza) Trattamenti che causano contaminazioni Un alimento è commercializzato utilizzando un marchio o una denominazione non corrispondente Parmesan tedesco Vino non corrispondente alla denominazione Un alimento è commercializzato sostituendo completamente o parzialmente il prodotto prodotto autentico con un’ un’alternativa simile ma meno costosa succo d’ d’arancio adulterato con succo di mela olio d’ d’oliva miscelato con altri oli vegetali Un alimento è prodotto con procedimenti non conformi olio d’ d’oliva extravergine prodotto per estrazione con solventi Un alimento è prodotto con pratiche non consentite zucchero nel vino o nei succhi di frutta Frodi antiche e moderne La falsificazione degli alimenti e delle bevande non è un fenomeno nuovo ma piuttosto una pratica molto antica della cui presenza nel passato esistono importanti testimonianze. Nell’antico Egitto si impiegavano speciali attrezzi per effettuare la bollatura delle carni macellate ed impedire che con esse venissero vendute parti di bestie morte per malattia. Un reperto di epoca romana imperiale (I secolo d.C.) mostra un’anfora gallica recante un sigillo con una falsa incisione del nome di un produttore campano (tale M. C. Lassius) apposto da mercanti per far credere che quella fosse la paternità del vino posto nei contenitori, mentre si trattava di vino proveniente dalla Narbona da cui essi l’avevano acquistato Ancora nel primo secolo d.C. Plinio il Vecchio descriveva la falsificazione di prodotti di largo consumo, come il pepe e la farina che, quando proveniva da cerali di scarso pregio, grazie ad una serie di trattamenti, poteva essere trasformata in un prodotto di prima qualità, per la cui vendita si poteva esigere prezzi superiori. Va detto che in tempi antichi le adulterazioni erano grossolane (es. annacquamento del latte) ma d’altra parte non c’era alcuna nessuna protezione del consumatore In Francia, tra il 1200 ed il 1400, si moltiplicarono editti ed ordinanze contro i malvagi frodatori che smerciavano carni alterate, rovinate, gonfie, panetti di burro rancido tinti con erbe e fiori gialli, birra ottenuta con misture di bacche selvatiche, peperoncino, loglio o pece resina In Germania, l’imperatore Federico III emise duri provvedimenti per contrastare i falsificatori di vino, a seguito di “casi di avvelenamento dovuti a certi mercanti di Franconia, che avevano venduto come vino puro una infusione in cui erano mescolate acqua di calce e varie droghe nocive” Anche Carlo V emanò rigide disposizioni contro le frodi alimentari ma, pare, senza ottenere grandi risultati Cronistoria delle frodi Medio Evo: primi esempi di adulterazione riportati Inizio del XVIII secolo: controllo su certi alimenti (birra, vino, alcolici, tè) al solo scopo fiscale 1861: Uso del microscopio per certificare l'autenticità del caffè (a quel tempo estremamente costoso 1875: Sale of Food and Drug Act (UK). Un alimento viene considerato adulterato se: Contiene ingredienti che lo rendono pericoloso per la salute del consumatore Contiene sostanze che ne aumentano il peso o il volume, a meno che queste non siano necessarie alla preparazione e vengano dichiarate al momento della vendita Un costituente importante è stato rimosso in tutto o in parte senza che questo venga dichiarato al momento della vendita È una imitazione, o viene venduto sotto il nome, di un altro alimento. 1931: Food and Drug Administration (FDA) (USA) 1962: Codex Alimentarius Commission (FAO) … Unione Europea Aspetti positivi Attualmente le condizioni sono diverse, non necessariamente migliori. Gli aspetti positivi sono i seguenti: l'industria produce alimenti confezionati secondo standard definiti i metodi di analisi sono sofisticati, quindi le frodi più grossolane vengono facilmente smascherate. Frodi recenti come il vino al metanolo non sono più possibili i metodi vengono usati dalle industrie stesse per far fronte al crescente grado di consapevolezza dei consumatori il valore nutrizionale degli alimenti è generalmente garantito c’è particolare attenzione alle qualità edonistiche in senso lato (origine geografica, genuinità, assenza di contaminazioni) generalmente le frodi non comportano più l'aggiunta di sostanze nocive (con notevoli eccezioni...) Aspetti negativi l’adulterazione è rivolta ad alimenti di alto valore commerciale (olio d'oliva, vini, tartufi, ecc.) sui quali il giro di affari è incredibilmente aumentato la frode è molto più sofisticata: pensata per frodare criteri quali l'origine controllata, la presenza di additivi naturali o artificiali, fino alla presenza di organismi geneticamente modificati Legislazione vigente Nazioni Argentina La legislazione vigente differisce a paese a paese. Si considerino le differenze relative ai limiti di metalli tossici nel vino Australia Brasile Canada Germania Italia Malta Nuova Zelanda Russia Sud Africa Svizzera USA As Cd Hg 0.01 Pb 0.20 0.1 0.05 0.030 0.20 0.1 0.50 0.100 0.1 0.01 0.010 0.20 0.50 0.20 0.25 0.30 0.2 0.20 0.2 0.20 0.2 0.03 0.005 0.30 0.2 0.01 0.050 0.20 0.2 0.01 0.10 0.30 FAO/WHO 0.20 EU 0.20 OIV 0.2 0.01 0.020 0.20 Parametri comuni Tuttavia, in molti Paesi un alimento viene considerato adulterato se: contiene materiale vegetale o animale sporco, putrefatto, decomposto o malato è infestato da insetti o inadatto al consumo umano è confezionato o conservato in condizioni non igieniche contiene ingredienti tossici è stato sostituito con sostanze inferiori o meno costose sono stati rimossi alcuni dei suoi costituenti è imballato con materiali tossici o nocivi contiene additivi proibiti, o additivi consentiti in quantità superiori ai limiti prescritti la sua qualità è inferiore allo standard prestabilito è di natura o qualità diversi dal dichiarato, o utilizza descrizioni false o fuorvianti Aspetti nutrizionali Dal punto di vista nutrizionale, l’analisi degli alimenti ci dà un’idea (evidentemente non esaustiva) dei potenziali benefici apportati dall’assunzione degli alimenti. Per questo motivo sull’etichetta di molti prodotti sono riportate le determinazioni di parametri quali: vitamine sali minerali (sottolineando a volte la carenza, a volte l’abbondanza) macromolecole (proteine, grassi, carboidrati, ecc.) principi nutritivi non meglio identificati (Omega 3, triplo acido di frutti...) Aspetti commerciali Va considerato che, spesso, l’aspetto nutrizionale è sfruttato ad arte a scopi commerciali, per evidenziare le caratteristiche di un prodotto in maniera non troppo realistica. Questo perchè l’analisi degli alimenti ha ormai assunto un’importanza notevole, vista l’espansione del mercato alimentare, soprattutto per quei settori dove la ricerca di valore aggiunto a tutti i costi fa leva su informazioni scientifiche o pseudo-scientifiche Parametri analitici studiati Il numero di sostanze di interesse nel campo agroalimentare è ovviamente elevatissimo. Soltanto in relazione agli aspetti sanitari, possiamo stimare in diverse decine di migliaia le specie chimiche classificate come indesiderate, comprendenti le seguenti classi: Metalli pesanti (As, Cd, Hg, Pb) e transizione (Cr, Co, Ni, Cu, Zn) Specie metalliche composti organometallici (metilmercurio, tetraetilpiombo, ecc.) ioni metallici a diverso stato di ossidazione, es. Cr(III) e Cr(VI) Composti inorganici sali minerali (nitriti, nitrati, fosfati, ecc.) Composti organici derivanti da reazioni chimiche (PAH, PCB, BTEX, diossine) derivanti da attività biologica (aflatossine) residui di composti impiegati nella produzione (pesticidi, fungicidi) Quali parametri analitici? Proprio per l’elevata quantità di sostanze potenzialmente indesiderate, risulta impossibile poter avere un quadro tossicologico completo di un alimento. A seguito di ricerche mirate, nel corso degli anni sono stati sviluppati test analitici che hanno come target un numero ristretto di composti o elementi tossici, in stretta relazione ai processi produttivi coinvolti nelle filiere alimentari o ai metodi di stoccaggio e conservazione delle derrate. I punti critici da tenere sotto controllo possono essere: La qualità delle materie prime (assenza di composti indesiderati) I processi di trasformazione delle materie prime (conversione di sostanze presenti nelle materie prime in composti indesiderati) L’addizione al prodotto di sostanze aventi funzioni varie (apporto di composti indesiderati) I materiali di contenimento (cessione dalla superficie) Le condizioni di conservazione (effetto di temperatura, umidità, esposizione alla luce) Evoluzione delle conoscenze Il quadro dei parametri analitici sugli alimenti è necessariamente in evoluzione, sull’onda emotiva degli eventi (vedi caso Mucca pazza...) o in risposta a studi tossicologici aggiornati Se consideriamo i secoli passati, è evidente che la mancanza di nozioni sufficienti rendevano desiderabile in campo agroalimentare l’impiego di sostanze che al giorno d’oggi non ci sogneremo di utilizzare Durante l'ultima metà del XIX secolo, i progressi in chimica organica resero disponibili una quantità di sostanze sintetiche, la cui utilità venne provata in vari campi, ad esempio la saccarina ed i coloranti azoici. Allo stesso tempo, essendo stata accertata l’origine batterica di certe malattie, furono introdotti vari agenti antimicrobici per la conservazione delle derrate (ad es. il creosoto, l'acido borico, l'acido salicilico). Tuttavia, le implicazioni tossicologiche collegate al loro uso emersero solo gradualmente e con ritardo. Da questo riconoscimento sorsero le prime regolamentazioni sull'uso degli tali additivi Progressi delle scienze mediche I progressi in microbiologia hanno reso possibile la connessione tra agenti patogeni e malattie, così da evidenziare il rapporto causale tra certe intossicazioni o malattie vere e proprie e agenti patogeni contenuti nei generi alimentari (ad es. Salmonella, botulismo, micotossine) Tuttavia le intossicazioni alimentari sono ancora possibile a causa di pratiche fraudolente Gli scherzi della Natura Spesso è accaduto che la Natura abbia fatto brutti scherzi, con conseguenze sanitarie drammatiche. Il caso di Minamata è sintomatico, dal punto di vista sia del rispetto ambientale, sia del progresso della conoscenza scientifica Negli anni ’50, scarichi industriali nella baia di Minamata (Giappone) provocarono un grave inquinamento da mercurio, con circa 10.000 avvelenati per danni al sistema nervoso centrale. L’avvelenamento fu causato da composti di Hg presenti nei pesci e nei molluschi che costituivano la principale fonte di proteine per la popolazione della baia Minamata Prima di questo incidente era noto soltanto il rischio occupazionale da esposizione, ma in seguito a Minamata furono focalizzati due aspetti: Alcuni organismi (tra cui pesci e molluschi) sono in grado di concentrare specie metalliche nei loro organi, in particolare nei tessuti lipidici Questi organismi sono in grado di attivare processi biochimici per limitare la tossicità delle specie assorbite: uno dei meccanismi è la biometilazione Hg2+ + CH3· ⇒ CH3Hg+ Prima di Minamata nessuno si sarebbe sognato di cercare composti organomercurici negli alimenti Parametri qualitativi Oltre ai parametri determinati di routine per motivi sanitari, sono poi in aumento i test che rispondono alla necessità di autenticare gli alimenti o di qualificarli dal punto di vista della qualità, soprattutto per i prodotti di maggior pregio. Sempre più spesso i disciplinari di produzione o le normative prevedono l’impiego di questi test per permettere lo sfruttamento commerciale di determinate etichette (es. olio extravergine) Alcuni tra i parametri analitici determinati a scopo qualitativo sono: Alcuni elementi (selenio, calcio, ferro, in dosi opportune) Composti antiossidanti come i polifenoli o i tocoferoli Vitamine Molecole con funzionalità particolari (es. resveratrolo nel vino rosso) Concentrazione ottimale La semplice indicazione della presenza o assenza delle sostanze non è di per sè informazioni sufficiente a valutare un alimento dal punto di vista sanitario. Ad esempio, il comportamento fisiologico dei metalli si può rappresentare con una curva gaussiana difetto ottimale eccesso A concentrazioni basse si ha carenza dell’elemento, a concentrazioni troppo alte si ha eccesso. La concentrazione ottimale corrisponde al massimo della curva Concentrazione o speciazione? Oltre al semplice dato di concentrazione, in certi casi sarebbe più utile indicare la specie in cui un certo analita si trova, ovvero effettuare la speciazione dell’analita. Come il citato caso di Minamata dimostra, la tossicità di un analita, o comunque le sue potenzialità di interazione con l’organismo, dipendono non solo dalla sua concentrazione ma anche dalla forma chimica in cui esso si trova. Nel caso del mercurio si ha una tossicità crescente nella serie sali inorganici, es. HgCl , Hg(NO ) 2 3 2 composti di organomercurio, es. metilmercurio, dimetilmercurio vapori di mercurio elementare Questa esigenza è a volte soddisfatta nei casi semplici, come nella coppia Cr(III)/Cr(VI) in cui i due stati di ossidazione del cromo hanno tossicità notevolmente diversa. Raramente, però, si va oltre. Ad esempio quasi mai si prende in considerazione la cosiddetta frazione disponibile di un analita, cioè quella più attiva dal punto di vista fisiologico in quanto può essere liberata facilmente da un campione solido ed entrare in contatto con l’organismo Ciò è dovuto principalmente al fatto che le analisi di speciazione sono più complesse e quindi costose Considerazioni sulle tecniche La chimica analitica degli alimenti è una disciplina piuttosto complessa, in quanto il numero di sostanze d’interesse (o analiti) è ovviamente elevato, comprendendo sia le specie di interesse nutrizionale (vitamine, principi attivi, carboidrati, micrelementi, ecc.) sia le sostanze indesiderate o contaminanti (metalli pesanti, pesticidi, fitofarmaci, ammine biogene, ecc.). Inoltre, le matrici considerate vanno dall’acqua potabile alle carni al miele, imponendo metodi di trattamento molto diversi da una matrice all’altra Per questi motivi, è praticamente impossibile adottare procedure analitiche comuni per la caratterizzazione di tutti i tipi di alimenti. Ogni alimento e ogni classe di analiti richiedono una procedura specifica. Esistono al proposito metodi standardizzati, frutto di anni di ricerche Tecniche analitiche utilizzate Le tecniche che si usano correntemente per determinare gli analiti si possono riassumere nell’elenco seguente: Tecniche di spettroscopia atomica (GF-AAS, FAAS, ICP-AES, ICP-MS) per la determinazione elementare Tecniche cromatografiche (HPLC, IC, GC) per la separazione e determinazione di miscele di composti organici ed inorganici Tecniche spettrofotometriche (UV-visibile, IR) per la determinazione di parametri analitici o di specie che assorbono nell’intervallo UV-IR Tecniche volumetriche (titolazione acido-base, redox) per la determinazione di parametri vari Sono saltuariamente utilizzate anche tecniche elettrochimiche (polarografia, potenziometria) e alcune tecniche di analisi su solido (Raman, NIR) Tecniche più sofisticate con la spettroscopia NMR o l’analisi degli isotopi stabili con spettrometria di massa sono utilizzate per determinazioni di autenticità Le tecniche utilizzate saranno richiamate o introdotte volta per volta Il pretrattamento L’analisi degli alimenti richiede generalmente uno stadio preliminare che consiste nel portare il campione (tecnicamente la matrice) nella forma più opportuna ai fini della determinazione analitica. L’insieme delle procedure richieste per avere l’analita o gli analiti di interesse in forma determinabile è definito pretrattamento. Esso è un punto essenziale del metodo analitico, importante quanto la determinazione quali-quantitativa La stragrande maggioranza delle analisi in chimica agroalimentare si effettuano per via umida. Ciò significa che il campione, se non è già liquido, va portato in soluzione o quantomeno va solubilizzata la parte che contiene l’analita o gli analiti di interesse. Generalmente, quindi, il pretrattamento coincide o termina con uno stadio di solubilizzazione. In rari casi è possibile effettuare l’analisi sul campione tal quale, utilizzando tecniche non distruttive come la spettrometria Raman o la spettrometria NIR La varietà delle matrici considerate in chimica agroalimentare fa sì che sia difficile enunciare regole valide per ogni tipo di alimento. A seconda della natura chimica dell’alimento (organica o inorganica; acida, basica o neutra; solubile in solvente acquoso o in solventi organici) e della tecnica analitica utilizzata, sarà selezionato il metodo di pretrattamento più opportuno Tipi di pretrattamento I metodi di pretrattamento più frequentemente utilizzati nell’analisi agroalimentare sono i seguenti: Incenerimento Digestione umida con reattivi di solubilizzazione e/o ossidazione In sistemi chiusi Con microonde Separazione con membrane Filtri Ultrafiltrazione Dialisi Estrazione Con solvente Con solvente accelerata (ASE) Con un fluido supercritico (SFE) Con fase solida (SPE) Incenerimento L’incenerimento (ashing in inglese) consiste nel trattare un campione solido sottoponendolo a temperature elevate senza fiamma, in modo da causare la parziale o totale decomposizione delle sostanze organiche presenti e di parte di quelle inorganiche Normalmente una temperatura compresa tra 450 e 600°C è sufficiente per degradare la maggior parte delle molecole organiche a molecole più semplici o semplicemente a vapore acqueo ed anidride carbonica: ∆ CmHnOn → H2O + CO2 Naturalmente nella scelta della temperatura va tenuto conto della possibile perdita di analiti, soprattutto per quanto riguarda elementi volatili come As, Cd, Hg, Pb, Sb, Sn e Zn, sia presenti come elementi puri, sia come composti. L’applicabilità va quindi verificata analizzando materiali certificati L’incenerimento può essere effettuato nei seguenti modi: con riscaldamento semplice con l’ausilio di microonde, se il campione contiene acqua che può assorbire l’energia, coadiuvando così l’effetto della temperatura e ottenendo tempi più brevi di ashing con l’ausilio di reagenti esterni, es. acido solforico o perossido di idrogeno in questo caso si parla di wet ashing Residuo dell’incenerimento Il residuo di questo trattamento termico può essere composto da ossidi e da sali poco volatili (fosfati, cloruri, solfati, silicati di metalli alcalini e alcalino-terrosi), di colore biancastro. Una colorazione nera o bruna è indice di un incenerimento parziale, in cui parte delle sostanze organiche sono rimaste incombuste Da quanto detto si deduce che questo pretrattamento è adatto principalmente alla determinazione di parametri inorganici, come il contenuto di metalli, anioni o il residuo secco Principio del metodo Il procedimento consiste nel pesare una quantità nota di campione e porla in un crogiolo o in un contenitore apposito (ovviamente termoresistente, es. vetro Pyrex). Il contenitore è poi inserito all’interno di un forno o muffola che viene sottoposto ad un ciclo di temperatura crescente, in cui la temperatura finale dipende dagli analiti e deve quindi essere inferiore al punto di ebollizione degli analiti stessi. Il trattamento in muffola può essere preceduto da un breve trattamento di essiccamento a 120-180°C per eliminare l’acqua ed evitare così reazioni violente di ebollizione a temperature più alte Al termine dell’incenerimento si attende il tempo necessario al raffreddamento e poi si preleva il contenitore. Se si è interessati soltanto al residuo secco è sufficiente pesare il crogiolo prima e dopo l’incenerimento, mentre se si è interessati a determinare alcuni analiti è necessario portare in soluzione il residuo che però solitamente è costituito da sostanze facilmente solubilizzabili in acqua o in acidi (nitrico, cloridrico) Vantaggi e svantaggi • VANTAGGI • non richiede l’uso di reagenti • molto economico • scarso pericolo di contaminazione • molto semplice da eseguire • elevato numero di campioni trattabili simultaneamente (dipende dalle dimensioni del forno) • SVANTAGGI • richiede muffola a temperatura controllata (costo iniziale) • processo lungo (12-18 ore) • richiede una certa attenzione per le reazioni che può provocare • perdite di campione ⇒ perdita di analita • combustione ⇒ danno al forno • emissione di vapori • non adatto per determinazione di composti volatili (es. Cd, Cr, Cu, Fe, Hg, Ni, P) • non adatto per la maggior parte dei composti organici • rischio potenziale di interazione tra i sali e il crogiolo Digestione umida Si tratta di una tecnica di pretrattamento molto utilizzata per la determinazione di specie inorganiche (metalli, anioni), mentre non è adatta per la determinazione di specie organiche che subiscono degradazione termica. Il processo di digestione avviene all’interno di un contenitore nel quale sono introdotti il campione finemente suddiviso e i reattivi di solubilizzazione, eventualmente coadiuvati da reattivi di ossidazione. Generalmente sono utilizzati acidi puri o in miscela: Acido nitrico, esercita azione ossidante a caldo ed è in grado di rompere i legami glicosidici Acido solforico, esercita azione ossidante e disidratante Acido perclorico, esercita azione ossidante Acqua regia (acido nitrico + cloridrico 1:3), esercita azione ossidante molto forte Acqua ossigenata, esercita azione ossidante Precauzioni nella digestione Le quantità di reagenti e di campione introdotte devono essere compatibili con il volume del sistema. Considerando che la maggior parte delle matrici alimentari contiene sostanze organiche, va considerata la liberazione di composti gassosi conseguenti alla digestione, che può provocare sovrapressioni: (C, H, O) + O2 (acido ossidante) ⇒ H2O + CO2 Il volume dei gas liberati è ovviamente molto maggiore rispetto alla miscela campione-reagenti di partenza Il contenuto di carbonio nei cibi è quindi un valore da tener presente nel progettare un pretrattamento per digestione umida Applicazioni della digestione La reazione di digestione può avvenire a temperatura controllata. Lavorando in sistema chiuso, è possibile raggiungere temperature superiori a quelle di ebollizione degli acidi a temperatura ambiente, con aumento delle proprietà solubilizzanti e ossidanti dei reagenti impiegati; inoltre il sistema chiuso limita le perdite di campione per volatilizzazione Nel dettaglio delle varie matrici, la digestione umida è particolarmente efficace per il pretrattamento di alimenti a base di carboidrati (zuccheri, amidi, cellulosa, ecc.) che sono facilmente mineralizzati con acido nitrico a 180°C; più complessa è la solubilizzazione di matrici contenenti grassi e proteine, che può richiedere l’addizione di acido perclorico per avere una dissoluzione completa. In questo caso il trattamento va effettuato con cautela Digestione umida con microonde Una variante più efficace della semplice digestione umida prevede l’utilizzo di microonde per il riscaldamento del sistema. L’energia associata alle microonde (600-1500 W nelle apparecchiature da laboratorio) non è in grado di rompere direttamente i legami molecolari, ma può essere assorbita da sostanze come l’acqua e gli acidi minerali, che in questo modo si scaldano rapidamente e, in un sistema chiuso, sono in grado di solubilizzare il campione in maniera più efficiente e in tempi minori La digestione avviene generalmente in contenitori di materiale inerte e trasparente alle microonde come il Teflon® o Politetrafluoroetilene (PTFE) e il Perfluoroalcossifluorocarbonio (PFA). Il trattamento delle matrici organiche va effettuato con grande attenzione, visto l’innalzamento rapido di temperatura e pressione che si ha all’interno dei contenitori. Per evitare che si inneschino reazioni incontrollabili se non esplosive, generalmente è possibile controllare con dei sensori temperatura e pressione dei contenitori Esempi di trattamento con microonde La maggior parte delle matrici organiche può essere solubilizzata con acido nitrico concentrato: 2 ml sono sufficienti per la digestione di 100200 mg di campione di tessuti animali come carne e pesce, frutta e verdura, bevande con alto contenuto di sostanze organiche (the, vino, birra), latte e derivati. Nei casi più difficoltosi è possibile addizionare acqua ossigenata, acido perclorico o solforico, ma sono necessarie particolari precauzioni per evitare reazioni esplosive Ciò è necessario, ad esempio, per la solubilizzazione di farine e prodotti da forno e in generale per alimenti con alto contenuto di grassi e proteine Spesso i sistemi di digestione con microonde esistenti in commercio prevedono la possibilità di trattare contemporaneamente più campioni, ciascuno nel proprio contenitore, e ciò abbrevia notevolmente i tempi di analisi Estrazione con solvente Si tratta di una tecnica di pretrattamento molto comune, utilizzata in tutti i casi in cui non è necessaria o è anzi controindicata la solubilizzazione totale del campione. Permette di portare in soluzione selettivamente gli analiti di interesse, lasciando la matrice quasi intatta. Si effettua in contenitore chiuso ponendo il campione a contatto con un solvente con esso immiscibile, nel quale siano però solubili gli analiti. Si può avere: Estrazione liquido/liquido se sono liquidi sia il campione sia il solvente estraente Estrazione liquido/solido se si effettua con un solvente liquida su un campione solido Esecuzione dell’estrazione L’estrazione si effettua ponendo in agitazione il campione e il solvente in un imbuto separatore per un tempo determinato (A), attendendo la separazione di fase (B) e recuperando la fase solvente che contiene gli analiti estratti di interesse (C) secondo una modalità che dipende dalla sua densità: prelevandola dal basso se è la fase più densa, scartando la fase inferiore e prelevando il residuo se è invece la fase meno densa L’ampia gamma di solventi disponibili permette di effettuare estrazioni molto selettive. Nell’esecuzione, va considerato il fatto che si utilizzano quasi sempre solventi organici e quindi tossici A B C Estrazione con Soxhlet Un strumento molto utilizzato nel pretrattamento di campioni agroalimentari agroalimentari è l’estrattore Soxhlet, Soxhlet, che consente di effettuare lunghi cicli di estrazione in modalità modalità semiautomatica con buon recuperi. recuperi. Il campione è posto all’ all’interno di un ditale poroso permeabile al solvente estraente. estraente. Attraverso un sistema ciclico di ebollizione, ebollizione, condensazione e ricaduta, ricaduta, il solvente è in grado di agire sul campione più più volte, volte, estraendo gli analiti con maggiore efficienze rispetto all’ all’estrazione classica in imbuto separatore La procedura è automatizzabile in batteria per poter agire su più più campioni contemporaneamente Modalità di estrazione Imbuto separatore: pochi campioni piccole quantità di campione oppure… elevate quantità di solvente Estrattore di Soxhlet: numerosi campioni grosse quantità batteria di estrattori (Soxhtec) Estrazione accelerata (ASE) L’estrazione con solvente tradizionale, pur garantendo ottime prestazioni, presenta alcuni inconvenienti tra cui i tempi lunghi di trattamento, le elevate quantità di solvente utilizzato e la scarsa adattabilità all’automazione. Per questo motivo, sono state sviluppate alcune varianti. Nell’estrazione pressurizzata o accelerata con solvente (PSE o ASE) si utilizza un solvente in condizioni sub-critiche, nelle quali l’efficienza di estrazione è molto maggiore. Si lavora in recipiente chiuso, pressurizzato e termostatato. Ciò consente di ridurre i tempi di estrazione e la quantità di solvente necessaria; inoltre è possibile automatizzare il processo La tecnica ASE è ormai d’uso corrente per il trattamento di campioni agroalimentari. Esempi di applicazioni in cui la tecnica è preliminare all’analisi cromatografica sono: Estrazione di pesticidi fosforici da frutta e verdura con acetato di etile Estrazione di idrocarburi policiclici aromatici (PAH) da cibi affumicati con miscela diclorometano/acetonitrile Estrazione di composti organico-arsenici da pesce con miscela acqua/metanolo Estrazione con fluidi supercritici In questa variante dell’estrazione liquido/solido si utilizza, al posto del solvente, un fluido supercritico, cioè una sostanza portata al di sopra della pressione e della temperatura critiche, quindi con un comportamento intermedio tra gas e liquidi: la diffusione nei solidi è paragonabile a quella dei gas, mentre la capacità di solubilizzazione è quella dei liquidi; inoltre i fluidi supercritici possono solvatare molecole grandi non volatili. Queste caratteristiche rendono i fluidi supercritici estremamente efficienti nel processo di estrazione, senza presentare gli inconvenienti dei solventi liquidi dal punto di vista di prezzo e pericolosità Il fluido più utilizzato per l’estrazione è la CO2 che ha caratteristiche di prezzo e inerzia chimica ottime e valori critici molto bassi: a 40°C e 378 Atm il suo potere solvatante è paragonabile a quello del benzene La tecnica SFE è utilizzata già da tempo in campo agroalimentare per l’estrazione della caffeina dai chicchi di caffè e degli olii essenziali dai prodotti vegetali. Attualmente le applicazioni sono numerose: la tecnica (preliminare all’analisi con cromatografia fluida supercritica, SFC) risulta particolarmente efficiente nell’estrazione di grassi dagli alimenti, ma è impiegata anche per pesticidi, glucosidi, vitamine, ecc. Estrazione con fasi solide (SPE) L’estrazione con fasi solide prevede l’utilizzo di una fase estraente, appunto, solida, normalmente costituita da una colonnina impaccata con materiale avente proprietà sorbenti. Si tratta di una tecnica molto diffusa e utilizzata in tutti campi della chimica analitica, sia per estrarre selettivamente gli analiti di interesse, sia per purificare i campioni che si vogliono analizzare (es. precolonne per cromatografia) La tecnica sfrutta quindi l’affinità di una fase sorbente per alcune sostanze presenti nel campione, che possono essere sia gli analiti di interesse sia sostanze interferenti che si desidera eliminare dal campione. La scelta del materiale sorbente più opportuno rende possibile modulare la procedura a seconda delle necessità Passaggi nella SPE Il procedimento consta delle seguenti fasi: Attivazione del materiale sorbente Passaggio del campione sulla colonnina con trattenimento selettivo degli analiti Lavaggio per eliminare specie indesiderate Desorbimento (eluizione) eluizione) degli analiti trattenuti con un opportuno solvente Se si desidera eliminare gli interferenti anzichè anzichè trattenere gli analiti, analiti, è sufficiente usare una fase solida con affinità affinità per i composti che si vuole eliminare dal campione Fasi sorbenti I meccanismi su cui si basa il trattenimento delle sostanze su fase solida sono tre: Adsorbimento, dovuto a forze di Van der Waals, legami idrogeno, interazioni dipolo-dipolo Ripartizione di un soluto tra due fasi immiscibili Interazione coulombiana tra cariche di segno opposto Su questi principi funziona la maggior parte delle fasi solide utilizzate per la SPE, che sono molto simili a quelle impiegate in cromatografia liquida. A seconda del tipo di composto che si vuole trattenere (non polare, polare o ionico) si possono scegliere le seguenti fasi: Non polari Polari A scambio ionico Silice-C18 Si-CN SCX, a scambio cationico con gruppi SO3Silice-C8 Silice a scambio cationico con gruppi chelanti Silice -fenile Allumina SAX, a scambio anionico con gruppi ammonio La fase non polare Si-C18 è una delle più utilizzate per l’analisi alimentare come filtro per la rimozione di interferenti idrofobici, es. composti organici nel vino e nel mosto Le fasi a scambio ionico sono utilizzate per il trattenimento di analiti ionici o ionizzabili come pesticidi, erbicidi, tossine, ecc. Fasi eluenti Il desorbimento degli analiti o eluizione è effettuato facendo passare sulla colonnina un piccolo volume di solvente che recupera le sostanze trattenute. Il volume dell’eluente può essere ridotto per incrementare la sensibilità del metodo analitico Per la scelta dell’eluente è necessario tenere conto del tipo di interazione stabilito tra la fase solida sorbente e l’analita; l’eluente deve avere un’interazione con l’analita maggiore di quella che quest’ultimo ha con la fase sorbente Eluenti tipici possono essere: una soluzione acida (HNO , HCl) per eluire ioni metallici da una fase a 3 scambio ionico un solvente organico a polarità varia (metanolo, diclorometano, acetonitrile) per eluire composti organici da una fase Si-C18 Compatibilità con la tecnica analitica Un parametro importante per scegliere il sistema SPE e in particolare la fase eluente consiste nella compatibilità con la tecnica analitica. In particolare, se successivamente al pretrattamento si impiega una tecnica cromatografica possono esserci dei vincoli: tolleranza del sistema cromatografico a solventi organici tolleranza a valori di pH estremi (eluente molto acido o molto basico) tolleranza a contenuto salino elevato Ad esempio, se dopo il trattamento SPE è prevista la separazione su una colonna Si-C18, stabile fino a pH 7, non si potrà evidentemente utilizzare un sistema SPE che preveda l’uso di un eluente basico Applicazioni della SPE Le applicazioni della tecnica SPE in campo agroalimentare sono numerosissime. Naturalmente i campioni liquidi sono quelli più idonei al trattamento con SPE preliminare all’analisi vera e propria; nell’analisi di campioni solidi è necessario uno stadio di solubilizzazione o di estrazione con solvente. Alcuni esempi di applicazioni sono i seguenti: Estrazione di composti volatili, acidi grassi ed esteri dal vino: si ottiene con una fase estraente a fase inversa del tipo Si-C18 o Si-C8 Estrazione di antocianine e polifenoli dal vino: si ottiene con una fase estraente polimerica a base di polivinilpirrolidone (PVP) Purificazione di un campione liquido da cloruri: si ottiene con una fase estraente contenente ioni Ag+, con i quali lo ione Cl- forma AgCl insolubile Verifica delle condizioni Per ottenere un trattenimento efficiente, è sempre opportuno verificare il campo di applicazione della fase estraente. In particolare il pH del campione può essere decisivo nel successo di una procedura SPE, in quanto a seconda del pH molte sostanze possono avere un comportamento ionico o non ionico, acido o basico, ecc. Nel caso, ad esempio del trattenimento di acidi carbossilici su fase inversa Si-C18, esso si può realizzare già a pH debolmente acido, al quale gli acidi carbossilici sono protonati e quindi hanno un comportamento non ionico; per valori di pH elevati nel campione, invece, gli acidi potrebbero essere parzialmente deprotonati e quindi non essere trattenuti su una fase estraente apolare Preconcentrazione con SPE Un impiego importante della SPE consiste nel preconcentrare gli analiti di interesse preliminarmente all’analisi, cioè nell’incrementare la concentrazione degli analiti nel campione se questa è troppo bassa per poter essere misurata con gli strumenti a disposizione La preconcentrazione si ottiene facendo fluire volumi elevati di campione sulle colonnine; se l’analita o gli analiti sono completamente trattenuti dalla fase estraente, è possibile ottenerne il rilascio utilizzando un piccolo volume di eluente. Se il volume di eluente è inferiore al volume di campione caricato e se il trattenimento e il rilascio degli analiti sono quantitativi, si avrà un incremento della concentrazione degli analiti che può essere quantificato in ragione del rapporto Vc/Ve con Vc = volume di campione caricato sulla fase estraente Ve = volume di eluente Naturalmente l’eluente dovrà essere scelto in modo che sia sufficientemente forte da desorbire tutto l’analita trattenuto in un piccolo volume Il sistema fase solida estraente/eluente può essere scelto in modo da ottenere contemporaneamente la preconcentrazione degli analiti e la rimozione delle sostanze interferenti Microestrazione in fase solida Nella microestrazione in fase solida (SPME) una fibra ricoperta di materiale sorbente è immersa in un campione liquido, oppure in recipiente chiuso nello spazio di testa di un campione liquido o solido (1); le sostanze che hanno affinità per la fase sorbente vengono estratte (2) e possono essere rilasciate per riscaldamento della fibra (3), cosa che può avvenire nell’iniettore di un gascromatografo (4). Il carico di sostanze che entrano in colonna è alquanto limitato, in particolare nella versione che agisce sullo spazio di testa 15.0e6 12.5e6 10.0e6 7500e3 5000e3 2500e3 5 1 2 3 10 15 20 25 30 35 4 40 45 50 55 60 65 In questa figura si vede meglio l’assemblaggio della sonda SPME. Il materiale attivo dal punto di vista della sorzione è limitato alla fibra interna, che viene esposta soltanto al momento opportuno, cioè a contatto con il campione o con il suo spazio di testa, per evitare assorbimento di sostanze volatili dall’aria Le fasi sorbenti disponibili sono analoghe a quelle impiegate in SPE ma principalmente utili per la determinazione di sostanze volatili o semivolatili a vario grado di polarità Esempio di analisi SPME/GC-MS L’applicazione tipica del metodo SPME si ha nella caratterizzazione di composti volatili in accoppiamento alla tecnica GC-MS. Ad esempio nell’analisi del vino esso permette di determinare un numero elevato di sostanze volatili, importanti per definirne il quadro aromatico. In un vino sono determinabili 50-100 sostanze aventi caratteristiche di volatilità, in prevalenza alcoli, terpeni ed esteri (nella figura estratto SPME da un Nebbiolo) Separazione con membrane Nelle determinazione di parametri inorganici nel latte (anioni, cationi) mediante cromatografia, il campione non può essere iniettato direttamente in colonna sia a causa del suo elevato contenuto salino, sia soprattutto a causa dei colloidi dispersi presenti in grande quantità, che intaserebbero la fase stazionaria. In casi come questo, in cui cioè il campione non sia omogeneo, è spesso consigliabile o necessario procedere alla separazione delle fasi che compongono il campione, in particolare quelle non in soluzione che potrebbero creare problemi al sistema di misura La separazione può essere effettuata in diversi modi: • precipitando le fasi interferenti e poi filtrando la soluzione restante • utilizzando filtri in base al peso molecolare (ultrafiltrazione) • sfruttando la dialisi La dialisi Il pretrattamento con dialisi sfrutta la migrazione di sostanze a basso peso molecolare attraverso una membrana di materiale polimerico (es. acetato di cellulosa), impermeabile al passaggio di particelle grandi (> 0.2 µm), fino a raggiungere l’equilibrio tra il campione e una soluzione accettore I pazienti che soffrono di insufficienza renale cronica utilizzano questo metodo. A causa di questa disfunzione, nel loro sangue i composti ionici a basso peso molecolare si accumulano a concentrazioni troppo elevate, alterando l’equilibrio elettrolitico e le funzioni metaboliche collegate. La concentrazione di questi ioni va quindi ridotta ad intervalli regolari attraverso la dialisi: una soluzione accettore a bassissima forza ionica – usualmente acqua ultrapura – è fatta scorrere lungo una membana semipermeabile, mentre il sangue del paziente scorre dall’altro lato della membrana. Gli ioni diffondono dalla soluzione a maggiore forza ionica, il sangue, alla soluzione a minore forza ionica, la quale è rinnovata in continuo per fare in modo che l’equilibrio non sia mai raggiunto e la migrazione dal sangue sia continua, fino ad ottenerne la purificazione Dialisi per il latte Il pretrattamento di campioni di latte a scopo analitico ha l’obiettivo opposto: la soluzione accettore è a contatto con la membrana in condizioni statiche, in modo che si raggiunga l’equilibrio al quale gli ioni sono totalmente migrati nella soluzione accettore, la quale può essere utilizzata per la determinazione degli analiti ionici in quanto non contiene le sostanze interferenti Il metodo di dialisi può essere automatizzato all’interno di un cromatografo ionico. Il tempo necessario per raggiungere l’equilibrio di dialisi è di circa 10 minuti, dopo il quale il campione (cioè la soluzione accettore) è iniettato in colonna; mentre l’eluizione è in corso è possibile preparare un nuovo campione con la dialisi Sulla soluzione trattata con dialisi è possibile determinare tutte le specie ioniche a basso peso molecolare, come anioni, cationi e oligosaccaridi
Scaricare