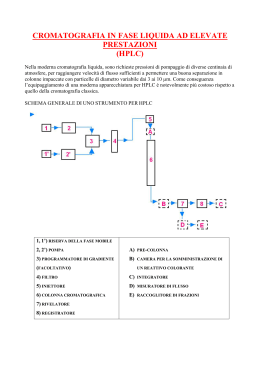
INTRODUZIONE La prima esperienza cromatografica fu eseguita dal botanico russo Twsett all’inizio del secolo scorso. Egli riempì una colonna con CaSO4 (gesso) in polvere, vi depositò in testa un estratto di foglie verdi ed eluì con etere di petrolio. I vari pigmenti fogliari si separarono in bande colorate, e per questo che fu coniato il termine cromatografia, tuttora usato per indicare tutta una serie di tecniche analitiche di separazione di una miscela nei suoi componenti, basate sulla distribuzione differenziale dei vari componenti tra due fasi, di cui una mobile ed una fissa (fase stazionaria). Nella Cromatografia Liquida la fase mobile è un liquido. A seconda della fase stazionaria esistono quattro processi distinti per il ritardo dei soluti: a) Cromatografia di ripartizione Liquido – Liquido b) Cromatografia Liquido – Solido o di adsorbimento c) Cromatografia a Scambio Ionico d) Cromatografia per esclusione o permeazione su Gel (Gel Permeation) L’apparecchiatura utilizzata in queste tecniche è sempre il cromatografo liquido ad alte prestazioni (HPLC) Confronto fra HPLC e GC In GC sono eluibili, direttamente senza alcuna modificazione del campione, solo circa il 20% dei composti organici noti. Le limitazioni maggiori sono dovute al fatto che i soluti devono essere volatili e termostabili. Non possono essere analizzati direttamente composti ionici e macromolecole. La sola fase stazionaria è disponibile per l’interazione con il campione La Cromatografia Liquida non presenta limitazioni di questo tipo. Per questo essa è adatta sia per analizzare composti con bassa tensione di vapore come macromolecole, proteine, polisaccaridi, composti ionici, che per analizzare prodotti termolabili come aminoacidi, coloranti, acidi nucleici etc. Sia la fase stazionaria che la fase mobile interagiscono con il campione Strumentazione Strumentazione Un Cromatografo Liquido è costituito da un serbatoio di solvente, una pompa che invia attraverso la colonna il solvente, un sistema di iniezione del campione, una colonna analitica, un sistema di rivelazione (detector) ed un sistema di elaborazione del segnale. Pompe Le pompe impiegate nei cromatografi HPLC devono soddisfare diversi requisiti. a) Il flusso deve essere costante, senza pulsazioni. I flussi devono poter essere impostati nell’intervallo fra 0.1 e 10 mL/min. Per l’uso analitico i flussi sono normalmente di 1 – 2 mL/min. b) Si deve avere la possibilità di operare anche a pressioni massime molto alte per consentire l’impiego di colonne lunghe. c) Non deve produrre apprezzabili segnali di fondo d) Le parti della pompa in contatto con l’eluente devono essere costituite da materiali chimicamente inerti. e) Devono essere caratterizzate da semplicità d’uso. Esistono quattro tipi principali di pompe: 1) Pneumatiche; 2) A siringa; 3) Reciprocanti; 4) Ad amplificazione idraulica. Syringe-Type Pumps Le pompe a siringa sono generalmente costituite da un cilindro contenente la fase mobile che viene poi spinta in colonna da un pistone. Queste pompe presentano notevoli vantaggi: sono robuste, possono dare pressioni elevatissime, non danno un flusso pulsato. Gli svantaggi sono dati soprattutto dal fatto che presentano una capacità limitata (20 mL) e che con esse non è possibile eseguire gradienti. Le pompe attualmente utilizzate sono le reciprocanti. Possono essere singolo o doppio pistone. Schematic of the reciprocating single piston pump. CAM is pushing a sapphire piston back and force. When the piston is moving backwards it sucks the eluent through the inlet check valve (on the bottom). The sapphire ball is lifted and opens the path for the eluent. When the piston moves forward, the liquid pushes the inlet ball down and closes the path, but the outlet ball is lifted and opens the outlet valve (upper). Schematic of a dual-head reciprocating pumps. Altro esempio di pompa reciprocante; essa produce un flusso quasi privo di pulsazioni. Pressure Dampers Flow and pressure profiles for different types of pumps and cam shape INJECTORS Rheodyne injector In HPLC i campioni vengono introdotti per mezzo di un iniettore. Esso consiste di una valvola ed un “loop”. Il volume del loop può variare da 10 a 500 μL. Esistono colonne di differenti dimensioni, la loro lunghezza è generalmente di 10 o 15 cm ed il diametro interno di 0,26 – 0,3 cm o 0,46 – 0,5 cm. Nelle colonne per HPLC in “Fase Inversa” la fase stazionaria più utilizzata è composta da particelle di silice derivatizzata con catene ad 8 o 18 atomi di carbonio. Qui è rappresentata una sezione di una particella di silice; possiamo notare la grande area superficiale (zone bianche) fuori e dentro la particella. La superficie delle particelle (internamente ed esternamente) è ricoperta da uno strato di molecole organiche chimicamente legate alla superficie della silice. Ingrandimento della sezione di particella in cui si possono notare le catene alchiliche legate alla superficie della silice. Schematic of monomeric and polymeric bonded layers Picture of dodecilsilane model on the silica surface and three octadecylsilane chains Anche in HPLC l’efficienza di una colonna viene valutata per mezzo del numero di piatti teorici. Il numero di piatti teorici viene calcolato utilizzando il tempo di ritenzione e la larghezza del picco (alla base o a metà altezza). Il fattore di capacità k’ viene calcolato utilizzando il tempo di ritenzione di un picco (tR) ed il tempo morto del del sistema (t0). Se il campione presenta due o più componenti, possiamo anche calcolare il rapporto di ritenzione (α) per ogni coppia di picchi. α è semplicemente il rapporto dei fattori di capacità dei due picchi. (k’ del secondo picco diviso k’ del primo picco). Esso ci dà informazioni cromatografico. sulla selettività del sistema La principale differenza chimica tra la fase stazionaria e la fase mobile, in HPLC “fase inversa”, può essere descritta in questo modo. Possiamo dire che la fase mobile acqua/solvente organico è polare, mentre la fase stazionaria legata alla silice è apolare. Possiamo descrivere la fase mobile come idrofila, mentre la fase stazionaria legata come idrofoba. La fase legata può essere paragonata ad una cera o ad un film oleoso che scaccia l’acqua ed i composti che si solubilizzano bene in essa. Quindi i composti polari preferiranno la fase mobile polare e percorreranno la colonna velocemente; composti non polari tenderanno a preferire la fase legata non polare e si muoveranno in colonna più lentamente. Osservando il cromatogramma a destra, vediamo che la ritenzione aumenta all’aumentare della non polarità del composto (il nitrobenzene è il più polare di questi composti) Separazione di composti nitroaromatici su colonna C18 con fase mobile composta dal 60% di metanolo in acqua. Generalmente, una diminuzione del 10% del contenuto d’acqua della fase mobile dà come risultato una diminuzione dei tempi di ritenzione di un fattore 2 o 3. Quindi, variando il contenuto d’acqua della fase mobile possiamo controllare i tempi d’analisi. Bisogna notare però che questo comporta un peggioramento della separazione; i picchi si avvicinano tra loro. Separazione dello stesso campione usando però il 70% di metanolo in acqua. DETECTORS Il detector misura la concentrazione del campione nel momento in cui esce dalla colonna e passa attraverso la sua cella a flusso. Quando la cella viene attraversata solamente dalla fase mobile, viene registrato un segnale costante detto linea di base del cromatogramma o del detector. Quando assieme alla fase mobile vi è un composto, il detector risponde dando un aumento della sua risposta che viene poi tradotta in segnale grafico (picco cromatografico). Il detector più usato in HPLC è quello spettrofotometrico, comunemente chiamato UV o UV-VISIBILE. Schema semplificato del detector UV a lunghezza d’onda fissa (254 nm). Oggi vengono utilizzati principalmente due tipi di detector UV: 1) A lunghezza d’onda variabile, comunemente chiamato “UV” 2) A serie di fotodiodi, detto comunemente “Diode Array” Il detector UV a lunghezza d’onda variabile usa un monocromatore (fenditura e reticolo) per selezionare una lunghezza d’onda della luce da far passare attraverso la cella a flusso Nel detector a serie di fotodiodi tutte le lunghezze d’onda della luce passano attraverso la cella a flusso, poi ogni lunghezza d’onda viene focalizzata su singoli sensori. Il detector elettrochimico è basato sulla misurazione della corrente risultante da una reazione di ossido/riduzione dell’analita con uno specifico elettrodo. Essendo la corrente prodotta direttamente proporzionale alla concentrazione dell’analita, questo detector può essere usato per analisi quantitative. Optical schematic of a typical fluorescence detector for liquid chromatography. I detector a fluorescenza sono probabilmente i più sensibili fra i moderni detector per HPLC. La loro sensibilità è tipicamente da 10 a 1000 volte più elevata di quella di un detector UV, per analiti fortemente rivelati in UV. I detector a fluorescenza sono molto più specifici e selettivi rispetto agli altri detector ottici. Questo risulta essere un grande vantaggio quando, in un campione, si devono quantificare analiti che presentano fluorescenza nativa.
Scaricare