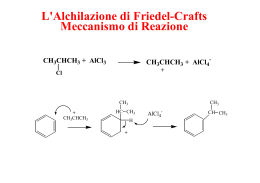
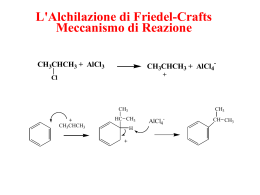
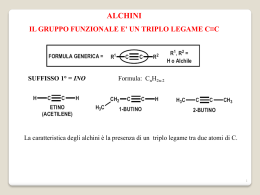
Università degli Studi di Parma _______________________________________________________________________________________ ACILAZIONE DI FRIEDEL-CRAFTS (reazione di sostituzione elettrofila aromatica) CH3 CH3 O O + AlCl3 O OH O O Reagenti acilanti: cloruri degli acidi anidridi esteri acidi carbossilici Catalizzatori: classici acidi di Lewis (AlCl3, FeCl3, …) acidi solidi (zeoliti, clays) reagente P.M. volume / peso moli rapporto molare Toluene 92.141 15 ml 0.140 14.0 An. succinica 100.075 1.0 g 0.010 1.0 AlCl3 133.34 2.0 g 0.015 1.5 1 Università degli Studi di Parma _______________________________________________________________________________________ O Ar-H + R O AlCl3 X + Ar HX R O O X = Cl, R , OR, OH O _ 1) R + AlCl3 Cl R C O + + AlCl4 O 2) + R C O + H R + O O 3) H R _ + R AlCl4 + HCl + AlCl3 + O O R Cl R + AlCl3 + 2 + HCl + AlCl3 Università degli Studi di Parma _______________________________________________________________________________________ CH3 O + AlCl3 O + O _ AlCl3 1) O O O O AlCl3 + O R C O + O + R C O _ O + O AlCl3 O O O O H AlCl3 + 2) H3C H3C O _ O H 3) _ O O AlCl3 O OH + + AlCl3 H3 C H 3C 3 Università degli Studi di Parma _______________________________________________________________________________________ REGIOCHIMICA CH3 O orto R CH3 CH3 meta R CH3 para O E O R intermedio =' =" meta orto para c.r. 4 Università degli Studi di Parma _______________________________________________________________________________________ CH3 CH3 CH3 + + + H O O H O AlCl _ 3 O O _ H O O O AlCl3 _ + H O 5 _ CH3 AlCl3 H O O AlCl _ 3 O CH3 O O AlCl _ 3 O CH3 + H O AlCl3 O + O Università degli Studi di Parma _______________________________________________________________________________________ ACILAZIONE DEL TOLUENE CON ANIDRIDE SUCCINICA Procedura sperimentale 1. In un pallone a fondo tondo da 100 ml munito di refrigerante di Liebig con valvola a CaCl2, si introducono nell’ordine l’ancoretta magnetica, 2.0 g di AlCl3 e 15 ml di toluene [NB: tutta la vetreria deve essere perfettamente asciutta] 2. Si inizia l’agitazione e quando la soluzione è omogenea si aggiunge 1.0 g di anidride succinica. 3. Dopo circa 10 minuti si inizia molto lentamente il riscaldamento ponendo il pallone in un bagno ad olio e si porta ad ebollizione la soluzione. Si lascia a riflusso per 20 minuti. 4. Dopo 10 minuti di ebollizione si preleva con una pipetta Pasteur circa 1 ml di miscela di reazione che viene versato cautamente in una provetta contenente 2 ml di H2O. Prelevando una goccia della fase organica soprastante si esegue una TLC (eluente indicativo: acetato di etile) per controllare l’andamento della reazione. 5. Alla fine dei 20 minuti di riscaldamento si raffredda la miscela di reazione che viene quindi versata cautamente in un beacker contenente ghiaccio e 100 ml di H2O [NB: la reazione è esotermica e sviluppa HCl]. 6. Si travasa il contenuto del beacker in un imbuto separatore lavando il beacker stesso con acetato di etile (∼70 ml) e si estrae la fase organica. 7. L’estratto organico viene lavato con H2O (50 ml) e quindi seccato su Na2SO4. 6 Università degli Studi di Parma _______________________________________________________________________________________ 8. Si filtra la soluzione con filtro a pieghe in un pallone precedentemente tarato, si elimina l’acetato di etile al rotavapor e si secca bene il pallone collegandolo alla linea a vuoto. 9. Il grezzo di reazione viene cristallizzato da CH2Cl2/esano (utilizzare la minima quantità di CH2Cl2). 10. I cristalli ottenuti vengono seccati e utilizzati per: • determinazione del p.f. (teorico: 129-130 °C) 1 • registrazione dello spettro H NMR (∼50 mg di prodotto in ∼0.5 ml di CDCl3). 7
Scaricare